
Инструкция по применению Цармустине Зентива
Инструкция, прилагаемая к упаковке: информация для пользователя
Кармустин Зентива, 100 мг, порошок и растворитель для приготовления концентрированного раствора
для инфузии
кармустин
Прежде чем использовать лекарство, необходимо внимательно ознакомиться с содержанием инструкции, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу, фармацевту или медсестре.
- Если у пациента出现ят любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу или медсестре. См. пункт 4.
Содержание инструкции
- 1. Что такое лекарство Кармустин Зентива и для чего оно используется
- 2. Важная информация перед использованием лекарства Кармустин Зентива
- 3. Как использовать лекарство Кармустин Зентива
- 4. Возможные нежелательные реакции
- 5. Как хранить лекарство Кармустин Зентива
- 6. Содержание упаковки и другие сведения
1. Что такое лекарство Кармустин Зентива и для чего оно используется
Кармустин Зентива, 100 мг, порошок и растворитель для приготовления концентрированного раствора
для инфузии, является лекарством, содержащим кармустин. Кармустин относится к группе противоопухолевых лекарств,
так называемых производных нитрозомочевины, которые замедляют рост опухолевых клеток.
Кармустин Зентива используется в паллиативном лечении (облегчении симптомов заболевания и предотвращении страданий у пациентов) как монотерапия или в установленном комбинированном лечении с другими разрешенными противоопухолевыми лекарствами при определенных видах опухолей, таких как:
- Опухоли мозга - глиобластома, медуллобластома, астроцитома и метастазы в мозг
- Множественная миелома (злокачественное новообразование, развивающееся в костном мозге)
- Болезнь Ходжкина (лимфома)
- Негерминативные лимфомы (лимфома)
- Опухоли системы пищеварения или желудочно-кишечного тракта
- Меланома (злокачественная опухоль кожи)
Кармустин также используется как условное лечение перед трансплантацией собственных стволовых клеток кроветворной системы (автологичная трансплантация стволовых клеток) при злокачественных гематологических заболеваниях лимфатической системы (лимфома Ходжкина и негерминативная лимфома)
2. Важная информация перед использованием лекарства Кармустин Зентива
Когда не использовать лекарство Кармустин Зентива:
- если пациент имеет аллергию на кармустин или любой другой компонент этого лекарства
(указанных в пункте 6);
- Кармустин Зентива не должен использоваться у пациентов, у которых наблюдается снижение количества тромбоцитов, лейкоцитов или эритроцитов в результате химиотерапии или по другим причинам;
- если у пациента имеются выраженные нарушения функции почек;
- у детей и подростков в возрасте до 18 лет;
- у кормящих женщин.
Предостережения и меры предосторожности
Прежде чем начать использовать лекарство Кармустин Зентива, необходимо обсудить это с врачом, фармацевтом или медсестрой.
Основным нежелательным действием этого лекарства является задержанная миелосупрессия, поэтому врач будет контролировать морфологию крови каждую неделю в течение как минимум 6 недель после введения дозы лекарства. Во время использования рекомендуемых доз курсов лечения лекарством Кармустин Зентива не будут вводиться чаще чем каждые 6 недель. Прежде чем ввести лекарство, врач будет контролировать морфологию крови.
Необходимо немедленно сообщить врачу, если у пациента появятся какие-либо из следующих симптомов:
- Симптомы инфекции (лихорадка, упорный боль в горле)
- Повышенная склонность к образованию синяков и (или) кровотечений
- Необычная усталость
- Ускоренное и (или) нерегулярное сердцебиение
Прежде чем начать лечение, будут проведены исследования функции печени, легких и почек, которые будут регулярно повторяться во время лечения.
Во время лечения могут появиться желудочно-кишечные симптомы в виде рвоты и тошноты.
Поскольку использование лекарства Кармустин Зентива может привести к повреждению легких, прежде чем начать лечение, будет проведено рентгенологическое исследование грудной клетки, а также исследования функции легких (см. также пункт «Возможные нежелательные реакции»).
Лечение высокими дозами кармустина (до 600 мг/м) используется только в комбинации с последующей трансплантацией стволовых клеток. Высокие дозы могут увеличить риск появления и усиления токсического действия на легкие, почки, печень, сердце и систему пищеварения, а также инфекций и нарушений электролитного баланса (низкая концентрация калия, магния и фосфора в крови).
Боль в животе (нейтропенический энтероколит) может появиться как нежелательное действие, связанное с терапией, после использования химиотерапевтических препаратов.
Пациенты, которые имеют несколько заболеваний и имеют более тяжелое состояние, более подвержены нежелательным реакциям. Это особенно важно для пациентов пожилого возраста.
Врач проинформирует пациента о возможности повреждения легких и аллергических реакциях, а также их симптомах.
В случае появления таких симптомов необходимо немедленно обратиться к врачу (см. пункт 4).
Женщины и мужчины детородного возраста должны использовать эффективные методы контрацепции во время лечения и как минимум 6 месяцев после лечения (просьба прочитать подраздел «Беременность, кормление грудью и плодность»).
Лекарство Кармустин Зентива и другие лекарства
Необходимо сообщить врачу или фармацевту о всех лекарствах, которые пациент принимает в настоящее время или принимал recently, а также о лекарствах, которые пациент планирует принимать, включая лекарства, отпускаемые без рецепта, такие как:
- Фенитоин, используемый при эпилепсии
- Циметидин, используемый при проблемах с желудком, таких как диспепсия
- Дигоксин, используемый при нарушении сердечного ритма
- Мелфалан - противоопухолевый препарат
- Дексаметазон, используемый как противовоспалительное и иммунодепрессивное средство
- Метотрексат, циклофосфамид, прокарбазин, хлорэтил, фторурацил, винбластин, актиномицин (дактиномицин), блеомицин, доксорубицин (адриамицин), используемые при лечении различных видов опухолей.
Беременность, кормление грудью и плодность
Если пациентка беременна или кормит грудью, предполагает, что может быть беременной, или планирует беременность, она должна обратиться к врачу или фармацевту перед использованием этого лекарства.
Беременность и плодность
Лекарство Кармустин Зентива не должно использоваться во время беременности, поскольку оно может иметь вредное влияние на нерожденного ребенка. Поэтому, как правило, не следует назначать это лекарство беременным женщинам.
В случае использования во время беременности пациентка должна быть осведомлена о потенциальных рисках для нерожденного ребенка. Женщины детородного возраста должны избегать беременности во время лечения этим лекарством. Женщинам, способным к беременности, необходимо проинформировать о необходимости использования эффективной контрацепции для предотвращения беременности во время лечения этим лекарством и как минимум 6 месяцев после лечения.
Мужчины должны использовать соответствующие методы контрацепции во время лечения лекарством Кармустин Зентива и как минимум 6 месяцев после лечения, чтобы предотвратить беременность у их партнеров. Кармустин Зентива может нарушать плодность у мужчин. Необходимо рекомендовать пациентам получить консультацию по вопросам плодности/планирования семьи перед началом лечения лекарством Кармустин Зентива.
Кормление грудью
Не разрешается кормить грудью во время приема этого лекарства и в течение 7 дней после лечения. Не можно исключить риск для новорожденных/младенцев.
Вождение транспортных средств и эксплуатация механизмов
Влияние лекарства на способность управлять транспортными средствами и эксплуатировать механизмы неизвестно. Необходимо проконсультироваться с врачом перед управлением транспортными средствами или эксплуатацией любых инструментов или механизмов, поскольку головокружение является нежелательным действием, сообщаемым при использовании этого лекарства, которое может нарушать способность управлять транспортными средствами или эксплуатировать механизмы.
Лекарство Кармустин Зентива содержит пропиленгликоль
Пропиленгликоль, содержащийся в этом лекарстве, может иметь такие же эффекты, как употребление алкоголя, и увеличивать вероятность появления нежелательных реакций.
Не использовать это лекарство у детей в возрасте до 5 лет.
Использовать это лекарство только в том случае, если его назначит врач. Врач может провести дополнительные исследования во время приема этого лекарства.
3. Как использовать лекарство Кармустин Зентива
Лекарство Кармустин Зентива всегда будет вводиться квалифицированным медицинским персоналом, имеющим опыт использования противоопухолевых препаратов.
Взрослые
Дозировка зависит от состояния здоровья, площади поверхности тела и реакции на лечение. Лекарство обычно вводится не чаще чем каждые 6 недель. Рекомендуемая доза лекарства Кармустин Зентива, используемого в монотерапии у пациентов, ранее не леченных, составляет от 150 до 200 мг/м площади поверхности тела (псс) внутривенно каждые 6 недель. Лекарство можно вводить в виде единой дозы или можно разделить на ежедневные инфузии в дозах 75-100 мг/м псс в течение двух последовательных дней. Дозировка также зависит от того, вводится ли лекарство Кармустин Зентива в комбинации с другими противоопухолевыми препаратами.
Дозы будут увеличиваться в зависимости от реакции пациента на лечение.
Рекомендуемая доза кармустина, вводимая внутривенно в комбинации с другими химиотерапевтическими препаратами перед трансплантацией стволовых клеток кроветворной системы, составляет 300-600 мг/м.
Чтобы избежать токсического влияния на костный мозг, морфология крови будет часто исследоваться, и доза будет корректироваться при необходимости.
Способ введения
После растворения и разбавления лекарство Кармустин Зентива вводится внутривенно в виде капельной инфузии в течение одной-двух часов. Время инфузии не должно быть короче одной часа - в противном случае может появиться жжение и боль в месте введения лекарства. Место введения лекарства будет наблюдаться во время инфузии.
Продолжительность лечения будет определяться врачом и может быть разной у разных пациентов.
Использование у детей и подростков (в возрасте до 18 лет)
Кармустин Зентива не должен использоваться у детей и подростков из-за высокого риска появления токсичности легких.
Использование у пожилых людей
Кармустин Зентива может использоваться у пациентов пожилого возраста с осторожностью.
Функция почек будет контролироваться.
Использование большей, чем рекомендованная, дозы лекарства Кармустин Зентива
Поскольку лекарство будет вводиться врачом или медсестрой, использование неправильной дозы маловероятно. Необходимо сообщить врачу или медсестре в случае любых сомнений относительно полученной дозы лекарства.
В случае любых дальнейших вопросов относительно использования этого лекарства необходимо обратиться к врачу, фармацевту или медсестре.
4. Возможные нежелательные реакции
Как и любой лекарственный препарат, это лекарство может вызывать нежелательные реакции, хотя они не появляются у каждого пациента.
Необходимо немедленно сообщить врачу или медсестре, если появятся какие-либо из следующих симптомов:
свистящее дыхание, проблемы с дыханием, отек век, лица или губ, сыпь или зуд (особенно если они распространяются на все тело), а также чувство надвигающегося обморока. Это могут быть симптомы тяжелой аллергической реакции.
Лекарство Кармустин Зентива может вызывать следующие нежелательные реакции:
Очень часто(могут появляться у более чем 1 из 10 пациентов)
- Задержанная миелосупрессия (снижение количества кровяных клеток, производимых костным мозгом);
- Атаксия (отсутствие добровольной координации движений мышц);
- Головокружение;
- Боль в голове;
- Временное покраснение глаза, нечеткое зрение, кровоизлияние в сетчатку, воспаление радужной оболочки и зрительного нерва;
- Гипотония (снижение артериального давления) при лечении высокими дозами;
- Воспаление вен, связанное с болью, отеком, покраснением, чувствительностью;
- Расстройства дыхания (расстройства, связанные с легкими) с трудностью дыхания. Это лекарство может вызывать тяжелые (потенциально опасные для жизни) повреждения легких. Повреждение легких может появиться после многих лет лечения. Необходимо немедленно сообщить врачу, если у пациента появятся какие-либо из следующих симптомов: одышка, упорный кашель, боль в груди, постоянная слабость/усталость;
- Сильная тошнота и рвота; появляющиеся в течение 2-4 часов после введения лекарства и продолжающиеся 4-6 часов;
- При контакте лекарства с кожей: воспаление кожи;
- Случайный контакт с кожей может вызвать временное изменение цвета (потемнение участка кожи или ногтей).
Часто(могут появляться у не более чем 1 из 10 пациентов)
- Острые лейкозы (новообразование крови) дисплазии костного мозга (неправильное развитие костного мозга) в результате длительного использования. Могут появиться следующие симптомы: кровотечение из десен, боль в костях, лихорадка, частые инфекции, частые или сильные кровотечения из носа, узлы, вызванные отеком лимфатических узлов в области шеи, предплечья, живота или паха, бледность кожи, одышка, слабость, усталость или общая недостаточность энергии;
- Анемия (снижение количества красных кровяных клеток в крови);
- Энцефалопатия (заболевание мозга) при лечении высокими дозами; возможные симптомы: слабость мышечной силы в одной области тела, невозможность принимать решения или концентрироваться, непроизвольное дрожание мышц, дрожание, трудности с речью или глотанием, судороги;
- Потеря аппетита (анорексия);
- Запор;
- Диарея;
- Воспаление полости рта и губ;
- Временная токсичность печени при лечении высокими дозами, задержанная до 60 дней после введения. Это расстройство может привести к увеличению активности ферментов печени и концентрации билирубина (это параметры, определяемые в анализах крови);
- Алопеция (потеря волос);
- Покраснение кожи;
- Реакции в месте введения.
Редко(могут появляться у не более чем 1 из 1000 пациентов)
- Заболевание, связанное с блокировкой мелких вен в печени (постепенная блокировка вен), при лечении высокими дозами, при котором очень мелкие вены в печени блокируются. Возможные симптомы: накопление жидкости в брюшной полости, увеличение селезенки, сильное кровотечение из пищевода, желтуха кожи и белков глаз;
- Трудности с дыханием, вызванные заболеванием легких, при котором ткань легких покрывается рубцами
(внутрилегочная фиброз) (при лечении малыми дозами); симптомы включают: сухой кашель, одышка, утомление, потеря веса;
- Заболевания почек;
- Гинекомастия (увеличение груди у мужчин);
- Кровотечение из желудочно-кишечного тракта;
- Воспаление зрительного нерва и прилегающей сетчатки глаза
Очень редко(могут появляться у не более чем 1 из 10 000 пациентов)
- Воспаление стенки вены с образованием тромба (тромбофлебит).
Неизвестно(частота не может быть определена на основе доступных данных)
- Боли в мышцах;
- Вторичные опухоли (новообразования, вызванные радиотерапией или химиотерапией);
- Судороги (включая статус эпилептикус);
- Повреждение тканей в результате утечки в месте введения лекарства;
- Неплодность;
- Нарушение развития плода и (или) эмбриона у беременных женщин;
- Любые симптомы инфекции;
- Ускоренное сердцебиение, боль в груди;
- Аллергические реакции;
- Нарушения электролитного баланса (низкая концентрация калия, магния, фосфора в крови);
- Боль в животе (нейтропенический энтероколит);
- При использовании высоких кумулятивных доз и после длительного лечения Кармустин Зентива и другими производными нитрозомочевины наблюдалась снижение функции почек, прогрессирующая кумуляция определенных метаболических продуктов в крови (азотемия) и недостаточность почек. При использовании меньших кумулятивных доз также наблюдалось повреждение почек
Сообщение о нежелательных реакциях
Если у пациента появятся какие-либо нежелательные реакции, включая любые нежелательные реакции, не указанные в инструкции, необходимо сообщить об этом врачу или медсестре. Нежелательные реакции можно сообщать直接 в:
Департамент мониторинга нежелательных реакций лекарственных средств Управления по регистрации лекарственных средств, медицинских изделий и биоцидных продуктов
ул. Ерозолимская, 181С
102 37 Прага 10
Чешская Республика
Импортер:
MIAS Pharma Limited
Сьюит 2, Стаффорд Хаус, Странд Роуд
Портмарнок, Ко. Дублин
Ирландия
Tillomed Malta Limited,
Мальта Лайф Сайенс Парк,
ЛС2.01.06 Индустриальный Эстейт,
Сан Гван, СГН 3000, Мальта
5. Как хранить лекарство Кармустин Зентива
Лекарство должно храниться в месте, недоступном для детей.
Хранить и перевозить в охлажденном состоянии (2°C-8°C).
Не использовать это лекарство после истечения срока годности, указанного на упаковке и этикетке: Срок годности (EXP). Срок годности указывает на последний день указанного месяца.
Лекарство будет храниться врачом или другим квалифицированным медицинским персоналом.
После реconstitution в соответствии с рекомендациями, кармустин для инъекций является стабильным в течение 480 часов в холодильнике (2°-8°C) и 24 часов при комнатной температуре (25°C ±2°C) в стеклянном контейнере. Прежде чем использовать, необходимо проверить реконструированные флаконы на наличие кристаллов. В случае обнаружения кристаллов можно их снова растворить, нагревая флакон до комнатной температуры с перемешиванием.
С микробиологической точки зрения, раствор после реconstitution должен быть использован немедленно.
Хранить флакон в наружной упаковке для защиты от света.
Приготовленный раствор основного раствора должен быть затем разбавлен до 500 мл раствором хлорида натрия для инъекций или 5-процентным раствором декстрозы для инъекций, в стеклянных или полипропиленовых контейнерах остается стабильным физически и химически в течение 8 часов при температуре 25°C± 2°C, если защищен от света. Эти растворы также стабильны до 48 часов при хранении в холодильнике (2°C–8°C) и в течение дополнительных 6 часов при температуре 25°C± 2°C, если защищены от света.
Раствор должен быть защищен от света до окончания введения.
Лекарства не должны выбрасываться в канализацию или домашние контейнеры для отходов. Необходимо спросить фармацевта, как утилизировать лекарства, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит лекарство Кармустин Зентива
Активным веществом лекарства является кармустин.
Одна флакон порошка для приготовления концентрированного раствора для инфузии содержит 100 мг кармустина.
Одна флакон растворителя содержит 3 мл пропиленгликоля.
После реconstitution при использовании поставляемого растворителя, один мл раствора содержит 33,3 мг кармустина.
Другие компоненты вспомогательные вещества являются:
- Порошок: не содержит вспомогательных веществ.
- Растворитель: пропиленгликоль.
Как выглядит лекарство Кармустин Зентива и что содержит упаковка
Кармустин Зентива имеет вид порошка и растворителя для приготовления концентрированного раствора для инфузии.
Порошок является бледно-желтым и поставляется в флаконе из оранжевого стекла типа I (30 мл) с темно-серой пробкой из бромобутиловой резины и полипропиленовой крышкой.
Растворитель является прозрачной, бесцветной, вязкой жидкостью и поставляется в флаконе из бесцветного стекла типа I (5 мл) с серой пробкой из бромобутиловой резины и полипропиленовой крышкой.
Одна упаковка содержит одну флакон с 100 мг порошка и одну флакон с 3 мл растворителя.
Ответственное лицо и производитель
Ответственное лицо
Зентива к.с.
У Кабельовны 130
Долни Мехолупы
102 37 Прага 10
Чешская Республика
Импортер:
MIAS Pharma Limited
Сьюит 2, Стаффорд Хаус, Странд Роуд
Портмарнок, Ко. Дублин
Ирландия
Tillomed Malta Limited,
Мальта Лайф Сайенс Парк,
ЛС2.01.06 Индустриальный Эстейт,
Сан Гван, СГН 3000, Мальта
Этот лекарственный препарат разрешен к обращению в странах-членах Европейского экономического пространства под следующими названиями:
Бельгия:
Кармустин Тилломед 100 мг порошок и растворитель для концентрированного раствора для инфузии
Чешская Республика:
Кармустин Зентива
Дания:
Кармустин Макуре
Финляндия:
Кармустин Макуре 100 мг порошок и растворитель для концентрированного раствора для инфузии, раствор
Греция:
Кармустин/Тилломед 100 мг порошок и растворитель для концентрированного раствора для инфузии
Венгрия:
Кармустин Зентива 100 мг порошок и растворитель для концентрированного раствора для инфузии
Ирландия:
Кармустин 100 мг порошок и растворитель для концентрированного раствора для инфузии
Италия:
БИКНУ
Литва
Кармустин Зентива 100 мг порошок и растворитель для концентрированного раствора для инфузии
Нидерланды:
Кармустин Гленмарк 100 мг порошок и растворитель для концентрированного раствора для инфузии
Норвегия:
Кармустин Макуре
Польша:
Кармустин Зентива
Португалия:
Кармустин Тилломед 100 мг порошок и растворитель для концентрированного раствора для инфузии
Словакия:
Кармустин Зентива
Словения:
Кармустин Тилломед 100 мг порошок и растворитель для концентрированного раствора для инфузии
Швеция:
Кармустин Макуре
Дата последней актуализации инструкции:март 2025
---------------------------------------------------------------------------------------------------------------------
Информация, предназначенная только для медицинских специалистов:
Ниже представлен краткий описания способа приготовления и (или) использования, несовместимости
фармацевтической, дозировки лекарства, передозировки или требуемых действий, связанных с
мониторингом, а также лабораторных исследований, на основе актуальной характеристики лекарственного препарата.
Лиофилизат для приготовления концентрированного раствора для инфузии не содержит консервантов и не предназначен для использования в флаконах для многократного использования. Лекарственный препарат предназначен только для одноразового использования. Необходимо проявлять осторожность при обращении с лекарственным препаратом и избегать его контакта с кожей. Реconstitution и дополнительное разбавление должны проводиться в асептических условиях.
При соблюдении рекомендуемых условий хранения можно избежать разложения веществ, содержащихся в неоткрытой флаконе, до даты истечения срока годности, указанной на упаковке.
Хранение кармустина при температуре 27°C или выше может привести к плавлению вещества, поскольку кармустин имеет низкую температуру плавления (около 30,5°C до 32,0°C). На разложение препарата может указывать наличие маслянистой пленки на дне флакона. Такой препарат не должен использоваться.
В случае сомнений относительно того, что препарат находился в соответствующих условиях охлаждения, необходимо немедленно проверить все флаконы в картонной упаковке. Для проверки необходимо поместить флакон в яркий свет.
Реconstitution и разбавление порошка для приготовления концентрированного раствора для инфузии должны проводиться следующим образом
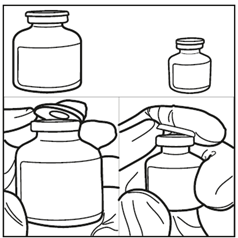
Шаг 1: Вынуть обе флаконы из упаковки и подождать, пока они достигнут комнатной температуры. (Мин. 10 минут).
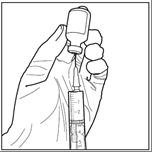
Шаг 2: В асептических условиях взять 3 мл стерильного растворителяиз флакона с растворителем с помощью стерильного шприца. Убедиться, что взята вся (3 мл) стерильного растворителя в шприц.
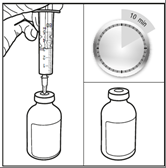
Шаг 3: Ввести стерильный растворитель в флакон, содержащий 100 мг кармустина, и оставить для намокания продукта не менее 10 минут.
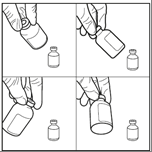
Шаг 4: Перемешать (выполняя круговые движения) не менее 60 секунд без остановки, чтобы получить прозрачный раствор
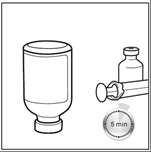
Шаг 5: Флакон необходимо держать в перевернутом положении в течение 5 минут перед извлечением восстановленного раствора
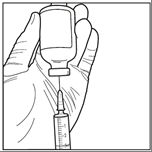
Шаг 6: Асептически извлечь приготовленный раствор исключительно в перевернутом положении и после дополнительного разбавления приготовить раствор для инфузии
Каждый миллилитр раствора, полученного в результате реconstitution, содержит 33,3 мг кармустина
Раствор после приготовления в соответствии с рекомендациями является желтоватым.
Раствор основного раствора необходимо немедленно разбавить до 500 мл раствором хлорида натрия для инъекций или 5-процентным раствором декстрозы для инъекций. Полученный раствор содержит конечную концентрацию 0,2 мг/мл кармустина, необходимо хранить вдали от света.
.
Прежде чем использовать, необходимо проверить реконструированные флаконы на наличие кристаллов. В случае обнаружения кристаллов можно их снова растворить, нагревая флакон до комнатной температуры с перемешиванием. Флаконы после реconstitution необходимо перед введением осмотреть на наличие частиц и изменений цвета.
Способ введения:
Кармустин предназначен для внутривенного введения после реconstitution и дополнительного разбавления.
Раствор, полученный после реconstitution и разбавления, необходимо ввести немедленно в виде капельной инфузии в течение 1-2 часов, защищая раствор от света. Время инфузии не должно быть короче 1 часа, поскольку выполнение инфузии в более короткое время может вызвать сильную боль и жжение в месте введения. Необходимо наблюдать за местом введения во время введения препарата.
Введение препарата должно быть завершено в течение 3 часов после его реconstitution/разбавления.
Инфузию необходимо выполнять с помощью инфузионного набора с ПЭ, не содержащего ПЦВ.
Необходимо соблюдать рекомендации по безопасному обращению с противоопухолевыми препаратами и их утилизации.
Дозировка и лабораторные исследования
Начальные дозы
Рекомендуемая доза препарата Кармустин Зентива, используемого в монотерапии у пациентов, ранее не леченных, составляет от 150 до 200 мг/м площади поверхности тела (псс) внутривенно каждые 6 недель. Препарат можно вводить в виде единой дозы или можно разделить на ежедневные инфузии в дозах 75-100 мг/м псс в течение двух последовательных дней.
Когда препарат Кармустин Тилломед используется в комбинации с другими препаратами, имеющими миелосупрессивное действие, или у пациентов, у которых снижена резерва костного мозга, дозы необходимо корректировать в соответствии с гематологическим профилем пациента, как указано ниже.
Мониторинг и последующие дозы
Следующий курс лечения препаратом Кармустин Зентива можно вводить только тогда, когда параметры морфологии крови вернутся к приемлемым значениям (количество тромбоцитов более 100 000/мм, лейкоцитов более 4000/мм), что обычно происходит в течение шести недель. Морфологию крови необходимо часто контролировать, и повторный курс лечения не должен вводиться до истечения шести недель из-за возможности появления задержанной гематологической токсичности.
После введения начальной дозы последующие дозы необходимо корректировать в зависимости от гематологической реакции пациента на предыдущую дозу, как в монотерапии, так и в комбинированной терапии с другими препаратами, имеющими миелосупрессивное действие. Рекомендуется следующая ориентировочная схема корректировки доз:
| Наименьшее значение после предыдущей дозы | Процент предыдущей дозы для введения | |
| Лейкоциты/мм3 | Тромбоциты/мм3 | |
| >4000 | >100 000 | 100% |
| 75 000 – 99 999 | 100% |
| 25 000 – 74 999 | 70% |
| <2000 | <25 000< td> | 50% |
Пожилые люди
В принципе, у пациентов пожилого возраста дозы необходимо подбирать осторожно, а в частности, необходимо начинать введение препарата с нижней границы диапазона доз, учитывая более частое появление нарушений функции печени, почек или сердца; также необходимо учитывать сопутствующие заболевания и проводимое лечение другими препаратами.
Поскольку у пациентов пожилого возраста существует более высокая вероятность нарушений функции почек, необходимо проявлять осторожность при выборе дозы и контролировать функцию почек, а также соответствующим образом снижать дозу.
Дети и подростки
Кармустин является противопоказанием для детей и подростков в возрасте до 18 лет (см. пункт 4.3) из-за высокого риска появления токсичности легких (см. пункт 4.4).
Совместимость/несовместимость с контейнерами
Раствор для инфузии нестабилен в контейнерах из полихлора винила (ПВХ). Раствор кармустина необходимо вводить только из стеклянных или полипропиленовых контейнеров.
Не смешивать препарат с другими препаратами, кроме указанных в пункте 6.6.
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- ИмпортерMIAS Pharma Ltd Tillomed Malta Limited
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги Цармустине ЗентиваФорма выпуска: Порошок, 100 мгАктивное вещество: КармустинПроизводитель: Accord Healthcare Polska Sp. z o.o. Laboratori Fundació DauТребуется рецептФорма выпуска: Порошок, 50 мгАктивное вещество: КармустинТребуется рецептФорма выпуска: Порошок, 300 мгАктивное вещество: КармустинТребуется рецепт
Аналоги Цармустине Зентива в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Цармустине Зентива в Испания
Аналог Цармустине Зентива в Украина
Врачи онлайн по Цармустине Зентива
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Цармустине Зентива – по решению врача и с учетом местных правил.






