SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada

Pergunte a um médico sobre a prescrição de SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada

Como usar SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada
Introdução
Prospecto:informação para o utilizador
Sibudel 250 mg solução injetável em seringa pré-carregada EFG
fulvestrante
Leia todo o prospecto atentamente antes de começar a usar este medicamento,pois contém informações importantes para si.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, pois pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Sibudel e para que é utilizado
- O que precisa saber antes de começar a usar Sibudel
- Como usar Sibudel
- Possíveis efeitos adversos
- Conservação de Sibudel
- Conteúdo do envase e informação adicional
1. O que é Sibudel e para que é utilizado
Sibudel contém o princípio ativo fulvestrante, que pertence ao grupo de bloqueantes de estrógeno. Os estrógenos, um tipo de hormonas sexuais femininas, podem estar em alguns casos implicados no desenvolvimento do cancro da mama.
Sibudel é utilizado:
- sozinho, para tratar mulheres pós-menopáusicas com um tipo de cancro da mama chamado cancro da mama com receptor de estrógeno positivo, que é localmente avançado ou que se espalhou para outras partes do corpo (metastásico) ou,
- em combinação com palbociclib para tratar mulheres com um tipo de cancro da mama chamado cancro da mama com receptor hormonal positivo, cancro da mama com receptor 2 do factor de crescimento epidérmico humano negativo, que está localmente avançado ou que se espalhou para outras partes do corpo (metastásico). As mulheres que não tenham alcançado a menopausa também serão tratadas com um medicamento chamado agonista da hormona liberadora de hormona luteinizante (LHRH).
Fulvestrante pode ser administrado em combinação com palbociclib. É importante que você também leia o prospecto de palbociclib. Se tiver alguma pergunta sobre palbociclib, consulte o seu médico.
2. O que precisa saber antes de começar a usar Sibudel
NÃO useSibudel:
- se é alérgica a fulvestrante ou a qualquer um dos outros componentes deste medicamento (incluídos na seção 6)
- se está grávida ou em período de amamentação (ver seção “Gravidez e amamentação”)
- se tem problemas hepáticos graves
Advertências e precauções
Consulte o seu médico, farmacêutico ou enfermeiro antes de começar a usar Sibudel se algo disto lhe aplicar:
- problemas de rim ou fígado
- contagem baixa de plaquetas (que ajudam à coagulação do sangue) ou alterações hemorrágicas
- problemas prévios de coágulos sanguíneos
- osteoporose (perda de densidade óssea)
- alcoolismo (ver seção “Sibudel contém etanol 96% (álcool)”).
Não se estudou a eficácia e segurança de fulvestrante (como monoterapia ou em combinação com palbociclib) em pacientes com doença visceral crítica.
Crianças e adolescentes
Sibudel NÃO está indicado em crianças e adolescentes menores de 18 anos.
Uso de Sibudelcomoutros medicamentos
Informa ao seu médico ou farmacêutico se está a tomar, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Em particular, deve dizer ao seu médico se está a utilizar anticoagulantes (medicamentos para prevenir os coágulos sanguíneos).
Gravidez eamamentação
NÃO deve utilizar Sibudel se está grávida. Se pode ficar grávida, deve utilizar um método anticonceptivo eficaz enquanto estiver em tratamento com Sibudel e durante 2 anos após a sua última dose.
NÃO deve amamentar enquanto estiver em tratamento com Sibudel.
Condução e uso de máquinas
Não se espera que Sibudel afete a sua capacidade para conduzir ou utilizar máquinas. No entanto, se se sentir cansada após o tratamento NÃO conduza nem utilize máquinas.
Sibudelcontém etanol 96% (álcool)
Este medicamento contém 474 mg de álcool (etanol) em cada seringa pré-carregada de 5 ml, que se corresponde a 94,8 mg/ml. A quantidade em uma dose de 10 ml deste medicamento equivale a menos de 24 ml de cerveja ou 10 ml de vinho.
A pequena quantidade de álcool neste medicamento não terá nenhum efeito notável.
Sibudelcontém álcool benzílico
Este medicamento contém 500 mg de álcool benzílico em cada seringa pré-carregada de 5 ml, equivalente a 100 mg por ml.
O álcool benzílico pode provocar reações alérgicas.
Consulte o seu médico ou farmacêutico se tiver doenças de fígado ou rim. Isto é devido a que se podem acumular no organismo grandes quantidades de álcool benzílico e provocar efeitos adversos (acidose metabólica).
Sibudelcontém benzoato de benzilo
Este medicamento contém 750 mg de benzoato de benzilo em cada seringa pré-carregada de 5 ml equivalente a 150 mg por ml.
3. Como usar Sibudel
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
A dose recomendada é 500 mg de fulvestrante (duas injeções de 250 mg/5ml) administrada uma vez ao mês com uma dose adicional de 500 mg administrada 2 semanas após a dose inicial.
O seu médico ou enfermeiro administrará Sibudel mediante uma injeção intramuscular lenta em cada um dos seus glúteos.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora não todas as pessoas os sofram.
Pode necessitar tratamento médico urgente se experimentar algum dos seguintes efeitos adversos:
- reações alérgicas (hipersensibilidade), incluindo inchaço do rosto, lábios, língua e/ou garganta que podem ser sinais de reações anafilácticas
- tromboembolismo (aumento do risco de coágulos sanguíneos)*
- inflamação do fígado (hepatite)
- insuficiência hepática.
Informa ao seu médico, farmacêutico ou enfermeiro se notar algum dos seguintes efeitos adversos:
Efeitos adversos notificados em pacientes tratados com fulvestrante em monoterapia:
Muito frequentes:podem afetar mais de 1 em cada 10 pessoas
- reações no local da injeção, como dor e/ou inflamação
- níveis anormais de enzimas hepáticos (em análise de sangue)*
- náuseas (sensação de mal-estar)
- debilidade, cansaço*
- dor articular e musculoesquelética
- suores
- erupção cutânea
- reações alérgicas (hipersensibilidade), incluindo inchaço do rosto, lábios, língua e/ou garganta
Todos os efeitos adversos restantes:
Frequentes: podem afetar até 1 em cada 10 pessoas
- dor de cabeça
- vómitos, diarreia ou perda de apetite*
- infecções do trato urinário
- dor de costas*
- aumento de bilirrubina (um pigmento da bile produzido pelo fígado).
- tromboembolismo (aumento do risco de coágulos sanguíneos)*
- níveis diminuídos de plaquetas (trombocitopenia)
- hemorragia vaginal
- dor lombar que se reflete em um lado da perna (ciática)
- debilidade súbita, entorpecimento, formigamento ou perda de movimento na sua perna, especialmente em um só lado do corpo, problemas súbitos para caminhar ou de equilíbrio (neuropatia periférica)
Pouco frequentes:podem afetar até 1 em cada 100 pessoas
- fluxo vaginal espesso, branco e candidíase (infecção)
- hematoma e hemorragia no local da injeção
- aumento de gamma-GT, uma enzima hepática que se identifica em uma análise de sangue
- inflamação do fígado (hepatite)
- insuficiência hepática
- entorpecimento, formigamento e dor
- reações anafilácticas
*Inclui efeitos adversos para os quais não se pode avaliar o papel exato de Sibudel devido à doença subjacente.
Efeitos adversos notificados em pacientes tratados com fulvestrante em combinação com palbociclib:
Muito frequentes:podem afetar mais de 1 em cada 10 pessoas
- diminuição da contagem de neutrófilos (neutropenia)
- diminuição da contagem de glóbulos brancos (leucopenia)
- infecções
- cansaço
- náuseas
- redução de glóbulos vermelhos (anemia)
- inflamação ou ulceração da boca
- diarreia
- diminuição dos níveis de plaquetas (trombocitopenia)
- vómitos
- perda de cabelo
- erupção
- perda de apetite
- febre
Frequentes: podem afetar até 1 em cada 10 pessoas
- sensação de debilidade
- aumento dos níveis de enzimas hepáticas
- perda de gosto
- hemorragia nasal
- olho excessivamente húmido
- pele seca
- visão borrada
- olho seco
Pouco frequentes:podem afetar até 1 em cada 100 pessoas
febre com outros sinais de infecção (neutropenia febril).
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Sibudel
Mantenhaeste medicamentofora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no envase ou nas etiquetas das seringas após CAD. A data de validade é o último dia do mês que se indica.
Não utilize este medicamento se observar partículas ou decoloração antes da sua administração.
Conservar e transportar em frigorífico (entre 2°C e 8°C).
As desvições de temperatura fora do intervalo de entre 2°C e 8°C devem ser controladas. Isto inclui evitar a conservação a temperaturas superiores a 25°C, e que não exceda um período de 4 meses, durante o qual a temperatura média de conservação do medicamento seja inferior a 25°C (mas acima de entre 2°C e 8°C). Após as desvições de temperatura, o medicamento deve ser retornado imediatamente às condições de conservação recomendadas (conservar e transportar em frigorífico entre 2°C e 8°C). As desvições de temperatura têm um efeito acumulativo na qualidade do medicamento, não devendo superar o período de 4 meses por cima da duração da validade de 2 anos de Sibudel. A exposição a temperaturas inferiores a 2°C não danificará o medicamento, desde que este não seja conservado por debaixo dos -20°C.
Conservar a seringa pré-carregada no embalagem original para protegê-la da luz.
O seu profissional de saúde será o responsável pela conservação, uso e eliminação corretos de Sibudel.
Este medicamento pode apresentar um risco para o meio aquático. Os medicamentos não devem ser jogados pelos ralos nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Sibudel
- O princípio ativo é fulvestrante. Cada seringa pré-carregada contém 250 mg de fulvestrante. Cada ml de solução contém 50 mg de fulvestrante.
- Os outros componentes (excipientes) são etanol (96%), álcool benzílico, benzoato de benzilo e óleo de rícino refinado.
Aspecto do produto e conteúdo do envase
Sibudel é uma solução viscosa, clara, de incolora a amarela em uma seringa pré-carregada equipada com um conector Luer-Lock que contém 5 ml de solução injetável. Devem ser administradas duas seringas para receber a dose mensal recomendada de 500 mg.
Sibudel apresenta 2 formatos:
- 1 envase que contém 1 seringa de vidro pré-carregada e 1 agulha com sistema de segurança para sua conexão com o corpo da seringa.
- 1 envase que contém 2 seringas de vidro pré-carregadas e são fornecidas além disso 2 agulhas com sistema de segurança para sua conexão com o corpo da seringa.
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
Teva Pharma, S.L.U.
C/ Anabel Segura, 11. Edifício Albatros B, 1ª planta
28108 Alcobendas, Madrid
Espanha
Responsável pela fabricação
Pliva Croatia Ltd.
Prilaz baruna Filipovica 25
10000 Zagreb
Croácia
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu com os seguintes nomes:
Alemanha: Fulvestrant AbZ 250 mg Injektionslösung in einer Fertigspritze
Espanha: Sibudel 250 mg solução injetável em seringa pré-carregada EFG
Data da última revisão desteprospecto: Julho 2025
Outras fontes de informação
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) https://www.aemps.gob.es/
Pode aceder a informação detalhada e atualizada sobre este medicamento escaneando com o seu telemóvel (smartphone) o código QR incluído no cartonagem. Também pode aceder a esta informação na seguinte direção de internet: https://cima.aemps.es/cima/dochtml/p/80999/P_80999.html
Código QR + URL
----------------------------------------------------------------------------------------------------------------------------------
Esta informação está destinada apenas a profissionais do setor sanitário:
Sibudel 500 mg (2 x 250 mg/5 ml solução injetável) deve ser administrado utilizando duas seringas pré-carregadas (ver seção 3).
Instruções de administração
Administre a injeção de acordo com as diretrizes locais para a injeção intramuscular de grandes volumes.
NOTA: Devido à proximidade do nervo ciático, deve ter precaução se injetar Sibudel na zona dorsoglútea (ver seção 4.4).
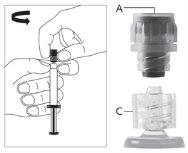
Advertência- NÃO esterilize em autoclave a agulha com sistema de segurança antes de sua utilização. As mãos devem permanecer por trás da agulha em todo o momento durante sua utilização e eliminação.
Para cada uma das duas seringas:
| Figura 1
|
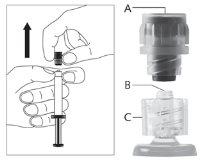
| Figura 2
|
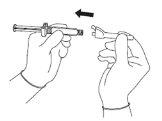
| Figura 3
|
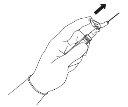
| Figura 4
|
NOTA: Ative afastado do seu corpo e dos outros. Escute o clique e confirme visualmente que a ponta da agulha está totalmente protegida. | Figura 5
|
Eliminação
As seringas pré-carregadas são apenaspara um único uso.
Este medicamento pode apresentar um risco para o meio aquático. A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele será realizada de acordo com a normativa local.

Quanto custa o SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada em Espanha em 2025?
O preço médio do SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada em dezembro de 2025 é de cerca de 225.7 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia225.7 EUR
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregadaForma farmacêutica: INJETÁVEL, 250 mg/5 mlSubstância ativa: fulvestrantFabricante: Bexal Farmaceutica S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 250 mgSubstância ativa: fulvestrantFabricante: Ever Valinject GmbhRequer receita médicaForma farmacêutica: INJETÁVEL, 250 mgSubstância ativa: fulvestrantFabricante: Astrazeneca AbRequer receita médica
Alternativas a SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada em Polónia
Alternativa a SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada em Ukraine
Médicos online para SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de SIBUDEL 250 mg Solução Injectável em Seringa Pré-carregada – sujeita a avaliação médica e regras locais.