
Fulvestrant Eugia
Pergunte a um médico sobre a prescrição de Fulvestrant Eugia

Como usar Fulvestrant Eugia
Folheto informativo para o doente: informações para o doente
Fulvestrant Eugia, 250 mg, solução injectável em seringa pré-cheia
Fulvestranto
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para que possa relê-lo se necessário.
- Em caso de alguma dúvida, deve consultar o médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é o medicamento Fulvestrant Eugia e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Fulvestrant Eugia
- 3. Como tomar o medicamento Fulvestrant Eugia
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Fulvestrant Eugia
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Fulvestrant Eugia e para que é utilizado
O medicamento Fulvestrant Eugia contém a substância ativa fulvestranto, que pertence a um grupo de medicamentos chamados antagonistas do estrogénio.
Os estrogénios, um tipo de hormona feminina, podem contribuir para o crescimento de alguns tipos de cancro da mama.
O medicamento Fulvestrant Eugia é utilizado:
- sozinho, no tratamento de mulheres na pós-menopausa com um tipo de cancro da mama chamado cancro da mama com receptores de estrogénio positivos, que é localmente avançado ou metastático, ou
- em combinação com palbociclib, no tratamento de mulheres com um tipo de cancro da mama chamado cancro da mama com receptores hormonais, sem sobre-expressão do receptor do fator de crescimento epidérmico humano 2, que é localmente avançado ou metastático. As mulheres que ainda não atingiram a menopausa também receberão um medicamento chamado análogo do hormona liberador do hormona luteinizante (LHRH).
Quando o medicamento Fulvestrant Eugia é administrado em combinação com palbociclib, é importante ler também o folheto do doente para palbociclib. Se tiver alguma dúvida sobre palbociclib, deve consultar o médico.
2. Informações importantes antes de tomar o medicamento Fulvestrant Eugia
Quando não tomar o medicamento Fulvestrant Eugia:
- se o doente tiver alergia ao fulvestranto ou a qualquer outro componente deste medicamento (listados no ponto 6)
- se o doente estiver grávida ou a amamentar
- se o doente tiver doença hepática grave
Precauções e advertências
Antes de começar a tomar o medicamento Fulvestrant Eugia, deve discutir com o médico, farmacêutico ou enfermeiro se alguma das seguintes situações se aplica ao doente:
- se o doente já teve doença renal ou hepática
- se o doente tiver contagem baixa de plaquetas (que ajudam a coagular o sangue) ou distúrbios da coagulação
- se o doente já teve trombose
- se o doente tiver osteoporose (perda de densidade óssea)
- se o doente for dependente de álcool
Crianças e adolescentes
O medicamento Fulvestrant Eugia não é recomendado para uso em crianças e adolescentes abaixo de 18 anos.
Interações com outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está a tomar atualmente ou recentemente, bem como sobre os medicamentos que o doente planeia tomar.
Em particular, deve informar o médico se o doente estiver a tomar medicamentos anticoagulantes (medicamentos que previnem a formação de trombos).
Gravidez e amamentação
O medicamento Fulvestrant Eugia não deve ser utilizado se o doente estiver grávida. Se o doente puder engravidar, deve usar métodos anticoncecionais eficazes durante o tratamento com o medicamento Fulvestrant Eugia e durante 2 anos após a última dose.
Durante o tratamento com o medicamento Fulvestrant Eugia, não deve amamentar.
Condução de veículos e utilização de máquinas
Não foi detectado que o medicamento Fulvestrant Eugia afete a capacidade de conduzir veículos ou utilizar máquinas. No entanto, se o doente se sentir cansado após a administração do medicamento, não deve conduzir veículos ou utilizar máquinas.
Excipientes:
Etanol:
Este medicamento contém 10% em volume de etanol (álcool), ou seja, até 500 mg por injeção. A quantidade de álcool em cada injeção (ou seja, em duas seringas) deste medicamento é equivalente a 25 mL de cerveja ou 10 mL de vinho.
A quantidade de álcool neste medicamento provavelmente não terá efeito nos adultos e adolescentes. O álcool neste medicamento pode alterar a ação de outros medicamentos. Se o doente estiver a tomar outros medicamentos, deve consultar o médico ou farmacêutico.
Se o doente estiver grávida ou a amamentar, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Se o doente for dependente de álcool, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Álcool benzílico:
Este medicamento contém 500 mg de álcool benzílico por injeção, o que corresponde a 100 mg/mL. O álcool benzílico pode causar reações alérgicas.
Benzoato de benzilo:
Este medicamento contém 750 mg de benzoato de benzilo por injeção, o que corresponde a 150 mg/mL.
3. Como tomar o medicamento Fulvestrant Eugia
Este medicamento deve ser sempre administrado de acordo com as instruções do médico ou farmacêutico. Em caso de dúvida, deve consultar o médico ou farmacêutico.
A dose usual é de 500 mg de fulvestranto (duas injeções de 250 mg/5 mL), administradas uma vez por mês, e uma dose adicional de 500 mg administrada duas semanas após a primeira dose.
O medicamento Fulvestrant Eugia é administrado por um médico ou enfermeiro, por injeção lenta intramuscular, uma injeção em cada nádega.
Em caso de mais perguntas sobre a administração deste medicamento, deve consultar o médico, farmacêutico ou enfermeiro.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não todos os doentes os experimentem.
Em caso de ocorrência dos seguintes efeitos não desejados, deve contactar imediatamente o médico:
- Reações alérgicas (hipersensibilidade), incluindo inchaço do rosto, lábios, língua e/ou garganta, que podem ser sintomas de reações anafiláticas
- Doença tromboembólica (aumento do risco de formação de trombos)*
- Inflamação do fígado (hepatite)
- Insuficiência hepática
Deve informar o médico, farmacêutico ou enfermeiro se notar algum dos seguintes efeitos não desejados:
Efeitos não desejados muito frequentes(podem ocorrer em mais de 1 em cada 10 doentes)
- Reações no local da injeção, como dor e/ou inflamação
- Nível anormal de enzimas hepáticas (no exame de sangue)*
- Náuseas (enjoo)
- Fraqueza, fadiga*
- Dor nas articulações e dor musculoesquelética
- Ondas de calor
- Erupções cutâneas
- Reações alérgicas (hipersensibilidade), incluindo inchaço do rosto, lábios, língua e/ou garganta
Todos os outros efeitos não desejados:
Efeitos não desejados frequentes(podem ocorrer em 1 em cada 10 doentes)
- Dor de cabeça
- Vômitos, diarreia ou perda de apetite*
- Infecções do trato urinário
- Dor nas costas*
- Aumento da bilirrubina (pigmento produzido pelo fígado)
- Doença tromboembólica (aumento do risco de formação de trombos)*
- Contagem baixa de plaquetas (trombocitopenia)
- Sangramento vaginal
- Dor na parte inferior das costas que irradia para a perna de um lado do corpo (ciática)
- Fraqueza súbita, entorpecimento, formigamento ou perda de mobilidade na perna, especialmente de um lado do corpo, dificuldade súbita em caminhar ou manter o equilíbrio (neuropatia periférica)
Efeitos não desejados não muito frequentes(podem ocorrer em 1 em cada 100 doentes)
- Descarga vaginal espessa e branca e candidíase vaginal (infecção)
- Hematoma e sangramento no local da injeção
- Aumento da atividade da gamma-GT, enzima hepática medida nos exames de sangue
- Inflamação do fígado
- Insuficiência hepática
- Entorpecimento, formigamento e dor
- Reações anafiláticas
* Inclui efeitos não desejados para os quais o papel exato do medicamento Fulvestrant Eugia não pode ser avaliado devido à doença subjacente.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Não Desejados de Medicamentos do Instituto Nacional de Farmácia e Medicamentos, Rua do Instituto Nacional de Farmácia e Medicamentos, 1400-038 Lisboa, telefone: +351 21 798 7000, fax: +351 21 798 7050, site: https://www.infarmed.pt/
Ao notificar efeitos não desejados, pode ajudar a obter mais informações sobre a segurança do medicamento.
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
5. Como conservar o medicamento Fulvestrant Eugia
O medicamento deve ser conservado em local seguro e fora do alcance das crianças.
Conservar no frigorífico (2°C – 8°C).
Não usar este medicamento após o prazo de validade impresso na caixa ou rótulo da seringa após: EXP. O prazo de validade é o último dia do mês indicado.
O profissional de saúde será responsável pela conservação, administração e eliminação adequadas deste medicamento. Este medicamento pode representar um perigo para o meio ambiente aquático.
Os medicamentos não devem ser jogados na canalização ou lixeiras domésticas. Deve perguntar ao farmacêutico como eliminar os medicamentos que já não são necessários. Este procedimento ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Fulvestrant Eugia
- A substância ativa do medicamento é o fulvestranto. Cada seringa pré-cheia de 5 mL (50 mg/mL) contém 250 mg de fulvestranto.
- Os outros componentes (excipientes) são: etanol (96%), álcool benzílico (E 1519), benzoato de benzilo e óleo de rícino purificado.
Como é o Fulvestrant Eugia e que conteúdo tem a embalagem
Solução injectável em seringa pré-cheia.
Líquido transparente, incolor a amarelo, viscoso, essencialmente livre de partículas visíveis.
O medicamento Fulvestrant Eugia, 250 mg, solução injectável em seringa pré-cheia, é embalado em um cilindro de 5 mL de vidro tipo I com um êmbolo fechado por uma tampa de borracha de bromobutilo com uma cobertura OVS. Uma agulha de segurança para injeções subcutâneas também está incluída para conexão com o cilindro para administração da solução de fulvestranto para injeção. O cilindro de vidro da seringa, juntamente com a agulha, é colocado em um suporte de plástico protetor com uma tampa transparente.
O medicamento Fulvestrant Eugia tem 6 apresentações: embalagem contendo 1 seringa pré-cheia de vidro, 2 seringas pré-cheias de vidro, 4 seringas pré-cheias de vidro, 5 seringas pré-cheias de vidro, 6 seringas pré-cheias de vidro e 10 seringas pré-cheias de vidro. As embalagens também incluem agulhas para administração do medicamento, com um sistema de segurança (BD Safety Glide).
Nem todos os tamanhos de embalagem precisam estar disponíveis.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização:
Eugia Pharma (Malta) Ltd.
Vault 14, level 2
Valletta Waterfront
Floriana, FRN 1914
Malta
e-mail: [email protected]
Fabricante/Importador:
APL Swift Services (Malta) Ltd.
HF26, Hal Far Industrial Estate, Hal Far
Birzebbugia, BBG 3000
Malta
Generis Farmacêutica S.A.
Rua João de Deus 19, Venda Nova
2700-487 Amadora
Portugal
Arrow Génériques
26 Avenue Tony Garnier
69007 Lyon
França
Este medicamento está autorizado para comercialização nos países membros da Área Económica Europeia sob as seguintes denominações:
Este medicamento está autorizado para comercialização nos seguintes países:
Bélgica:
Fulvestrant Eugia 250 mg oplossing voor injectie in voorgevulde spuit / solution injectable en seringue préremplie / Injektionslösung in einer Fertigspritze
França:
Fulvestrant Arrow 250 mg, solution injectable en seringue pré-remplie
Alemanha:
Fulvestrant Eugia 250 mg Injektionslösung in einer Fertigspritze
Itália:
Fulvestrant Eugia
Países Baixos:
Fulvestrant Eugia 250 mg, oplossing voor injectie in een voorgevulde spuit
Polónia:
Fulvestrant Eugia
Portugal:
Fulvestrant Eugia
Roménia:
Fulvestrant Eugia 250 mg soluție injectabilă în seringă preumplută
Espanha:
Fulvestrant Eugia 250 mg solución inyectable en jeringa precargada EFG
Data da última revisão do folheto:
----------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas a profissionais de saúde:
O medicamento Fulvestrant Eugia, 500 mg (2 x 250 mg/5 mL, solução injectável em seringa pré-cheia), deve ser administrado usando duas seringas pré-cheias, ver ponto 3.
Instruções de administração
Nota – Não deveesterilizar a agulha com sistema de proteção (BD Safety Glide Shielding Hypodermic Needle) antes de usá-la.
Ao administrar o medicamento e eliminar os resíduos, deve evitar o contato das mãos com a agulha.
Para cada uma das duas seringas:
- Retirar o cilindro de vidro da seringa do recipiente e verificar se não está danificado.
- Remover a embalagem externa da agulha com sistema de proteção (Safety Glide).
- As soluções para administração parenteral devem ser inspecionadas visualmente antes da administração para verificar a presença de partículas e alterações de cor.
- Segurar a seringa na parte estrangulada (C) e, com a outra mão, segurar a tampa (A) e inclinar suavemente para a frente e para trás até que a tampa se separe e possa ser removida, não girando (ver Figura 1).
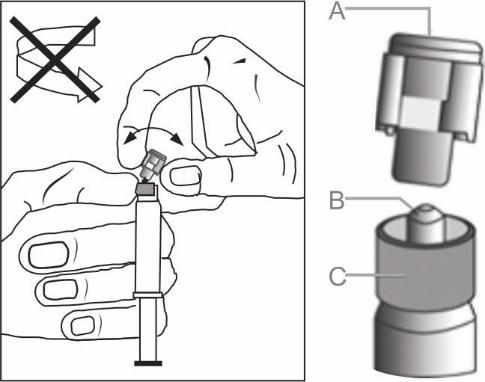
Figura 1
- Remover a tampa (A) para cima. Para manter a esterilidade, não tocar na ponta da seringa (B) (ver Figura 2).
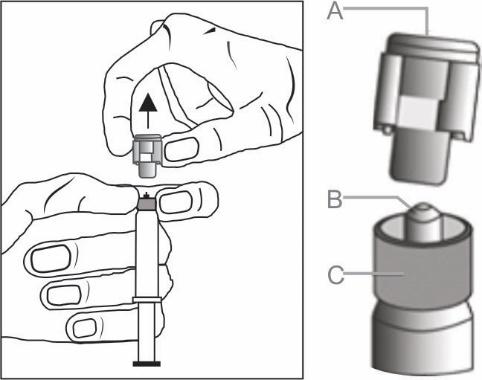
Figura 2
- Conectar a agulha com sistema de proteção à ponta Luer-Lok e apertar para fixar firmemente (ver figura 3).
- Verificar se a agulha está bloqueada na conexão Luer antes de passar para a posição vertical.
- Remover a cobertura da agulha para evitar danificar a ponta da agulha.
- Transportar a seringa carregada para o local de administração.
- Remover a tampa da agulha.
- Remover o excesso de ar da seringa.
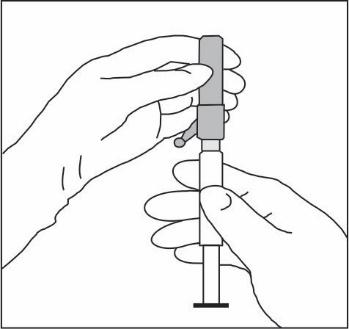
Figura 3
- Administrar o medicamento por via intramuscular, lentamente (1-2 minutos por injeção) no músculo da nádega (local na nádega). Para a conveniência da pessoa que administra, a ponta da agulha está no mesmo lado da agulha que o braço da alavanca do sistema de proteção da agulha (ver figura 4).
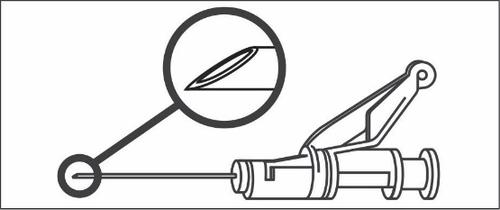
Figura 4
- Imediatamente após a administração do medicamento, deve ativar o sistema de proteção da agulha empurrando a alavanca para a frente (ver Figura 5).
- ATENÇÃO: Ativar longe de si e de outros. Ouça o clique e verifique visualmente que a ponta da agulha está completamente coberta.
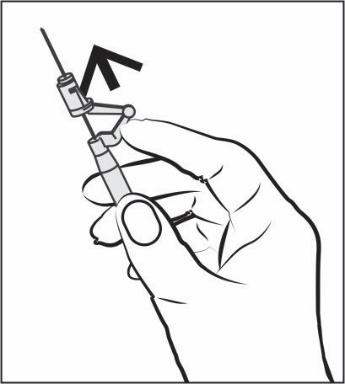
Figura 5
Eliminação de resíduos
As seringas pré-cheias são para uso único.
Este medicamento pode representar um perigo para o meio ambiente aquático. Todos os resíduos não utilizados do medicamento ou seus resíduos devem ser eliminados de acordo com as regulamentações locais (ver ponto 5.3 do RCM).
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorAPL Swift Services (Malta) Ltd. Arrow Generiques Generis Farmaceutica S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Fulvestrant EugiaForma farmacêutica: Solução, 250 mgSubstância ativa: fulvestrantNão requer receita médicaForma farmacêutica: Solução, 250 mg/ 5 mlSubstância ativa: fulvestrantRequer receita médicaForma farmacêutica: Solução, 250 mg/5 mlSubstância ativa: fulvestrantFabricante: Laboratorios Farmalán, S.A.Requer receita médica
Alternativas a Fulvestrant Eugia noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Fulvestrant Eugia em Espanha
Alternativa a Fulvestrant Eugia em Ukraine
Médicos online para Fulvestrant Eugia
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Fulvestrant Eugia – sujeita a avaliação médica e regras locais.












