
Fulvestrant Fresenius Kabi
Pergunte a um médico sobre a prescrição de Fulvestrant Fresenius Kabi

Como usar Fulvestrant Fresenius Kabi
Folheto informativo para o utilizador
Fulvestrant Fresenius Kabi, 250 mg/5 ml, solução injectável em seringa pré-cheia
Fulvestranto
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder reler se necessário.
- Em caso de dúvidas, deve consultar o médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode ser prejudicial a outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver secção 4.
Índice do folheto
- 1. O que é Fulvestrant Fresenius Kabi e para que é utilizado
- 2. Informações importantes antes de tomar Fulvestrant Fresenius Kabi
- 3. Como tomar Fulvestrant Fresenius Kabi
- 4. Efeitos não desejados
- 5. Como conservar Fulvestrant Fresenius Kabi
- 6. Conteúdo da embalagem e outras informações
1. O que é Fulvestrant Fresenius Kabi e para que é utilizado
Fulvestrant Fresenius Kabi contém a substância ativa fulvestranto, que pertence a uma classe de medicamentos que bloqueiam a ação dos receptores de estrogénio. Os estrogénios, hormonas sexuais femininas, podem por vezes influenciar o desenvolvimento do cancro da mama.
Fulvestrant Fresenius Kabi é utilizado:
- como medicamento único, no tratamento de mulheres pós-menopáusicas com um tipo específico de cancro da mama conhecido como cancro da mama com receptores de estrogénio, que é localmente avançado ou metastático ou
- em combinação com palbociclib no tratamento de mulheres com um tipo específico de cancro da mama conhecido como cancro da mama com receptores hormonais, sem expressão excessiva do receptor de crescimento epidérmico humano 2, que é localmente avançado ou metastático. As mulheres que ainda não atingiram a menopausa também receberão um medicamento conhecido como agonista do hormona liberador de hormona luteinizante (LHRH).
Quando Fulvestrant Fresenius Kabi é administrado em combinação com palbociclib, é importante também ler o folheto informativo do palbociclib. Em caso de dúvidas sobre palbociclib, deve consultar o médico assistente.
2. Informações importantes antes de tomar Fulvestrant Fresenius Kabi
Quando não tomar Fulvestrant Fresenius Kabi
- se o doente tiver alergia a fulvestranto ou a qualquer outro componente deste medicamento (listados na secção 6);
- se o doente estiver grávida ou a amamentar;
- se o doente tiver doença hepática grave.
Precauções e advertências
Deve informar o médico ou farmacêutico ou enfermeiro antes de tomar Fulvestrant Fresenius Kabi, se já teve algum dos seguintes problemas de saúde:
- doenças renais ou hepáticas;
- redução do número de plaquetas (que permitem a coagulação do sangue) ou distúrbios da coagulação;
- doença tromboembólica;
- osteoporose (problemas relacionados com a diminuição da densidade mineral óssea);
- dependência de álcool.
Crianças e jovens
Fulvestrant Fresenius Kabi não é recomendado para uso em crianças e jovens com menos de 18 anos.
Fulvestrant Fresenius Kabi e outros medicamentos
Deve dizer ao médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar.
Em particular, deve informar o médico se estiver a tomar medicamentos anticoagulantes (medicamentos que previnem a formação de coágulos sanguíneos).
Gravidez e amamentação
Fulvestrant Fresenius Kabi não deve ser tomado durante a gravidez. Se o doente puder engravidar, deve usar uma contracepção eficaz durante o tratamento com Fulvestrant Fresenius Kabi e durante 2 anos após a última dose.
Enquanto estiver a tomar Fulvestrant Fresenius Kabi, não deve amamentar.
Condução de veículos e utilização de máquinas
Não foi detectado que o fulvestranto afete a capacidade de conduzir veículos ou utilizar máquinas.
Se após a administração deste medicamento ocorrer sensação de fadiga, não deve conduzir veículos ou utilizar máquinas.
Fulvestrant Fresenius Kabi contém 500 mg de álcool (etanol) por injeção
, o que é equivalente a 100 mg/ml (10% v/v). A quantidade de álcool em cada injeção deste medicamento é equivalente a 13 ml de cerveja ou 5 ml de vinho.
A quantidade de álcool neste medicamento provavelmente não terá efeito nos adultos e jovens.
O álcool neste medicamento pode alterar a ação de outros medicamentos. Se estiver a tomar outros medicamentos, deve consultar o médico ou farmacêutico.
Se estiver grávida ou a amamentar, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Se for dependente de álcool, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Fulvestrant Fresenius Kabi contém 500 mg de álcool benzílico por injeção
, o que corresponde a 100 mg/ml.
O álcool benzílico pode causar reações alérgicas.
Fulvestrant Fresenius Kabi contém 750 mg de benzoato de benzoíla por injeção
, o que corresponde a 150 mg/ml.
3. Como tomar Fulvestrant Fresenius Kabi
Fulvestrant Fresenius Kabi é administrado por um médico ou enfermeiro. O medicamento será injectado lentamente por via intramuscular em duas injeções consecutivas de 5 ml, cada uma em um glúteo diferente.
A dose recomendada é de 500 mg de fulvestranto (duas injeções de 250 mg/5 ml), administradas uma vez por mês e uma dose adicional de 500 mg administrada 2 semanas após a primeira dose.
Em caso de dúvidas adicionais sobre a administração deste medicamento, deve consultar o médico, farmacêutico ou enfermeiro.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não ocorram em todos.
Efeitos não desejados graves
Em caso de ocorrência dos seguintes efeitos não desejados, deve contactar imediatamente o médico:
- reações de hipersensibilidade (alergia), incluindo inchaço da face, lábios, língua e (ou) garganta, que podem ser sintomas de reações anafiláticas;
- doença tromboembólica (aumento do risco de formação de coágulos venosos)*;
- hepatite;
- insuficiência hepática.
Se ocorrer algum dos seguintes efeitos não desejados, deve informar o médico, farmacêutico ou enfermeiro:
Efeitos não desejados muito frequentes(podem ocorrer em mais de 1 em 10 pessoas):
- sintomas no local da injeção, como dor e (ou) inflamação;
- alterações na atividade de enzimas hepáticos (em exames de sangue)*;
- náuseas;
- sensação de fraqueza, fadiga*;
- dor nas articulações e dores musculoesqueléticas;
- ondas de calor;
- erupções cutâneas;
- reações de hipersensibilidade (alergia), incluindo inchaço da face, lábios, língua e (ou) garganta.
Outros efeitos não desejados:
Efeitos não desejados frequentes(podem ocorrer em até 1 em 10 pessoas):
- dor de cabeça;
- vômitos, diarreia ou perda de apetite*;
- infecções do trato urinário;
- dor nas costas*;
- aumento da bilirrubina (pigmento produzido pelo fígado);
- doença tromboembólica (aumento do risco de formação de coágulos venosos)*;
- redução do número de plaquetas (trombocitopenia);
- sangramento vaginal;
- dor na parte inferior das costas que irradia para a perna de um lado do corpo (ciática);
- fraqueza súbita, formigamento ou perda de mobilidade na perna, especialmente de um lado do corpo, dificuldade súbita em caminhar ou manter o equilíbrio (neuropatia periférica).
Efeitos não desejados não muito frequentes(podem ocorrer em até 1 em 100 pessoas):
- corrimento vaginal espesso e branco e candidíase vaginal (infecção);
- hematoma e sangramento no local da injeção;
- aumento da atividade da gamma-glutamiltransferase, enzima hepático medido em exames de sangue;
- hepatite;
- insuficiência hepática;
- formigamento, fraqueza e dor;
- reações anafiláticas. * Inclui efeitos não desejados para os quais o efeito do fulvestranto não pode ser avaliado devido à doença subjacente.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Não Desejados de Medicamentos da Agência Nacional de Medicamentos e Produtos de Saúde.
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos não desejados permite reunir mais informações sobre a segurança do medicamento.
5. Como conservar Fulvestrant Fresenius Kabi
O medicamento deve ser conservado em local não visível e inacessível a crianças.
Não use este medicamento após o prazo de validade impresso na embalagem: EXP. O prazo de validade é o último dia do mês indicado.
Conservar e transportar a uma temperatura de 2°C - 8°C.
Deve limitar a conservação do medicamento a uma temperatura diferente de 2°C - 8°C. Deve evitar a conservação a uma temperatura superior a 30°C e não exceder o período de 28 dias com uma temperatura média de conservação abaixo de 25°C (mas acima do intervalo de 2°C - 8°C). Se o intervalo de temperatura for excedido, deve aplicar imediatamente as condições de conservação recomendadas (conservar e transportar em frigorífico a 2°C - 8°C). O excesso da temperatura de conservação pode ter um efeito cumulativo na qualidade do medicamento, e o período de 28 dias não pode ser excedido durante o prazo de validade do medicamento Fulvestrant Fresenius Kabi (ver secção 6.3). A exposição a uma temperatura abaixo de 2°C não danifica o medicamento, desde que não seja conservado a uma temperatura abaixo de -20°C.
Conservar a seringa pré-cheia na embalagem original para proteger da luz.
O pessoal médico é responsável pela conservação, uso e eliminação adequados do medicamento Fulvestrant Fresenius Kabi.
Este medicamento pode representar um perigo para o meio ambiente aquático. Os medicamentos não devem ser jogados na canalização ou nos contentores de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos de que já não precisa. Este procedimento ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém Fulvestrant Fresenius Kabi
- A substância ativa do medicamento é fulvestranto. Cada seringa pré-cheia (5 ml) contém 250 mg de fulvestranto.
- Os outros componentes são: etanol (96%), álcool benzílico, benzoato de benzoíla, óleo de rícino purificado.
Como é Fulvestrant Fresenius Kabi e que conteúdo tem a embalagem
Fulvestrant Fresenius Kabi é uma solução injectável transparente, incolor a amarela, viscosa em seringa pré-cheia de vidro incolor tipo I, com êmbolo de poliestireno com uma tampa de elastómero, com uma proteção na ponta em uma caixa de cartão, contendo 5 ml de solução de fulvestranto. Devem ser usadas 2 seringas pré-cheias para administrar a dose mensal recomendada de 500 mg.
Estão disponíveis 3 tamanhos de embalagens do medicamento Fulvestrant Fresenius Kabi, contendo 1, 2 ou 6 seringas pré-cheias. As embalagens também contêm, respectivamente, 1, 2 ou 6 agulhas para administração do medicamento com um sistema de proteção (BD SafetyGlide).
Nem todos os tamanhos de embalagens precisam estar disponíveis.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Fresenius Kabi Portugal, Unipessoal Lda.
Rua da Cêrca, 4050-015 Porto
Fabricante
Laboratorios Farmalán, S.A.
Calle La Vallina s/n, Edificio 2
Polígono Industrial Navatejera
24193, Villaquilambre, León
Espanha
Este medicamento está autorizado para comercialização nos Estados-Membros do Espaço Económico Europeu sob as seguintes designações:
| Áustria | Fulvestrant Fresenius Kabi 250 mg Injektionslösung in einer Fertigspritze |
| Bélgica | Fulvestrant Fresenius Kabi 250 mg oplossing voor injectie in een voorgevulde spuit, solution injectable en seringue préremplie , Injektionslösung in einer Fertigspritze |
| República Checa | Fulvestrant Fresenius Kabi |
| Dinamarca | Fulvestrant Fresenius Kabi |
| Finlândia | Fulvestrant Fresenius Kabi 250 mg injektioneste, liuos, esitäytetty ruisku |
| Alemanha | Fulvestrant Fresenius Kabi 250 mg Injektionslösung in einer Fertigspritze |
| Itália | Fulvestrant Fresenius Kabi |
| Países Baixos | Fulvestrant Fresenius Kabi 250 mg, oplossing voor injectie in een voorgevulde spuit |
| Noruega | Fulvestrant Fresenius Kabi |
| Polónia | Fulvestrant Fresenius Kabi |
| Portugal | Fulvestrant Fresenius Kabi |
| Eslovénia | Fulvestrant Fresenius Kabi 250 mg raztopina za injiciranje v napolnjeni injekcijski brizgi |
| Suécia | Fulvestrant Fresenius Kabi 250 mg injektionsvätska, lösning i förfylld spruta |
| Eslováquia | Fulvestrant Fresenius Kabi 250 mg |
| Reino Unido | Fulvestrant Fresenius Kabi 250 mg solution for injection in pre-filled syringe |
Data da última revisão do folheto: ---------------------------------------------------------------------
Informações destinadas apenas a profissionais de saúde:
Fulvestrant Fresenius Kabi 500 mg (2 x 250 mg/5 ml solução injectável) deve ser administrado usando 2 seringas pré-cheias, ver secção 3.
Instruções de administração
Atenção – não deve esterilizar a agulha com sistema de proteção (BD SafetyGlide Shielding Hypodermic Needle) antes de usá-la. Ao usar o medicamento e eliminar os resíduos, deve evitar o contacto das mãos com a agulha.
Aplica-se a ambas as seringas:
- Deve remover o frasco de vidro do contentor e verificar se não está danificado.
- Abrir o pacote exterior da agulha com sistema de proteção (SafetyGlide).
- Antes da administração de soluções parenterais, deve realizar uma inspeção visual para detectar a presença de partículas sólidas e alterações da cor.
- Segurar a seringa na vertical na parte estrangulada (C). Com a outra mão, segurar a tampa (A) e inclinar para a frente e girar a tampa de plástico no sentido contrário ao dos ponteiros do relógio (ver Figura 1).
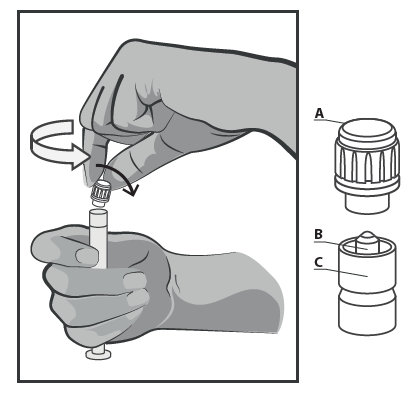
Figura 1
- Remover a tampa (A) na posição vertical para cima. Para manter a esterilidade, não tocar na ponta da seringa (B) (ver Figura 2).
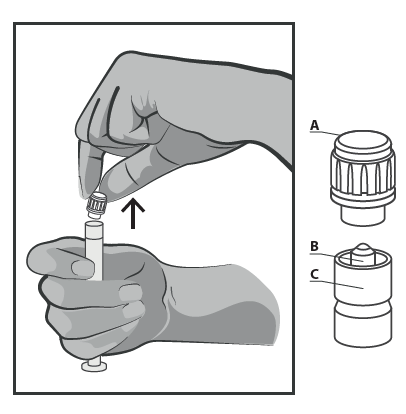
Figura 2
- Acoplar a agulha com sistema de proteção à ponta Luer-Lock e apertar para fixar firmemente (ver Figura 3).
- Verificar se a agulha está conectada à ponta Luer antes de passar para a posição vertical.
- Ao apertar a agulha, deve proceder de forma a não danificar a ponta afiada.
- Aproximar a agulha com a tampa ao local da injeção.
- Remover a tampa da agulha.
- Remover o excesso de ar da seringa.
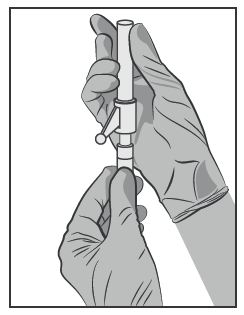
Figura 3
- O medicamento deve ser administrado por via intramuscular, lentamente (1-2 minutos por injeção), no músculo do glúteo (local no glúteo). Para a conveniência da pessoa que administra, a corte da agulha está no mesmo lado da agulha que a alavanca do sistema de proteção da agulha (ver Figura 4).
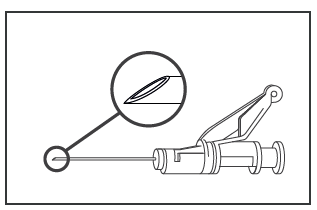
Figura 4
- Imediatamente após a injeção, deve ativar o sistema de proteção da agulha empurrando a alavanca para a frente (ver Figura 5).
ATENÇÃO: Deve proceder de forma a garantir a segurança para si e para os outros. Deve ouvir o clique e verificar visualmente se a ponta da agulha está completamente oculta.
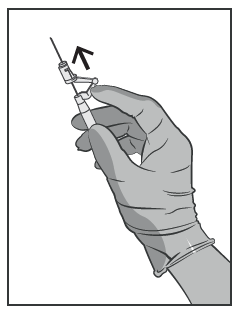
Figura 5
Eliminação dos resíduos
As seringas pré-cheias são para uso único.
Este medicamento pode representar um perigo para o meio ambiente aquático. Todos os resíduos não utilizados do medicamento ou seus resíduos devem ser eliminados de acordo com as regulamentações locais.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorLaboratorios Farmalán, S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Fulvestrant Fresenius KabiForma farmacêutica: Solução, 250 mgSubstância ativa: fulvestrantNão requer receita médicaForma farmacêutica: Solução, 250 mgSubstância ativa: fulvestrantRequer receita médicaForma farmacêutica: Solução, 250 mg/ 5 mlSubstância ativa: fulvestrantRequer receita médica
Alternativas a Fulvestrant Fresenius Kabi noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Fulvestrant Fresenius Kabi em Spain
Alternativa a Fulvestrant Fresenius Kabi em Ukraine
Médicos online para Fulvestrant Fresenius Kabi
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Fulvestrant Fresenius Kabi – sujeita a avaliação médica e regras locais.












