CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO

Como usar CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO
Introdução
Prospecto: informação para o paciente
Cabazitaxel Zentiva 60 mg concentrado e dissolvente para solução para perfusão EFG
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Cabazitaxel Zentiva e para que é utilizado
- O que precisa saber antes de que lhe administrem Cabazitaxel Zentiva
- Como usar Cabazitaxel Zentiva
- Possíveis efeitos adversos
- Conservação de Cabazitaxel Zentiva
- Conteúdo do envase e informações adicionais
1. O que é Cabazitaxel Zentiva e para que é utilizado
Cabazitaxel Zentiva contém o princípio ativo cabazitaxel que pertence a um grupo de medicamentos denominado “taxanos”, utilizados para tratar cancros.
Cabazitaxel é utilizado para o tratamento do cancro da próstata que progrediu após ter recebido outra quimioterapia. Actua detendo o crescimento das células e sua multiplicação.
Como parte do seu tratamento, tomará também todos os dias um corticosteroide (prednisona ou prednisolona), por via oral. Peça informações ao seu médico sobre este outro medicamento.
2. O que precisa saber antes de começar a usar Cabazitaxel Zentiva
Não use Cabazitaxel Zentiva:
- se é alérgico (hipersensível) a cabazitaxel, a outros taxanos, ao polissorbat 80 ou a algum dos outros componentes deste medicamento (incluídos na secção 6),
- se o número dos seus glóbulos brancos é muito baixo (número de neutrófilos menor ou igual a 1.500/mm3),
- se tem problemas graves de fígado,
- se recentemente foi ou vai ser vacinado contra a febre amarela.
Não deve receber Cabazitaxel Zentiva se lhe suceder alguma das circunstâncias anteriores. Se não tiver certeza, consulte o seu médico antes de receber Cabazitaxel Zentiva.
Advertências e precauções
Antes de iniciar o tratamento com Cabazitaxel Zentiva, farão análises de sangue para comprovar que tem células sanguíneas suficientes e que os seus rins e fígado funcionam adequadamente para receber Cabazitaxel Zentiva.
Informa ao seu médico imediatamente se:
- tem febre. Durante o tratamento com Cabazitaxel Zentiva é mais provável que se reduza o número dos seus glóbulos brancos. O médico controlará o seu sangue e o seu estado geral para detectar sinais de infecções. Podia administrar-lhe outros medicamentos para manter o número das suas células sanguíneas. As pessoas com recuentos celulares baixos podem desenvolver infecções que podem pôr em perigo a vida. O primeiro sinal de infecção podia ser febre, por isso se tiver febre, informa ao seu médico imediatamente.
- alguma vez teve alguma alergia. Durante o tratamento com Cabazitaxel Zentiva podem produzir-se reações alérgicas graves.
- tem diarreia grave ou duradoura, sente-se mal (náuseas) ou está mal (vómitos). Qualquer destas situações pode produzir desidratação grave. O seu médico teria que pôr-lhe um tratamento.
- tem sensação de insensibilidade, formigueiro, ardor ou diminuição das sensações em mãos e pés.
- tem algum problema de sangramento no intestino ou tem alterações na cor das suas fezes ou dor de estômago. Se o sangramento ou a dor for grave, o seu médico interromperá o tratamento com Cabazitaxel Zentiva. Isto é porque Cabazitaxel Zentiva podia aumentar o risco de sangramento ou desenvolvimento de perfurações na parede intestinal.
- tem problemas de rim.
- tem pele e olhos amarelentos, urina escura, náuseas intensas (sensação de malestar) ou vómitos, pois podem ser sinais ou sintomas de problemas hepáticos.
- nota que o volume da sua urina aumenta ou diminui significativamente.
- tem sangue na sua urina.
Se lhe suceder alguma das circunstâncias anteriores, informa ao seu médico imediatamente. O seu médico podia reduzir a dose de Cabazitaxel Zentiva ou interromper o tratamento.
Uso de Cabazitaxel Zentivacom outros medicamentos
- Informa ao seu médico, farmacêutico ou enfermeiro se está utilizando ou utilizou recentemente outros medicamentos, mesmo os adquiridos sem receita. Isto é devido a que alguns medicamentos podem afetar a eficácia de Cabazitaxel Zentiva ou Cabazitaxel Zentiva pode afetar a eficácia de outros medicamentos. Estes medicamentos incluem os seguintes:
- cetoconazol, rifampicina (para infecções);
- carbamazepina, fenobarbital ou fenitoína (para convulsões);
- erva de São João ou hipérico (Hypericum perforatum) (planta medicinal utilizada para tratar a depressão e outros problemas);
- estatinas (tais como simvastatina, lovastatina, atorvastatina, rosuvastatina, ou pravastatina) (para reduzir o colesterol no seu sangue);
- valsartano (para a hipertensão);
- repaglinida (para a diabetes).
Enquanto estiver em tratamento com Cabazitaxel Zentiva, consulte com o seu médico antes de se vacinar.
Gravidez, lactação e fertilidade
Cabazitaxel Zentiva não é indicado para o uso em mulheres.
Use preservativos nas suas relações sexuais se a sua parceira está ou podia estar grávida. Cabazitaxel pode estar presente no seu sêmen e afetar o feto. Recomenda-se não gerar um filho durante e até 4 meses após o tratamento e solicitar informações sobre a conservação do sêmen antes do tratamento, pois Cabazitaxel Zentiva podia alterar a fertilidade masculina.
Condução e uso de máquinas
Durante o tratamento com este medicamento podia sentir-se cansado ou mareado. Se isto suceder, não conduza nem use ferramentas ou máquinas até que se sinta melhor.
Cabazitaxel Zentivacontém etanol (álcool)
Este medicamento contém 709,8 mg de álcool (etanol) em cada frasco de dissolvente. A quantidade na dose deste medicamento é equivalente a 14 ml de cerveja ou 6 ml de vinho. A pequena quantidade de álcool que contém este medicamento não produz qualquer efeito perceptível. Se tem adicção ao álcool, tem uma doença hepática ou epilepsia, consulte o seu médico ou farmacêutico antes de tomar este medicamento.
3. Como usar Cabazitaxel Zentiva
Instruções de uso
Antes de receber cabazitaxel, administrar-lhe-ão medicamentos antialérgicos para reduzir o risco de reações alérgicas.
- Cabazitaxel será administrado por um médico ou um enfermeiro.
- Cabazitaxel deve ser preparado (diluído) antes de ser administrado. Com este prospecto é fornecida informação prática para a manipulação e administração de cabazitaxel para médicos, enfermeiros e farmacêuticos.
- Cabazitaxel será administrado no hospital mediante um gotejador (perfusão) numa das suas veias (via intravenosa) durante aproximadamente 1 hora.
- Como parte do seu tratamento, tomará também um medicamento corticosteroide (prednisona ou prednisolona) por via oral todos os dias.
Quanto e com que frequência se administra
- A dose habitual depende da sua área de superfície corporal. O seu médico calculará a sua área de superfície corporal em metros quadrados (m2) e decidirá a dose que deve receber.
- Normalmente receberá uma perfusão cada 3 semanas.
Em caso de sobredose ou ingestão acidental, consulte o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone: 91 562 04 20, indicando o medicamento e a quantidade ingerida.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Possíveis efeitos adversos
Como todos os medicamentos, Cabazitaxel Zentiva pode produzir efeitos adversos, embora nem todas as pessoas os sofram. O seu médico comentará isto consigo e explicará os riscos e os benefícios potenciais do seu tratamento.
Dirija-se imediatamente ao médico se notar algum dos seguintes efeitos adversos:
- febre (temperatura alta). Isto é frequente (podia afetar até 1 de cada 10 pessoas).
- perda grave de fluidos corporais (desidratação). Isto é frequente (podia afetar até 1 de cada 10 pessoas). Isto pode ocorrer se tiver diarreia grave ou duradoura, ou febre, ou se tem estado a vomitar.
- dor de estômago grave ou dor de estômago que não se resolve. Isto pode suceder se tiver uma perfuração no estômago, esófago, intestino (perfuração gastrointestinal). Isto pode causar a morte.
Se lhe suceder alguma das circunstâncias anteriores, comunique ao seu médico imediatamente.
Outros efeitos adversos incluem:
Muito frequentes (podem afetar mais de 1 de cada 10 pessoas):
- redução do número de células sanguíneas vermelhas (anemia), ou brancas (que são importantes para combater as infecções)
- redução do número de plaquetas (o que resulta num aumento do risco de ter hemorragias)
- perda de apetite (anorexia)
- molestias de estômago, incluindo náuseas, vómitos, diarreia ou constipação
- dor de costas
- sangue na urina
- cansaço, fraqueza ou falta de energia
Frequentes (podem afetar até 1 de cada 10 pessoas):
- alteração do gosto
- respiração entrecortada
- tosse
- dor abdominal
- perda de cabelo a curto prazo (na maioria dos casos o cabelo volta a crescer com normalidade)
- dor das articulações
- infecção do trato urinário
- escassez de glóbulos brancos associada com febre e infecções
- sensação de insensibilidade, formigueiro, ardor ou diminuição das sensações em mãos e pés
- mareio
- dor de cabeça
- aumento ou diminuição da tensão arterial
- malestar de estômago, ardor de estômago ou arrotos
- dor de estômago
- hemorroides
- espasmos musculares
- urinar com frequência ou com dor
- incontinência urinária
- problemas ou alteração dos rins
- úlceras na boca ou nos lábios
- infecções ou risco de infecções
- nível de açúcar no sangue elevado
- insónia
- confusão mental
- sensação de ansiedade
- sensação rara ou perda de sensação ou dor em mãos e pés
- problemas de equilíbrio
- batimentos rápidos ou irregulares do coração
- coágulos de sangue nas pernas ou no pulmão
- sensação de sufocação na pele
- dor de boca ou garganta
- hemorragia retal
- molestias, distúrbios, fraqueza ou dores musculares
- inflamação de pés ou pernas
- arrepios.
- distúrbios nas unhas (mudança de cor nas suas unhas; as unhas se podem desprender).
Pouco frequentes (podem afetar até 1 de cada 100 pessoas):
- nível de potássio no sangue baixo
- zumbido nos ouvidos
- sensação de calor na pele
- inflamação da bexiga, que pode ocorrer quando a sua bexiga esteve previamente exposta a radioterapia (cistite devido a fenómenos de recorde de radiação).
Frequência não conhecida (não pode ser estimada a partir dos dados disponíveis):
- doença pulmonar intersticial (inflamação dos pulmões causando tosse e dificuldade para respirar).
Comunicação de efeitos adversos:
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Cabazitaxel Zentiva
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de caducidade que aparece no envase e na etiqueta dos frascos após CAD. A data de caducidade é o último dia do mês que se indica.
Não refrigerar.
Na secção “Informação prática para médicos ou profissionais de saúde sobre a preparação, administração e manipulação de Cabazitaxel Zentiva” é incluída informação sobre a conservação e o tempo de uso de Cabazitaxel Zentiva, uma vez que se tem diluído e está pronto para usar.
A eliminação do medicamento não utilizado será realizada de acordo com a normativa local. Estas medidas ajudarão a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Cabazitaxel Zentiva
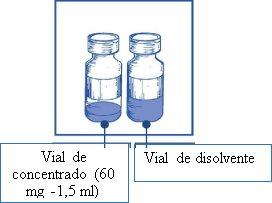
O princípio ativo é cabazitaxel. Um ml de concentrado contém 40 mg de cabazitaxel. Um frasco de concentrado contém 60 mg de cabazitaxel.
Os demais componentes são: polissorbato 80, ácido cítrico e etanol absoluto no concentrado, e etanol 96% e água para preparações injetáveis no dissolvente (ver seção 2 “Cabazitaxel Zentiva contém etanol (álcool)”).
Nota: tanto o frasco do concentrado de Cabazitaxel Zentiva 60 mg/1,5 ml (volume de enchimento: 1,83 ml) como o do frasco de dissolvente (volume de enchimento: 5,67 ml) contêm um excesso de enchimento para compensar a perda de líquido durante a preparação. Este excesso de enchimento assegura que após a diluição com o conteúdo completo do dissolvente fornecido, haja uma solução contendo 10 mg/ml de cabazitaxel para injeção.
Aspecto do produto e conteúdo do envase
Cabazitaxel Zentiva é um concentrado e dissolvente para solução para perfusão (concentrado estéril).
O concentrado é uma solução viscosa transparente entre incolor e amarela pálida.
O dissolvente é uma solução transparente e incolora.
Um envase de Cabazitaxel Zentiva contém:
Concentrado: 1,5 ml de concentrado em um frasco de 15 ml de vidro tubular transparente (tipo I), fechado com uma tampa de elastômero de borracha de cor cinza, selado com um selo de alumínio dobrável com um disco de plástico de cor amarela. Cada frasco contém 60 mg de cabazitaxel em 1,5 ml (volume nominal).
Dissolvente: 5,67 ml em um frasco de vidro de 15 ml transparente (tipo I), fechado com uma tampa de elastômero de borracha de cor cinza, selado com um selo de alumínio dobrável com um disco de plástico de cor azul escuro. Cada frasco contém 5,67 ml (volume nominal).
Título da autorização de comercialização e responsável pela fabricação
Título da autorização de comercialização
Zentiva, k.s.,
U kabelovny 130,
Praga 10 – Dolní Mecholupy,
102 37 República Tcheca
Responsável pela fabricação
Mias Pharma Limited
Suite 2, Stafford House, Strand Road
Portmarnock, Co. Dublin
Irlanda
Tillomed Malta Limited,
Malta Life Sciences
Park, LS2.01.06
Industrial Estate,
San Gwann, SGN 3000,
Malta
Podemsolicitar mais informações sobre estemedicamentodirigindo-se ao representante local do título da autorização de comercialização:
Zentiva Spain S.L.U.
Avenida de Europa, 19, Edificio 3, Planta 1.
28224 Pozuelo de Alarcón, Madrid
Espanha
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu e no Reino Unido (Irlanda do Norte) com os seguintes nomes:
País | Nome do produto |
Alemanha | Cabazitaxel Tillomed 60 mg Concentrado e Dissolvente para Solução para Perfusão |
Espanha | Cabazitaxel Zentiva 60 mg concentrado e dissolvente para solução para perfusão EFG |
Itália | Cabazitaxel Tillomed |
França | Cabazitaxel Tillomed 60 mg solução para diluir e dissolvente para solução para perfusão |
Data da última revisão deste prospecto:julho 2023
A informação detalhada deste medicamento está disponível no site da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
<------------------------------------------------------------------------------------------------------>
A seguinte informação é destinada apenas a profissionais de saúde.
INFORMAÇÃO PRÁTICA PARA MÉDICOS OU PROFISSIONAIS DE SAÚDE SOBRE A PREPARAÇÃO, ADMINISTRAÇÃO E MANIPULAÇÃO DE Cabazitaxel Zentiva60 mg CONCENTRADO E DISSOLVENTE PARA SOLUÇÃO PARA PERFUSÃO
Esta informação complementa as seções 3 e 5 para o usuário.
É importante que leia o conteúdo completo deste procedimento antes de preparar a solução para perfusão.
Incompatibilidades
Este medicamento não deve ser misturado com outros medicamentos, exceto os utilizados para as diluições.
Período de validade e precauções especiais de conservação
Para o envase de Cabazitaxel Zentiva 60 mg concentrado e dissolvente
Não refrigerar.
Após a abertura do frasco
Os frascos de concentrado e dissolvente devem ser utilizados imediatamente. Se não forem utilizados imediatamente, o tempo e as condições de conservação são responsabilidade do usuário. Desde um ponto de vista microbiológico, o processo de diluição em duas etapas deve ser realizado em condições controladas e assépticas (ver a seguir “Precauções de preparação e administração”).
Após a diluição inicialde Cabazitaxel Zentiva 60 mg concentrado com o conteúdo completodo frasco de dissolvente, demonstrou-se a estabilidade química e física em uso durante 1 hora, a temperatura ambiente (15°C - 30°C).
Após a diluição final na bolsa/botija de perfusão
Demonstrou-se a estabilidade química e física da solução de perfusão durante 8 horas a temperatura ambiente (15°C – 30°C) incluindo 1 hora de tempo de perfusão e durante 48 horas na geladeira incluindo 1 hora de tempo de perfusão.
Desde um ponto de vista microbiológico, a solução de perfusão deve ser utilizada imediatamente. Se não for utilizada imediatamente, os tempos e as condições de conservação são responsabilidade do usuário e normalmente não devem ser mais de 24 horas a 2°C - 8°C, a menos que a diluição tenha sido realizada em condições assépticas controladas e validadas.
Precauções de preparação e administração
Assim como outros agentes antineoplásicos, deve-se agir com precaução durante a preparação e administração das soluções de cabazitaxel, tendo em conta o uso de dispositivos de segurança, equipamento de proteção individual (por exemplo, luvas) e procedimentos de preparação.
Se em qualquer uma das etapas de preparação, cabazitaxel entrar em contato com a pele, lavar imediatamente e minuciosamente com água e sabão. Se entrar em contato com membranas mucosas, lavar imediatamente e minuciosamente com água.
Cabazitaxel só deve ser preparado e administrado por pessoal treinado no manejo de agentes citotóxicos. As trabalhadoras grávidas não devem manipulá-lo.
Always diluir o concentrado para solução para perfusão com o dissolvente completo que se fornece antes de adicioná-lo às soluções de perfusão.
Etapas da preparação
Leia atentamente TODAesta seção antes de misturar e diluir. Cabazitaxel Zentiva requer DUASdiluições antes da administração. Siga as instruções de preparação que se fornecem a seguir.
Nota: tanto o frasco do concentrado de Cabazitaxel Zentiva 60 mg/1,5 ml (volume de enchimento: 1,83 ml) como o do frasco de dissolvente (volume de enchimento: 5,67 ml) contêm um excesso de enchimento para compensar a perda de líquido durante a preparação. Este excesso de enchimento assegura que após a diluição com o conteúdo COMPLETOdo dissolvente fornecido, haja uma solução contendo 10 mg/ml de cabazitaxel.
Para preparar a solução para perfusão, o seguinte processo de diluição deve ser realizado em duas etapas de forma asséptica.
Etapa 1: diluição inicial do concentrado de solução para perfusão com o dissolvente fornecido.
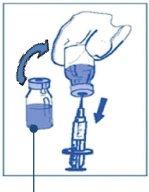
Etapa 1.1 Inspeccionar o frasco de concentrado e o dissolvente fornecido. A solução de concentrado e de dissolvente devem ser transparentes |
|
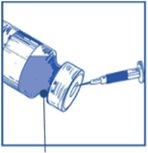
Etapa 1.2 Utilizando uma seringa provida de uma agulha fixa, extrair de forma asséptica o conteúdo completodo dissolvente fornecido invertendo parcialmente o frasco. |
|
| |
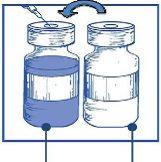
Etapa 1.3 Injetar o conteúdo completono correspondente frasco de concentrado. Para limitar todo o possível a formação de espuma ao injetar o dissolvente, dirigir a agulha para a parede interior do frasco de solução de concentrado e injetar lentamente. Uma vez reconstituído, a solução resultante contém 10 mg/ml de cabazitaxel. |
|
Etapa 1.4 Sacar a seringa e a agulha e misturar manual e suavemente, mediante inversões repetidas, até que se obtenha uma solução transparente e homogênea. Podem ser necessários uns 45 segundos. |
|
| |
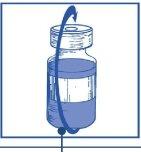
Etapa 1.5 Deixar repousar a solução durante aproximadamente 5 minutos e a seguir verificar que a solução é homogênea e transparente. É normal que persista a espuma passado este tempo. |
|
Esta mistura concentrado-dissolvente resultante contém 10 mg/ml de cabazitaxel (pelo menos 6 ml de volume liberado). A segunda diluição deve ser realizada imediatamente (antes de 1 hora) como se detalha na Etapa 2.
Pode ser necessário mais de um frasco de mistura concentrado-dissolvente para administrar a dosagem prescrita.
Etapa 2: segunda diluição (final) para perfusão
Etapa 2.1 De forma asséptica extrair a quantidade necessária de mistura concentrado-dissolvente (10 mg/ml de cabazitaxel), com uma seringa graduada provida de uma agulha fixa. Como exemplo, uma dosagem de 45 mg de Cabazitaxel Zentiva requereria 4,5 ml da mistura de concentrado-dissolvente preparada na Etapa 1. Como pode seguir havendo espuma na parede do frasco desta solução, após a preparação descrita na Etapa 1, é preferível situar a agulha da seringa na metade do conteúdo durante a extração. |
|
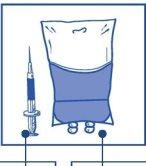
Etapa 2.2 Injetar em um envase estéril sem PVC de solução de glicose a 5% ou solução de cloreto de sódio 9 mg/ml (0,9%) para perfusão. A concentração da solução para perfusão deve estar entre 0,10 mg/ml e 0,26 mg/ml. |
|
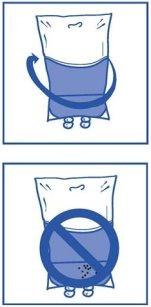
Etapa 2.3 Sacar a seringa e misturar o conteúdo da bolsa ou botija de perfusão manualmente, mediante movimento de balanço. Etapa 2.4 Assim como todos os produtos parenterais, a solução de perfusão resultante se deve inspecionar visualmente antes de usá-la. Como a solução de perfusão está sobressaturada, pode cristalizar com o tempo. Neste caso, não se deve utilizar a solução e deve ser eliminada. |
|
A solução para perfusão deve ser utilizada imediatamente. No entanto, o tempo de conservação em uso pode ser mais longo sob as condições específicas mencionadas na seção Período de validade e precauções especiais de conservação.
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele, será realizada de acordo com a normativa local.
Método de administração
Cabazitaxel Zentiva é administrado em perfusão durante 1 hora.
Recomenda-se o uso de um filtro em linha de 0,22 micrómetros de tamanho de poro nominal (também denominado 0,2 micrómetros) durante a administração.
Não devem ser utilizados envases de perfusão de PVC ou conjuntos de perfusão de poliuretano para a preparação e administração da solução para perfusão.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃOForma farmacêutica: PERFURAÇÃO INJETÁVEL, 20 mg/mlSubstância ativa: cabazitaxelFabricante: Accord Healthcare S.L.U.Requer receita médicaForma farmacêutica: PERFURAÇÃO INJETÁVEL, 20 mgSubstância ativa: cabazitaxelFabricante: Eugia Pharma (Malta) LimitedRequer receita médicaForma farmacêutica: PERFURAÇÃO INJETÁVEL, 60 mgSubstância ativa: cabazitaxelFabricante: Reddy Pharma Iberia S.A.Requer receita médica
Alternativas a CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO em Polónia
Alternativa a CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO em Ukraine
Médicos online para CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de CABAZITAXEL ZENTIVA 60 mg CONCENTRADO E SOLVENTE PARA SOLUÇÃO PARA PERFUSÃO – sujeita a avaliação médica e regras locais.