

Fulvestrant Sandoz

Pergunte a um médico sobre a prescrição de Fulvestrant Sandoz

Como usar Fulvestrant Sandoz
Folheto informativo para o doente:
Fulvestrant Sandoz, 250 mg/5 ml, solução para injeção em seringa pré-cheia
Fulvestranto
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o seu médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é Fulvestrant Sandoz e para que é utilizado
- 2. Informações importantes antes de tomar Fulvestrant Sandoz
- 3. Como tomar Fulvestrant Sandoz
- 4. Efeitos não desejados
- 5. Como conservar Fulvestrant Sandoz
- 6. Conteúdo da embalagem e outras informações
1 O que é Fulvestrant Sandoz e para que é utilizado
Fulvestrant Sandoz contém a substância ativa fulvestranto, que pertence a uma classe de medicamentos que bloqueiam a ação dos receptores de estrogénio.
Os estrogénios, hormonas sexuais femininas, podem contribuir para o desenvolvimento de cancro da mama em alguns casos.
Fulvestrant Sandoz é utilizado:
- como medicamento único no tratamento de mulheres na pós-menopausa com um tipo específico de cancro da mama, conhecido como cancro da mama com receptores de estrogénio, que é localmente avançado ou metastático,
- em combinação com palbociclib no tratamento de mulheres com um tipo específico de cancro da mama, conhecido como cancro da mama com receptores hormonais, sem superexpressão do receptor de crescimento epidérmico humano 2, que é localmente avançado ou metastático. As mulheres na pré-menopausa também receberão um medicamento conhecido como agonista do hormona liberador de hormona luteinizante (LHRH).
Quando o medicamento Fulvestrant Sandoz for administrado com palbociclib, é importante ler também o folheto informativo do medicamento que contém palbociclib. Em caso de dúvidas sobre palbociclib, deve consultar o seu médico.
2. Informações importantes antes de tomar Fulvestrant Sandoz
Quando não tomar Fulvestrant Sandoz
se o doente tiver alergia a fulvestranto ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6);
se o doente estiver grávida ou a amamentar;
se o doente tiver doença hepática grave.
Precauções e advertências
Antes de tomar Fulvestrant Sandoz, deve discutir com o seu médico, farmacêutico ou enfermeiro se algum dos seguintes problemas de saúde o afeta:
doenças renais ou hepáticas;
baixa contagem de plaquetas (envolvidas no processo de coagulação) ou distúrbios de sangramento;
história de doença tromboembólica;
osteoporose (densidade óssea reduzida);
doença alcoólica.
Crianças e adolescentes
Fulvestrant Sandoz não é destinado a ser utilizado em crianças e adolescentes com menos de 18 anos.
Fulvestrant Sandoz e outros medicamentos
Deve informar o seu médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar.
Em particular, deve informar o seu médico sobre a utilização de medicamentos anticoagulantes (medicamentos que previnem a formação de coágulos sanguíneos).
Gravidez e amamentação
Se uma mulher estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planeiar ter um filho, deve consultar o seu médico antes de tomar este medicamento.
Fulvestrant Sandoz não deve ser utilizado durante a gravidez. As mulheres em idade fértil devem utilizar métodos anticoncecionais eficazes durante o tratamento e durante 2 anos após a última dose.
Durante a utilização de Fulvestrant Sandoz, não se deve amamentar.
Condução de veículos e utilização de máquinas
O efeito de Fulvestrant Sandoz na capacidade de conduzir veículos ou utilizar máquinas não é esperado. No entanto, se o tratamento causar fadiga, o doente não deve realizar essas atividades.
Fulvestrant Sandoz contém etanol, álcool benzílico e benzoato de benzoíla
Este medicamento contém 1000 mg de etanol (96%) por dose, o que é equivalente a 100 mg/ml (10% m/m). A quantidade de etanol nesta dose é equivalente a menos de 24 ml de cerveja ou 10 ml de vinho. A pequena quantidade de etanol neste medicamento não terá efeitos notáveis.
Este medicamento contém 1000 mg de álcool benzílico por dose, o que é equivalente a 100 mg/ml.
O álcool benzílico pode causar reações alérgicas.
A administração de álcool benzílico a crianças pequenas está associada a um risco de efeitos não desejados graves, incluindo distúrbios respiratórios (síndrome de "gasping").
Não administrar a recém-nascidos (até 4 semanas de vida) sem recomendação médica.
Não administrar a crianças pequenas (com menos de 3 anos) por mais de uma semana sem recomendação médica ou farmacêutica.
Os doentes com doenças hepáticas ou renais devem consultar o seu médico antes de tomar o medicamento, pois uma grande quantidade de álcool benzílico pode acumular-se no seu organismo e causar efeitos não desejados (acidose metabólica).
Este medicamento contém 1500 mg de benzoato de benzoíla por dose, o que é equivalente a 150 mg/ml.
O benzoato de benzoíla pode aumentar o risco de icterícia (amarelamento da pele e brancos dos olhos) em recém-nascidos (até 4 semanas de vida).
3. Como tomar Fulvestrant Sandoz
Este medicamento deve ser sempre utilizado de acordo com as recomendações do seu médico ou farmacêutico. Em caso de dúvidas, deve consultar o seu médico ou farmacêutico.
A dose recomendada de fulvestranto é de 500 mg (duas injeções de 250 mg), administradas uma vez por mês, e uma dose adicional de 500 mg administrada 2 semanas após a primeira dose.
Fulvestrant Sandoz é administrado por um médico ou enfermeiro por injeção lenta intramuscular, uma injeção em cada nádega.
Em caso de dúvidas adicionais sobre a utilização deste medicamento, deve consultar o seu médico, farmacêutico ou enfermeiro.
4. Efeitos não desejados
Como qualquer medicamento, Fulvestrant Sandoz pode causar efeitos não desejados, embora não todos os doentes os experimentem.
Em caso de ocorrência de algum dos seguintes efeitos não desejados, pode ser necessária assistência médica imediata:
reações alérgicas (hipersensibilidade), incluindo inchaço facial, labial, lingual e (ou) faríngeo, que podem ser sintomas de reações anafiláticas
embolia com trombose (risco aumentado de formação de coágulos sanguíneos)*
hepatite
insuficiência hepática
Deve informar o seu médico, farmacêutico ou enfermeiro sobre a ocorrência de algum dos seguintes efeitos não desejados:
Efeitos não desejados muito frequentes(podem ocorrer em mais de 1 em 10 doentes)
reação no local da injeção, como dor e (ou) inflamação;
atividade anormal das enzimas hepáticas (detectada em análises sanguíneas)*
náuseas
fraqueza, fadiga*
dor articular e dor óssea
ondas de calor
erupções cutâneas
reações alérgicas (hipersensibilidade), incluindo inchaço facial, labial, lingual e (ou) faríngeo
Todos os outros efeitos não desejados
Efeitos não desejados frequentes(podem ocorrer em menos de 1 em 10 doentes)
dor de cabeça
vómitos, diarreia ou perda de apetite*
infecções do trato urinário
dor nas costas*
aumento da bilirrubina (pigmento da bile produzido no fígado)
embolia com trombose (risco aumentado de formação de coágulos sanguíneos)*
plaquetopenia (baixa contagem de plaquetas)
sangramento vaginal
dor na parte inferior das costas, irradiando para uma perna (ciática)
fraqueza súbita, entorpecimento, formigamento ou perda de mobilidade em uma perna (especialmente de um lado do corpo), dificuldade súbita em caminhar ou manter o equilíbrio (neuropatia periférica)
Efeitos não desejados pouco frequentes(podem ocorrer em menos de 1 em 100 doentes):
secreção vaginal espessa e branca e infecção por leveduras (infecção)
formação de hematomas e sangramento no local da injeção do medicamento
aumento da atividade da enzima hepática gama-GT (detectada em análise sanguínea)
hepatite
insuficiência hepática
entorpecimento, formigamento e dor
reações anafiláticas
* efeitos não desejados em que o papel exacto de Fulvestrant Sandoz não é estabelecido devido à doença subjacente
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o seu médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados directamente ao Departamento de Monitorização de Efeitos Não Desejados de Medicamentos da Agência Nacional de Medicamentos e Produtos de Saúde: Rua [inserir rua], [inserir cidade], [inserir código postal]
telefone: [inserir telefone]/fax: [inserir fax]/site da Internet: [inserir site].
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos não desejados pode ajudar a recolher mais informações sobre a segurança do medicamento.
5. Como conservar Fulvestrant Sandoz
Manter o medicamento fora do alcance e da vista das crianças.
Não utilizar este medicamento após o prazo de validade impresso na caixa de cartão ou na etiqueta da seringa pré-cheia após EXP. O prazo de validade é o último dia do mês indicado.
Este medicamento não requer condições especiais de conservação.
O pessoal de saúde é responsável pela conservação, utilização e eliminação correcta da embalagem do medicamento Fulvestrant Sandoz após a utilização.
Não utilizar o medicamento se verificar algum sinal de danificação da seringa pré-cheia ou deterioração do seu conteúdo, como turvação da solução, partículas flutuantes ou alteração da cor.
Os medicamentos não devem ser eliminados na canalização ou nos contentores de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos de que já não precisa. Este procedimento ajudará a proteger o ambiente.
6. Conteúdo da embalagem e outras informações
O que contém Fulvestrant Sandoz
A substância ativa é fulvestranto.
Uma seringa pré-cheia contém 250 mg de fulvestranto em 5 ml de solução (50 mg/ml).
Os outros componentes são etanol (96%), álcool benzílico, benzoato de benzoíla e óleo de rícino.
Como é Fulvestrant Sandoz e que conteúdo tem a embalagem
Fulvestrant Sandoz é uma solução para injeção transparente, incolor a amarela, viscosa, em seringa pré-cheia.
A embalagem contém uma ou duas seringas pré-cheias individuais. Além disso, a embalagem contém uma agulha estéril.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Sandoz GmbH
Biochemiestrasse 10
6250 Kundl, Áustria
Fabricante
Lek Pharmaceuticals d.d.
Verovškova 57
1526 Liubliana, Eslovénia
EBEWE Pharma Ges.m.b.H. Nfg.KG
Mondseestrasse 11
4866 Unterach, Áustria
Fareva Unterach GmbH
Mondseestraße 11
4866 Unterach, Áustria
Para obter informações mais detalhadas sobre o medicamento e os seus nomes nos Estados-Membros do Espaço Económico Europeu, deve contactar:
Sandoz Portugal, Lda.
Rua [inserir rua], [inserir cidade], [inserir código postal]
telefone: [inserir telefone]
Data da última revisão do folheto:01/2022
Logótipo Sandoz
Informações destinadas exclusivamente a profissionais de saúde:
A dose de Fulvestrant Sandoz de 500 mg (2 x 250 mg/5 ml solução para injeção) deve ser administrada utilizando duas seringas pré-cheias (ver ponto 3).
Instruções de administração
Aviso – não esterilize a agulha com sistema de proteção em autoclave antes da utilização.
Evite o contacto das mãos com a agulha durante a administração do medicamento e a eliminação dos resíduos.
As seringas são fornecidas com agulha com sistema de proteção BD SafetyGlide ou Terumo SurGuard .
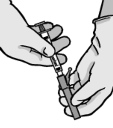
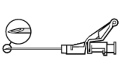
Instruções para a agulha com sistema de proteção BD SafetyGlide
Aplica-se a cada seringa:
| |
| |
| |
|  |
| |
|
| |
|  |
| 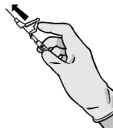 |
| ATENÇÃO: Proceda de forma a garantir a segurança para si e para os outros. Escute o clique e verifique visualmente se a ponta da agulha está completamente coberta. | |
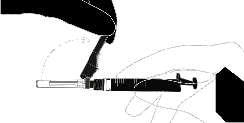
Instruções para a agulha com sistema de proteção Terumo SurGuard
Aplica-se a cada seringa:
| |
|  |
|  |
| |
| |
| |
| 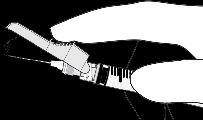 |
| o ativação com o dedo indicador | |
| o ativação com o polegar | 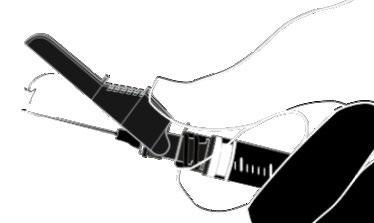 |
| o ativação no suporte | 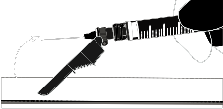 |
| A ativação é confirmada por um clique audível e (ou) palpável, e também pode ser verificada visualmente. Em caso de dúvida se a proteção cobriu completamente a agulha, deve repetir a etapa final. | |
Eliminação
As seringas pré-cheias são destinadas a uso único.
Todos os resíduos do medicamento ou embalagens não utilizados devem ser eliminados de acordo com as regulamentações locais.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorEbewe Pharma Ges.m.b.H Nfg. KG Fareva Unterach GmbH LEK Pharmaceuticals d.d.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Fulvestrant SandozForma farmacêutica: Solução, 250 mgSubstância ativa: fulvestrantNão requer receita médicaForma farmacêutica: Solução, 250 mgSubstância ativa: fulvestrantRequer receita médicaForma farmacêutica: Solução, 250 mg/ 5 mlSubstância ativa: fulvestrantRequer receita médica
Alternativas a Fulvestrant Sandoz noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Fulvestrant Sandoz em Espanha
Alternativa a Fulvestrant Sandoz em Ukraine
Médicos online para Fulvestrant Sandoz
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Fulvestrant Sandoz – sujeita a avaliação médica e regras locais.












