
Гаврикс Адулт

Спросите врача о рецепте на Гаврикс Адулт

Инструкция по применению Гаврикс Адулт
Инструкция для пациента: информация для пользователя
Havrix Adult, суспензия для инъекций
Вакцина против вирусного гепатита А, инактивированная, адсорбированная
Необходимо внимательно ознакомиться с содержанием инструкции перед применением вакцины, поскольку она содержит
информацию, важную для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу, фармацевту или медсестре.
- Эту вакцину назначили строго определённому человеку. Не следует её передавать другим.
- Если у пациента出现ят любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре. См. пункт 4.
Содержание этой инструкции сформулировано с учетом того, что она будет читаться человеком, получающим вакцину. Однако, поскольку эта вакцина может быть введена подросткам в возрасте от 16 лет, возможно, что содержание инструкции будет ознакомлено родителем или опекуном ребенка.
Содержание инструкции:
- 1. Что такое вакцина Havrix Adult и для чего она используется
- 2. Информация, важная перед применением вакцины Havrix Adult
- 3. Как применять вакцину Havrix Adult
- 4. Возможные нежелательные реакции
- 5. Как хранить вакцину Havrix Adult
- 6. Содержание упаковки и другие сведения
1. Что такое вакцина Havrix Adult и для чего она используется
Для чего используется вакцина Havrix Adult
Вакцину Havrix Adult используют для профилактики вирусного гепатита А (ВГА) у людей в возрасте 16 лет и старше, подверженных риску заражения вирусом гепатита А (HAV).
Что такое вирусный гепатит А:
‐
ВГА является болезнью печени, вызванной вирусом гепатита А (HAV).
‐
Вирус HAV передается от одного человека к другому или через контакт с загрязненной водой, пищей и напитками.
‐
Симптомы гепатита А варьируются от легких до тяжелых и могут включать лихорадку, плохое самочувствие, потерю аппетита, диарею, тошноту, дискомфорт в животе, темную окраску мочи и желтуху (желтизну глаз и кожи). Большинство пациентов полностью выздоравливают, но иногда болезнь может иметь тяжелое течение и требовать госпитализации, а в редких случаях может привести к острой печеночной недостаточности.
Как работает Havrix Adult:
‐
Havrix Adult помогает организму выработать собственную защиту (антитела) против вируса. Эти антитела помогают защитить организм от болезни.
‐
Как и в случае со всеми вакцинами, Havrix Adult может не полностью защитить всех вакцинированных людей.
2. Информация, важная перед применением вакцины Havrix Adult
Когда не применять вакцину Havrix Adult
‐
если пациент имеет аллергию на активное вещество или любой из других компонентов этой вакцины (перечисленных в пункте 6) или на нейомицин, или на формальдегид,
‐
если ранее возникала аллергическая реакция на любую вакцину против вирусного гепатита А.
Симптомы аллергической реакции могут включать зудящую кожную сыпь, трудности с дыханием, отек лица или языка.
Не следует применять препарат Havrix Adult, если любое из вышеуказанных состояний относится к пациенту. В случае сомнений перед применением вакцины Havrix Adult необходимо проконсультироваться с врачом, фармацевтом или медсестрой.
Предостережения и меры предосторожности
Перед применением вакцины Havrix Adult необходимо обсудить это с врачом, если:
‐
у пациента имеется тяжелое инфекционное заболевание с высокой температурой (лихорадкой). В этом случае вакцинация будет отложена. Легкое инфекционное заболевание, такое как простуда, не должно быть противопоказанием для вакцинации, но необходимо предварительно сообщить об этом врачу,
‐
пациент имеет ослабленную иммунную систему из-за заболевания и(или) применяемых препаратов. Врач решит, необходимы ли дополнительные дозы,
‐
пациент имеет проблемы с кровотечением или легко образуются синяки.
После или даже до применения любой вакцины в форме инъекции может возникнуть обморок. В связи с этим необходимо проинформировать врача, фармацевта или медсестру, если у пациента ранее возникал обморок при введении инъекции.
Вакцина Havrix Adult и другие препараты
Необходимо сообщить врачу, фармацевту или медсестре о всех препаратах, которые пациент принимает в настоящее время или принимал недавно, а также о препаратах, которые пациент планирует принимать, и о недавно полученных вакцинах.
Вакцину Havrix Adult можно применять одновременно с некоторыми другими вакцинами и иммуноглобулинами, однако места инъекции должны быть разными.
Беременность и грудное вскармливание
Если пациентка беременна или кормит грудью, предполагает, что может быть беременной, или планирует иметь ребенка, она должна проконсультироваться с врачом, фармацевтом или медсестрой перед применением этой вакцины.
Вождение транспортных средств и использование машин
Вакцина Havrix Adult не влияет или имеет незначительное влияние на способность управлять транспортными средствами и использовать машины.
Havrix Adult содержит фенилаланин, натрий и калий
Эта вакцина содержит 0,166 мг фенилаланина в каждой дозе.
Фенилаланин может быть вредным для пациентов с фенилкетонурией, редким генетическим заболеванием, при котором фенилаланин накапливается в организме, поскольку организм не удаляет его должным образом.
Эта вакцина содержит менее 1 ммоль (23 мг) натрия на дозу и менее 1 ммоль (39 мг) калия на дозу, то есть вакцину считают «свободной от натрия и калия».
3. Как применять вакцину Havrix Adult
Как вводится вакцина Havrix Adult
‐
Havrix Adult вводится путем внутримышечной инъекции, обычно в верхнюю часть руки.
‐
У пациентов с пониженным количеством тромбоцитов или с тяжелыми нарушениями свертываемости крови вакцина Havrix Adult в исключительных случаях может быть введена подкожно.
Дозировка
‐
Пациент получает 1 дозу вакцины Havrix Adult (1 мл суспензии) в день, согласованный с врачом или медсестрой.
‐
Вторую дозу (повторную дозу) рекомендуется вводить через 6-12 месяцев после первой дозы, но ее можно ввести в течение 5 лет после первой дозы для обеспечения длительной защиты.
Применение большей, чем рекомендуемая, дозы вакцины Havrix Adult
Передозировка очень маловероятна, поскольку вакцина поставляется в флаконе или шприце с единичной дозой и вводится врачом или медсестрой. Были зарегистрированы несколько случаев непреднамеренного введения большей дозы, и зарегистрированные нежелательные реакции были аналогичны тем, которые зарегистрированы при нормальном введении вакцины (перечислены в разделе 4).
Если следующая доза вакцины Havrix Adult не была введена в назначенный срок
Необходимо связаться с врачом, который решит, необходима ли дополнительная доза.
4. Возможные нежелательные реакции
Как и любой препарат, эта вакцина может вызывать нежелательные реакции, хотя они не возникают у каждого человека.
Тяжелые нежелательные реакции
Необходимо немедленно сообщить врачу в случае возникновения любого из следующих тяжелых нежелательных реакций - может потребоваться срочное лечение:
‐
аллергические реакции - симптомы могут включать местные или обширные сыпи, которые могут зудеть или покрываться пузырями, отек глаз и лица, трудности с дыханием или глотанием, внезапное падение артериального давления и потерю сознания.
Эти реакции могут возникнуть до выхода из кабинета врача.
В случае возникновения любого из вышеуказанных тяжелых нежелательных реакций необходимо немедленно сообщить врачу.
Во время клинических испытаний Havrix Adult возникли следующие нежелательные реакции:
Очень часто(могут возникнуть чаще, чем в 1 случае на 10 доз вакцины):
- головная боль
- боль и покраснение в месте инъекции
- усталость
Часто(могут возникнуть не чаще, чем в 1 случае на 10 доз вакцины):
- понижение аппетита
- тошнота (рвота)
- рвота
- диарея
- общее плохое самочувствие
- лихорадка ≥ 37,5°C
- отек или уплотнение в месте инъекции
Не очень часто(могут возникнуть не чаще, чем в 1 случае на 100 доз вакцины):
- инфекция верхних дыхательных путей
- заложенность носа или насморк
- головокружение
- боль в мышцах, скованность мышц, не связанная с упражнениями
- симптомы, подобные гриппу, такие как высокая температура, боль в горле, насморк, кашель и озноб
Редко(могут возникнуть не чаще, чем в 1 случае на 1000 доз вакцины):
- понижение или потеря чувствительности кожи к боли или прикосновению
- онемение
- зуд
- озноб
Следующие нежелательные реакции возникли после введения вакцины Havrix Adult в обращение:
‐
судороги
‐
сужение или блокирование кровеносных сосудов
‐
тяжелая аллергическая реакция, вызывающая отек лица, языка или горла, что может привести к трудностям с глотанием или дыханием
‐
крапивница, красные, часто зудящие пятна, которые начинаются на конечностях, а иногда на лице и остальной части тела
‐
боль в суставах
Сообщение о нежелательных реакциях
Если возникают любые нежелательные реакции, включая любые нежелательные реакции, не указанные в инструкции, необходимо сообщить об этом врачу, фармацевту или медсестре. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных средств Управления регистрации лекарственных средств, медицинских изделий и биоцидных продуктов: Ал. Ерозолимских 181С, 02-222 Варшава, тел.: 22 49-21-301, факс: 22 49-21-309, веб-сайт: https://smz.ezdrowie.gov.pl
Нежелательные реакции также можно сообщать ответственному лицу.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности применения препарата.
5. Как хранить вакцину Havrix Adult
Препарат следует хранить в месте, недоступном для детей.
Хранить в холодильнике (2 ° C – 8 ° C).
Не замораживать.
Хранить в оригинальной упаковке для защиты от света.
Не использовать эту вакцину после истечения срока годности, указанного на упаковке после «EXP». Срок годности указывает последний день указанного месяца.
Аббревиатура «Lot» обозначает номер серии продукта.
6. Содержание упаковки и другие сведения
Что содержит вакцина Havrix Adult
- Активное вещество вакцины Havrix Adult является:
Вирус гепатита А, штамм HM175 (инактивированный)
не менее 1440 единиц ELISA
выращенный в культуре человеческих диплоидных клеток MRC-5
адсорбированный на гидроксиде алюминия, гидратированном
0,5 мг Al
- Другие компоненты являются: полисорбат 20, аминокислоты для инъекций (в том числе фенилаланин), фосфат натрия, фосфат калия, хлорид натрия, хлорид калия, вода для инъекций.
Как выглядит вакцина Havrix Adult и что содержит упаковка
Havrix Adult является слегка не прозрачной, белой суспензией в флаконе или шприце-ампуле.
Доступные упаковки:
1 флакон по 1 мл в картонной коробке
1 шприц-ампула с иглой по 1 мл в картонной коробке
1 шприц-ампула по 1 мл с иглой, прикрепленной к упаковке в картонной коробке
Ответственное лицо и производитель
GlaxoSmithKline Biologicals S.A.
ру де л'Институт 89
1330 Риксенсарт, Бельгия
Для получения более подробной информации необходимо обратиться к местному представителю ответственного лица:
GSK Services ООО
ул. Рымовского 53
02-697 Варшава
тел. +48 (22) 576-90-00
Этот препарат разрешен к обращению в государствах-членах Европейского экономического пространства под следующими названиями:
| Чешская Республика, Дания, Эстония, Финляндия, Греция, Исландия, Италия | HAVRIX |
| Норвегия, Швеция | Havrix |
| Австрия, Бельгия, Венгрия, Люксембург, Нидерланды | HAVRIX 1440 |
| Германия | Havrix 1440 |
| Болгария | ХАВРИКС 1440 инъекционна суспензия (доза за възрастни) |
| Кипр | HAVRIX 1440 IU |
| Франция | HAVRIX 1440 U/1ml ADULTES |
| Ирландия, Мальта | HAVRIX MONODOSE |
| Латвия | HAVRIX 1440 ELISA units/ml vienības/ml suspensija injekcijām |
| Литва | Havrix 1440 ELISA vienetų/ml injekcinė suspensija |
| Польша | HAVRIX ADULT |
| Португалия | HAVRIX 1440 ADULTO |
| Румыния | HAVRIX ADULT 1440 suspensie injectabilă |
| Словакия | HAVRIX 1440 Dosis adulta |
| Словения | HAVRIX 1440 ELISA enot suspenzija za injiciranje |
Дата последнего обновления инструкции:
08/2024
Информация предназначена только для медицинских работников или сотрудников здравоохранения:
Во время хранения на дне флакона или шприца-ампулы может образоваться белый осад и прозрачная, бесцветная жидкость над ним. Перед применением вакцину необходимо осмотреть на предмет возможного присутствия посторонних частиц и (или) изменений физических свойств.
Перед использованием необходимо встряхнуть флакон или шприц-ампулу для получения слегка не прозрачной, белой суспензии.
В случае обнаружения любых изменений внешнего вида вакцины не следует ее применять.
| за оdrasle | |
| Испания | HAVRIX 1440 suspensión inyectable en jeringa precargada |
Инструкции для шприца-ампулы
Необходимо держать шприц-ампулу за корпус, а не за поршень.
Необходимо открутить насадку шприца-ампулы, повернув ее в направлении, противоположном движению часовой стрелки.
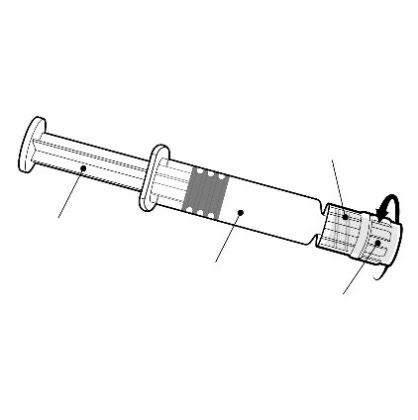
Адаптер типа Luer Lock
Поршень
Корпус
Нasadка
Необходимо прикрепить иглу к шприцу-ампуле, присоединив насадку иглы к адаптеру Luer Lock и повернув ее на четверть оборота в направлении, совпадающем с движением часовой стрелки, до тех пор, пока не будет чувствоваться блокировка иглы.
Не следует вынимать поршень из корпуса шприца-ампулы. Если это произошло, не следует применять вакцину.
Утилизация
Все неиспользованные остатки продукта или его отходы необходимо утилизировать в соответствии с местными правилами.
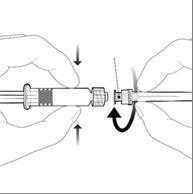
Нasadка иглы
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- Производитель
- ИмпортерGlaxoSmithKline Biologicals S.A.
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги Гаврикс АдултФорма выпуска: Суспензия, 160 единиц антигена ELISA вируса гепатита A, штамм GBM/0,5 мл; 1 доза (0,5 мл)Активное вещество: hepatitis A, inactivated, whole virusТребуется рецептФорма выпуска: Суспензия, не менее 720 единиц ELISA вируса гепатита A, штамм HM175/0,5 мл; 1 доза (0,5 мл)Активное вещество: hepatitis A, inactivated, whole virusПроизводитель: GlaxoSmithKline Biologicals S.A.Требуется рецептФорма выпуска: Суспензия, 25 МЕ вируса гепатита А, штамм CR326F/0,5 мл; 1 доза (0,5 мл), для детей и подростковАктивное вещество: hepatitis A, inactivated, whole virusПроизводитель: Merck Sharp & Dohme B.V.Требуется рецепт
Аналоги Гаврикс Адулт в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Гаврикс Адулт в Испания
Аналог Гаврикс Адулт в Украина
Врачи онлайн по Гаврикс Адулт
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Гаврикс Адулт – по решению врача и с учетом местных правил.














