
MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL


Como usar MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o utilizador
Meriofert Kit 75 UIpó e diluente para solução injectável
menotropina
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que o ler novamente.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
- Neste prospecto, Meriofert 75 UI de pó e diluente para solução injectável é denominado Meriofert Kit.
Conteúdo do prospecto
- O que é Meriofert Kit e para que é utilizado
- O que necessita saber antes de começar a usar Meriofert Kit
- Como usar Meriofert Kit
- Possíveis efeitos adversos
- Conservação de Meriofert Kit
- Conteúdo do envase e informações adicionais
1. O que é Meriofert Kit e para que é utilizado
- Meriofert Kit é usado para estimular a ovulação em mulheres que não ovulam e que não responderam a outro tratamento (citrato de clomifeno).
respondeu a outro tratamento.
- Meriofert Kit é usado para provocar o desenvolvimento de vários folículos (e, portanto, de vários
óvulos) em mulheres submetidas a um tratamento de fertilidade.
Meriofert Kit é uma gonadotropina menopáusica humana muito purificada, que pertence a um grupo de medicamentos denominados gonadotropinas.
Cada frasco contém pó liofilizado com 75 UI de atividade de hormona foliculoestimulante (FSH) humana e 75 UI de atividade de hormona luteinizante humana (LH).
A gonadotropina menopáusica humana (HMG) é extraída da urina de mulheres pós-menopáusicas. É adicionada gonadotropina coriónica humana (hCG), extraída da urina de mulheres grávidas, para contribuir para a atividade de LH total.
Este medicamento deve ser usado sob a supervisão de um médico.
2. O que necessita saber antes de começar a usar Meriofert Kit
Antes de começar o tratamento, será avaliada a sua fertilidade e a da sua parceira.
Não use Meriofert Kit
- Se apresentar um aumento do tamanho dos seus ovários, ou quistes cuja causa não seja um distúrbio hormonal (doença ovárica poliquística).
- Se tiver sangramentos de origem desconhecida.
- Se padece câncer de ovários, útero ou mama.
- Se apresentar uma inflamação anormal (tumor) da hipófise ou do hipotálamo (cérebro).
- Se é alérgica à menotropina ou a qualquer um dos outros componentes deste
medicamento (incluídos na secção 6).
Não deve utilizar este medicamento se sofre de menopausa precoce, malformação dos órgãos genitais ou determinados tumores do útero que impediriam um gravidez normal.
Advertências e precauções
Consulte o seu médico antes de começar a usar Meriofert Kit.
Embora não sejam descritas reações alérgicas a Meriofert Kit, deverá informar o seu médico se padece alguma reação alérgica a medicamentos semelhantes.
Este tratamento aumenta o risco de sofrer uma doença denominada síndrome de hiperestimulação ovárica (SHO)(ver secção 4). Se se produzir uma hiperestimulação ovárica, será suspenso o tratamento e deverão ser evitadas as gravidezes. Os primeiros sinais de hiperestimulação ovárica são dor na região inferior do abdômen, náuseas (mal-estar), vômitos e ganho de peso. Se se produzirem esses sintomas, deverá examiná-lo um médico o mais breve possível. Em casos graves, mas raros, podem aumentar os ovários e acumular-se líquido no abdômen ou no peito.
O medicamento empregado para provocar o desprendimento definitivo dos óvulos maduros (que contém gonadotropina coriónica humana, hCG) pode aumentar a probabilidade de sofrer um SHO. Por tanto, não é recomendável utilizar hCG nos casos em que se esteja produzindo um SHO e não deverão manter relações sexuais durante um mínimo de 4 dias, embora se utilize um método anticonceptivo de barreira.
Cabe destacar que as mulheres com problemas de fertilidade têm uma taxa de abortos superior à da população normal.
A frequência de gravidezes e partos múltiplos nas pacientes submetidas a um tratamento para estimular a ovulação é maior do que nas mulheres que concebem de forma natural. No entanto, este risco pode ser reduzido ao mínimo se for usada a dose recomendada.
O risco de gravidez ectópica (gravidez fora do útero) é ligeiramente maior nas mulheres com lesões nas trompas de Falópio.
As gravidezes múltiplas e as características dos progenitores submetidos a tratamentos de fertilidade (por exemplo, a idade da mãe ou as características do sêmen) podem estar associadas a um aumento do risco de defeitos de nascimento.
O tratamento com Meriofert Kit, assim como a própria gravidez, pode aumentar a probabilidade de sofrer uma trombose. A trombose é a formação de um coágulo de sangue em um vaso sanguíneo, a maioria das vezes nas veias das pernas ou nos pulmões.
Comente este facto com o seu médico antes de começar o tratamento, em especial:
- Se já sabe que tem uma maior probabilidade de sofrer uma trombose.
- Se si ou algum familiar próximo sofreu alguma vez uma trombose.
- Se padece obesidade grave.
População pediátrica
O medicamento não é indicado para uso pediátrico.
Uso deMeriofert Kit com outros medicamentos
Informa o seu médico ou farmacêutico se está a tomar, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Gravidez, lactação e fertilidade
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico antes de utilizar este medicamento.
Condução e uso de máquinas
A influência de Meriofert Kit sobre a capacidade para conduzir e utilizar máquinas é nula ou insignificante.
Meriofert Kit contém sódio
Este medicamento contém menos de 23 mg (1 mmol) de sódio, pelo que se considera essencialmente “isento de sódio”
3. Como usar Meriofert Kit
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico.
Dose e duração do tratamento
Mulheres que não ovulam e têm períodos irregulares ou ausência de menstruação
Por norma geral, a primeira injeção de um frasco de 75 UI de menotropina é administrada durante a primeira semana do ciclo após a menstruação espontânea ou induzida.
Posteriormente, é injetada todos os dias a dose deste medicamento prescrito pelo médico e continua-se com o tratamento até que sejam formados um ou mais folículos maduros no ovário. O médico ajustará a dose deste medicamento dependendo da resposta ovárica, que é determinada por meio de exames clínicos.
Assim que um folículo atingir a fase de desenvolvimento necessária, será interrompido o tratamento com este medicamento e será provocada a ovulação com outra hormona (gonadotropina coriónica, hCG).
A ovulação ocorre, por norma, num prazo de entre 32 e 48 horas.
Nesta fase do tratamento, existe a possibilidade de fertilização. Será recomendado que mantenha relações sexuais todos os dias a partir do dia anterior à administração de hCG. Se, apesar da ovulação, não se consiga uma gravidez, pode ser repetido o tratamento.
Mulheres submetidas a uma estimulação ovárica para o desenvolvimento folicular múltiplo antes de uma fertilizaçãoin vitroou outras técnicas de reprodução assistida
O objetivo deste método é obter um desenvolvimento folicular múltiplo simultâneo. O tratamento começará no segundo ou terceiro dia do ciclo com injeções de entre 150 e 300 UI deste medicamento (1 ou 2 frascos de Meriofert Kit 150 UI). O médico pode optar por administrar doses mais elevadas se for necessário. A dose deste medicamento que é injetada é maior do que a do método empregado para a fertilização natural. O médico se encarrega de ajustar a continuação do tratamento de forma individualizada.
Assim que se tenha desenvolvido um número suficiente de folículos, será interrompido o tratamento com este medicamento e será provocada a ovulação mediante a injeção de outra hormona (gonadotropina coriónica, hCG).
Como administrar Meriofert Kit
Este medicamento é administrado sob a forma de injeção sob a pele (por via subcutânea) ou no músculo (por via intramuscular).
Os frascos apenas devem ser usados uma vez e a injeção deve ser administrada assim que estiver preparada.
Depois de aconselhá-lo e instruí-lo devidamente, é possível que o médico o peça para se administrar a injeção de Meriofert Kit si mesmo.
A primeira vez que o fizer, o médico deve
- permitir que pratique a autoadministração de uma injeção subcutânea,
- indicar os locais onde pode administrar a injeção,
- ensinar a preparar a solução injectável,
- explicar como preparar a dose correcta para a injeção.
Antes de se administrar a injeção de Meriofert Kit, leia atentamente as seguintes instruções.
Como preparar e injetar 1 frasco de Meriofert Kit
A injeção deve ser preparada justo antes de si estar pronto para usá-la, empregando para isso a seringa pré-carregada de diluente (uma solução de cloreto de sódio de 9 mg/ml em água para injectáveis) incluída em cada embalagem de Meriofert Kit.
Prepare uma superfície limpa e lave as mãos. É importante que as mãos e os artigos que utilize estejam o mais limpos possível.
Coloque sobre a superfície os artigos seguintes:
- dois algodões com álcool (não incluídos),
- um frasco com pó de Meriofert Kit,
- uma seringa pré-carregada com diluente,
- uma agulha para preparar a injeção,
- uma agulha fina para a injeção subcutânea.
LEMBRE-SE: não retire a lingueta de apoio (peça branca) da seringa pré-carregada, porque evita a extracção involuntária do pistão e melhora o manuseio da seringa durante a injeção.
Reconstituição da solução injectável
Preparação da injeção
- • Retire o capuchão da seringa pré-carregada; introduza a agulha de
reconstituição (agulha longa) na seringa.
• Coloque com cuidado a seringa sobre a superfície limpa.
• Evite tocar a agulha.
Prepare a solução para a injeção
- • Retire a cápsula de plástico colorida (verde claro na apresentação
de 75 UI e verde escuro na de 150 UI) do frasco de Meriofert Kit
empurrando-a suavemente para cima.
- Limpe a parte superior de borracha com o algodão impregnado de
álcool e espere até que seque.
- • Pegue a seringa, retire o capuchão protetor da agulha e introduza a
agulha através do centro de borracha da parte superior do frasco de
Meriofert Kit.
- Empurre com firmeza o êmbolo para baixo para rociar toda a
solução sobre o pó.
- NÃO AGITE O FRASCO; mova-o suavemente em círculos até
obter uma solução transparente.
Por norma, o medicamento se dissolve imediatamente.
- • Com a agulha ainda introduzida, dê a volta ao frasco.
- Certifique-se de que a ponta da agulha esteja por baixo do nível do
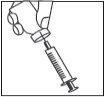 líquido.
líquido.
- Tire com cuidado do êmbolo para introduzir toda a solução de
Meriofert Kit na seringa.
•Verifique se a solução reconstituída é transparente.
Quando reconstituir mais de 1 frasco de Meriofert Kit, introduza de novo o conteúdo do primeiro frasco na seringa e injete lentamente num segundo frasco após repetir os passos do 2 ao 4.
Injeção do medicamento por via subcutânea
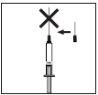
 Quando a seringa contiver a dose descrita, coloque o capuchão protetor da agulha. Retire a agulha da seringa e substitua-a pela agulha fina para injeção subcutânea com o seu capuchão protetor.
Quando a seringa contiver a dose descrita, coloque o capuchão protetor da agulha. Retire a agulha da seringa e substitua-a pela agulha fina para injeção subcutânea com o seu capuchão protetor.- Introduza com firmeza a agulha fina no cilindro da seringa e, a seguir, gire-a ligeiramente para se certificar de que está totalmente enroscada e conseguir uma conexão estanque.
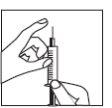
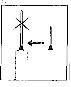
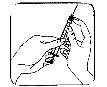 Retire o capuchão protetor da agulha. Segure a seringa com a agulha apontando para cima e dê golpes suaves no lateral da seringa para que as bolhas de ar subam até a parte superior;
Retire o capuchão protetor da agulha. Segure a seringa com a agulha apontando para cima e dê golpes suaves no lateral da seringa para que as bolhas de ar subam até a parte superior;- Empurre o êmbolo até que apareça uma gota de líquido na ponta da agulha.
- Não o utilize se contiver partículas ou estiver turvo.
Zona de injeção
- O médico ou o enfermeiro já lhe explicou em que parte do corpo deve administrar o medicamento. Os locais habituais são a coxa ou a parede inferior do abdômen abaixo do umbigo.
- Limpe a zona de injeção com um algodão com álcool.
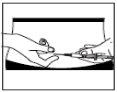 Inserção da agulha
Inserção da agulha
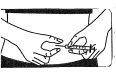
? Puxe e aperte com firmeza a pele. Com a outra mão, introduza
a agulha com um movimento seco e rápido, formando um ângulo de
45° ou 90°.
Injeção da solução
- Injete a seringa sob a pele tal como lhe indicaram. Não a injete directamente numa veia. Empurre o êmbolo lentamente e sem interrupções, para que a solução seja injetada correctamente e os tecidos cutâneos não sofram danos.
Leve o tempo que necessitar para injetar o volume de solução que lhe foi prescrito. Dependendo da dose que lhe foi prescrita, é possível que não utilize todo o volume da solução.
Extração da agulha
- Extraia rapidamente a seringa e pressione a zona de injeção com um algodão com desinfectante. Os massagens suaves na zona (enquanto se mantém a pressão) ajudam a dispersar a solução de Meriofert Kit e aliviam as possíveis molestias.
Injeção do medicamento por via intramuscular
No caso das injeções intramusculares, o profissional de saúde preparará e injetará este medicamento no lateral da coxa ou no glúteo.
Elimine todos os artigos utilizados
Uma vez finalizada a injeção, introduza todas as agulhas, os frascos e seringas vazias no contentor para objectos pontiagudos. A eliminação da solução não utilizada e de todos os materiais que estiveram em contacto com ela, será realizada de acordo com a normativa local.
Se usar mais Meriofert Kitdo que deve
Desconhecem-se os efeitos da sobredose deste medicamento, no entanto, caberia esperar que se produzisse um síndrome de hiperestimulação ovárica (ver secção 4). Se usar mais medicamento do que deve, consulte o seu médico ou enfermeiro.
Se esquecer de usar Meriofert Kit
Use-o no prazo em que lhe tocaria normalmente a seguinte injeção. Não tome uma dose dupla para compensar as doses esquecidas.
Se interromper o tratamento com Meriofert Kit
Não o interrompa por iniciativa própria.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
O seguinte efeito adverso é importante e exigirá uma intervenção imediata se o sofrer. Deverá deixar de tomar este medicamento e acudir ao médico imediatamente se se produzir o seguinte:
Frequentes, pode afectar até 1 de cada 10 pessoas
- Síndrome de hiperestimulação ovárica (os sintomas incluem a formação de quistes ováricos ou o aumento do tamanho de quistes existentes, dor na parte inferior do estômago, sensação de sede e náuseas com vômitos ocasionais, evacuação de pequenas quantidades de urina concentrada e ganho de peso) (ver secção 2 para obter informações adicionais).
Também foram comunicados os seguintes efeitos adversos:
Muito frequentes: podem afectar mais de 1 de cada 10 pessoas
- Cefaleia
- Inchaço do estômago ou meteorismo
Frequentes: podem afectar até 1 de cada 10 pessoas
- Dor ou desconforto abdominal
- Dor pélvica
- Dor de costas
- Sensação de peso
- Desconforto na mama
- Tontura
- Sofocos
- Sede
- Sensação de doença
- Cansaço
- Desconforto geral
- Reacções na zona de injeção, tais como dor e inflamação (mais habituais com a injeção IM do que com a SC).
Raros: podem afectar até 1 de cada 1.000 pessoas
- Torsão ovárica (rotação do ovário que causa uma dor de grande intensidade na parte inferior do abdômen)
- Tromboembolia (formação de um coágulo em um vaso sanguíneo que se desprende e viaja através do torrente sanguíneo para bloquear outro vaso).
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, si pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação do Meriofert Kit
Mantenha este medicamento fora da vista e do alcance das crianças.
Não conserve a uma temperatura superior a 25°C. Conservar o frasco e a seringa pré-carregada de solvente no embalagem exterior para protegê-los da luz.
Não utilize este medicamento após a data de validade que aparece no embalagem exterior, no frasco e na seringa pré-carregada de solvente após CAD. Se a data de validade for indicada como mês/ano, a data de validade é o último dia do mês indicado.
Utilize imediatamente após a reconstituição.
Não utilize este medicamento se observar que a solução não é transparente. Após a reconstituição, a solução deve ser transparente e incolor.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Deposite os recipientes e os medicamentos que não precisa no Ponto SIGRE  da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos recipientes e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos recipientes e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição do Meriofert Kit
O princípio ativo é menotropina.
Cada frasco contém pó liofilizado com 75 UI de atividade de hormona foliculoestimulante (FSH) humana e 75 UI de atividade de hormona luteinizante humana (LH).
A gonadotropina menopáusica humana (HMG) é extraída da urina de mulheres pós-menopáusicas.
É adicionada gonadotropina coriónica humana (hCG), extraída da urina das mulheres grávidas, para contribuir para a atividade de LH total.
Se forem utilizados vários frascos de pó, a quantidade de menotropina em 1 ml de solução reconstituída será a seguinte:
Meriofert Kit 75UI pó e solvente para solução injetável | |
Número de frascos utilizados | Quantidade total de menotropina em 1 ml de solução |
1 | 75 UI |
2 | 150 UI |
3 | 225 UI |
4 | 300 UI |
5 | 375 UI |
6 | 450 UI |
Os demais componentes são
Frasco de pó: lactosa monohidrato
Seringa pré-carregada com solvente: solução de 9 mg/ml de cloreto de sódio
Aspecto do produto e conteúdo do envase
Pó: torta ou pó branco liofilizado
Solvente: solução transparente e incolor
Meriofert Kit é apresentado como pó e solvente para solução injetável.
1 estojo contém o seguinte:
- Um frasco com torta ou pó branco liofilizado
- Uma seringa pré-carregada (1 ml) com solução transparente e incolor
- Uma agulha para a reconstituição e a injeção intramuscular (agulha longa)
- Uma agulha para a injeção subcutânea (agulha curta)
É fornecido em caixas de 1, 5 ou 10 estojos.
Pode ser que apenas alguns tamanhos de embalagens sejam comercializados.
Título da autorização de comercialização e responsável pela fabricação
Título da autorização de comercialização:
IBSA Farmaceutici Italia Srl
Via Martiri di Cefalonia 2
26900 Lodi, Itália
Responsável pela fabricação:
IBSA Farmaceutici Italia srl
Via Martiri di Cefalonia, 2
26900 Lodi – Itália
ou (para Reino Unido)
IBSA Pharma Limited
Units 4-6
Colonial Business Park
Colonial Way
Watford D24 4PR
Reino Unido
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do título da autorização de comercialização:
Instituto Bioquímico Ibérico IBSA S.L.
Avenida Diagonal 605,
Planta 8, Local 1,
08028 Barcelona (Espanha)
Este medicamento está autorizado nos estados membros do Espaço Econômico Europeu com os seguintes nomes (as concentrações e formas farmacêuticas são idênticas em todos os países, apenas mudam os nomes comerciais):
Áustria: Meriofert PFS
Bélgica: Fertinorm Kit
Bulgária: Meriofert PFS
Chipre: Meriofert PFS
República Checa: Meriofert Set
Dinamarca: Meriofert Set
Estônia: Meriofert Set
Finlândia: Meriofert Set
França: Fertistartkit
Grécia: Meriofert
Hungria: Meriofert Kit
Itália: Meriofert
Letônia: Meriofert Set
Lituânia: Meriofert Set
Luxemburgo: Fertinorm Kit
Noruega: Meriofert Set
Polônia: Mensinorm Set
Romênia: Meriofert PFS
Eslováquia: Meriofert Kit
Espanha: Meriofert Kit
Países Baixos: Meriofert spuit
Reino Unido: Meriofert PFS
Suécia: Meriofert Set
Data da última revisão deste prospecto: Maio 2024
A informação detalhada e atualizada sobre este medicamento está disponível no site da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, -Substância ativa: human menopausal gonadotrophinFabricante: Angelini Pharma Espana S.L.Requer receita médicaForma farmacêutica: INJETÁVEL, 1200 UISubstância ativa: human menopausal gonadotrophinFabricante: Ferring S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 1200 UISubstância ativa: human menopausal gonadotrophinFabricante: Ferring S.A.U.Requer receita médica
Alternativas a MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Polónia
Alternativa a MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Ukraine
Médicos online para MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de MERIOFERT KIT 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.





