
Como usar Mensinorm Set
Folheto informativo para o doente
Mensinorm Set, 900 UI
pó e solvente para solução injetável
Menotropina
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que tenham os mesmos sintomas que o senhor.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
- Neste folheto, o medicamento Mensinorm Set 900 UI pó e solvente para solução injetável é denominado por Mensinorm Set.
Índice do folheto
- 1. O que é o Mensinorm Set e para que é utilizado
- 2. Informações importantes antes de tomar o Mensinorm Set
- 3. Como tomar o Mensinorm Set
- 4. Efeitos não desejados
- 5. Como conservar o Mensinorm Set
- 6. Conteúdo da embalagem e outras informações
1. O que é o Mensinorm Set e para que é utilizado
- O Mensinorm Set é utilizado para estimular a ovulação em mulheres que não ovulam e em que o tratamento com outros medicamentos (citrato de clomifeno) não teve o efeito desejado.
- O Mensinorm Set é utilizado para estimular o desenvolvimento de vários folículos ovarianos (e, portanto, vários ovócitos) em mulheres submetidas a tratamento de infertilidade.
O Mensinorm Set é uma gonadotropina menopáusica humana altamente purificada, que pertence a um grupo de medicamentos denominados gonadotropinas.
Cada frasco multidose contém um pó liofilizado que contém 900 UI de hormona folículo-estimulante humana (FSH) e 900 UI de hormona luteinizante humana (LH).
A gonadotropina menopáusica humana (HMG) é obtida a partir da urina de mulheres pós-menopáusicas. Para aumentar a atividade total de LH, foi adicionada gonadotropina coriônica humana (hCG) - um hormônio obtido a partir da urina de mulheres grávidas.
Este medicamento deve ser utilizado sob supervisão médica.
2. Informações importantes antes de tomar o Mensinorm Set
Antes de iniciar o tratamento, será realizada uma avaliação da fertilidade de ambos os parceiros.
Quando não tomar o Mensinorm Set:
- se a paciente tiver ovários aumentados ou cistos ovarianos não causados por distúrbios hormonais (síndrome do ovário policístico);
- se a paciente tiver sangramento de causa desconhecida;
- se a paciente tiver tumor de ovário, útero ou mama;
- se a paciente tiver aumento (tumor) da pituitária ou hipotálamo (partes do cérebro);
- se a paciente for alérgica à menotropina ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6).
Este medicamento não deve ser utilizado em mulheres com menopausa precoce, anomalias congénitas dos órgãos reprodutivos ou certos tumores uterinos que impeçam o desenvolvimento de uma gravidez normal.
Advertências e precauções
Até à data, não foram relatados casos de reações alérgicas ao Mensinorm Set, no entanto, se a paciente já teve reações alérgicas a medicamentos semelhantes no passado, deve informar o médico.
A tomada deste medicamento aumenta o risco de desenvolver uma condição denominada síndrome de hiperestimulação ovariana(ver ponto 4 Efeitos não desejados).
Em caso de desenvolvimento da síndrome de hiperestimulação ovariana, o tratamento será interrompido e será necessário evitar a gravidez. Os primeiros sintomas de hiperestimulação ovariana são dor na parte inferior do abdômen, náuseas (enjoo), vómitos e aumento de peso.
Em caso de ocorrência desses sintomas, deve consultar o médico o mais rápido possível. Em casos graves, embora raros, pode ocorrer aumento dos ovários e acúmulo de líquido na cavidade abdominal ou tórax.
Este medicamento, utilizado para induzir a libertação de ovócitos maduros (contendo gonadotropina coriônica humana, hCG), também pode aumentar a probabilidade de desenvolver a síndrome de hiperestimulação ovariana. Por isso, não se recomenda a utilização de hCG em caso de desenvolvimento da síndrome de hiperestimulação ovariana.
Não deve ter relações sexuais durante pelo menos 4 dias, mesmo que utilize métodos anticoncepcionais mecânicos.
Em mulheres com problemas de fertilidade, o risco de aborto é maior do que na população em geral.
Em mulheres submetidas a tratamento para induzir a ovulação, o risco de gravidez múltipla é maior do que no caso de fertilização natural. No entanto, este risco pode ser reduzido utilizando a dose recomendada do medicamento.
Em mulheres com anomalias nos tubos uterinos, há um risco ligeiramente aumentado de gravidez ectópica (fora do útero).
A gravidez múltipla e as características dos parceiros submetidos a tratamento de infertilidade (por exemplo, idade da mulher, parâmetros do sêmen) podem estar associadas a um risco aumentado de anomalias congénitas.
A utilização do Mensinorm Set, assim como a gravidez, pode aumentar o risco de desenvolver trombose. A trombose é a formação de um coágulo sanguíneo num vaso sanguíneo, geralmente nas veias dos membros inferiores ou nos pulmões.
Antes de iniciar a utilização do medicamento, deve discutir com o médico, especialmente nos seguintes casos:
- se a paciente tem um histórico de risco aumentado de trombose;
- se a paciente ou um familiar direto teve trombose no passado;
- se a paciente tem obesidade mórbida.
Crianças
Este medicamento não é destinado a ser utilizado em crianças.
Mensinorm Set e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que a paciente está a tomar atualmente ou recentemente, bem como sobre os medicamentos que a paciente planeia tomar.
Gravidez, amamentação e fertilidade
O Mensinorm Set não deve ser utilizado durante a gravidez ou amamentação.
Condução de veículos e utilização de máquinas
O Mensinorm Set não tem efeito ou tem um efeito não significativo na capacidade de conduzir veículos ou utilizar máquinas.
O Mensinorm Set contém sódio
O medicamento contém menos de 1 mmol (23 mg) de sódio por solução preparada, ou seja, o medicamento é considerado "livre de sódio".
3. Como tomar o Mensinorm Set
Dose recomendada e duração do tratamento:
Este medicamento deve ser sempre utilizado de acordo com as recomendações do médico. Em caso de dúvidas, deve consultar o médico.
Mulheres que não ovulam, com menstruações irregulares ou ausência de menstruação:
Em geral, a primeira injeção de 75 UI é administrada na primeira semana do ciclo menstrual, após um sangramento menstrual natural ou induzido.
Em seguida, o Mensinorm Set é administrado diariamente na dose prescrita pelo médico, e o tratamento é continuado até que se desenvolva pelo menos um folículo ovariano maduro no ovário. O médico ajustará a dose do Mensinorm Set com base na resposta ovariana determinada por exames diagnósticos.
Quando um folículo ovariano atingir o estágio de desenvolvimento necessário, a administração do Mensinorm Set será interrompida e a ovulação será induzida com um outro hormônio (gonadotropina coriônica, hCG).
A ovulação ocorre geralmente 32-48 horas após a administração.
Nesta etapa do tratamento, é possível a fertilização. Recomenda-se ter relações sexuais diariamente, começando no dia anterior à administração da hCG. Se, apesar da ovulação, não ocorrer desenvolvimento da gravidez, o tratamento pode ser repetido.
Mulheres submetidas a estimulação ovariana para induzir o desenvolvimento de vários folículos ovarianos antes de uma fertilização in vitroou outras técnicas de reprodução assistida:
O objetivo desta técnica é obter o desenvolvimento simultâneo de vários folículos ovarianos. O tratamento começa no 2º ou 3º dia do ciclo menstrual com uma injeção de 150-300 UI do Mensinorm Set. O médico pode recomendar a administração de doses mais altas do medicamento, se necessário.
A dose do Mensinorm Set é maior do que a utilizada para a fertilização natural. O médico ajustará o tratamento posterior com base nas necessidades individuais.
Quando um número adequado de folículos ovarianos atingir o estágio de desenvolvimento necessário, a administração do Mensinorm Set será interrompida e a ovulação será induzida com uma injeção de um outro hormônio (gonadotropina coriônica, hCG).
Como tomar o Mensinorm Set:
O Mensinorm Set é administrado por injeção subcutânea.
Cada frasco deve ser reconstituído apenas uma vez, e cada injeção deve ser administrada imediatamente após a retirada da dose necessária.
Após a devida consulta e treinamento da paciente, o médico pode recomendar que a paciente administre as injeções do Mensinorm Set por conta própria.
Antes da primeira injeção do medicamento, o médico deve:
- permitir que a paciente pratique a auto-injeção subcutânea;
- indicar os locais no corpo onde a paciente pode administrar as injeções por conta própria;
- demonstrar como preparar a solução para injeção;
- explicar como preparar a dose correta do medicamento para injeção.
Antes de administrar a injeção do Mensinorm Set por conta própria, a paciente deve ler atentamente as seguintes instruções.
Como o frasco contém medicamento para vários dias de tratamento, é importante garantir que apenas a dose prescrita pelo médico seja retirada. O médico prescreverá a dose do Mensinorm Set em UI (unidades internacionais). Para obter a dose correta, deve utilizar uma das 12 seringas para administração com graduação em UI de FSH/LH.
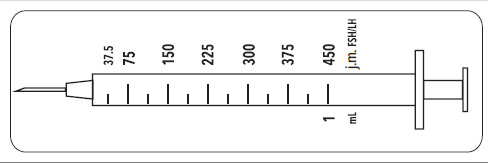
Essas seringas são para uso único e devem ser descartadas após cada administração, de acordo com as regulamentações locais.
Como preparar e administrar 1 frasco do Mensinorm Set
A solução para injeção que contém 900 UI de menotropina deve ser preparada imediatamente antes da administração da primeira dose, adicionando o solvente para reconstituição na seringa-ampola (incluída em cada embalagem) ao frasco que contém o pó.
Preparar uma superfície limpa e lavar as mãos com sabão e água quente. É importante que as mãos e os objetos utilizados sejam o mais limpos possível.
Preparar os seguintes materiais:
- frasco que contém o pó do Mensinorm Set;
- seringa-ampola que contém o solvente para reconstituição;
- agulha para reconstituição;
- uma seringa para uso único com agulha inserida para administração subcutânea com graduação em UI de FSH/LH;
- um cotonete com álcool;
- um cotonete e solução de desinfecção (não incluídos na embalagem).
LEMBRE-SE: Antes da reconstituição e de cada administração subsequente, desinfetar a parte superior do frasco que contém a solução com um cotonete e solução de desinfecção (por exemplo, álcool) e deixar secar. Não retire a proteção do tipo backstop(anilha branca) da seringa-ampola, pois evita a retirada acidental da tampa e facilita a manipulação da seringa durante a injeção.Reconstituição da solução para injeção
Preparação da seringa-ampola:
- 1.
- Retirar a tampa da seringa-ampola que contém o solvente; colocar a agulha para reconstituição com tampa de proteção na seringa.
- Colocar a seringa cuidadosamente em uma superfície limpa.
Preparação do frasco:
- 2.
- Retirar a tampa de plástico colorida do tipo flip-offdo frasco, empurrando-a suavemente para cima com o polegar.
- Limpar a tampa de borracha com um cotonete com álcool e deixar secar.
- 3.
- Levantar a seringa, retirar a tampa de proteção da agulha e inserir a agulha no centro da tampa de borracha do frasco.
- Empurrar firmemente o êmbolo para despejar todo o solvente no pó.
- Enquanto adiciona o solvente ao frasco, um ligeiro aumento de pressão ocorre. Por isso, é necessário soltar o êmbolo da seringa para que ele suba por cerca de 10 segundos, o que removerá o aumento de pressão no frasco.
NÃO AGITE a solução reconstituída, mas gire-a suavemente até que a solução seja clara.
Na maioria dos casos, o Mensinorm Set se dissolve imediatamente.
Verifique se a solução resultante é clara.
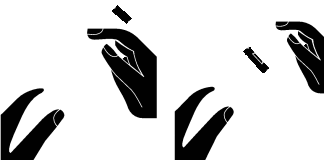

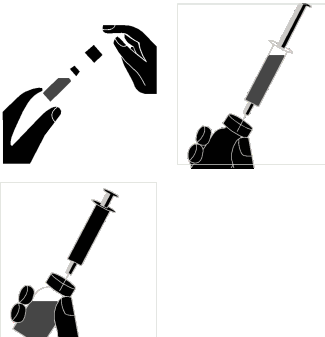
Antes da injeção:
- 4.
- Verifique se a solução resultante é clara, incolor e livre de partículas visíveis a olho nu. NÃO USE se a solução contiver partículas visíveis, estiver turva ou não for incolor.
- Limpe a tampa de borracha do frasco com um cotonete com álcool.
Preparação da injeção:
- 5.
- Pegue uma das seringas para uso único com agulha inserida para administração subcutânea com graduação em UI de FSH/LH, retire a tampa de proteção da agulha e insira a agulha verticalmente no centro da parte superior do frasco.
- Empurre o êmbolo até que seja completamente empurrado.
- Vire o frasco de cabeça para baixo. Certifique-se de que a agulha esteja abaixo da superfície do medicamento e retire a dose prescrita do Mensinorm Set para a seringa de administração.
- Retire a agulha do frasco. Deve segurar a seringa com a agulha apontando para cima e dar leves batidas na lateral da seringa para fazer com que as bolhas de ar subam.
- Empurre lentamente o êmbolo até que uma gota do líquido apareça na ponta da agulha.
LEMBRE-SE: Como o frasco contém medicamento para vários dias de tratamento, é importante garantir que apenas a dose prescrita pelo médico seja retirada.
Administração da injeção
Local da injeção:
- A paciente deve ter sido previamente instruída pelo médico ou enfermeiro sobre a escolha do local no corpo onde a injeção pode ser administrada. Geralmente, o local da injeção é a coxa ou a parte inferior da parede abdominal, abaixo do umbigo.
- Limpe o local da injeção com um cotonete com álcool.
- Com os dedos, pegue firmemente a dobra da pele. Com a outra mão, insira a agulha com um movimento curto e firme em um ângulo de 45° ou 90°.
Administração da solução:
- Administre a solução sob a pele, de acordo com as instruções. Não administre a solução diretamente na veia. Pressione o êmbolo lentamente e a uma velocidade constante, para que a solução seja administrada corretamente e os tecidos da pele ao redor da punção não sejam danificados.
Administre a dose prescrita sem pressa.
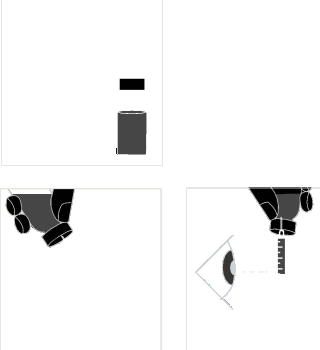
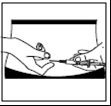
Retire a agulha e pressione o local da injeção com um cotonete com álcool.
Massageie suavemente o local da injeção enquanto pressiona, para ajudar a distribuir o Mensinorm Set e reduzir o desconforto.
Injeções subsequentes:
Repita as injeções subsequentes do Mensinorm Set preparado a partir do passo 4.
Uso de dose maior do que a recomendada do Mensinorm Set:
Os efeitos de uma superdose do Mensinorm Set não são conhecidos, mas é provável que ocorra a síndrome de hiperestimulação ovariana (ver ponto 4 "Efeitos não desejados"). Em caso de administração de dose maior do que a recomendada do Mensinorm Set, deve consultar o médico ou enfermeiro.
Omissão da dose do Mensinorm Set:
A próxima dose do medicamento deve ser administrada no horário planejado. Não deve administrar uma dose dupla para compensar a dose omitida.
Interrupção do tratamento com o Mensinorm Set:
Não deve interromper o tratamento por conta própria. Em caso de dúvidas sobre a continuação do tratamento, deve sempre consultar o médico.
Em caso de dúvidas adicionais sobre a utilização deste medicamento, deve consultar o médico ou farmacêutico.
4. Efeitos não desejados
Como todos os medicamentos, o Mensinorm Set pode causar efeitos não desejados, embora não ocorram em todos.
O efeito não desejado descrito abaixo é grave e requer ação imediata se ocorrer. Em caso de ocorrência do seguinte efeito não desejado, deve interromper a utilização do Mensinorm Set e consultar imediatamente o médico.
Frequente (pode ocorrer em até 1 em cada 10 pessoas):
- Síndrome de hiperestimulação ovariana (sintomas incluem formação de cistos nos ovários ou aumento de cistos existentes, dor na parte inferior do abdômen, sensação de sede, náuseas, vómitos, redução da quantidade de urina concentrada e aumento de peso) (informações adicionais - ver ponto 2 "Informações importantes antes de tomar o Mensinorm Set").
Foram relatados casos de ocorrência dos seguintes efeitos não desejados:
Muito frequente (pode ocorrer em mais de 1 em cada 10 pessoas):
- dor de cabeça,
- abdomen inchado ou distendido.
Frequente (pode ocorrer em até 1 em cada 10 pessoas):
- dor abdominal ou desconforto,
- dor na pélvis,
- dor nas costas,
- sensação de peso,
- desconforto nos seios,
- tontura,
- ondas de calor,
- sensação de sede,
- náuseas,
- fadiga,
- mal-estar geral,
- reação no local da injeção, como dor e inflamação (mais frequente em injeções intramusculares do que subcutâneas).
Raro (pode ocorrer em até 1 em cada 1000 pessoas):
- torção do ovário (rotação do ovário que causa dor abdominal severa),
- doença tromboembólica (formação de um coágulo sanguíneo num vaso sanguíneo, que se desprende e se move com o sangue, bloqueando outro vaso sanguíneo).
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou farmacêutico. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos Médicos e Produtos Biocidas
Al. Jerozolimskie 181C
02-222 Varsóvia
Telefone: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Sítio web: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos não desejados permitirá reunir mais informações sobre a segurança do medicamento.
5. Como conservar o Mensinorm Set
O medicamento deve ser conservado em um local fora do alcance e da vista das crianças.
Não utilize este medicamento após o prazo de validade impresso na embalagem exterior, frasco e seringa-ampola com solvente após: EXP. Se a data de validade for indicada como mês/ano, o prazo de validade é o último dia do mês indicado.
Antes da reconstituição: conservar a uma temperatura de 2-8°C.
Após a reconstituição, a solução pode ser conservada por no máximo 28 dias a uma temperatura não superior a 25°C.
Não congelar antes ou após a reconstituição.
Não utilize o Mensinorm Set se notar turvação da solução. Após a reconstituição, a solução deve ser clara e incolor.
Os medicamentos não devem ser jogados na canalização ou em lixeiras domésticas. Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o Mensinorm Set
A substância ativa do medicamento é a menotropina.
Cada frasco multidose contém um pó liofilizado que contém 900 UI de hormona folículo-estimulante humana (FSH) e 900 UI de hormona luteinizante humana (LH).
A gonadotropina menopáusica humana (HMG) é obtida a partir da urina de mulheres pós-menopáusicas. Para aumentar a atividade total de LH, foi adicionada gonadotropina coriônica humana (hCG) - um hormônio obtido a partir da urina de mulheres grávidas.
Excipientes
Pó: lactose monoidratada, polissorbato 20, fosfato dissódico diidratado, ácido fosfórico, hidróxido de sódio.
Solvente: m-cresol, água para injeção.
Como é o Mensinorm Set e que conteúdo tem a embalagem
Pó: disco ou pó liofilizado branco
Solvente: solução clara e incolor
O Mensinorm Set é um pó e solvente para solução injetável, embalados em uma caixa de cartão.
1 conjunto contém os seguintes componentes:
- 1 frasco que contém o pó do Mensinorm Set;
- 1 seringa-ampola que contém o solvente para reconstituição;
- 1 agulha para reconstituição;
- 12 cotonetes com álcool para injeções;
- 12 seringas para uso único com agulhas inseridas para injeções.
Titular da autorização de comercialização e fabricante:
IBSA Farmaceutici Italia srl
Via Martiri di Cefalonia, 2
26900 Lodi
Itália
Para obter informações mais detalhadas, deve contatar o representante local do titular da autorização de comercialização:
IBSA Poland Sp. z o.o.
Al. Jana Pawła II 29
00-867 Varsóvia
telefone: +48 22 653 68 60
Este medicamento está autorizado para comercialização nos Estados-membros da Área Económica Europeia e no Reino Unido (Irlanda do Norte) sob os seguintes nomes: (a força e forma farmacêutica são idênticas em todos os países, apenas o nome comercial muda)
Áustria: Meriofert PFS
Bélgica: Fertinorm Kit
Bulgária: Meriofert PFS
Chipre: Meriofert PFS
República Checa: Meriofert Set
Dinamarca: Meriofert Set
Estônia: Meriofert Set
Finlândia: Meriofert Set
França: Fertistartkit
Grécia: Meriofert
Espanha: Meriofert Kit
Países Baixos: Meriofert spuit
Lituânia: Meriofert Set
Luxemburgo: Fertinorm Kit
Letônia: Meriofert Set
Noruega: Meriofert Set
Polônia: Mensinorm Set
Romênia: Meriofert PFS
Eslováquia: Meriofert Kit
Suécia: Meriofert Set
Hungria: Meriofert Kit
Reino Unido (Irlanda do Norte): Meriofert PFS
Itália: Meriofert
Data da última atualização do folheto:maio de 2024
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorIBSA Farmaceutici Italia S.r.l.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Mensinorm SetForma farmacêutica: Pó, 75 UI FSH + 75 UI LHSubstância ativa: human menopausal gonadotrophinFabricante: Ferring GmbHRequer receita médicaForma farmacêutica: Pó, 600 UI FSH + 600 UI LHSubstância ativa: human menopausal gonadotrophinRequer receita médicaForma farmacêutica: Pó, 1200 UI FSH + 1200 UI LHSubstância ativa: human menopausal gonadotrophinRequer receita médica
Alternativas a Mensinorm Set noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Mensinorm Set em Espanha
Alternativa a Mensinorm Set em Ukraine
Médicos online para Mensinorm Set
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Mensinorm Set – sujeita a avaliação médica e regras locais.







