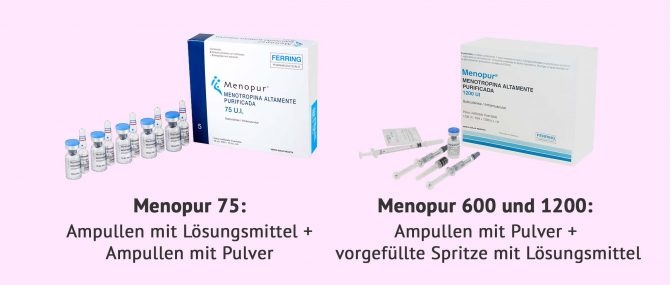
Como usar Menopur
folheto PARA O DOENTE
Para Uso Interno - Interno
Folheto anexado à embalagem: informação para o doente
MENOPUR 1200 IU solução injectável em injetor
Menotropina
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder reler quando necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto:
- 1. O que é MENOPUR e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento MENOPUR
- 3. Como tomar MENOPUR
- 4. Efeitos não desejados
- 5. Como conservar MENOPUR
- 6. Conteúdo da embalagem e outras informações
1. O que é MENOPUR e para que é utilizado
MENOPUR é uma solução injectável em injetor semi-automático. A injeção é administrada por via subcutânea (injeção subcutânea) - geralmente na barriga.
MENOPUR contém menotropina, que é uma mistura de dois hormônios naturais chamados:
- hormona folículo-estimulante (FSH) e
- hormona luteinizante (LH). Eles permitem o funcionamento normal dos órgãos do aparelho reprodutor. Os hormônios FSH e LH presentes na menotropina são obtidos a partir da urina de mulheres pós-menopáusicas.
Para que é utilizado o MENOPUR
O Menopur é utilizado no tratamento de mulheres que não conseguem engravidar, nas seguintes situações:
em mulheres que não conseguem engravidar porque os ovários não produzem óvulos
(também no caso da chamada síndrome dos ovários policísticos). O MENOPUR é utilizado em mulheres,
que, para o tratamento da infertilidade, já receberam um medicamento chamado "citrato de clomifeno", mas o medicamento
se revelou ineficaz;
em mulheres que participam em programas de reprodução assistida, tais como:
fecundação in vitro (FIV, em inglês in vitro fertilisation) ou transferência de embrião (ET,
em inglês embryo transfer),
transferência de gametas para o oviduto (GIFT, em inglês gamete intra-fallopian transfer),
injeção intracitoplasmática de espermatozoides no óvulo (ICSI, em inglês intracytoplasmic sperm injection).
Como funciona o MENOPUR
O MENOPUR ajuda a produzir vários folículos ovarianos nos ovários, onde os óvulos podem
desenvolver-se. Isso é chamado de desenvolvimento de vários folículos ovarianos.
Para Uso Interno - Interno
2. Informações importantes antes de tomar o medicamento MENOPUR
O que deve verificar antes de começar a tomar o medicamento MENOPUR
Antes de começar a tomar o medicamento MENOPUR, o médico deve avaliar as causas
dos distúrbios da fertilidade em ambos os parceiros. Deve verificar especialmente se não existem as seguintes
doenças, que exigem um tratamento diferente e adequado:
hipotireoidismo e hipoadrenalismo;
concentração elevada de um hormônio chamado prolactina - chamado de hiperprolactinemia;
tumores da glândula pituitária - um órgão localizado na base do cérebro;
tumores do hipotálamo - uma área localizada sob a parte do cérebro chamada tálamo.
Se o doente tiver alguma das doenças mencionadas acima, deve informar
o médico antes de começar o tratamento com o medicamento MENOPUR.
Quando não tomar o medicamento MENOPUR
se o doente tiver alergia à menotropina ou a qualquer um dos outros componentes deste medicamento
(listados no ponto 6);
se o doente tiver tumores do útero, ovários, seios ou partes do cérebro, como
a glândula pituitária ou hipotálamo;
se o doente tiver cistos ovarianos ou aumento dos ovários - não causados
pela síndrome dos ovários policísticos;
se o doente tiver malformações do útero ou de outros órgãos genitais;
se o doente tiver sangramentos vaginais de causa desconhecida;
se o doente tiver miomas uterinos - são tumores no útero que não são
câncer;
se o doente estiver grávida ou amamentando.
Advertências e precauções Síndrome de Hiperestimulação Ovariana (OHSS)
Um efeito não desejado grave deste medicamento, especialmente em mulheres com síndrome dos ovários policísticos, é a "síndrome de hiperestimulação ovariana" ou "OHSS" (ver ponto 4).
Deve informar imediatamente o médico se o doente apresentar sintomas de OHSS, mesmo que:
- tenha passado alguns dias desde a última administração do medicamento
- o doente tenha parado de tomar o medicamento MENOPUR. Pode ser um sinal de atividade ovariana excessiva, o que pode ter um curso grave. Nesse caso, o médico interromperá o tratamento com o medicamento MENOPUR e iniciará o tratamento adequado no hospital.
A observância da dose prescrita e a monitorização cuidadosa do tratamento reduzem
a probabilidade de ocorrência desses sintomas.
Exames e testes
Durante o tratamento com este medicamento, o médico geralmente encaminha o doente para exames de ultrassom (USG)
e, às vezes, para exame de sanguepara verificar a resposta ao tratamento.
Riscos associados à gravidez
O tratamento com hormônios, como o MENOPUR, pode aumentar o risco de:
gravidez ectópica (fora do útero) em mulheres com doenças dos tubos uterinos previamente diagnosticadas;
aborto;
gravidez múltipla (gêmeos, trigêmeos, etc.);
defeitos físicos presentes no bebê ao nascimento (defeitos congênitos).
Em algumas mulheres tratadas por infertilidade, desenvolveram-se tumores ovarianos ou de outros
órgãos do aparelho reprodutor. Até o momento, não se sabe se isso foi causado pelo tratamento
com hormônios como o MENOPUR.
Para Uso Interno - Interno
Coágulos sanguíneos
A probabilidade de ocorrência de coágulos nos vasos sanguíneos ou artérias é maior em mulheres grávidas. O tratamento da infertilidade pode aumentar a probabilidade de coágulos, especialmente se:
o doente tiver excesso de peso;
o doente tiver uma doença de coagulação sanguínea "trombofilia";
coágulos ocorreram previamente ou em alguém da família do doente.
O doente deve informar o médico se achar que isso se aplica a ele.
Crianças e adolescentes
O uso do produto medicamentoso MENOPUR em crianças e adolescentes não é apropriado.
MENOPUR e outros medicamentos
Deve informar o médico sobre todos os medicamentos que o doente está tomando atualmente ou
recentemente, bem como sobre os medicamentos que o doente planeja tomar.
O citrato de clomifeno é outro medicamento utilizado no tratamento da infertilidade. Se o MENOPUR
for administrado ao mesmo tempo que o citrato de clomifeno, o efeito nos ovários pode ser aumentado.
Gravidez e amamentação
O medicamento MENOPUR não deve ser utilizado durante a gravidez ou amamentação.
Condução de veículos e operação de máquinas
É pouco provável que o MENOPUR afete a capacidade de conduzir veículos
e operar máquinas.
Informações importantes sobre alguns componentes do medicamento MENOPUR
O MENOPUR contém menos de 1 mmol de sódio (23 mg) por dose, ou seja, o medicamento é considerado
essencialmente "livre de sódio".
3. Como tomar MENOPUR
Este medicamento deve ser sempre utilizado de acordo com as recomendações do médico. Em caso de dúvidas, deve consultar o médico.
Mulheres que não produzem óvulos (não ovulam)
O tratamento deve começar dentro dos primeiros 7 dias do ciclo menstrual.
Dia 1. é o primeiro dia da menstruação.
O medicamento deve ser administrado diariamente durante pelo menos 7 dias.
Qual é a dose de MENOPUR a ser utilizada?
A dose inicial é geralmente de 75 IU (unidades internacionais, em inglês International Units) a
150 IU por dia.
Dependendo da resposta do doente, a dose pode ser aumentada - até um máximo de 225 IU.
A dose determinada deve ser administrada durante pelo menos 7 dias, antes de qualquer alteração da dose pelo
médico.
Recomenda-se que, a cada alteração, a dose seja aumentada em 37,5 IU, mas não mais de 75 IU.
O médico verificará os resultados do tratamento com o medicamento MENOPUR. O ciclo de tratamento deve ser interrompido se, após 4 semanas, não for detectada resposta ao tratamento.
Quando a resposta ao tratamento com o medicamento MENOPUR for satisfatória:
O doente receberá uma injeção única de um hormônio chamado "gonadotropina coriônica humana" (hCG).
A dose será de 5 000 IU a 10 000 IU.
O doente receberá hCG no dia seguinte à última injeção do medicamento MENOPUR.
Para Uso Interno - Interno
Recomenda-se que o doente tenha relações sexuais no dia da administração e no dia seguinte à administração do hCG.
Alternativamente, pode ser realizada uma inseminação (administração de sêmen diretamente no útero).
O doente permanecerá sob observação cuidadosa do médico por pelo menos 2 semanas.
Quando não houver resposta ao tratamento com o medicamento MENOPUR:
O médico verificará os resultados do uso do medicamento MENOPUR.
Dependendo do progresso do tratamento, o médico pode decidir interromper a administração do medicamento
MENOPUR e não administrar o hCG.
Mulheres que participam de programas de reprodução assistida
As pacientes que participam de um programa de reprodução assistida também receberão um medicamento que ajuda a estimular o hormônio chamado "hormônio liberador de gonadotropinas", em inglês Gonadotropin Releasing
Hormone– GnRH. Este medicamento é chamado de "agonista de GnRH". A administração do medicamento Menopur deve
ser iniciada cerca de 2 semanas após o início do tratamento com o agonista de GnRH.
A paciente também pode receber um medicamento chamado "antagonista de GnRH".
A administração do medicamento MENOPUR deve ser iniciada no 2. ou 3. dia do ciclo menstrual (1. dia
de sangramento menstrual é o 1. dia do ciclo).
Qual é a dose de MENOPUR a ser utilizada?
O medicamento MENOPUR deve ser administrado diariamente durante pelo menos 5 dias.
A dose inicial do medicamento Menopur é geralmente de 150 a 225 IU.
Dependendo da resposta da paciente ao tratamento, a dose pode ser aumentada até um máximo de 450 IU por dia.
Não deve aumentar a dose de uma vez por mais de 150 IU.
Geralmente, o tratamento não deve durar mais de 20 dias.
Após a detecção de um número suficiente de folículos ovarianos de tamanho apropriado, a paciente
receberá uma injeção única do medicamento hCG em uma dose de até 10 000 IU para induzir a ovulação
(liberação do óvulo).
A paciente permanecerá sob observação cuidadosa do médico por pelo menos 2 semanas após a administração do hCG.
O médico verificará os resultados do uso do medicamento MENOPUR.
Dependendo do progresso do tratamento, o médico pode decidir interromper a administração do medicamento
MENOPUR e não administrar o hCG.
Nesse caso, a paciente será informada sobre a necessidade de usar um método anticoncepcional mecânico (por exemplo, preservativo).
Caso contrário, deve abster-se de relações sexuais até a próxima menstruação.
Administração do medicamento MENOPUR
Deve seguir muito atentamente as "Instruções de uso" fornecidas com a embalagem do injetor.
A primeira injeção do medicamento MENOPUR deve ser realizada sob supervisão do médico ou enfermeira.
O médico decidirá se a paciente pode realizar as injeções subsequentes sozinha em casa - após treinamento completo.
O MENOPUR será administrado por injeção subcutânea (injeção subcutânea), geralmente na barriga. Cada injetor pré-enchido pode ser usado para várias injeções.
Uso de dose maior do que a recomendada do medicamento MENOPUR
Em caso de uso de dose maior do que a recomendada do medicamento MENOPUR, deve informar o médico.
Para Uso Interno - Interno
Omissão da administração do medicamento MENOPUR
Não deve tomar uma dose dupla para compensar a dose omitida. Em caso de omissão da administração do medicamento MENOPUR, deve informar o médico.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não ocorram em todos.
Para Uso Interno - Interno
Efeitos não desejados graves
Síndrome de Hiperestimulação Ovariana (OHSS)
Deve informar imediatamente o médico,se o doente apresentar algum dos seguintes
sintomas, que podem ser sintomas de OHSS:
dor abdominal ou inchaço abdominal;
mal-estar (sensação de estar doente)
diarreia;
aumento de peso;
dificuldade para respirar
redução da frequência de urinação.
Em caso de ocorrência de algum desses sintomas, deve entrar em contato com o médico imediatamente, mesmo que o sintoma ocorra alguns dias após a administração da última dose do medicamento ou se
o doente parou de tomar o medicamento MENOPUR.O doente pode precisar de atendimento médico de emergência. Esses efeitos não desejados podem ser um sinal de atividade ovariana excessiva, conhecida como síndrome de hiperestimulação ovariana (OHSS). Em casos graves de OHSS, ocorreram complicações, como acúmulo de líquido na cavidade abdominal, cavidade pélvica ou cavidade pleural, dificuldade para respirar e redução da frequência ou quantidade de urina eliminada, formação de coágulos sanguíneos nos vasos sanguíneos (distúrbios tromboembólicos) e torção do ovário.
Reações alérgicas (hipersensibilidade)
Deve informar imediatamente o médico se ocorrer:
erupção cutânea;
coceira;
inchaço da garganta e dificuldade para respirar.
Em caso de ocorrência de algum desses sintomas, deve entrar em contato com o médico imediatamente.
Outros efeitos não desejados
Os seguintes efeitos não desejadosocorrem frequentemente, ou seja, em 1 a 10 em cada 100 doentes tratados:
dor de cabeça;
sensação de náusea (enjoo);
dor ou inchaço abdominal;
dor na região pélvica;
reações no local da injeção, como dor, vermelhidão, inchaço, coceira ou hematoma.
Os seguintes efeitos não desejadosocorrem menos frequentemente, ou seja, em 1 a 10 em cada 1000 doentes tratados:
vômito;
problemas abdominais;
diarreia;
fadiga;
tontura;
cistos ovarianos (cistos cheios de líquido nos ovários);
problemas mamários, incluindo dor mamária, sensibilidade mamária, desconforto, dor nos mamilos e inchaço mamário;
ondas de calor.
Para Uso Interno - Interno
Os seguintes efeitos não desejadosocorrem raramente, ou seja, em 1 a 10 em cada 10 000 doentes tratados:
acne.
Além dos mencionados acima, foram observados outros efeitos não desejados, cuja
frequênciade ocorrência é desconhecida:
distúrbios da visão;
febre;
mal-estar;
aumento de peso;
dor muscular e articular;
torção do ovário, como uma complicação da hiperestimulação ovariana induzida pela estimulação excessiva;
urticária;
coágulos sanguíneos, como uma complicação da hiperestimulação ovariana induzida pela estimulação excessiva.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico. Os efeitos não desejados podem ser notificados diretamente ao
Departamento de Monitoramento de Efeitos Não Desejados de Produtos Medicinais da Agência Reguladora de Produtos Medicinais:
Aleje Jerozolimskie 181C, 02-222 Varsóvia
Tel: +48 22 49 21 301
Fax: +48 22 49 21 309
site na internet: https://smz.ezdrowie.gov.pl .
Os efeitos não desejados também podem ser notificados ao responsável pelo produto.
5. Como conservar MENOPUR
O medicamento deve ser conservado em um local não visível e inacessível às crianças.
Não use este medicamento após a data de validade impressa na etiqueta do injetor pré-enchido e na caixa de papelão após "EXP". A data de validade é o último dia do mês indicado.
Antes de usar:
Conservar na geladeira a uma temperatura entre 2°C e 8°C.
Não congelar.
Após a abertura:
Use cada injetor semi-automático dentro de 28 dias após a abertura. Conservar a uma temperatura abaixo de 25 °C.
O injetor deve ser sempre conservado com a tampa colocada para protegê-lo da luz.
Os medicamentos não devem ser jogados na canalização ou nos lixos domésticos. Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais utilizados. Esse procedimento ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
Para Uso Interno - Interno
O que contém o MENOPUR
- O princípio ativo do medicamento é a menotropina altamente purificada (gonadotropina menopáusica humana, hMG)
MENOPUR 1200 IU solução injectável em injetor:
Um injetor semi-automático pré-enchido contém menotropina na quantidade equivalente a 1200
IU de FSH (hormona folículo-estimulante) e 1200 IU de LH (hormona luteinizante).
Os outros componentes são:
Fenol
Metionina
Cloridrato de arginina
Polissorbato 20
Hidróxido de sódio
Ácido clorídrico diluído
Água para injeção
Como é o MENOPUR e o que contém a embalagem
O MENOPUR é uma solução injectável transparente e incolor em injetor.
MENOPUR 1200 IU solução injectável em injetor semi-automático está disponível em embalagens contendo 1 injetor e 21 agulhas para injeção.
Responsável e importador:
Ferring GmbH
Wittland 11, D-24109 Kiel, Alemanha
Representante local do responsável:
Ferring Pharmaceutical Portugal, Unipessoal Lda.
Rua do Polo Norte, 18 - Quinta da Fonte
2774-004 Paço de Arcos
Tel.: + 351 214 416 150
Este medicamento está autorizado para comercialização nos Estados-Membros do Espaço Econômico Europeu sob as seguintes denominações:
Este medicamento está autorizado para comercialização nos Estados-Membros do Espaço Econômico Europeu sob as seguintes denominações:
Bélgica, República Checa, Irlanda, Luxemburgo, Eslováquia: Menotropin Ferring
Bulgária, Croácia, Chipre, Dinamarca, Estônia, Finlândia, Grécia, Hungria, Islândia, Letônia, Lituânia, Malta,
Noruega, Polônia, Portugal, Romênia, Eslovênia, Espanha, Suécia: Menopur
Alemanha: Menogon HP
Itália: Meropur
Data da última revisão do folheto:julho de 2024
Para Uso Interno - Interno
Instruções de uso
MENOPUR injetor semi-automático
Menotropinum, solução injectável

Antes da primeira injeção, um profissional de saúde (médico, enfermeira ou farmacêutico)
deve demonstrar como preparar e injetar corretamente o medicamento MENOPUR.
Deve ler atentamente o conteúdo desta instrução antes de usar o injetor MENOPUR e sempre que receber um novo injetor. Pode haver novas informações.
Deve seguir completamente as instruções, mesmo que tenha usado um injetor semelhante anteriormente. O uso inadequado do injetor pode resultar na administração de uma dose incorreta do medicamento.
Em caso de dúvidas sobre a injeção do medicamento MENOPUR, deve entrar em contato com um profissional de saúde.
O injetor MENOPUR é um injetor semi-automático com ajuste de dose, que permite a administração de mais de 1 dose do medicamento MENOPUR. Os números visíveis na janela de dose correspondem ao número de unidades internacionais (UI) do medicamento MENOPUR. Estão disponíveis 2 versões diferentes do injetor com diferentes potências:
- 600 UI
- 1200 UI
Injetor semi-automático MENOPUR e seus componentes
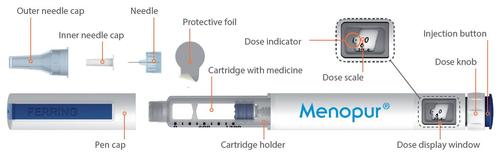
Instruções de uso - Injetor semi-automático MENOPUR
Para Uso Interno - Interno
Informações importantes
- O injetor MENOPUR e as agulhas são para uso exclusivo de uma pessoa e não devem ser emprestados a outros.
- O injetor deve ser usado apenas para a doença para a qual foi prescrito e de acordo com as recomendações do médico.
- Pessoas cegas ou com visão reduzida que não possam ler a escala de doses na janela de dose não devem usar este injetor sem ajuda. Essas pessoas devem pedir ajuda a alguém com visão boa que tenha sido treinado no uso do injetor.
Informações sobre o injetor MENOPUR
O injetor permite ajustar doses de 6,25 UI a 450 UI do medicamento MENOPUR, em incrementos definidos de 6,25 UI.
- A escala de doses do injetor tem uma marcação numérica de 0 a 450 UI.
- O movimento de um incremento de dose marcado para o próximo incremento de dose não marcado aumenta ou diminui a dose em 6,25 UI, dependendo se está aumentando ou diminuindo a dose. Ver "Exemplos ilustrando como ajustar a dose" nas páginas 20 a 21.
- Ao girar o botão de ajuste de dose para ajustar a dose, é possível ouvir um clique e sentir uma resistência no botão. Isso ajuda a ajustar a dose correta.
Limpeza
- Se necessário, a superfície externa do injetor pode ser limpa com um pano umedecido com água.
- Não mergulhe o injetor em água ou qualquer outro líquido.
Conservação
- Não congelar.
- Antes de usar, conservar o injetor na geladeira a uma temperatura entre 2°C e 8°C.
- Após a primeira uso, o injetor pode ser conservado por até 28 dias a uma temperatura abaixo de 25°C.
- Always conservar o injetor com a tampa colocada e sem a agulha.
- Não use o injetor após a data de validade (EXP), que está impressa na etiqueta. A data de validade é o último dia do mês indicado.
- Não conservar o injetor em temperaturas extremas, nem em locais expostos à luz solar direta ou a temperaturas muito baixas, como em um carro ou congelador. Conservar o injetor em um local inacessível às crianças.
Materiais necessários para a injeção do medicamento MENOPUR
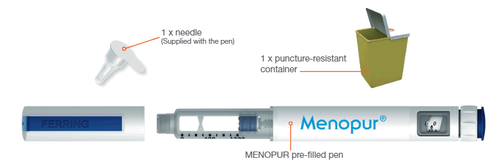
Para Uso Interno - Interno
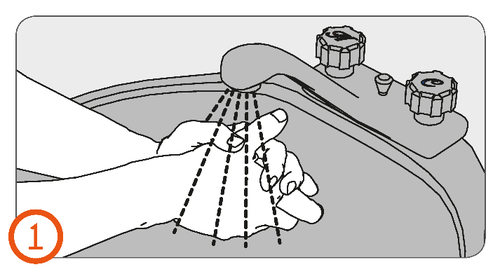
Antes de usar – (Passo 1)
1.
- Lavar as mãos.
- Verificar se está usando o injetor com a potência correta do medicamento.
- Verificar a data de validade na etiqueta do injetor.
Colocação da agulha – (Passos 2 a 6)
Importante:
- Use sempre uma agulha nova para cada injeção.
- Use apenas agulhas descartáveis com mecanismo de travamento, fornecidas com o injetor.

Para Uso Interno - Interno
2.
- Remover a tampa do injetor.
- Verificar se o injetor não está danificado.
- Verificar se a solução é transparente e não contém partículas sólidas não dissolvidas.
- Não use o injetor se estiver danificado, contiver partículas sólidas no frasco ou a solução estiver turva.
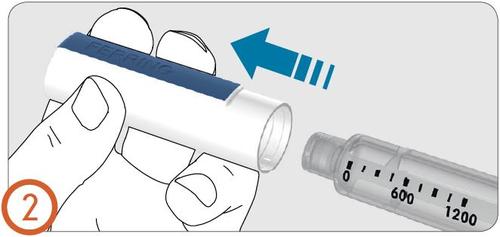
3.
- Remover a cobertura protetora da agulha.
Para Uso Interno - Interno
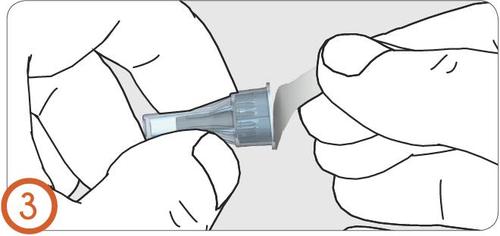
4.
- Insira a agulha no injetor.
- Quando a agulha estiver seguramente fixada, deve ser possível ouvir um clique ou sentir uma resistência.
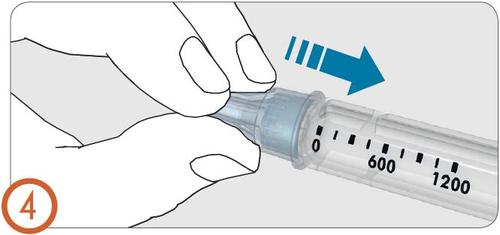
5.
- Remover a cobertura externa da agulha.
- Nãodescartar a cobertura externa da agulha . Ela será necessária para remover e descartar a agulha após a injeção.
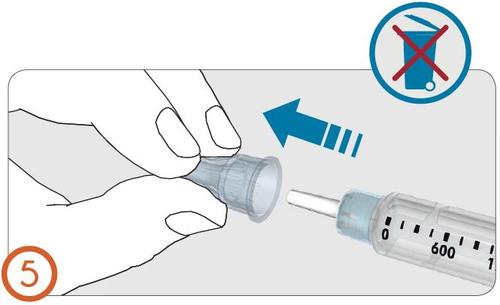
6.
- Remover e descartar a cobertura interna da agulha.
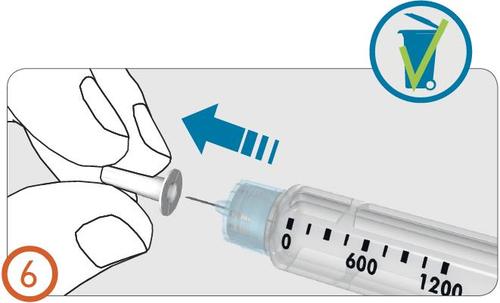
Remoção de bolhas de ar – (Passos 7 a 9)
- Antes de usar o injetor pela primeira vez, é necessário remover as bolhas de ar do frasco para garantir que a dose possa ser ajustada corretamente.
- A ventilação é realizada apenas antes do primeiro uso do injetor.
- Deve realizar os Passos 7 a 9, mesmo que não veja bolhas de ar.
- Se o injetor já foi usado anteriormente , vá diretamente para o Passo 10 .
7.
- Girar o botão de ajuste de dose no sentido horário até que o símbolo de gota se alinhe com o indicador de dose.
Para Uso Interno - Interno
- Se a dose ajustada para a ventilação do injetor for incorreta, a dose pode ser corrigida para cima ou para baixo sem perda de medicamento, girando o botão de ajuste de dose em qualquer direção até que o símbolo de gota se alinhe com o indicador de dose.
Indicador de dose
Símbolo de gota
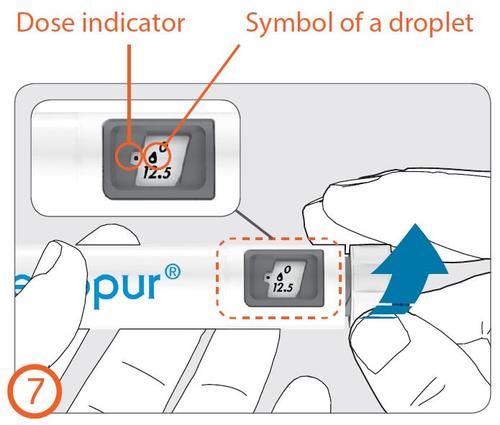
Indicador de dose
Símbolo de gota
8.
- Segurar o injetor na vertical com a agulha apontando para cima.
- Bater levemente com o dedo na câmara do frasco para que as bolhas de ar no frasco sejam direcionadas para a parte superior do frasco.
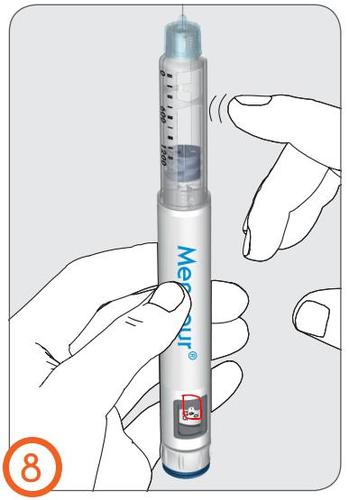
9.
- Segurando o injetor com a agulha ainda apontando para cima (longe do rosto), pressione completamente o botão de injeção até que o número "0" se alinhe com o indicador de dose .
- Verificar se uma gota de líquido apareceu na ponta da agulha .
Para Uso Interno - Interno
- Se não aparecer uma gota, repetir os Passos 7 a 9 (ventilação), até que a gota apareça.
- Se, após 5 tentativas, a gota ainda não aparecer, remover a agulha (ver Passo 13.), colocar uma nova agulha (ver Passos 3 a 6.) e repetir a ventilação (ver Passos 7 a 9.).
- Se, após a troca da agulha, a gota ainda não aparecer, experimente um novo injetor.
Ajuste da dose - (Passo 10)
- Girar o botão de ajuste de dose no sentido horário até que a dose prescrita se alinhe com o indicador de dose na janela de dose.
- A dose pode ser ajustada para cima ou para baixo sem perda de medicamento, girando o botão de ajuste de dose em qualquer direção até que a dose correta se alinhe com o indicador de dose.
- Não pressione o botão de injeção enquanto ajusta a dose para evitar perda de medicamento. Ver "Exemplos ilustrando como ajustar a dose" nas páginas 20 a 21 .
Divisão da dose:
- Às vezes, é necessário usar mais de um injetor para administrar a dose prescrita completa.
- Se não for possível ajustar a dose completa no injetor, isso significa que não há medicamento suficiente no injetor para administrar a dose completa. Será necessário realizar injeções de dose dividida ou descartar (eliminar) o injetor atual e usar um novo injetor para a injeção.
Ver “Administração de dose dividida do medicamento MENOPUR” nas páginas 22 a 23
Indicador de dose
Janela de exibição
da dose
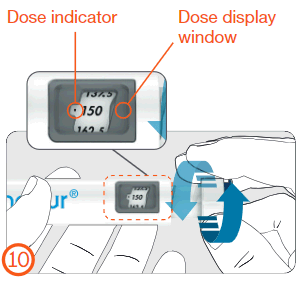
Para Uso Interno - Interno
Para Uso Interno - Interno
onde são fornecidos exemplos de como calcular e registrar a dose dividida.
Injeção da dose – (Passos 11 e 12)
Importante:
- Leia a descrição dos Passos 11 e 12 nas páginas 14 a 15 antes de realizar a injeção.
- O medicamento deve ser injetado sob a pele (subcutâneo) na barriga, na área do estômago .
- Cada injeção subsequente deve ser realizada em um local diferente para reduzir o risco de reações na pele, como vermelhidão e irritação.
- Não injete em um local que seja doloroso (sensível), azul, vermelho, endurecido, cicatricial ou com estrias.
11.
- Segurar o injetor de modo que a janela de dose seja visível durante a injeção.
- Pegar um dobra da pele e inserir a agulha reta na pele, como demonstrado pelo profissional de saúde. Não pressione o botão de injeção ainda. (Ver Figura 11.).
- Colocar o polegar no botão de injeção.
- Pressionar completamente o botão de injeção e segurar .
- Segurar o botão de injeção pressionado e, quando o número "0" se alinhar com o indicador de dose , contar lentamente até 8 (oito) (Ver Figura 12.) . Isso garante que a dose completa tenha sido administrada.
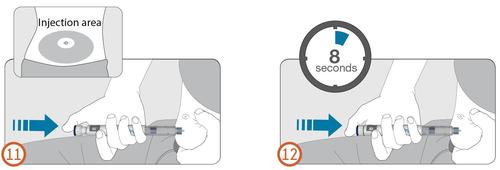
segundos
12.
- Após segurar o botão de injeção pressionado por 8 segundos, soltar o botão de injeção. Em seguida, remover a agulha lentamente do local da injeção, puxando-a reta para fora da pele.
- Se houver sangue no local da injeção, pressione suavemente um pedaço de gaze ou uma bola de algodão sobre o local da injeção.
Atenção:
- Não incline o injetor durante a injeção e remoção da agulha da pele.
- Inclinar o injetor pode causar a flexão ou quebra da agulha.
- Se a agulha quebrar e ficar presa no corpo ou sob a pele, procure imediatamente atendimento médico.
Remoção da agulha - (Passo 13)
13.
Para Uso Interno - Interno
- Colocar cuidadosamente a cobertura externa da agulha, pressionando-a firmemente (Ver Figura 13 A ).
- Desrosquear a agulha, girando-a no sentido anti-horário, para desconectá-la do injetor (Ver Figuras 13 B e 13 C ).
- Descartar a agulha usada com cuidado (Ver Figura 13 D ).
- Ver "Eliminação" na página 18 .
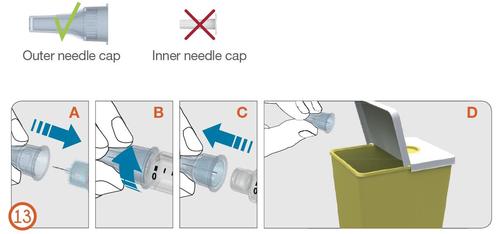
Cobertura externa da agulha
Cobertura interna da agulha
Atenção:
- Após cada uso, sempre remover a agulha. As agulhas são para uso único.
- Não armazenar o injetor com a agulha colocada.
Colocação da tampa do injetor - (Passo 14)
14.
- Colocar firmemente a tampa no injetor para protegê-lo durante as pausas entre as injeções.
Atenção:
- A tampa do injetor não cabe na agulha.
- Quando o injetor não estiver em uso, deve ser protegido com a tampa.
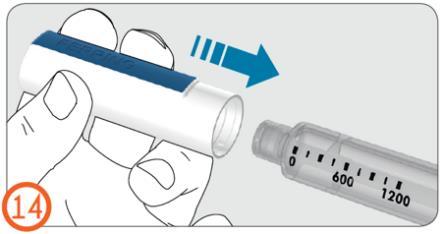
Eliminação
Agulhas:
As agulhas usadas devem ser colocadas imediatamente em um recipiente resistente a perfurações, como um recipiente para objetos cortantes, após o uso.
Para Uso Interno - Interno
Se não tiver um recipiente para objetos cortantes, pode usar um recipiente que atenda a todos os requisitos abaixo:
- é feito de plástico resistente,
- pode ser fechado hermeticamente com uma tampa resistente a perfurações para evitar que os objetos cortantes caiam,
- fica de pé e estável durante o uso,
- é resistente a vazamentos, e
- está adequadamente rotulado com um aviso de resíduos perigosos dentro do recipiente.
O recipiente para objetos cortantes deve ser descartado quando estiver quase cheio. Deve perguntar ao médico, enfermeira ou farmacêutico sobre o método correto de eliminação. Não descartar o recipiente cheio de objetos cortantes no lixo doméstico, a menos que as regulamentações locais permitam. Não descartar o medicamento no sistema de esgoto ou em recipientes de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais utilizados. Esse procedimento ajudará a proteger o meio ambiente.
Injetores MENOPUR:
- Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais utilizados.
Nas páginas seguintes, você pode encontrar mais informações sobre os seguintes tópicos
:
- Exemplos ilustrando como ajustar a dose.................. página 20 a 21
- Administração de dose dividida do medicamento MENOPUR.................. página 22
- Doses divididas .................................................. página 23
E também:
- Perguntas frequentes……………........................... página 24
- Advertências............................................................................ página 25
- Contato.................................................................................. página 25
Exemplos ilustrando como ajustar a dose
Exemplos ilustrando como ajustar a dose no injetor MENOPUR.
A tabela à direita apresenta exemplos de doses prescritas, como ajustar as doses prescritas e a aparência da janela de dose para as doses prescritas.

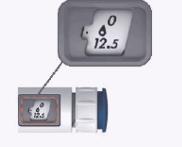
Para Uso Interno - Interno





Administração de dose dividida do medicamento MENOPUR
Se não for possível ajustar a dose completa no injetor, isso significa que não há medicamento suficiente no injetor para administrar a dose completa. Será necessário realizar injeções de dose dividida ou descartar (eliminar) o injetor atual e usar um novo injetor para a injeção. Alternativamente, pode descartar (eliminar) o injetor atual e usar um novo injetor para administrar a dose completa em 1 injeção. Se optar pelo método de injeção de dose dividida, siga as instruções abaixo e registre as quantidades de medicamento a serem administradas, como mostrado no diário de doses divididas na página 23 .
- A Coluna A apresenta exemplos de doses prescritas. Registre a dose prescrita na Coluna A .
- A Coluna B apresenta exemplos de valores de dose que restam no injetor (é igual ao valor que pode ser ajustado no injetor).
- Registre o valor da dose que resta no injetor na Coluna B . Realize a injeção, usando o medicamento restante no injetor.
- Prepare e ventile um novo injetor (Passos 1 a 9.).
- Calcule e registre a dose restante a ser injetada na Coluna C , subtraindo o valor da Coluna B do valor da Coluna A . Se necessário, verifique os cálculos em uma calculadora.
- Se necessário, ver "Exemplos ilustrando como ajustar a dose" nas páginas 20 a 21 .
- Em caso de dúvidas sobre o cálculo da dose dividida, entre em contato com um profissional de saúde.
- Administre a dose restante do medicamento (valor da Coluna C ), usando o novo injetor, para completar a dose prescrita.
Diário de doses divididas
Perguntas mais frequentes
Para uso interno - Interno
- 1. É necessário ventilar a seringa antes de cada injeção?
- Não. A ventilação deve ser realizada apenas antes da primeira injeção com uma seringa nova.
- 2. Como saber que a injeção terminou?
- O botão de administração da dose é pressionado até o fim.
- O número "0" é exibido na linha com o indicador de dose.
- Contar lentamente até 8, segurando o botão de administração da dose pressionado com a agulha ainda inserida sob a pele.
- 3. Por que é necessário contar até 8 enquanto segura o botão de administração da dose pressionado?
- Segurar o botão de administração da dose por 8 segundos permite a injeção da dose completa e sua absorção sob a pele.
- 4. E se os controles de ajuste da dose não puderem ser ajustados para a dose necessária?
- O cartucho na seringa pode não conter quantidade suficiente de medicamento para administrar a dose prescrita.
- A seringa não permite ajustar uma dose maior do que a dose restante no cartucho.
- Pode-se injetar o medicamento restante na seringa e completar a administração da dose prescrita usando uma seringa nova (dose dividida) ou usar uma seringa nova para administrar a dose prescrita completa.
- 5. O que fazer se não tiver agulhas suficientes?
- Se precisar de agulhas adicionais, deve contatar o médico. Deve usar apenas agulhas fornecidas com a seringa MENOPUR ou prescritas pelo médico.
Advertências
- Não usar a seringa que foi derrubada ou atingida em uma superfície dura.
- Se o botão de administração da dose não for fácil de pressionar, não force. Deve trocar a agulha. Se o botão de administração da dose ainda não for fácil de pressionar após trocar a agulha, deve usar uma seringa nova.
- Não tentar reparar a seringa danificada. Se a seringa estiver danificada, deve contatar um profissional de saúde ou o representante local da entidade responsável.
Contacto
Em caso de alguma dúvida ou problema relacionado à seringa, deve contatar um profissional de saúde ou o representante da entidade responsável.
O representante local da entidade responsável:
Ferring Pharmaceutical Poland Sp. z o.o.
rua Szamocka 8
01-748 Varsóvia
Tel.: + 48 22 246 06 80
Última atualização: março 2025
Para uso interno - Interno
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorFerring GmbH
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MenopurForma farmacêutica: Pó, 75 UI FSH + 75 UI LHSubstância ativa: human menopausal gonadotrophinFabricante: Ferring GmbHRequer receita médicaForma farmacêutica: Pó, 600 UI FSH + 600 UI LHSubstância ativa: human menopausal gonadotrophinRequer receita médicaForma farmacêutica: Pó, 1200 UI FSH + 1200 UI LHSubstância ativa: human menopausal gonadotrophinRequer receita médica
Alternativas a Menopur noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Menopur em Espanha
Alternativa a Menopur em Ukraine
Médicos online para Menopur
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Menopur – sujeita a avaliação médica e regras locais.