
MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL


Como usar MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Introdução
Prospecto: informação para o paciente
Menopur75 Unidades Internacionais pó e dissolvente para solução injetável
Leia todo o prospecto atentamente antes de começar a utilizar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito para si, e não deve dá-lo a outras pessoas, mesmo que apresentem os mesmos sintomas de doença que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. (Ver seção 4).
Conteúdo do prospecto
- O que é Menopur e para que é utilizado
- O que precisa saber antes de começar a usar Menopur
- Como usar Menopur
- Possíveis efeitos adversos
- Conservação de Menopur
- Conteúdo do envase e informações adicionais
1. O que é Menopur e para que é utilizado
Menopur apresenta-se sob a forma de pó que deve ser misturado com líquido (dissolvente) antes do seu uso. É administrado como uma injeção sob a pele ou no músculo.
Menopur contém duas hormonas chamadas hormona foliculo-estimulante (FSH) e hormona luteinizante (LH). A FSH e LH são hormonas naturais produzidas tanto em homens como em mulheres. Auxiliam os órgãos reprodutivos a funcionar normalmente. A FSH e LH em Menopur são obtidas da urina de mulheres pós-menopáusicas. O princípio ativo está altamente purificado e é conhecido como menotropina.
Menopur é utilizado para tratar a esterilidade feminina nas duas situações seguintes:
i Mulheres que não podem engravidar porque os seus ovários não produzem óvulos (incluindo síndrome de ovário poliquístico). Menopur é usado em mulheres que foram tratadas com um medicamento chamado citrato de clomifeno para tratar a sua infertilidade, mas este medicamento não teve efeito.
iiMulheres em programas de reprodução assistida (PRA) (incluindo fecundação in vitro/transferência embrionária (FIV/TE), transferência intratubárica de gametas (GIFT); e injeção intracitoplasmática de espermatozoides (ICSI)). Menopur ajuda os ovários a desenvolver muitos sacos de óvulos (folículos) onde um óvulo pode se desenvolver (desenvolvimento folicular múltiplo).
2. O que precisa saber antes de começar a usar Menopur
Antes de começar o tratamento com Menopur, si e o seu parceiro devem ser avaliados por um médico para ver as causas do problema de infertilidade. Em particular, devem ser controladas as seguintes doenças para que possam administrar-lhe o tratamento mais adequado:
- Disfunção da glândula tireoide e da corteza das glândulas supra-renais
- Níveis elevados de uma hormona chamada prolactina (hiperprolactinemia)
- Tumores na hipófise (uma glândula localizada na base do cérebro)
- Tumores no hipotálamo (uma área localizada sob a parte do cérebro chamada tálamo).
Se sabe que padece de alguma das doenças listadas acima, por favor comunique-o ao seu médico antes de começar o tratamento com Menopur.
Não use Menopur:
- Se é alérgico (hipersensível) a Menopur ou a qualquer um dos outros componentes deste medicamento (incluídos na seção 6).
- se tem um tumor no útero, ovários, mamas, ou algumas partes do cérebro como o hipotálamo-hipófise
- Se tem sacos de quistes de líquido (quistes ováricos) nos ovários ou ovários aumentados (a menos que seja causado por uma doença de ovário poliquístico)
- se tem malformações nos órgãos sexuais ou matriz (útero)
- se apresenta sangramento vaginal de causa desconhecida
- se tem fibromas (tumores benignos) no útero (matriz)
- se está grávida ou em período de amamentação
- se tem menopausa precoce.
Advertências e precauções
Informa ao seu médico se tem:
- Dor no abdômen
- Inchaço do abdômen
- Náuseas
- Vômitos
- Diarréia
- Ganho de peso
- Dificuldade para respirar
- Diminuição da urina.
Consulte diretamente com o seu médico, mesmo que os sintomas se desenvolvam alguns dias após a administração da última injeção. Estes podem ser sinais de altos níveis de atividade nos ovários que podem se tornar graves.
Se estes sintomas se tornam graves, o tratamento de infertilidade deve ser retirado e deve receber tratamento em um hospital.
Mantendo a dose recomendada e um seguimento cuidadoso do tratamento, reduzir-se-á a probabilidade de sofrer estes sintomas.
Se deixar de usar Menopurpode experimentar ainda estes sintomas. Por favor, contacte com o seu médico imediatamente se sofrer qualquer um destes sintomas.
Enquanto estiver em tratamento com este medicamento, o seu médico normalmente lhe realizará ecografiase algumas vezes análises de sanguepara controlar a sua resposta ao tratamento.
Quando se está a tratar com hormonas como Menopur, pode aumentar o risco de:
- Gravidez ectópica (gravidez fora da matriz) se tiver histórico de doença nas trompas de Falópio
- Aborto
- Gravidez múltipla (gémeos, trigémeos, etc.)
- Malformações congénitas (defeitos físicos presentes no bebê ao nascer).
Algumas mulheres que foram tratadas com vários medicamentos por infertilidade desenvolveram tumores nos ovários e outros órgãos reprodutivos. Não se sabe ainda se o tratamento com hormonas como este Menopur causa estes problemas.
É mais provável que se formem coágulos dentro dos vasos sanguíneos (veias ou artérias) em mulheres grávidas. O tratamento de infertilidade pode aumentar a probabilidade de que isso ocorra, especialmente se si tiver sobrepeso ou doença de coagulação do sangue conhecida (trombofilia) ou se si ou algum familiar (consanguíneo) teve problemas de coagulação. Se pensa que isso lhe pode acontecer, informe o seu médico.
Uso em crianças
Menopur não tem indicações adequadas para o seu uso em crianças.
Outros medicamentos e Menopur
Comunique ao seu médico ou farmacêutico se está a utilizar, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento.
O citrato de clomifeno é outro medicamento utilizado no tratamento de infertilidade. Se Menopur for utilizado ao mesmo tempo que o citrato de clomifeno, o efeito nos ovários pode aumentar.
Gravidez, amamentação e fertilidade
Se está grávida ou em período de amamentação, ou acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Menopur não é indicado em nenhum caso para tratar mulheres grávidas ou em período de amamentação.
Condução e uso de máquinas
É muito raro que Menopur afete a capacidade de conduzir e utilizar máquinas.
Informação importante sobre alguns dos componentes de Menopur:
Menopur contém menos de 1 mmol de sódio (23 mg) por dose, por tanto está essencialmente livre de sódio.
3. Como usar Menopur
Siga exatamente as instruções de administração de Menopur indicadas pelo seu médico.
Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
- Mulheres que não ovulam (não produzem óvulos):
O tratamento começará dentro dos 7 dias iniciais do ciclo menstrual (dia 1 é o primeiro dia do período). O tratamento deverá ser administrado todos os dias durante pelo menos 7 dias.
A dose inicial é normalmente 75-150 UI diárias (1-2 frascos), que pode ser ajustada de acordo com a resposta individual da paciente (até um máximo de 225 UI, 3 frascos de pó). Esta dose individual deverá ser administrada pelo menos 7 dias antes de ajustar a dose pelo médico. O aumento de dose recomendado é 37,5 UI por ajuste, e não deve exceder 75 UI. O ciclo de tratamento deve ser abandonado se não responder adequadamente após 4 semanas.
Quando se obtém uma resposta óptima, será administrada uma injeção única de outra hormona chamada gonadotropina coriónica humana (hCG), de 5.000 a 10.000 UI, um dia após a última injeção de Menopur. Recomenda-se à paciente ter relações sexuais no mesmo dia e no dia seguinte à administração de gonadotropina coriónica humana. Pode ser realizada inseminação intrauterina (injeção de esperma diretamente na matriz) alternativamente. O seu médico deverá seguir o seu progresso muito de perto durante pelo menos 2 semanas após a administração de hCG.
O seu médico controlará o efeito do tratamento de Menopur. Dependendo do progresso, o seu médico decidirá interromper o tratamento com Menopur e não administrar-lhe a injeção de hCG. Neste caso, deve utilizar um método anticonceptivo (preservativo) ou não ter relações sexuais até que comece o próximo período.
ii. Mulheres em programas de reprodução assistida:
Se si também está a receber tratamento com agonistas de GnRH, o tratamento com Menopur deve começar aproximadamente 2 semanas após iniciar o tratamento com agonistas de GnRH.
Se si também está a receber tratamento com antagonistas de GnRH, o tratamento com Menopur deve começar no dia 2 ou 3 do ciclo menstrual (dia 1 é o primeiro dia do período).
Menopur será administrado diariamente durante pelo menos 5 dias. A dose inicial recomendada de Menopur é 150-225 UI (2-3 frascos de pó).
Esta dose pode ser aumentada de acordo com a sua resposta ao tratamento até um máximo de 450 UI (6 frascos) por dia. A dose não deve ser aumentada mais de 150 UI por ajuste. Normalmente, o tratamento não é recomendado durante mais de 20 dias.
Se houver sacos de óvulos suficientes (folículos), será administrada uma injeção única de um medicamento chamado gonadotropina coriónica humana (hCG) a uma dose de até 10.000 UI para induzir a ovulação (liberação de um óvulo).
O seu médico deverá seguir o seu progresso muito de perto durante pelo menos 2 semanas após a administração de hCG.
O seu médico controlará o efeito do tratamento de Menopur. Dependendo do progresso, o seu médico decidirá interromper o tratamento com Menopur e não administrar-lhe a injeção de hCG. Neste caso, deve utilizar um método anticonceptivo (preservativo) ou não ter relações sexuais até que comece o próximo período.
INSTRUÇÕES DE USO:
Se o seu médico lhe disser que se injete Menopur si mesmo, deve seguir qualquer instrução que lhe forneça.
A primeira injeção deste medicamento deve ser administrada sob a supervisão de um médico ou enfermeira.
RECONSTITUIÇÃO DE MENOPUR
Menopur é fornecido como um pó e deve ser reconstituído antes do seu uso. O dissolvente (líquido) que deve ser utilizado para reconstituir este medicamento é fornecido junto com o pó. Menopur só deve ser reconstituído imediatamente antes do seu uso. Deve ser reconstituído como se mostra a seguir:
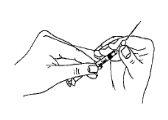 Ajuste firmemente a agulha longa e fina (agulha de preparação/reconstituição) à seringa.
Ajuste firmemente a agulha longa e fina (agulha de preparação/reconstituição) à seringa.
- Abra a ampola do líquido (dissolvente) com o ponto mirando para si.
- Insira a agulha na ampola de dissolvente.
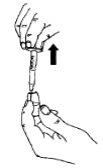 Retire todo o líquido da ampola para a seringa.
Retire todo o líquido da ampola para a seringa.
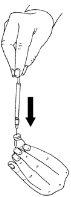
- Insira a agulha através do tampão de borracha do frasco de pó e injete suavemente tudoo líquido. Faça-o em um lado do frasco, para evitar a formação de bolhas.
- O pó se dissolverá rapidamente (em 2 minutos) formando uma solução transparente. Embora isso normalmente ocorra quando se têm adicionado apenas algumas gotas do dissolvente, deve-se adicionar toda a quantidade de dissolvente da ampola.
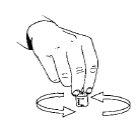
- Para ajudar a dissolução do pó, remova a solução. Não agite,pois pode causar bolhas de ar. Não deve utilizara solução reconstituída se contém partículas ou se não está transparente.
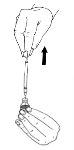
- Retire a solução com a seringa.
Se lhe foi prescrito mais de um frasco de Menopur pó para injeção, pode retirar a solução (a primeira dissolução de Menopur) de novo na seringa e injetá-la em um segundo frasco de pó. Pode fazer-se isso até em três frascos de pó no total, mas só deve ser feito como o médico lhe comentou.
INJEÇÃO DE MENOPUR
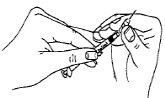
- Uma vez que tenha a sua dose prescrita retirada na seringa, troque a agulha (de preparação/reconstituição) por uma agulha curta e fina (agulha de injeção).
- Coloque a seringa boca para cima e golpeie-a suavemente para que as bolhas de ar fiquem na parte superior. Empurre devagar o êmbolo até que saia todo o ar e apareça na ponta da agulha uma gota da solução.
- O seu médico ou enfermeira lhe dirá onde se injetar (por exemplo, na parte frontal da coxa, abdômen, etc.).
- Desinfete o local da injeção.
- Para injetar, puxe a pele para produzir um dobra, e insira a agulha em um movimento rápido a 90 graus do corpo. Pressione o êmbolo para injetar a dissolução, e depois retire a a
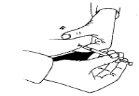 guila.
guila.
- Após retirar a agulha, aplique pressão no local da injeção para evitar o sangramento. Um massageado cuidadoso no local da injeção ajudará a dispersar a solução sob a pele.
- Não jogue o material usado no lixo; deve ser descartado corretamente.
Se usar mais Menopur do que deve
Em caso de sobredose ou se engolir a solução por acidente, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone 91 562 04 20, indicando o medicamento e a quantidade utilizada.
Se esquecer de usar Menopur,não se administre uma dose dupla para compensar as doses esquecidas. Por favor, diga-o ao seu médico ou farmacêutico.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico
4. Possíveis efeitos adversos
Como todos os medicamentos, Menopur pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
O tratamento com Menopur pode causar altos níveis de atividade nos ovários, que podem dar origem a uma doença chamada Síndrome de Hiperestimulação Ovárica (SHO), especialmente em mulheres com ovários poliquísticos. Os sintomas incluem: distensão e desconforto no abdômen, náusea, vômito, diarreia, ganho de peso. Em alguns casos graves de SHO, foram notificadas como complicações raras a acumulação de fluido no abdômen, pélvis e/ou na cavidade pleural, dificuldade para respirar e diminuição da quantidade de urina. formação de coágulos de sangue nos vasos sanguíneos (tromboembolismo) e torção dos ovários. Se experimentar qualquer um destes sintomas, por favor, contacte imediatamente o seu médico, mesmo que se desenvolvam alguns dias após a administração da última injeção.
Podem produzir-se reações alérgicas (hipersensibilidade), quando se usa este medicamento. Os sintomas destas reações podem incluir: erupção, picazão, inchaço da garganta e dificuldade para respirar.Se experimentar qualquer um destes sintomas, contacte imediatamente o seu médico.
Os seguintes efeitos adversos frequentes afetam entre 1 e 10 de cada 100 pacientes tratados):
- Dor abdominal
- Dor de cabeça
- Náuseas
- Inchaço (plenitude) abdominal
- Dor pélvica
- Hiperestimulação dos ovários que dão origem a altos níveis de atividade (Síndrome de Hiperestimulação Ovárica)
- Reações locais no local da injeção (como dor, vermelhidão, contusão, inchaço e/ou irritação).
Os seguintes efeitos adversos pouco frequentes afetam entre 1 e 10 de cada 1.000 pacientes tratados:
- Vômitos
- Desconforto no abdômen
- Diarréia
- Fadiga
- Tontura
- Sacos de fluido dentro dos ovários (quiste ovárico)
- Complicações nas mamas (inclui dor de peito, tensão mamária, desconforto nas mamas, dor do pezinho e inchaço do peito)
- Sofocos
Os seguintes efeitos adversos raros afetam entre 1 e 10 de cada 10.000 pacientes tratados:
- Acne
- Erupção cutânea
Além dos efeitos adversos indicados acima, foram comunicados após a comercialização de Menopur e com uma frequência desconocida, os seguintes efeitos adversos:
- Alterações na visão
- Febre
- Sentir-se mal
- Reações alérgicas
- Aumento do peso
- Dor no músculo e articulações (por exemplo, dor de costas, pescoço, braços e pernas)
- Torsão dos ovários como uma complicação do aumento da atividade dos ovários devido à hiperestimulação.
- Prurido
- Urticária
- Coágulos de sangue como uma complicação do aumento da atividade dos ovários devido à hiperestimulação.
Se experimentar qualquer efeito adverso, fale com o seu médico ou enfermeiro. Isso inclui qualquer efeito secundário não mencionado neste prospecto.
Comunicação de efeitos adversos.
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano https://www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
.
5. Conservação de Menopur
Não conservar a temperatura superior a 25 º C. Não congelar.
Conservar no embalagem exterior para protegê-lo da luz.
Para uso imediato e único após a reconstituição.
Mantenha fora da vista e do alcance das crianças.
Não utilize Menotropina Ferring após a data de caducidade que aparece na caixa após CAD. A data de caducidade é o último dia do mês que se indica.
Os medicamentos não devem ser jogados nos deságues nem na lixeira. Deposite os recipientes e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos recipientes e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição deMenopur
O princípio ativo é menotropina altamente purificada (gonadotropina menopáusica humana, hMG) que corresponde a 75 UI de atividade hormona foliculoestimulante (FSH) e 75 UI de atividade hormona luteinizante (LH).
Os demais componentes do pó são: lactosa monohidrato, polissorbato 20, hidróxido de sódio e ácido clorídrico.
Os componentes do solvente são: cloreto de sódio, ácido clorídrico diluído, hidróxido de sódio e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Menopur é um pó e solvente para solução injetável.
O envase contém cinco ou dez frascos de vidro transparente que contém um pó liofilizado apelmazado branco a grisáceo. O envase, além disso, contém um número igual de ampolas de vidro transparente que contém o solvente, solução transparente incolor, para sua reconstituição.
Pode ser que apenas alguns tamanhos de envase sejam comercializados.
Titular da Autorização de Comercialização e responsável pela fabricação:
Titular da autorização de comercialização
Ferring, S.A.U.
C/ do Arquiteto Sánchez Arcas nº 3, 1º
28040 Madrid
Espanha
Responsável pela fabricação:
FERRING GmbH
Wittland 11,
D-24109 Kiel
Alemanha
Este medicamento está autorizado nos estados membros do Espaço Económico Europeucom os seguintes nomes:
Bélgica, Irlanda, Luxemburgo, Eslováquia: Menotrophin Ferring
República Checa: Menotrophin Ferring-Léciva
Bulgária, Croácia, Chipre, Dinamarca, Estônia, Finlândia, Alemanha, Grécia, Hungria, Islândia, Letônia, Lituânia, Malta, Noruega, Portugal, Romênia, Eslovênia, Espanha, Suécia: Menopur
Itália: Meropur
Data da última revisão deste prospecto maio 2025.
A informação detalhada e atualizada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, -Substância ativa: human menopausal gonadotrophinFabricante: Angelini Pharma Espana S.L.Requer receita médicaForma farmacêutica: INJETÁVEL, 1200 UISubstância ativa: human menopausal gonadotrophinFabricante: Ferring S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 1200 UISubstância ativa: human menopausal gonadotrophinFabricante: Ferring S.A.U.Requer receita médica
Alternativas a MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Polónia
Alternativa a MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL em Ukraine
Médicos online para MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de MENOPUR 75 UI PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL – sujeita a avaliação médica e regras locais.





