DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA

Pergunte a um médico sobre a prescrição de DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA

Como usar DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA
Introdução
Prospecto : informação para o utilizador
Decapeptyl mensal 3,75 mg pó e dissolvente para suspensão de libertação prolongada injectável
Triptorelina
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Decapeptyl mensal e para que é utilizado.
- O que necessita de saber antes de começar a usar Decapeptyl mensal.
- Como usar Decapeptyl mensal.
- Posíveis efeitos adversos.
- Conservação de Decapeptyl mensal.
- Conteúdo do envase e informação adicional
1. O que é Decapeptyl mensal e para que é utilizado
Este medicamento contém triptorelina. A triptorelina pertence a um grupo de medicamentos conhecidos como análogos da hormona liberadora de gonadotropinas (GnRH). Uma das suas ações é a de diminuir os níveis das hormonas sexuais no organismo.
Decapeptyl mensal está indicado em adultos para tratar o cancro da próstata hormono-dependente localmente avançado e o cancro da próstata hormono-dependente que se disseminou para outras partes do corpo (cancro metastásico). Também é utilizado para tratar o cancro da próstata localizado de alto risco ou localmente avançado, em combinação com radioterapia.
Decapeptyl mensal também está indicado em mulheres para tratar a endometriose, os fibromiomas uterinos, a infertilidade feminina e o cancro da mama em estádio inicial hormonosensível, em mulheres pré-menopáusicas que receberam quimioterapia e em crianças, na puberdade precoce central.
No cancro da mama, Decapeptyl mensal é utilizado conjuntamente com outros medicamentos hormonais:
- Um medicamento chamado tamoxifeno (ser-lhe-á prescrito este medicamento se tiver um risco alto de cancro recorrente) ou,
- Um “inibidor da aromatase” como exemestano (ser-lhe-á prescrito Decapeptyl mensal durante pelo menos 6 a 8 semanas antes de que comece a tomar este medicamento).
Lembre-se de ler o prospecto do medicamento que está a tomar com Decapeptyl mensal.
2. O que necessita de saber antes de começar a usar Decapeptyl mensal
Não use Decapeptyl mensal:
- se é alérgico (hipersensível) a triptorelina, à hormona liberadora de gonadotropina (GnRH), a outros análogos da GnRH ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- se está grávida ou em período de amamentação.
- Se está a tomar Decapeptyl mensal para o cancro da mama, não utilize um medicamento “inibidor da aromatase” (como exemestano) até que tenha sido tratado com Decapeptyl mensal durante pelo menos 6 a 8 semanas.
Advertências e precauções:
Consulte o seu médico ou farmacêutico antes de começar a usar Decapeptyl mensal:
Foram notificados casos de depressão em pacientes tratados com Decapeptyl mensal que pode ser grave. Se está em tratamento com Decapeptyl mensal e apresenta depressão, informe o seu médico. Pode ser que o seu médico queira monitorizar a sua depressão durante o tratamento.
Em adultos, triptorelina pode causar que os ossos sejam menos densos (osteoporose) com um aumento do risco de fracturas ósseas. Por tanto, informe o seu médico se padece algum dos factores de risco que se apresentam a seguir, porque pode prescrever-lhe um bifosfonato (medicamento que se usa para tratar os ossos débeis) para tratar a perda óssea. Os factores de risco podem incluir:
- Se si ou algum familiar próximo padece de ossos menos densos.
- Se si bebe quantidades excessivas de álcool, e/ou é um fumador inveterado.
Se si durante muito tempo tem tomado medicamentos que podem causar que os seus ossos sejam menos densos, por exemplo, medicamentos para a epilepsia ou esteroides (como hidrocortisona ou prednisolona).
Em caso de convulsões, informe imediatamente o seu médico. Foram notificados casos de convulsões em pacientes que recebiam triptorelina ou medicamentos semelhantes. Estes ocorreram em pacientes com ou sem antecedentes médicos de epilepsia.
Se si padece um tumor benigno da hipófise que desconhecia, isto pode ser descoberto durante o tratamento com Decapeptyl mensal. Os sintomas incluem dor de cabeça, problemas visuais e paralisia dos olhos.
Se usa medicamentos para prevenir a coagulação do sangue, porque podem aparecer hematomas no local de injeção.
Se si padece diabetes ou se padece problemas cardíacos, informe o seu médico.
Homens
- Ao começar o tratamento aumentará a quantidade de testosterona no seu organismo, o que pode fazer com que os sintomas do cancro piorem. Consulte com o seu médico se isto sucede. O médico pode dar-lhe algum medicamento (um antiandrógeno) para impedir que os sintomas piorem.
- Se padece obstrução urinária ou compressão da medula espinal (nervos da sua coluna vertebral) como consequência da disseminação do cancro, durante as primeiras semanas de tratamento o seu médico fará um seguimento estreito. Se si experimenta dificuldade para urinar, dor óssea, fraqueza dos membros inferiores ou sensação de formigueiro, consulte com o seu médico imediatamente que o avaliará e tratará adequadamente.
- Depois da castração quirúrgica, triptorelina não induz qualquer descida adicional dos níveis de testosterona sérica e por tanto, não deve ser utilizado após a orquidectomia (extirpação quirúrgica dos testículos).
- Os testes de diagnóstico da função gonadal pituitária ou órgãos sexuais realizados durante o tratamento ou após a interrupção do tratamento com Decapeptyl mensal podem ser erróneos.
- Se si padece algum problema nos vasos sanguíneos ou no coração, incluindo problemas no ritmo cardíaco (arritmia) ou se está a ser tratado com medicamentos para esta afeção, consulte com o seu médico. O risco de problemas no ritmo cardíaco pode ser aumentado com Decapeptyl mensal.
- Os medicamentos que diminuem a testosterona podem provocar alterações no ECG associadas a anomalias no ritmo cardíaco (prolongação do QT).
- O tratamento com análogos da GnRH como Decapeptyl mensal pode aumentar o risco de anemia (definido como uma descida no recuento de glóbulos vermelhos).
Mulheres
Devido à ausência de experiência clínica em mulheres com menos de 18 anos, não se recomenda o uso de triptorelina em adolescentes e mulheres jovens porque pode provocar uma descida da densidade óssea.
Durante o primeiro mês de tratamento pode experimentar algum sangramento vaginal. Depois disso, a sua menstruação será interrompida. Informe o seu médico em caso de que continue a apresentar sangramento após o primeiro mês. Após a última injeção, voltará a ter a menstruação ao cabo de aproximadamente 2 meses. Deve usar um método anticonceptivo que não seja a pílula durante o primeiro mês de tratamento e, posteriormente após a última injeção, sempre que o tratamento não seja para a infertilidade.
Se si é uma mulher com miomas submucosos (tumores benignos no músculo que se encontra debaixo do revestimento do útero), triptorelina pode causar hemorragias quando os miomas se rompem dentro das primeiras 6-10 semanas após o início do tratamento. Contacte com o seu médico imediatamente se experimentar uma hemorragia ou uma dor intensa ou incomum.
Durante o tratamento da infertilidade, as gonadotropinas (hormonas que estimulam os ovários) combinadas com o fármaco podem induzir um aumento do tamanho dos ovários ou uma hiperestimulação ovárica que pode provocar dor pélvica e/ou abdominal e dificuldades para respirar. Se isto ocorrer, consulte o seu médico imediatamente.
Se está a utilizar Decapeptyl mensal para o tratamento adjuvante do cancro da mama:
- Se tiver algum problema que afeta os seus ossos, como osteoporose, informe o seu médico. Isto pode afetar a maneira como o seu médico decide tratar-lhe. O seu médico fará um escaneamento ósseo antes de que comece o tratamento se si apresentar risco de osteoporose e o controlará durante o tratamento.
- Se si apresenta diabetes ou pressão arterial elevada, informe o seu médico. O seu médico controlará os seus níveis de açúcar no sangue e a pressão arterial durante o tratamento.
- Se si padece depressão, informe o seu médico. O seu médico pode querer fazer um seguimento da sua depressão durante o tratamento.
- Se interromper o tratamento com triptorelina, deve interromper ao mesmo tempo o tratamento com o inibidor da aromatase (como exemestano).
Crianças
As meninas com puberdade precoce podem apresentar algum sangramento vaginal durante o primeiro mês de tratamento.
Se apresenta um tumor cerebral progressivo, informe o seu médico. Isto pode mudar a maneira como o seu médico decide tratar-lhe.
O seu médico deve descartar a puberdade precoce causada por outras doenças.
A quantidade de minerais nos ossos diminui durante o tratamento mas volta aos níveis normais após a interrupção do tratamento.
Após a interrupção do tratamento pode produzir-se uma patologia da anca (deslizamento da epífise da cabeça femoral da anca). Produz rigidez da anca, coxeadura e/ou dor intensa na virilha que se irradia para a coxa. Se isto ocorrer, deve consultar o seu médico.
Se o seu filho sofre dor de cabeça intensa ou recorrente, problemas de visão e zumbidos ou assobios nos ouvidos, ponha-se em contacto com um médico imediatamente (ver secção 4).
Consulte com o seu médico se está preocupado com algum destes temas.
Outros medicamentos eDecapeptyl mensal
Informe o seu médico ou farmacêutico se está a utilizar, ou utilizou recentemente outros medicamentos, mesmo os adquiridos sem receita.
Para homens
Decapeptyl mensal pode interferir com alguns medicamentos utilizados para tratar problemas do ritmo cardíaco (p.ex. quinidina, procainamida, amiodarona e sotalol) ou pode aumentar o risco de problemas no ritmo cardíaco quando se utiliza com outros medicamentos (p.ex. metadona (utilizada para o alívio da dor e como parte da desintoxicação de drogas), moxifloxacino (um antibiótico), antipsicóticos utilizados para doenças mentais graves).
Gravidez e amamentação
Decapeptyl mensal não deve ser utilizado durante a gravidez ou a amamentação.
Não use Decapeptyl se está a tentar engravidar (a menos que Decapeptyl faça parte de um tratamento para a infertilidade).
Condução e uso de máquinas
Pode sentir-se mareado, estar cansado ou apresentar problemas na visão, como visão borrosa. Estes são possíveis efeitos adversos do tratamento ou devidos à doença subjacente. Se experimentar algum destes efeitos adversos não deve conduzir nem manejar máquinas.
Decapeptyl mensal 3,75 mg contém sódio
Este medicamento contém sódio, mas menos de 1 mmol (23 mg) de sódio por frasco; isto é, essencialmente “isento de sódio”.
3. Como usar Decapeptyl mensal
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte de novo o seu médico ou farmacêutico.
Decapeptyl mensal deve ser administrado exclusivamente por via intramuscular. O seu médico ou enfermeira o administrarão. Ver as instruções de uso, no final deste prospecto.
Para o cancro da próstata localizado de alto risco ou localmente avançado, em combinação com radioterapia, a duração recomendada do tratamento é de 2-3 anos.
A dose será estabelecida pelo médico em função das necessidades de cada paciente. As doses normais são as seguintes:
Cancro da próstata: Uma injeção intramuscular profunda de Decapeptyl mensal cada quatro semanas.
Endometriose: O tratamento deve ser iniciado durante os primeiros cinco dias do ciclo. Uma injeção intramuscular profunda de Decapeptyl mensal cada quatro semanas.
A duração do tratamento depende da gravidade inicial da endometriose e da evolução das suas manifestações clínicas (funcionais e anatómicas) durante o tratamento. Em princípio, a duração do tratamento deveria ser de quatro a seis meses. Não se aconselha um segundo tratamento com Decapeptyl mensal ou com outro medicamento do mesmo grupo.
Fibromas uterinos: O tratamento deve ser iniciado durante os cinco primeiros dias do ciclo. A dose recomendada é uma injeção intramuscular profunda cada quatro semanas. A duração do tratamento depende da evolução do volume dos fibromas, determinado por ecografia. Em princípio, os fibromas devem ser tratados durante não mais de seis meses (ver reacções adversas). Não se aconselha um segundo tratamento com Decapeptyl mensal ou com outro medicamento do mesmo grupo.
Infertilidade feminina: Uma injeção intramuscular profunda de Decapeptyl mensal administrada no segundo dia do ciclo. Em geral, a estimulação com este medicamento deveria ser realizada quando os níveis plasmáticos de estrógenos são inferiores a 50 pg/ml (normalmente ao redor do dia 15 do ciclo).
Cancro da mama
A dose recomendada de Decapeptyl mensal é de uma injeção intramuscular cada 4 semanas (28 dias). O tratamento pode durar até 5 anos.
Decapeptyl mensal é utilizado em conjunto com um medicamento denominado tamoxifeno ou um “inibidor da aromatase”, como exemestano. Se precisa tomar um “inibidor da aromatase”, deve ser tratado com Decapeptyl mensal durante pelo menos 6 a 8 semanas antes de que comece a tomar-lo.
Puberdade precoce central:
Nas crianças: a dose é ajustada ao peso corporal.
Crianças com mais de 30 kg de peso: uma injeção intramuscular cada 4 semanas (28 dias).
Crianças entre 20 e 30 kg de peso: dois terços da dose por via intramuscular cada 4 semanas (28 dias), isto é, administrar dois terços do volume da suspensão reconstituída.
Crianças com menos de 20 kg de peso corporal: a metade da dose por via intramuscular, cada 4 semanas (28 dias), isto é, administrar a metade do volume da suspensão reconstituída.
Se usar mais Decapeptyl mensaldo que deve
Em caso de sobredose ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico.
Se esquecer de usar Decapeptyl mensal
Assim que se dê conta de que esqueceu uma injeção, consulte com o seu médico e ele decidirá quando deve ser administrada a próxima injeção.
Se interromper o tratamento comDecapeptyl mensal
Não interrompa o tratamento com Decapeptyl mensal sem falar antes com o seu médico. Isto é especialmente importante se está a utilizar Decapeptyl mensal em conjunto com um inibidor da aromatase. Isto é devido a que interromper o tratamento pode provocar um aumento dos níveis de estrógenos. O seu médico controlará os níveis de estrógenos durante o tratamento com Decapeptyl mensal.
Se interromper o tratamento com Decapeptyl mensal, também deve interromper o tratamento com o inibidor da aromatase, no prazo de 1 mês desde a interrupção do tratamento.
4. Possíveis efeitos adversos
Assim como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Em casos raros pode experimentar uma reação alérgica grave (angioedema, reação anafiláctica). Informe ao seu médico imediatamente se desenvolver sintomas como problemas para engolir ou respirar, tonturas, inchaço dos lábios, face, garganta ou língua, ou uma erupção.
Se você apresentar um aumento (tumor benigno) da glândula pituitária que desconhecia, pode ser descoberto durante o tratamento com Decapeptyl mensal. Os sintomas incluem cefaleia súbita, problemas de visão e paralisia dos olhos.
Assim como com outros análogos da GnRH, pode ocorrer um aumento do recuento de glóbulos brancos nos pacientes tratados com Decapeptyl mensal.
Homens
Muitos desses efeitos adversos são esperados devido à mudança no nível de testosterona no seu organismo. Esses efeitos incluem sofocos, impotência e diminuição da libido.
Efeitos adversos muito frequentes, podem afetar mais de 1 de cada 10 pacientes:
- Sofocos
- Debilidade
- Sudorese excessiva
- Dor de costas
- Sensação de formigamento e adormecimento nas pernas
- Redução da libido
- Impotência
Efeitos adversos frequentes, podem afetar de 1 a 10 de cada 100 pacientes:
- Náuseas, secura da boca
- Dor, hematomas, enrubescimento e inchaço no local da injeção, dor muscular e óssea, dor nos braços e pernas, edema (concentração de líquidos nos tecidos corporais), dor abdominal inferior
- Reação alérgica
- Aumento de peso
- Tonturas, dor de cabeça
- Perda de libido, depressão, mudanças de humor
- Pressão arterial elevada
Efeitos adversos pouco frequentes, podem afetar de 1 a 10 de cada 1000 pacientes:
- Aumento do recuento de plaquetas
- Sentir os batimentos do coração
- Zumbidos nos ouvidos, vertigem
- Visão borrada
- Dor abdominal, constipação, diarreia, vômitos
- Sonolência, tremores intensos associados a suores e febre, sonolência, dor
- Certos parâmetros analíticos afetados (incluindo aumento das provas de função hepática), aumento da pressão arterial
- Perda de peso
- Perda de apetite, incremento do apetite, gota (dor severa e inchaço das articulações habitualmente no dedo gordo do pé), diabetes, excesso de lípidos no sangue
- Dor articular, cãibras musculares, debilidade muscular, dor muscular, inchaço dos tornozelos, pés ou dedos, dor óssea
- Formigamento ou entumecimento
- Incapacidade para dormir, sensação de irritabilidade
- Acordar para urinar, problemas para urinar
- Desenvolvimento das mamas nos homens, dor no peito, redução do tamanho testicular, dor nos testículos
- Dificuldade para respirar
- Sangramento do nariz
- Acne, perda de cabelo, picor, erupção, enrubescimento da pele, urticária
Efeitos adversos raros, podem afetar de 1 a 10 de cada 10.000 pacientes:
- Descoloração vermelha ou roxa da pele
- Sensação anormal no olho, alteração da visão ou visão borrada
- Sensação de abdômen cheio, flatulência, sentido anormal do gosto
- Dor no tórax
- Dificuldade para ficar de pé
- Sintomas semelhantes à gripe, febre
- Reação alérgica grave que pode causar tonturas ou dificuldade para respirar, inchaço da face ou garganta
- Inflamação do nariz/garganta
- Aumento da temperatura corporal
- Rigidez articular, inchaço das articulações, rigidez musculoesquelética, osteoartrite (alteração das articulações que afeta cartilagem e ocasiona dor, inchaço e perda de movimento)
- Perda de memória
- Sensação de confusão, diminuição da atividade, sensação de euforia
- Dificuldade para respirar ao estar deitado
- Bolhas
- Pressão arterial baixa
Durante a vigilância pós-comercialização também foram comunicados os seguintes efeitos adversos:
- Reação alérgica grave que pode provocar inflamação da face, língua e garganta, dificuldade para respirar ou tonturas (edema de Quincke, choque anafilático)
- Mudanças no ECG (prolongação do QT)
- Malestar geral
- Ansiedade
- Formação rápida de pápulas causadas pela inflamação da pele ou das membranas mucosas
- Incontinência urinária
- Se houver um tumor hipofisário, há um maior risco de sangramento na zona
- Anemia (diminuição do recuento de glóbulos vermelhos)
Os pacientes que estão recebendo tratamento de longa duração com análogos da GnRH em combinação com radiação podem ter mais efeitos adversos, especialmente gastrointestinais, relacionados com radioterapia.
Mulheres:
Muitos desses efeitos adversos são esperados devido à mudança no nível de estrógenos do organismo.
Efeitos adversos muito frequentes (afetam mais de 1 paciente de cada 10):
- mudanças de humor, dificuldade para dormir
- dor de cabeça
- diminuição da libido
- sofocos
- sudorese excessiva, acne, pele oleosa
- distúrbios no peito
- dor durante ou após as relações sexuais, menstruações dolorosas, sangramento genital
- síndrome de hiperestimulação ovárica (com aumento do tamanho dos ovários e retenção de líquidos)
- dor pélvica, ovários aumentados
- secura da vagina
- debilidade
Efeitos adversos frequentes (afetam de 1 a 10 pacientes de cada 100):
- reação alérgica
- depressão (tratamento a longo prazo), nervosismo
- tonturas
- aumento de peso, náuseas, dor ou desconforto abdominal
- dor no peito
- cãibras musculares, articulações dolorosas
- dor nos braços e pernas
- reação no local da injeção (incluindo dor, inchaço, enrubescimento e inflamação)
- inflamação dos tornozelos, pés e dedos
Efeitos adversos pouco frequentes (afetam de 1 a 10 pacientes de cada 1000):
- diminuição de peso, diminuição do apetite
- retenção de líquidos
- mudanças de humor, ansiedade, desorientação, depressão (tratamento a curto prazo)
- sabor anormal
- perda de sensações
- perda temporária de consciência, perda de memória, falta de concentração
- formigamento ou entumecimento, movimento muscular involuntário
- secura dos olhos, visão borrada
- vertigem
- sentir os batimentos do coração
- dificuldade para respirar, sangramento do nariz
- inchaço abdominal, vômitos, secura da boca, flatulência, úlceras na boca
- perda de cabelo, excesso de pelos corporais
- secura da pele, unhas quebradiças, picor, erupção cutânea
- dor de costas, dor muscular
- sangramento após as relações sexuais, prolapso, menstruação irregular, menstruação dolorosa e intensa
- pequenos cistos (inflamação) nos ovários que podem causar dor, secreção vaginal
Durante a experiência pós-comercialização também foram comunicados os seguintes efeitos adversos:
- reação alérgica grave que pode causar inflamação da face, língua e garganta, dificuldade para respirar ou tonturas (edema de Quincke, choque anafilático)
- convulsões
- confusão, sensações anormais nos olhos e/ou mudanças na vista
- urticária (rápida formação de pápulas devido à inflamação da pele ou membranas mucosas)
- debilidade muscular
- ausência de períodos menstruais
- febre e malestar geral
- afetação de algum exame de sangue (incluindo elevação das provas de função hepática)
- diarreia
- aumento da pressão arterial
- se houver um tumor hipofisário preexistente, há um incremento do risco de sangramento na zona
Durante o tratamento de infertilidade, as gonadotropinas combinadas com o produto podem induzir um aumento do tamanho dos ovários ou uma hiperestimulação ovárica que pode provocar dor pélvica e/ou abdominal ou dificuldade para respirar. Em caso de que isso ocorra, consulte seu médico imediatamente.
No tratamento da endometriose, os distúrbios para os quais se justificou o tratamento (dor pélvica, dismenorreia) podem se agravar no início do tratamento, mas devem desaparecer em uma ou duas semanas. Isso pode ocorrer mesmo se o tratamento produzir um efeito favorável. No entanto, você deve informar imediatamente ao seu médico sobre esse fenômeno.
Efeitos adversos quando utilizado para câncer de mama em combinação com tamoxifeno ou um inibidor da aromatase:
Os seguintes efeitos adversos foram observados quando triptorelina é utilizada para o câncer de mama em combinação com tamoxifeno ou um inibidor da aromatase.
Efeitos adversos muito frequentes (afetam mais de 1 paciente de cada 10):
- náuseas
- sentir-se muito cansado
- dor articular e muscular, osteoporose
- sofocos
- sudorese excessiva
- dificuldade para dormir, depressão
- diminuição da libido, secura vaginal, dor durante ou após as relações sexuais
- incontinência urinária
- aumento da pressão arterial
Efeitos adversos frequentes (afetam de 1 a 10 pacientes de cada 100):
- diabetes, elevação de açúcar no sangue (hiperglicemia)
- dor, hematomas
- enrubescimento e inflamação no local da injeção
- reação alérgica
- fraturas ósseas
- formação de coágulos de sangue em um vaso sanguíneo
Efeitos pouco frequentes (afetam 1 de cada 10 pacientes de cada 1000):
- sangramento no cérebro
- falta de suprimento de sangue no cérebro ou no coração
Efeitos adversos raros (afetam de 1 a 10 pacientes de cada 10.000):
- mudança no ECG (prolongação do QT)
Crianças
Efeitos adversos muito frequentes (afetam mais de 1 paciente de cada 10):
- sangramento vaginal, que pode ocorrer durante o primeiro mês, em meninas
Efeitos adversos frequentes (afetam de 1 a 10 pacientes de cada 100):
- dor no abdômen
- hematomas dolorosos
- enrubescimento e inflamação no local da injeção
- dor de cabeça, sofocos
- aumento de peso
- acne
- reação alérgica
Efeitos adversos pouco frequentes (afetam 1 de cada 10 pacientes de cada 1000):
- visão borrada
- vômitos, constipação, náuseas
- malestar geral
- sobrepeso
- dor no pescoço, dor no peito
- mudanças de humor
- sangramento do nariz
- picor, erupção cutânea ou urticária na pele
Durante a experiência pós-comercialização também foram comunicados os seguintes efeitos adversos:
- reação alérgica grave que pode causar dificuldade para respirar ou tonturas e inflamação da face, garganta ou pescoço (edema de Quincke, choque anafilático)
- convulsões
- pressão sanguínea elevada
- visão anormal
- alguns exames de sangue afetados incluem os níveis hormonais
- dor muscular
- mudanças de humor, depressão, nervosismo
- Hipertensão intracraniana idiopática (aumento da pressão intracraniana ao redor do cérebro caracterizado por dor de cabeça, visão dupla e outros sintomas visuais, e zumbidos ou tinidos nos ouvidos)
Comunicação de efeitos adversos
Se você experimentar qualquer tipo de efeito adverso, consulte seu médico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Você também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano. www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Decapeptyl mensal
Mantenha este medicamento fora da vista e do alcance das crianças.
Conservar Decapeptyl mensal em seu envase original. Não conservar a temperatura superior a 25ºC.
Não utilize Decapeptyl mensal após a data de validade que aparece no envase após CAD. A data de validade é o último dia do mês que se indica.
Os medicamentos não devem ser jogados nos deságues nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, você ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Decapeptyl mensal
- O princípio ativo é triptorelina (acetato), 3,75 mg por frasco.
Os outros componentes são:
- Pó: polímero DL lactido-co-glicolídeo, manitol, carmelosa de sódio, polissorbato 80
- Veículo: manitol e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
Este medicamento é um pó e veículo para suspensão injetável, o pó é um pó liofilizado de cor esbranquiçada e o veículo para a reconstituição da suspensão é uma solução incolor e transparente.
Envase com 1 frasco, 1 ampola e 1 blister com 1 seringa e 2 agulhas para a reconstituição e administração.
Título da autorização de comercialização e responsável pela fabricação
Título da autorização de comercialização:
IPSEN PHARMA, S.A.U.
Gran Via de les Corts Catalanes 130-136
08038 Barcelona
Espanha
Responsável pela fabricação:
IPSEN PHARMA-BIOTECH
Parc d'Activité du Plateau de Signes, C.D. 402,
83870 Signes
França
Data da última revisão deste prospecto: fevereiro 2025
A informação detalhada e atualizada deste medicamento está disponível no site da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es
Esta informação está destinada apenas a profissionais do setor sanitário:
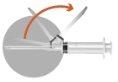
INSTRUÇÕES PARA A RECONSTITUIÇÃO
1 –PREPARAÇÃO DO PACIENTE ANTES DA RECONSTITUIÇÃO | |
Prepare o paciente desinfetando o local da injeção, no glúteo. Esta operação deve ser realizada primeiro, pois uma vez reconstituído, o produto deve ser injetado imediatamente. | |
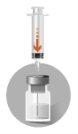
2 – PREPARAÇÃO DA INJEÇÃO | |
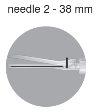
Na caixa estão incluídas duas agulhas:
| |
A presença de bolhas na parte superior do liofilizado faz parte do aspecto normal do produto. Os seguintes passos devem ser completados em uma sequência contínua. | |
2a
|
|
2b
|
|
2c
|
|
2d
|
|
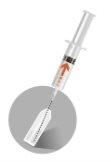
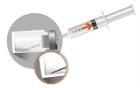
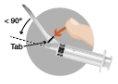
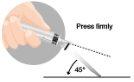
3 – INJEÇÃO INTRAMUSCULAR | |
|
|
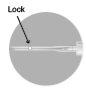
4 – DEPOIS DO USO | |
Há dois métodos alternativos para ativar o sistema de segurança.
As agulhas usadas, qualquer resto de suspensão não utilizado ou outro material residual devem ser descartados de acordo com as diretrizes locais. |
Método A
Método B
|
Qualquer incidente que ocasione perda notável de produto a injetar deve ser comunicado ao médico, que determinará a conveniência de repetir a injeção em um prazo mais breve.
|
TABELA DE TRATAMENTO
SOBRENOMES
NOME
Data de pedido | Data de injeção | |
Injeção 1 | ||
Injeção 2 | ||
Injeção 3 | ||
Injeção 4 | ||
Injeção 5 | ||
Injeção 6 |

Quanto custa o DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA em Espanha em 2025?
O preço médio do DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA em dezembro de 2025 é de cerca de 127.95 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia127.95 EUR
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADAForma farmacêutica: INJETÁVEL, 0,1 mgSubstância ativa: triptorelinFabricante: Ipsen Pharma S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 22.5 mgSubstância ativa: triptorelinFabricante: Ipsen Pharma S.A.U.Requer receita médicaForma farmacêutica: INJETÁVEL, 11,25 mg de triptorelinaSubstância ativa: triptorelinFabricante: Ipsen Pharma S.A.Requer receita médica
Alternativas a DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA em Polónia
Alternativa a DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA em Ukraine
Médicos online para DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de DECAPEPTYL MENSUAL 3,75 mg PÓ E SOLVENTE PARA SUSPENSÃO INJETÁVEL DE LIBERTAÇÃO PROLONGADA – sujeita a avaliação médica e regras locais.