
AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal
Pergunte a um médico sobre a prescrição de AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal

Como usar AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal
Introdução
Prospecto: informação para o paciente
Avancort duo 137 microgramas/50 microgramas/aplicação suspensão para pulverização nasal
azelastina hidrocloruro / fluticasona propionato
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Avancort duo e para que se utiliza
- O que precisa saber antes de começar a usar Avancort duo
- Como usar Avancort duo
- Posíveis efeitos adversos
- Conservação de Avancort duo
- Conteúdo do envase e informação adicional
1. O que é Avancort duo e para que se utiliza
Avancort duo contém duas substâncias ativas: hidrocloruro de azelastina e propionato de fluticasona.
- O hidrocloruro de azelastina pertence a um grupo de medicamentos chamados antihistamínicos. Os antihistamínicos atuam prevenindo os efeitos de substâncias como a histamina, produzidas pelo organismo como parte de uma reação alérgica; desta forma, reduz os sintomas da rinite alérgica.
- O propionato de fluticasona pertence a um grupo de medicamentos chamados corticosteroides, que reduzem a inflamação.
Este medicamento é utilizado para aliviar os sintomas da rinite alérgica estacional de moderada a grave e da rinite alérgica perene, se o tratamento com antihistamínico ou corticosteroide intranasal por separado for considerado insuficiente.
A rinite alérgica estacional ou perene são reações alérgicas frente a substâncias como o pólen (febre do feno), ácaros do lar, mohos, pó ou animais domésticos.
Este medicamento alivia os sintomas das alergias, por exemplo: rinorreia, gotejamento pós-nasal, espirros, coceira ou entupimento nasal.
2. O que precisa saber antes de começar a usar Avancort duo
Não use Avancort duo
- Se for alérgico ao hidrocloruro de azelastina ou ao propionato de fluticasona, ou a algum dos outros componentes deste medicamento (incluídos na seção 6).
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar este medicamento se:
- Sofreu uma operação recente de nariz.
- Padece uma infecção nasal. As infecções nasais devem ser tratadas com antibacterianos ou antifúngicos. Se lhe foi dado medicamento para uma infecção nasal, pode continuar usando este medicamento para tratar a sua alergia.
- Têm tuberculose ou uma infecção não tratada.
- Têm alterações de visão ou antecedentes de pressão intraocular elevada, glaucoma e/ou cataratas. Se padece alguns destes problemas, será vigilada estreitamente durante o uso deste medicamento.
- Têm função adrenal deteriorada. Deve ter precaução quando se muda um tratamento sistémico de esteroides por este medicamento.
- Padece doença grave do fígado. O risco de apresentar efeitos adversos sistémicos aumenta.
Nestes casos, o seu médico decidirá se pode utilizar este medicamento:
É importante que tome a dose indicada na seção 3 ou a indicada pelo seu médico. O tratamento com doses maiores do que as recomendadas de corticoides nasais pode levar a uma supressão adrenal, o que pode produzir perda de peso, fadiga, fraqueza muscular, níveis baixos de glicose no sangue, necessidade de sal, dor de articulações, depressão e escurecimento da pele. Se lhe ocorrer algum destes efeitos adversos, o seu médico pode recomendar outro medicamento durante períodos de stresse ou cirurgia seletiva.
Para evitar a supressão adrenal, o seu médico aconselhará que tome a dose mais baixa que mantenha um controlo eficaz dos sintomas da rinite.
O uso de corticosteroides nasais (como este medicamento) pode causar um crescimento mais lento em crianças e adolescentes quando o usam durante um longo período de tempo. O médico controlará regularmente o crescimento das crianças e se assegurará de que tomem a menor dose eficaz possível.
Entre em contato com o seu médico se experimentar visão borrosa ou outras alterações visuais.
Se não tiver certeza se se encontra em alguma das situações acima, consulte o seu médico ou farmacêutico antes de usar este medicamento.
Crianças
Não se recomenda o uso deste medicamento em crianças menores de 12 anos.
Outros medicamentos e Avancort duo
Informa o seu médico ou farmacêutico se está tomando, tomou recentemente ou pode ter que tomar qualquer outro medicamento, mesmo os adquiridos sem receita.
Alguns medicamentos podem aumentar os efeitos deste medicamento, por isso o seu médico fará controles minuciosos se está tomando estes medicamentos (incluídos alguns para o VIH: ritonavir, cobicistat e medicamentos para o tratamento de infecções por fungos: cetoconazol).
Gravidez e lactação
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Condução e uso de máquinas
Este medicamento exerce uma influência mínima sobre a capacidade para conduzir e usar máquinas.
Muito raramente, pode experimentar fadiga ou tontura devido à própria doença ou durante o uso deste medicamento. Nestes casos, não conduza nem maneje máquinas. Tenha em conta que o consumo de álcool pode potenciar estes efeitos.
Avancort duo contém cloruro de benzalconio
Este medicamento contém 0,014 mg de cloruro de benzalconio em cada aplicação.
O cloruro de benzalconio pode causar irritação ou inflamação dentro da nariz, especialmente quando é usado durante um tratamento a longo prazo.
3. Como usar Avancort duo
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
É essencial que o uso deste medicamento seja regular para que o benefício terapêutico seja completo.
Evite o contato com os olhos.
Adultos e adolescentes (maiores de 12 anos)
- A dose recomendada é de uma aplicação em cada fossa nasal, pela manhã e à noite.
Uso em crianças menores de 12 anos
- Não se recomenda o uso deste medicamento em crianças menores de 12 anos.
Uso em caso de insuficiência renal e hepática
Não há dados disponíveis em pacientes com insuficiência renal e hepática.
Forma de administração
Via nasal.
Leia detenidamente as seguintes instruções e utilize o produto apenas como está indicado.
INSTRUÇÕES DE USO
Preparação da pulverização
- Agite o frasco suavemente durante 5 segundos inclinando-o de cima para baixo e, seguidamente, retire o tampão de proteção (ver figura 1).
Figura 1
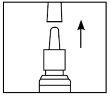
- A primeira vez que se usa o pulverizador nasal, deve-se ativar a bomba pulverizando ao ar.
- Ative a bomba colocando dois dedos de cada lado da bomba de pulverização e pondo o polegar na base do frasco.
- Pulse e libere a bomba 6 vezes, até que apareça uma pulverização fina (ver figura 2).
- Agora, a bomba está ativada e pronta para ser usada.
Figura 2
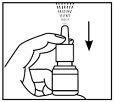
- Se não se usou o pulverizador nasal durante mais de 7 dias, terá que reativar a bomba, pressionando e liberando a mesma.
Método de pulverização
- Agite o frasco suavemente durante 5 segundos inclinando-o de cima para baixo e, seguidamente, retire o tampão de proteção (ver figura 1).
- Assoe o nariz para despejar as fossas nasais.
- Mantenha a cabeça inclinada para os pés. Não incline a cabeça para trás.
- Mantenha o frasco em posição reta e insira com cuidado a ponta do pulverizador em uma fossa nasal. 5. Tape com o dedo a outra fossa nasal, pulse rapidamente uma vez e, ao mesmo tempo, faça uma suave inspiração (ver figura 3).
- Respire pela boca.
Figura 3

- Repita a operação na outra fossa nasal.
- Respire suavemente e não incline a cabeça para trás após a aplicação. Assim, impede-se que o medicamento chegue à garganta, provocando um sabor desagradável (ver figura 4).
Figura 4

- Depois de cada uso, limpe a ponta do pulverizador com um lenço ou pano limpo, e volte a colocar o tampão de proteção.
- Não aperte a boquilla em caso de que não se obtenha a pulverização. Limpe a válvula com água. É importante que utilize a dose prescrita pelo seu médico. Use apenas a quantidade que lhe foi recomendada pelo seu médico.
Duração do tratamento
Este medicamento é apropriado para o uso prolongado. A duração do tratamento corresponde ao período em que experimenta sintomas alérgicos.
Se usa mais Avancort duo do que deve
Se se aplica mais quantidade deste medicamento no nariz, é improvável que sofra algum tipo de problema.
Em caso de dúvida, ou se usou uma dose maior do que a recomendada durante um longo período de tempo, consulte o seu médico.
Em caso de sobredose ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone 91 562 04 20, indicando o medicamento e a quantidade ingerida.
Se esqueceu de usar Avancort duo
Use o pulverizador nasal assim que se lembrar e, seguidamente, administre a dose seguinte à hora habitual. Não utilize uma dose dupla para compensar as doses esquecidas.
Se interrompeu o tratamento com Avancort duo
Não interrompa o tratamento sem consultar o seu médico, porque põe em risco o sucesso do seu tratamento.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Posíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Efeitos adversos muito frequentes (podem afetar mais de 1 de cada 10 pessoas):
- Hemorragia nasal.
Efeitos adversos frequentes (podem afetar até 1 de cada 10 pessoas):
- Dor de cabeça.
- Sabor amargo na boca, especialmente se inclina a cabeça para trás durante o uso do pulverizador nasal. Este sabor deve desaparecer se beber um refresco alguns minutos após usar este medicamento.
- Cheiro desagradável.
Efeitos adversos pouco frequentes (podem afetar até 1 de cada 100 pessoas):
- Leve irritação do interior da nariz, que pode causar leve coceira, picor ou espirros.
- Secura nasal, tosse, secura de garganta ou irritação de garganta.
Efeitos adversos raros (podem afetar até 1 de cada 1.000 pessoas):
- Secura de boca.
Efeitos adversos muito raros (podem afetar até 1 de cada 10.000 pessoas):
- Tontura ou sonolência.
- Cataratas, glaucoma ou aumento da pressão no olho, com possível perda de visão e/ou vermelhidão e dor de olhos. Estes efeitos adversos foram observados com tratamentos prolongados com pulverizações nasais de propionato de fluticasona.
- Lesões da pele e mucosa da nariz.
- Sensação de mal-estar, cansaço, fraqueza ou debilidade.
- Exantema, vermelhidão ou coceira da pele, urticária.
- Broncoespasmo (estreitamento das vias aéreas dos pulmões).
Solicite imediatamente atenção médica se desenvolver algum dos seguintes sintomas:
- Inchaço do rosto, lábios, língua ou garganta, que possam dificultar a deglutição/respiração e súbita aparência de exantema na pele. Estes poderiam ser sinais de uma reação alérgica grave. Tenha em conta que isto é muito raro.
Efeitos adversos com frequência não conhecida (a frequência não pode ser estimada a partir dos dados disponíveis)
- Visão borrosa
- Úlceras no nariz
Quando este medicamento é administrado a doses elevadas durante um período prolongado de tempo, podem produzir-se efeitos adversos sistémicos (efeitos adversos que afetam todo o organismo). A probabilidade de que se produzam estes efeitos é muito menor se se utiliza uma pulverização nasal de corticosteroides em vez de corticosteroides por via oral. Estes efeitos podem variar entre pacientes individuais e entre as diferentes preparações de corticosteroides (ver seção 2).
Os corticosteroides nasais podem afetar a produção normal de hormonas no seu corpo, especialmente se forem usados altas doses durante largo tempo. Em crianças e adolescentes, este efeito adverso pode provocar um crescimento mais lento.
Em casos raros, produz-se uma redução da densidade óssea (osteoporose) quando os corticosteroides são administrados por via nasal durante um longo período de tempo.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Avancort duo
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no frasco e caixa após “CAD”. A data de validade é o último dia do mês que se indica.
Este medicamento não requer condições especiais de conservação. Não refrigerar ou congelar.
Validade após a abertura: Descarte qualquer resto não utilizado do medicamento 6 meses após abrir pela primeira vez o pulverizador nasal.
Os medicamentos não devem ser jogados nos deságues nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Avancort duo
Os princípios ativos são: azelastina hidrocloruro e fluticasona propionato.Cada g de suspensão contém 1.000 microgramas de azelastina hidrocloruro e 365 microgramas de fluticasona propionato.
Cada aplicação (0,14 g) libera 137 microgramas de azelastina hidrocloruro (=125 microgramas de azelastina) e 50 microgramas de fluticasona propionato.
Os demais componentes (excipientes) são: edetato de disódio, glicerol (E-422), celulosa microcristalina e carmelosa sódica, polissorbato 80, cloruro de benzalconio, álcool feniletílico e água purificada.
Aspecto do produto e conteúdo do envase
Avancort duo é uma suspensão homogênea de cor branca.
Avancort duo é apresentado em um frasco de vidro âmbar de Tipo I, equipado com uma bomba pulverizadora, um aplicador nasal de polipropileno (acionador) e um tampão de proteção contra o pó, que contém 23 g (pelo menos 120 aplicações) de suspensão.
Tamanho do envase:
Um frasco com 23 g de suspensão em frasco de 25 ml (pelo menos 120 aplicações).
Titular da autorização de comercialização e responsável pela fabricação
Titular da Autorização de Comercialização
Laboratórios Cinfa, S.A
Carretera Olaz-Chipi, 10. Polígono Industrial Areta
31620 Huarte (Navarra) – Espanha
Responsável pela fabricação
ELPEN Pharmaceutical Co Inc
Marathonos Avenue, 95, Pikermi
19009, Grécia
ou
Laboratórios Cinfa, S.A
Carretera Olaz-Chipi, 10. Polígono Industrial Areta
31620 Huarte (Navarra) – Espanha
Data da última revisão deste prospecto: Abril 2025
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) (http://www.aemps.gob.es/)
Pode aceder a informação detalhada e atualizada sobre este medicamento escaneando com o seu telemóvel (smartphone) o código QR incluído no prospecto e no cartonagem. Também pode aceder a esta informação na seguinte direção de internet:
https://cima.aemps.es/cima/dochtml/p/90298/P_90298.html
Código QR a: https://cima.aemps.es/cima/dochtml/p/90298/P_90298.html
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasalForma farmacêutica: PRODUTO PARA USO NASAL, 137 microgramas/50 microgramas/ativaçãoSubstância ativa: fluticasone, combinationsFabricante: Teva B.V.Requer receita médicaForma farmacêutica: PRODUTO PARA USO NASAL, 137 microgramas/50 microgramas/aplicaçãoSubstância ativa: fluticasone, combinationsFabricante: Especialidades Farmaceuticas Centrum S.A.Requer receita médicaForma farmacêutica: PRODUTO PARA USO NASAL, 1 mg/g - 0,365 mg/gSubstância ativa: fluticasone, combinationsFabricante: Viatris Healthcare LimitedRequer receita médica
Alternativas a AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal em Polónia
Alternativa a AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal em Ukraine
Médicos online para AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de AVANCORT DUO 137/50 microgramas/aplicação suspensão para spray nasal – sujeita a avaliação médica e regras locais.









