
Dazlaris
Pergunte a um médico sobre a prescrição de Dazlaris

Como usar Dazlaris
folheto para o doente
Folheto anexado ao embalagem: informação para o utilizador
Dazlaris
(137 microgramas + 50 microgramas)/dose nasal
aerossol nasal, suspensão
Azelastina hidroclorido + Propionato de fluticasona
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto, para que possa relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o seu médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é Dazlaris e para que é utilizado
- 2. Informações importantes antes de tomar Dazlaris
- 3. Como tomar Dazlaris
- 4. Efeitos não desejados
- 5. Como conservar Dazlaris
- 6. Conteúdo do embalagem e outras informações
1. O que é Dazlaris e para que é utilizado
O medicamento Dazlaris contém duas substâncias ativas: azelastina hidroclorido e propionato de fluticasona.
- A azelastina hidroclorido pertence a um grupo de medicamentos chamados de anti-histamínicos. Os anti-histamínicos actuam impedindo a acção de substâncias como a histamina, que o organismo produz como parte da reacção alérgica e, assim, reduzem os sintomas de rinite alérgica.
- O propionato de fluticasona pertence a um grupo de medicamentos chamados de corticosteroides, que reduzem a inflamação.
O medicamento Dazlaris é utilizado para aliviar os sintomas de rinite alérgica sazonal e perene, de intensidade moderada a grave, quando a utilização de outros produtos medicinais nasais que contenham apenas um anti-histamínico ou um corticoide é considerada insuficiente.
2. Informações importantes antes de tomar Dazlaris
Quando não tomar Dazlaris
- se o doente for alérgico à azelastina hidroclorido ou ao propionato de fluticasona ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6).
Precauções e advertências
Antes de começar a tomar Dazlaris, deve discutir com o seu médico ou farmacêutico:
- Se o doente teve recentemente uma operação nasal.
- Se o doente tiver uma infecção nasal. A infecção nasal deve ser tratada com antibióticos ou antifúngicos. Os doentes que receberam antibióticos ou antifúngicos para tratar a infecção nasal podem continuar a tratar a alergia com Dazlaris.
- Se o doente tiver tuberculose ou uma infecção não tratada.
- Se o doente notar uma alteração na visão ou se tiver sido diagnosticado com aumento da pressão intra-ocular, glaucoma e (ou) catarata. Os doentes que estão nestas situações serão cuidadosamente monitorizados durante a utilização de Dazlaris.
- Se o doente tiver distúrbios da função adrenal. Deve ter cuidado ao mudar de um tratamento com esteroides administrados por via oral para a terapia com Dazlaris.
- Se o doente tiver uma doença hepática grave. Neste caso, aumenta o risco de efeitos não desejados sistémicos.
Nestes casos, o médico decidirá se Dazlaris pode ser utilizado.
Crianças e adolescentes
Não se recomenda a utilização deste medicamento em crianças com menos de 12 anos de idade.
Dazlaris e outros medicamentos
Deve informar o seu médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar, incluindo os medicamentos disponíveis sem receita médica.
Gravidez e amamentação
Se a paciente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planeiar ter um filho, deve consultar o seu médico ou farmacêutico antes de tomar este medicamento.
Condução de veículos e utilização de máquinas
O medicamento Dazlaris tem um efeito mínimo na capacidade de conduzir veículos e utilizar máquinas.
Dazlaris contém cloreto de benzalcônio
Este medicamento contém 14 microgramas de cloreto de benzalcônio em cada dose. O cloreto de benzalcônio pode causar irritação ou inchaço no interior do nariz, especialmente se for utilizado por um longo período.
3. Como tomar Dazlaris
Este medicamento deve ser sempre utilizado de acordo com as instruções do médico. Em caso de dúvidas, deve consultar o seu médico ou farmacêutico.
Utilização em adultos e adolescentes (a partir de 12 anos de idade)
Recomenda-se a utilização de uma dose em cada narina, de manhã e à noite.
Utilização em crianças com menos de 12 anos de idade
Não se recomenda a utilização deste medicamento em crianças com menos de 12 anos de idade.
Utilização em doentes com distúrbios da função renal e hepática
Não há dados disponíveis sobre a utilização em doentes com distúrbios da função renal e hepática.
Modo de administração
Administração nasal.
INSTRUÇÕES DE UTILIZAÇÃO
Preparação do aerossol
- 1. Agite suavemente a garrafa durante 5 segundos, fazendo um movimento para cima e para baixo, e retire a tampa de protecção.
- 2. Se o aerossol nasal for utilizado pela primeira vez, deve encher a bomba libertando uma dose do medicamento no ar.
- 3. Encher a bomba colocando dois dedos de cada lado da bomba e o polegar na base da garrafa.
- 4. Pressione e liberte a bomba 6 vezes, até que uma nuvem fina seja produzida (ver figura a).
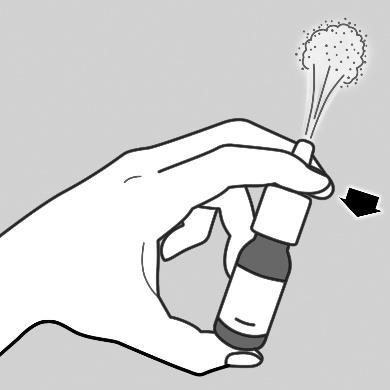
a
- 5. Agora a bomba está cheia e pronta para uso.
- 6. Se o aerossol nasal não for utilizado durante mais de 7 dias, deve reencher a bomba, pressionando-a e libertando-a uma vez.
Utilização do aerossol
- 1. Agite suavemente a garrafa durante 5 segundos, fazendo um movimento para cima e para baixo, e retire a tampa de protecção.
- 2. Assoe o nariz para limpar as narinas.
- 3. Incline a cabeça para baixo, na direcção dos pés. Não incline a cabeça para trás.
- 4. Segure a garrafa na vertical e coloque suavemente a ponta do bico na narina.
- 5. Feche a outra narina com o dedo e pressione a bomba rapidamente uma vez, enquanto inspira suavemente (ver figura b).
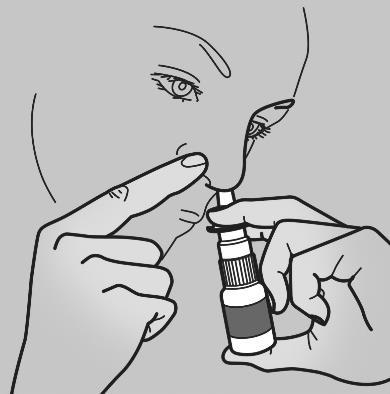
b
- 6. Expire pela boca.
- 7. Repita o processo com a outra narina.
- 8. Após a administração do medicamento, inspire suavemente e não incline a cabeça para trás. Isso evitará que o medicamento entre na garganta e cause um sabor desagradável.
- 9. Após cada utilização, limpe a ponta do bico com um lenço limpo ou um pano macio e recoloque a tampa de protecção.
- 10. Se a ponta do bico estiver obstruída, não a perfure nem use uma ferramenta afiada para desobstruí-la. Lave a ponta do bico com água.
É importante utilizar a dose prescrita pelo médico. Não deve utilizar uma dose diferente da prescrita pelo médico.
Duração do tratamento
O medicamento Dazlaris pode ser utilizado por um longo período. A duração do tratamento deve corresponder ao período durante o qual os sintomas da alergia estão presentes.
Utilização de uma dose maior do que a recomendada de Dazlaris
Em caso de utilização de uma dose excessiva do medicamento, existe um pequeno risco de complicações. Deve consultar o seu médico se algo o preocupar ou se tiver sido administrada uma dose maior do que a recomendada por um longo período. Se alguém, especialmente uma criança, ingerir acidentalmente o medicamento Dazlaris, deve contactar imediatamente o seu médico ou o serviço de emergência mais próximo.
Omissão da utilização de Dazlaris
Deve utilizar o aerossol nasal assim que se lembrar, e depois utilizar a próxima dose no horário habitual. Não deve utilizar uma dose dupla para compensar a dose omitida.
Interrupção da utilização de Dazlaris
Não deve interromper a utilização de Dazlaris sem consultar o seu médico, devido ao risco de ineficácia do tratamento.
4. Efeitos não desejados
Como qualquer medicamento, Dazlaris pode causar efeitos não desejados, embora não todos os doentes os experimentem.
- Sangramento nasal
Os efeitos não desejados muito frequentes (podem ocorrer em mais de 1 em 10 doentes):
- Dor de cabeça
- Sabor amargo na boca, especialmente se o doente inclinar a cabeça para trás durante a administração do aerossol nasal. Este sabor deve desaparecer se o doente beber um refrigerante sem álcool alguns minutos após a administração do medicamento
- Cheiro desagradável
Os efeitos não desejados frequentes (podem ocorrer em menos de 1 em 10 doentes):
- Irritação leve no interior do nariz. Pode causar uma sensação de picada, coceira ou espirros
- Secura no nariz, tosse, secura na garganta ou irritação da garganta
Os efeitos não desejados pouco frequentes (podem ocorrer em menos de 1 em 100 doentes):
- Secura na boca
Os efeitos não desejados raros (podem ocorrer em menos de 1 em 1000 doentes):
- Tontura ou sonolência
- Catarata, glaucoma ou aumento da pressão intra-ocular, o que pode causar perda de visão e (ou) vermelhidão e dor nos olhos. Estes efeitos não desejados foram relatados após a utilização prolongada do aerossol nasal que contém propionato de fluticasona.
- Lesões na pele e na mucosa nasal
- Mal-estar, sensação de fadiga, fraqueza ou cansaço
- Erupções cutâneas, coceira ou vermelhidão da pele, bolhas pruriginosas na pele
- Espasmo brônquico (constricção das vias respiratórias inferiores)
Deve procurar imediatamente ajuda médica se ocorrer algum dos seguintes sintomas:
Inchaço do rosto, lábios, língua ou garganta, que pode causar dificuldade em engolir
e (ou) respirar, bem como uma erupção cutânea súbita.Estes podem ser sintomas de uma reacção alérgica grave.
Nota: estes sintomas são muito raros.
Os efeitos não desejados com frequência desconhecida (a frequência não pode ser estimada com base nos dados disponíveis):
- Visão turva
- Úlceras na mucosa nasal
Em caso de utilização do medicamento em doses elevadas durante um longo período, podem ocorrer efeitos não desejados sistémicos (efeitos não desejados que afetam todo o organismo). A probabilidade de ocorrência destes efeitos é muito menor quando se utilizam corticosteroides na forma de aerossol nasal do que durante o tratamento com corticosteroides administrados por via oral. Estes efeitos podem variar de doente para doente e após a utilização de diferentes medicamentos corticosteroides (ver ponto 2).
Notificação de efeitos não desejados
Se ocorrer algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o seu médico ou farmacêutico. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Não Desejados de Medicamentos do Instituto Nacional de Farmácia e Medicamentos, Rua do Instituto Nacional de Farmácia e Medicamentos, 1649-022 Lisboa, telefone: +351 21 798 73 00, fax: +351 21 798 73 01, site: https://www.infarmed.pt
5. Como conservar Dazlaris
Deve conservar o medicamento em um local seguro e fora do alcance das crianças.
Não utilize este medicamento após o prazo de validade impresso na etiqueta da garrafa e na embalagem exterior, após a indicação "Validade". O prazo de validade é o último dia do mês indicado.
Não conserve o medicamento no refrigerador nem o congele.
Prazo de validade após a primeira abertura: O medicamento não utilizado deve ser eliminado após 6 meses a partir da primeira abertura do aerossol nasal.
Os medicamentos não devem ser eliminados na canalização nem nos contentores de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos de que já não precisa. Este procedimento ajudará a proteger o ambiente.
6. Conteúdo do embalagem e outras informações
O que contém o medicamento Dazlaris
- As substâncias ativas do medicamento são: azelastina hidroclorido e propionato de fluticasona. Cada grama da suspensão contém 1000 microgramas de azelastina hidroclorido e 365 microgramas de propionato de fluticasona.
A cada pressão do bico (0,14 g), são libertados 137 microgramas de azelastina hidroclorido (= 125 microgramas de azelastina) e 50 microgramas de propionato de fluticasona.
- Os outros componentes são: edetato dissódico, glicerol, celulose microcristalina, carmelose sódica, polissorbato 80, cloreto de benzalcônio, álcool feniletilico e água purificada.
Como é o medicamento Dazlaris e que embalagem contém
Dazlaris é uma suspensão branca ou quase branca, homogênea.
Dazlaris é apresentado em uma garrafa de vidro marrom com uma bomba de doseamento, um aplicador e uma tampa de protecção, em uma embalagem de cartão.
A garrafa de 25 mL contém 23 g de aerossol nasal em suspensão (pelo menos 120 doses).
Dazlaris é apresentado em:
embalagem contendo 1 garrafa com 23 g de aerossol nasal em suspensão.
Titular da autorização de introdução no mercado e fabricante
Titular da autorização de introdução no mercado
SUBSTIPHARM
24 rue Erlanger
75016 Paris
França
Fabricante
FARMEA
10, rue Bouché Thomas
ZAC d’Orgemont
49007 Angers
França
FARMACLAIR
440 Avenue Du Général De Gaulle
14200 Hérouville-Saint-Clair
França
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu sob as seguintes denominações:
Polónia: Dazlaris
Suécia: Dazlaris
República Checa: Dazlaris
Data da última revisão do folheto: 17/04/2025
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorFarmaclair FARMEA
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a DazlarisForma farmacêutica: Aerossol, (137 mcg + 50 mcg)/doseSubstância ativa: fluticasone, combinationsRequer receita médicaForma farmacêutica: Aerossol, (137 mcg + 50 mcg)/ doseSubstância ativa: fluticasone, combinationsRequer receita médicaForma farmacêutica: Aerossol, (137 mcg + 50 mcg)/dose nasalSubstância ativa: fluticasone, combinationsRequer receita médica
Alternativas a Dazlaris noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Dazlaris em Espanha
Alternativa a Dazlaris em Ukraine
Médicos online para Dazlaris
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Dazlaris – sujeita a avaliação médica e regras locais.








