
Diphereline Sr 3,75

Pergunte a um médico sobre a prescrição de Diphereline Sr 3,75

Como usar Diphereline Sr 3,75
Folheto de informação para o utilizador
Diphereline SR 3,75
3,75 mg
pó e solvente para suspensão de libertação prolongada para injeção
Triptorelina
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Se tiver alguma dúvida, deve consultar o seu médico ou farmacêutico.
- Este medicamento foi prescrito apenas para si. Não o deve dar a outros.
- Se ocorrerem efeitos secundários, incluindo quaisquer efeitos secundários não mencionados neste folheto, informe o seu médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é Diphereline SR 3,75 e para que é utilizado
- 2. Antes de tomar Diphereline SR 3,75
- 3. Como tomar Diphereline SR 3,75
- 4. Efeitos secundários
- 5. Como conservar Diphereline SR 3,75
- 6. Conteúdo da embalagem e outras informações
1. O que é Diphereline SR 3,75 e para que é utilizado
Este medicamento contém triptorelina. A triptorelina pertence a um grupo de medicamentos conhecidos como análogos do hormona liberador de gonadotropina (GnRH). Uma das suas ações é reduzir a produção de hormonas sexuais no organismo.
A administração prolongada de triptorelina, após a estimulação inicial, causa a inibição da secreção de hormonas gonadotrópicas (FSH e LH), o que tem como efeito final a inibição da função testicular e ovariana.
Também é referido um outro mecanismo de ação do medicamento: o efeito direto nos testículos e ovários através da redução da sensibilidade dos seus receptores ao hormona liberador de hormonas sexuais (gonadoliberina).
O medicamento Diphereline SR 3,75 é indicado em:
- Câncer de próstata Tratamento do câncer de próstata quando é necessário reduzir os níveis de testosterona para níveis característicos da ausência de função sexual (níveis de castração). O efeito benéfico do tratamento é mais acentuado e frequente se o doente não tiver recebido previamente qualquer outro tratamento hormonal.
- Câncer de mama em mulheres antes e após a menopausa, quando é indicado o tratamento hormonal
- Desenvolvimento sexual precoce de origem central (antes dos 8 anos de idade nas raparigas e antes dos 10 anos de idade nos rapazes).
- Endometriose dos órgãos sexuais e externos (estágio I a IV) O tratamento não deve ser realizado por mais de 6 meses (ver ponto 4.8). Não se recomenda iniciar um segundo ciclo de tratamento com triptorelina ou outro análogo de GnRH.
- Miomas uterinos Tratamento de miomas uterinos no âmbito da preparação para a cirurgia ou em doentes que não são candidatas à cirurgia.
- Infertilidade em mulheres
Tratamento de apoio em combinação com a administração de gonadotropinas (hMG, FSH, hCG) para induzir a ovulação, na preparação para a fertilização in vitro e transferência de embrião para o útero.
2. Antes de tomar Diphereline SR 3,75
Quando não tomar Diphereline SR 3,75
- se o doente for alérgico à triptorelina, gonadoliberina (GnRH), outros análogos de GnRH ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6)
- se ocorrer desenvolvimento sexual precoce gonadotrópico independente
- se a doente estiver grávida ou a amamentar
Advertências e precauções
Antes de iniciar o tratamento com Diphereline SR 3,75, deve discutir com o seu médico ou farmacêutico.
Em adultos, o tratamento prolongado com triptorelina pode causar enfraquecimento dos ossos (osteoporose) relacionado com o aumento do risco de fraturas ósseas. Deve informar o seu médico se o doente tiver algum dos seguintes fatores de risco, pois o médico pode recomendar a administração de bisfosfonatos (medicamentos utilizados no tratamento da osteoporose) para tratar a perda de massa óssea.
Os fatores de risco podem incluir:
- ocorrência de osteoporose no doente ou na família do doente;
- abuso de álcool, tabagismo, desnutrição;
- administração prolongada de medicamentos que possam causar perda de massa óssea, como medicamentos utilizados no tratamento da epilepsia ou corticosteroides (como hidrocortisona, prednisolona).
Existem relatos de ocorrência de depressão, incluindo casos de depressão grave, em doentes que tomam Diphereline SR 3,75. Se ocorrerem humores depressivos durante o tratamento com Diphereline SR 3,75, deve informar o seu médico.
Se ocorrerem convulsões, deve informar imediatamente o seu médico. Foram relatadas convulsões em doentes que tomam triptorelina ou medicamentos semelhantes. Ocorreram em doentes com epilepsia previamente diagnosticada ou sem ela.
Durante o tratamento com Diphereline SR 3,75, pode ocorrer um aumento (tumor benigno) da glândula pituitária, do qual o doente não era consciente. Os sintomas incluem dor de cabeça súbita, vómitos, distúrbios da visão e paralisia dos músculos oculares.
Homens
Em caso de administração de medicamentos anticoagulantes, pode ocorrer hemorragia no local da injeção.
No início do tratamento, foi observado um aumento dos níveis de testosterona no organismo. Isso pode causar um agravamento dos sintomas relacionados com o tumor. Nesse caso, deve contactar o seu médico. O médico pode recomendar um medicamento adicional (antagonista de andrógenos) para prevenir o agravamento desses sintomas.
Se o doente tiver obstrução das vias urinárias ou compressão da medula espinhal devido à propagação do tumor, o médico irá monitorizar o doente de perto durante as primeiras semanas de tratamento. Em caso de dificuldade em urinar, dor óssea, fraqueza nos membros inferiores ou sensação de formigamento, deve contactar imediatamente o seu médico, que avaliará o estado do doente e implementará o tratamento adequado.
A triptorelina não induz uma redução adicional dos níveis de testosterona em doentes que já foram submetidos a orquiectomia (remoção do testículo).
Os resultados dos exames diagnósticos da função gonadal da glândula pituitária e dos órgãos reprodutivos, realizados durante o tratamento ou após a interrupção da terapêutica com Diphereline SR 3,75, podem ser enganosos.
Deve informar o seu médico se o doente tiver doenças cardíacas ou vasculares, incluindo distúrbios do ritmo cardíaco (arritmia) ou se o doente estiver a tomar medicamentos utilizados no tratamento dos distúrbios do ritmo cardíaco. O risco de distúrbios do ritmo cardíaco pode ser aumentado durante o tratamento com Diphereline SR 3,75.
Os medicamentos que reduzem os níveis de testosterona podem causar alterações no eletrocardiograma (ECG) relacionadas com distúrbios do ritmo cardíaco (prolongamento do intervalo QT).
Deve informar o seu médico se o doente tiver diabetes e (ou) doenças cardíacas.
Mulheres
Miomas uterinos e endometriose
No primeiro mês de tratamento, pode ocorrer sangramento vaginal. Depois, em condições normais, a menstruação será interrompida. Se ocorrer sangramento após o primeiro mês de tratamento, deve dizer ao seu médico.
A menstruação deve retornar 2-3 meses após a última injeção. Quando o tratamento não é realizado devido à infertilidade, no primeiro mês de tratamento e após a última injeção, deve-se utilizar um método anticoncepcional não hormonal.
Se a doente tiver miomas submucosos (tumores benignos do músculo uterino localizados sob a mucosa), nos primeiros 6-10 semanas após o início do tratamento, o medicamento Diphereline SR 3,75 pode causar sangramento quando os miomas se degeneram. Em caso de sangramento intenso ou anormal ou dor, deve contactar imediatamente o seu médico.
Infertilidade em mulheres
O efeito do tratamento pode ser acentuado em um pequeno número de doentes predispostas.
O efeito do tratamento pode variar em diferentes doentes após a administração das mesmas doses, e em alguns casos, entre diferentes ciclos na mesma doente.
A administração de gonadotropinas em combinação com este medicamento para tratar a infertilidade pode causar um aumento dos ovários ou hiperestimulação dos ovários, manifestada por dor na pélvis e (ou) abdômen, bem como dificuldade em respirar. Nesse caso, deve contactar imediatamente o seu médico.
Câncer de mama em mulheres antes e após a menopausa
A administração de Diphereline SR 3,75 pode ser útil em casos em que outros métodos de tratamento não tenham levado a uma resposta clínica ou tenham perdido a eficácia.
Crianças
Em raparigas com desenvolvimento sexual precoce, no primeiro mês de tratamento, pode ocorrer sangramento vaginal.
Deve informar o seu médico se o doente tiver um tumor cerebral em progressão. Isso pode afetar a decisão do médico sobre o tratamento.
Após a interrupção do tratamento com Diphereline SR 3,75 mg no doente, ocorrerão sintomas de desenvolvimento sexual.
Em raparigas, a menstruação geralmente ocorre um ano após a interrupção do tratamento.
O médico deve excluir a possibilidade de que o desenvolvimento sexual precoce seja causado por outras doenças.
A quantidade de minerais nos ossos diminui durante o tratamento, mas retorna aos níveis normais após a interrupção do tratamento.
Após a interrupção do tratamento, pode ocorrer uma doença da articulação do quadril (necrose avascular da cabeça do fêmur), causando rigidez do quadril, fraqueza e (ou) dor intensa na virilha que irradia para a coxa. Nesse caso, deve consultar o seu médico.
Se o doente tiver dores de cabeça fortes ou recorrentes, problemas de visão e zumbido ou tinido nos ouvidos, deve contactar imediatamente o seu médico (ver ponto 4).
Em caso de preocupações relacionadas com as situações descritas acima, deve falar com o seu médico.
Diphereline SR 3,75 e outros medicamentos
Deve dizer ao seu médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar.
O medicamento Diphereline SR 3,75 pode afetar a ação de outros medicamentos utilizados no tratamento dos distúrbios do ritmo cardíaco (por exemplo, quinidina, procainamida, amiodarona, sotalol) ou pode aumentar o risco de distúrbios do ritmo cardíaco quando administrado com outros medicamentos (por exemplo, metadona utilizada no tratamento da dor e como parte do programa de desintoxicação em caso de dependência de drogas), moxifloxacina (antibiótico), medicamentos antipsicóticos utilizados no tratamento de doenças psiquiátricas graves).
Gravidez e amamentação
Se a doente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planeiar ter um filho, deve consultar o seu médico antes de tomar este medicamento.
O medicamento Diphereline SR 3,75 não deve ser utilizado durante a gravidez e amamentação.
Não deve tomar Diphereline SR 3,75 durante as tentativas de engravidar (a menos que Diphereline SR 3,75 seja parte do tratamento da infertilidade).
Condução de veículos e utilização de máquinas
Durante o tratamento, podem ocorrer tonturas, fadiga ou problemas de visão, como visão turva. Estes sintomas podem ser efeitos secundários do tratamento ou resultar da doença subjacente. Em caso de ocorrência de qualquer um desses efeitos secundários, não deve conduzir veículos ou operar máquinas.
Diphereline SR 3,75 mg contém sódio
O medicamento contém menos de 1 mmol (23 mg) de sódio por dose, ou seja, o medicamento é considerado "livre de sódio".
3. Como tomar Diphereline SR 3,75
O medicamento será administrado pelo seu médico ou enfermeira na dose adequada para o doente, dependendo da indicação para a qual foi prescrito.
Tratamento de crianças: a dose deve ser adaptada ao peso corporal.
Crianças com peso corporal superior a 30 kg: uma injeção intramuscular a cada 4 semanas (28 dias).
Crianças com peso corporal entre 20 e 30 kg: duas terças partes da dose por injeção intramuscular a cada 4 semanas (28 dias), ou seja, administrar duas terças partes do volume da suspensão preparada.
Crianças com peso corporal inferior a 20 kg: metade da dose por injeção intramuscular a cada 4 semanas (28 dias), ou seja, administrar metade do volume da suspensão preparada.
Não deve interromper o tratamento sem consultar o seu médico.
Administração de uma dose maior do que a recomendada de Diphereline SR 3,75
Em caso de sobredosagem, é recomendado o tratamento sintomático.
4. Efeitos secundários
Como qualquer medicamento, Diphereline SR 3,75 pode causar efeitos secundários, embora não todos os doentes os experimentem.
Em casos raros, pode ocorrer uma reação alérgica grave (angioedema, reação anafilática). Se ocorrerem sintomas como dificuldade em engolir ou respirar, tonturas, inchaço dos lábios, face, garganta ou língua, ou erupção cutânea, deve contactar imediatamente o seu médico.
Homens
Pode-se esperar que muitos dos efeitos secundários sejam causados pela alteração dos níveis de testosterona no organismo. Estes efeitos incluem: ondas de calor, impotência e diminuição da libido.
Muito frequentes- efeitos secundários que ocorrem em mais de 1 em cada 10 doentes
- Ondas de calor
- Fraqueza
- Sudorese intensa
- Dor nas costas
- Sensação de formigamento nos membros inferiores
- Diminuição da libido
- Impotência
Frequentes- efeitos secundários que ocorrem em até 1 em cada 10 doentes
- Náuseas, secura da boca
- Dor, hemorragia, vermelhidão e inchaço no local da injeção
- Dor muscular e óssea, dor nos braços e pernas, inchaço (acúmulo de líquido nos tecidos), dor na parte inferior do abdômen
- Hipertensão
- Reação alérgica
- Aumento de peso
- Tonturas, dor de cabeça
- Perda de libido, depressão, alterações de humor
Pouco frequentes- efeitos secundários que ocorrem em até 1 em cada 100 doentes
- Aumento do número de plaquetas
- Sensação de batimento cardíaco
- Zumbido nos ouvidos, tonturas, visão turva
- Dor abdominal, constipação, diarreia, vômitos
- Adormecimento, calafrios, sonolência, dor
- Alterações nos resultados de alguns exames (incluindo aumento da atividade de algumas enzimas), pressão arterial elevada
- Diminuição de peso
- Perda de apetite, aumento de apetite, gota (dor e inchaço nas articulações, mais frequentemente afetando o dedão do pé), diabetes, níveis elevados de gordura no sangue
- Dor articular, espasmo muscular, fraqueza muscular, dor muscular, inchaço nos tornozelos, pés ou dedos, dor óssea
- Formigamento e adormecimento
- Distúrbios do sono, irritabilidade
- Aumento da glândula mamária nos homens, dor nas mamas (seios), diminuição do tamanho dos testículos, dor nos testículos
- Dificuldade respiratória
- Acne, perda de cabelo, coceira, erupção cutânea, vermelhidão da pele, urticária
- Micção frequente à noite, distúrbios da micção
- Sangramento nasal
Raros- efeitos secundários que ocorrem em até 1 em cada 1000 doentes
- Manchas vermelhas ou roxas na pele
- Sensações anormais nos olhos, visão turva ou alterada
- Sensação de plenitude no abdômen, inchaço, alterações do paladar
- Dor no peito
- Dificuldade em manter a posição ereta
- Sintomas semelhantes aos da gripe, febre
- Reação alérgica grave (reação anafilática), que pode causar tonturas ou dificuldade em respirar, inchaço da face ou garganta
- Conjuntivite, faringite
- Estiffness articular, inchaço articular, estiffness musculoesquelética, artrite degenerativa
- Perda de memória
- Confusão, diminuição da atividade, excitação
- Dificuldade respiratória ao deitar
- Bolhas na pele
- Pressão arterial baixa
Efeitos secundários relatados após a comercialização do medicamento (frequência desconhecida):
- Estado geral de mal-estar, febre
- Convulsões
- Pressão arterial elevada
- Reação alérgica grave (reação anafilática) que pode causar inchaço da face, língua e garganta, tonturas ou dificuldade em respirar (angioedema, choque anafilático)
- Alterações em alguns parâmetros dos exames de sangue (incluindo aumento da atividade de algumas enzimas)
- Fraqueza muscular
- Confusão, sensações anormais nos olhos e (ou) alterações da visão
- Ausência de menstruação
- Diarréia
- Em caso de tumor pituitário existente, aumento do risco de sangramento na pituitária
- Urticária
Durante o tratamento da infertilidade, a administração de gonadotropinas em combinação com Diphereline SR 3,75 pode causar dor na pélvis menor e (ou) abdômen, bem como dificuldade respiratória. Em caso de ocorrência desses sintomas, deve dizer ao seu médico.
Sintomas devido aos quais o tratamento da endometriose foi justificado (dor pélvica, dor menstrual) podem piorar no início do tratamento, mas devem melhorar dentro de uma a duas semanas. Isso pode ocorrer mesmo que o tratamento seja eficaz. Deve informar imediatamente o seu médico.
Crianças
Muito frequentes- efeitos secundários que ocorrem em mais de 1 em cada 10 doentes
- Em raparigas, no primeiro mês de tratamento, pode ocorrer sangramento vaginal
Frequentes- efeitos secundários que ocorrem em até 1 em cada 10 doentes
- Dor abdominal
- Dor, hemorragia, vermelhidão e inchaço no local da injeção
- Dor de cabeça, ondas de calor
- Aumento de peso, acne
- Reação alérgica
Pouco frequentes- efeitos secundários que ocorrem em até 1 em cada 100 doentes
- Visão turva
- Vômitos, constipação, náuseas
- Obesidade
- Dor no pescoço, dor no peito
- Alterações de humor, mal-estar
- Sangramento nasal
- Coceira, erupção cutânea ou urticária
Efeitos secundários relatados após a comercialização do medicamento (frequência desconhecida):
- Pressão arterial elevada
- Convulsões
- Visão anormal
- Reação alérgica grave (reação anafilática) que pode causar inchaço da face, língua e garganta, tonturas ou dificuldade em respirar (angioedema, choque anafilático)
- Alterações em alguns parâmetros dos exames de sangue, incluindo níveis hormonais
- Dor muscular
- Alterações de humor, depressão, irritabilidade
- Idiopatia da hipertensão intracraniana (aumento da pressão dentro do crânio em torno do cérebro, caracterizado por dor de cabeça, visão dupla e outros distúrbios da visão, bem como zumbido ou tinido nos ouvidos)
Notificação de efeitos secundários
Se ocorrerem efeitos secundários, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve dizer ao seu médico ou farmacêutico, ou enfermeira. Os efeitos secundários podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Secundários de Medicamentos da Agência Reguladora de Medicamentos.
Endereço:
Al. Jerozolimskie 181C
02-222 Varsóvia
Telefone: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Sítio web: https://smz.ezdrowie.gov.pl
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
Ao notificar os efeitos secundários, é possível reunir mais informações sobre a segurança do medicamento.
5. Como conservar Diphereline SR 3,75
Deve conservar o medicamento em um local onde as crianças não possam alcançá-lo.
Não utilize este medicamento após o prazo de validade impresso na embalagem. O prazo de validade é o último dia do mês indicado.
Prazo de validade (EXP)
Número do lote (Lote)
Conservar a uma temperatura inferior a 25°C.
6. Conteúdo da embalagem e outras informações
O que contém Diphereline SR 3,75
O princípio ativo do medicamento é a triptorelina na forma de acetato de triptorelina. Cada frasco contém 3,75 mg de triptorelina.
Os outros componentes são:
- O frasco com pó contém polímero lactídico-glicólico, manitol, carmelose sódica, polissorbato 80
- A ampola com solvente contém manitol, água para injeção
Como é o medicamento Diphereline SR 3,75 e que embalagem contém
Pó e solvente para suspensão de libertação prolongada para injeção.
Frasco com pó e ampola com solvente.
Caixa contendo 1 frasco e 1 ampola com 1 seringa (de polipropileno) e 2 agulhas.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização
Ipsen Pharma
65 Quai Georges Gorse
92100 Boulogne Billancourt
França
Fabricante
Ipsen Pharma Biotech
Parc d’Activités du Plateau de Signes
Chemin départemental nº 402
83870 Signes
França
Para obter informações mais detalhadas sobre este medicamento, deve contactar o representante local do titular da autorização de comercialização:
Ipsen Poland Sp. z o.o.
ul. Chmielna 73
00-801 Varsóvia
telefone: 22 653 68 00
fax: 22 653 68 22
Data da última atualização do folheto:outubro de 2024
<-------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico:
Dosagem e modo de administração
Câncer de próstata
São possíveis dois esquemas de dosagem:
- injeção subcutânea de Diphereline 0,1 mg de libertação imediata uma vez por dia durante 7 dias consecutivos, seguida de uma injeção intramuscular de Diphereline SR 3,75 no oitavo dia, a cada 4 semanas.
- ou injeção intramuscular de Diphereline SR 3,75 a cada 4 semanas.
Em doentes com câncer de próstata com metástases resistentes à castração, que não se submetem à cirurgia, e que recebem triptorelina e são candidatos ao tratamento com inibidores da biossíntese de andrógenos, o tratamento com triptorelina deve ser continuado.
Câncer de mama em mulheres antes e após a menopausa, quando é indicado o tratamento hormonal
Uma injeção de Diphereline SR 3,75 a cada 4 semanas. Não interrompa o tratamento sem consultar o seu médico.
Desenvolvimento sexual precoce de origem central (antes dos 8 anos de idade nas raparigas e antes dos 10 anos de idade nos rapazes)
O tratamento de crianças com triptorelina deve ser realizado sob supervisão de um endocrinologista pediátrico ou pediatra ou endocrinologista com experiência no tratamento do desenvolvimento sexual precoce de origem central.
- Crianças com peso corporal superior a 30 kg: uma injeção intramuscular a cada 4 semanas (28 dias).
- Crianças com peso corporal entre 20 e 30 kg: duas terças partes da dose por injeção intramuscular a cada 4 semanas (28 dias), ou seja, administrar duas terças partes do volume da suspensão preparada.
- Crianças com peso corporal inferior a 20 kg: metade da dose por injeção intramuscular a cada 4 semanas (28 dias), ou seja, administrar metade do volume da suspensão preparada.
Endometriose
O tratamento deve ser iniciado dentro dos primeiros 5 dias do ciclo menstrual.
Esquema de administração do medicamento: uma injeção de Diphereline SR 3,75 a cada 4 semanas.
Duração do tratamento: depende do estágio inicial da endometriose e das alterações clínicas observadas durante o tratamento (funcionais e anatômicas). Em geral, o tratamento deve ser realizado por pelo menos 4 meses e no máximo 6 meses. Não se recomenda iniciar um segundo ciclo de tratamento com triptorelina ou outro análogo de GnRH.
Miomas uterinos
O tratamento deve ser iniciado dentro dos primeiros 5 dias do ciclo menstrual. Diphereline SR 3,75 deve ser administrado a cada 4 semanas. Em doentes que serão submetidas à cirurgia, o tratamento é realizado por 3 meses. Já em doentes que não são candidatas à cirurgia, o tratamento é limitado a 6 meses.
Infertilidade em mulheres
Administra-se uma ampola de Diphereline SR 3,75 por via intramuscular no segundo dia do ciclo. A administração de gonadotropinas deve ser iniciada após a redução da sensibilidade da pituitária (nível de estrogênio no sangue abaixo de 50 pg/ml), geralmente por volta de 15 dias após a injeção do medicamento Diphereline SR 3,75.
Em caso de mulheres, o especialista deve avaliar cuidadosamente a justificação da administração prolongada do medicamento por mais de 6 meses para determinar se o benefício esperado supera os efeitos secundários possíveis relacionados com a inibição prolongada da produção de estrogênio, especialmente nos ossos.
Deve seguir as instruções do seu médico e não interromper o tratamento sem consultar o seu médico.
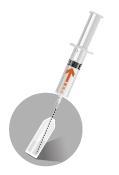
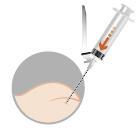
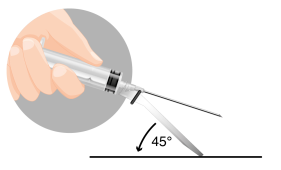
O medicamento é administrado por injeção intramuscular após a preparação.
Importante: é fundamental que a injeção seja realizada estritamente de acordo com o modo de administração.
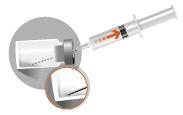
INSTRUÇÕES DE RECONSTITUIÇÃO DO MEDICAMENTO
| |
| A preparação do paciente consiste em desinfetar o local da injeção planejada na nádega. O paciente deve estar preparado para a injeção antes da reconstituição do medicamento, pois o medicamento deve ser administrado imediatamente após a sua reconstituição. | |
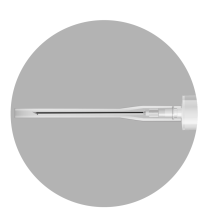 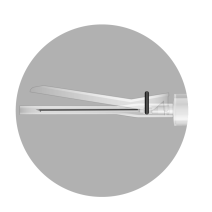 | |
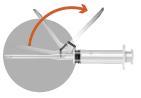
No pacote, existem 2 agulhas:
| |
2a
|  |
2b
|  |
2c
| |
2d
|  |
|  |
|  |
| 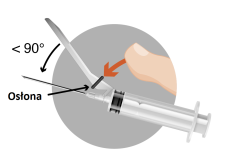 |
| Método A Método B 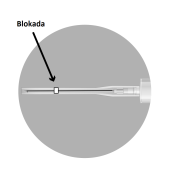 |
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorIpsen Pharma Biotech SAS
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Diphereline Sr 3,75Forma farmacêutica: Solução, 0.1 mg/mlSubstância ativa: triptorelinFabricante: Ferring GmbHRequer receita médicaForma farmacêutica: Pó, 3,75 mgSubstância ativa: triptorelinFabricante: Ferring GmbHRequer receita médicaForma farmacêutica: Pó, 0,1 mgSubstância ativa: triptorelinFabricante: Ipsen Pharma Biotech SASRequer receita médica
Alternativas a Diphereline Sr 3,75 noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Diphereline Sr 3,75 em Ukraine
Alternativa a Diphereline Sr 3,75 em Espanha
Médicos online para Diphereline Sr 3,75
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Diphereline Sr 3,75 – sujeita a avaliação médica e regras locais.











