
ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO

Pergunte a um médico sobre a prescrição de ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO

Como usar ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO
Introdução
PROSPECTO
Ultra-TechneKow FM2,15-43,00 GBq gerador de radionuclídeo
Solução de pertecnetato (99mTc) de sódio
Leia todo o prospecto detenidamente antes que lhe seja administrado este medicamento porque contém informações importantes para si.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico nuclear que supervisiona o procedimento.
- Se experimentar efeitos adversos, consulte o seu médico nuclear, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto:
1.O que é Ultra-TechneKow FM e para que é utilizado
2.O que necessita saber antes de começar a usar a solução de pertecnetato (99mTc) de sódio obtida com Ultra-TechneKow FM
3.Como usar a solução de pertecnetato (99mTc) de sódio obtida com Ultra-TechneKow FM
4.Possíveis efeitos adversos
5.Conservação de Ultra-TechneKow FM
- Conteúdo do envase e informações adicionais
1. O que é Ultra-TechneKow FM e para que é utilizado
Este medicamento é um radiofármaco unicamente para uso diagnóstico.
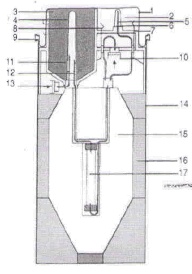
Ultra-TechneKow FM é um gerador de tecnécio (99mTc), o que significa que é um dispositivo utilizado para obter uma solução injetável de pertecnetato (99mTc) de sódio.
Quando se injeta esta solução radioativa, acumula-se temporariamente em certas zonas do corpo. A baixa quantidade de radioatividade injetada pode ser detectada fora do corpo por câmaras especiais. O médico nuclear tirará uma imagem (escâner) do órgão em questão, que pode dar informações valiosas sobre a estrutura e a função deste órgão.
Depois da injeção, a solução de pertecnetato (99mTc) de sódio é utilizada para obter imagens de várias partes do corpo, tais como:
- glândula tireoide
- glândulas salivais
- aparição de tecido do estômago em um local anormal (Divertículo de Meckel)
- condutos lagrimais dos olhos
A solução de pertecnetato (99mTc) de sódio também pode ser utilizada em combinação com outro produto para preparar outro medicamento radiofármaco. Neste caso, consulte o prospecto correspondente.
O médico nuclear explicará a si que tipo de exame será realizado com este produto.
A administração da solução de pertecnetato (99mTc) de sódio implica receber uma pequena quantidade de radioatividade. O seu médico e o médico nuclear consideraram que o benefício clínico que si obterá do procedimento com o radiofármaco supera o risco da radiação.
2. O que necessita saber antes de usar a solução de pertecnetato (99mTc) de sódio obtida com Ultra-Technekow FM
A solução de pertecnetato (99mTc) de sódio obtida comUltra-TechneKow FM não deve ser utilizada
- Se si é alérgico a pertecnetato (99mTc) de sódio ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
Advertências e precauções
Informa ao seu médico nuclear nos seguintes casos:
- se si sofre de alergias, pois se observaram alguns casos de reações alérgicas após a administração de pertecnetato (99mTc) de sódio
- se si sofre de doença renal
- se está grávida ou acredita que possa estar
- se está em período de amamentação
O seu médico nuclear informará se necessita tomar precauções especiais após utilizar este medicamento. Consulte com o seu médico nuclear se tiver alguma dúvida.
Antes da administração da solução de pertecnetato (99mTc) de sódio deve:
- beber muita água antes de começar o procedimento para urinar muito frequentemente durante as primeiras horas após a sua finalização.
- estar em jejum durante 3 a 4 horas antes da gammagrafia de divertículo de Meckel para manter baixo o peristaltismo do intestino delgado.
Crianças e adolescentes
Comunique ao seu médico nuclear se tem menos de 18 anos.
Uso da solução de pertecnetato (99mTc) de sódio com outros medicamentos:
Informa ao seu médico nuclear se está tomando, tomou recentemente ou pode ter que tomar qualquer outro medicamento, pois alguns medicamentos podem interferir na interpretação das imagens:
- atropina, usada por exemplo:
- para reduzir os espasmos do estômago, intestinos ou vesícula biliar
- para reduzir as secreções do pâncreas
- em oftalmologia
- antes da administração de uma anestesia
- para tratar o ritmo cardíaco reduzido ou
- como antídoto
- isoprenalina, um medicamento para tratar o ritmo cardíaco reduzido
- analgésicos
- laxantes(não devem ser tomados durante este procedimento, pois irritam o trato gastrointestinal)
- se tiver exames com contraste(ex. com bário como agente de contraste) ou exame gastrointestinal superior (já que estes se devem evitar nas 48 horas antes da gammagrafia do Divertículo de Meckel)
- medicamentos antitiroideos(ex. carbimazol ou outros derivados imidazólicos como o propiltiouracilo),
- salicilatos, esteroides, nitroprussiato de sódio, sulfobromoftaleína de sódio, perclorato(já que não se devem tomar durante 1 semana antes da gammagrafia)
- fenilbutazonapara tratar a febre, a dor e a inflamação no corpo (já que não se deve tomar durante 2 semanas antes da gammagrafia)
- expectorantes(já que não se devem tomar durante 2 semanas antes da gammagrafia)
- preparações tiroideas naturais ou sintéticas(ex. tiroxina sódica, liotironina de sódio, extrato de tireoide) (já que não se devem tomar durante 2-3 semanas antes da gammagrafia)
- amiodaronaum agente antiarrítmico (já que não se deve tomar durante 4 semanas antes da gammagrafia)
- benzodiazepinasutilizadas por exemplo para a sedação, ou como ansiolíticos ou anticonvulsivantes ou como medicação relaxante muscular ou lítioutilizado como estabilizador do humor na doença maníaco-depressiva (já que ambos não se devem tomar durante 4 semanas antes da gammagrafia)
- agentes de contraste por via intravenosapara exames radiológicos do corpo (já que não devem ter sido administrados durante 1-2 meses antes da gammagrafia)
Por favor, consulte com o médico nuclear antes de tomar qualquer medicamento.
Gravidez, amamentação e fertilidade
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de ficar grávida, consulte o seu médico nuclear antes de que lhe seja administrado este medicamento.
Deve informar o médico nuclear antes da administração da solução de pertecnetato (99mTc) de sódio se há alguma possibilidade de que possa estar grávida, se apresenta um atraso no período ou se está em período de amamentação. Em caso de dúvida, é importante que consulte o seu médico nuclear que supervisiona o procedimento.
Se está grávida, o médico nuclear só lhe administrará este medicamento durante a gravidez se se espera que o benefício supere o risco.
Se si está em período de amamentação, informe o seu médico nuclear, ele/ela aconselhará que a deixe até que a radioatividade se tenha ido do seu corpo. Isso leva aproximadamente 12 horas. O leite extraído deve ser descartado. A reanudação da amamentação materna deve ser acordada com o especialista em Medicina Nuclear que supervisionará o procedimento.
Condução e uso de máquinas
A solução de pertecnetato (99mTc) de sódio não tem influência sobre a capacidade para conduzir e utilizar máquinas.
A solução de pertecnetato (99mTc)desódio contém sódio
A solução de pertecnetato de sódio contém 3,5 mg/ml de sódio. Dependendo do volume injetado, pode exceder-se o limite de 1 mmol (23 mg) de sódio por dose administrada. Isso deve ser considerado se si segue uma dieta baixa em sal.
3. Como usar a solução de pertecnetato (99mTc) de sódio obtida com Ultra-TechneKow FM
Há normas estritas sobre o uso, manipulação e eliminação de radiofármacos. Ultra-TechneKow FM será utilizado unicamente em áreas controladas especiais. Este produto só será manuseado e lhe será administrado por pessoal treinado e qualificado para usá-lo de forma segura. Essas pessoas colocarão especial cuidado no uso seguro deste produto e lhe informarão das suas ações.
O médico nuclear que supervisiona o procedimento decidirá a quantidade de solução de pertecnetato (99mTc) de sódio que deve ser usada no seu caso. Esta será a quantidade mínima necessária para obter a informação desejada.
A quantidade geralmente recomendada para administrar a um adulto varia dependendo do exame a realizar e oscila entre 2 e 400 MBq (MegaBecquerelios, a unidade utilizada para expressar a radioatividade).
Uso em crianças e adolescentes
Em crianças e adolescentes a quantidade a administrar será adaptada ao seu peso corporal.
Administração da solução de pertecnetato (99mTc) de sódio e realização do procedimento
Dependendo do propósito do exame, o produto será administrado por injeção em uma veia do braço ou pode ser instilado nos olhos em forma de gotas.
Uma administração é suficiente para realizar o procedimento que o seu médico necessita.
Duração do procedimento
O seu médico nuclear informará sobre a duração habitual do procedimento.
As gammagrafias podem ser realizadas em qualquer momento, entre o momento da injeção e até 24 horas após a administração, dependendo do tipo de exame.
Depois da administração da solução de pertecnetato (99mTc) de sódio si deve:
- evitar o contato direto com crianças pequenas e mulheres grávidas durante as 12 horas após a injeção
- urinar frequentemente para eliminar o produto do seu organismo
- depois da administração, será oferecido algo para beber e será pedido que urine imediatamente antes da prova.
O médico nuclear informará se necessita tomar precauções especiais após que lhe seja administrado este medicamento. Consulte com o seu médico nuclear se tiver alguma dúvida.
Se lhe foi administrada mais solução de pertecnetato (99mTc) de sódio obtida com Ultra-TechneKow FM do que devia
É improvável uma sobredose porque si receberá uma dose única de solução de pertecnetato (99mTc) de sódio controlada com precisão pelo médico nuclear que supervisiona o procedimento. No entanto, em caso de sobredose, si receberá o tratamento apropriado. Particularmente, o médico nuclear a cargo do procedimento pode recomendar que si beba grande quantidade de líquidos para eliminar as trazas de radioatividade do seu corpo.
Se tiver alguma outra dúvida sobre o uso deste produto, pergunte ao médico nuclear que supervisiona o procedimento.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Efeitos adversos com frequência não conhecida, (não pode ser estimada a partir dos dados disponíveis):
- reações alérgicas, com sintomas tais como:
- erupção cutânea, picazón
- habões
- inflamação em várias zonas, por exemplo na face
- falta de ar
- vermelhidão da pele
- coma
- reações circulatórias, com sintomas tais como:
- ritmo cardíaco rápido, ritmo cardíaco lento
- desmaios
- visão borrosa
- tonturas
- dor de cabeça
- vermelhidão
- distúrbios gastrointestinais, com sintomas tais como:
- estar doente (vómitos)
- encontrar-se mal (náuseas)
- diarreia
- reações no local da injeção, com sintomas tais como:
- inflamação da pele
- dor
- inflamação
- vermelhidão
A administração deste radiofármaco implica receber uma pequena quantidade de radiação ionizante com um risco muito baixo de desenvolver câncer e defeitos hereditários.
Comunicação de efeitos adversos
Se experimentar efeitos adversos, consulte o seu médico nuclear, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através
do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano:
https://www.notificaram.es. Mediante a comunicação de efeitos adversos si pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Ultra-TechneKow FM
Não terá que armazenar este medicamento. Este medicamento é armazenado sob a responsabilidade do especialista em instalações apropriadas. O armazenamento de radiofármacos será realizado conforme a normativa nacional sobre materiais radioativos.
A seguinte informação está destinada unicamente ao especialista.
Não utilize este medicamento após a data de validade que aparece no envase.
6. Conteúdo do envase e informações adicionais
Composição de Ultra-TechneKow FM
- O princípio ativo é pertecnetato (99mTc) de sódio.
- Os outros componentes são: cloreto de sódio e água para preparações injetáveis.
Aspecto doprodutoe conteúdo do envase
O produto é uma solução de pertecnetato (99mTc) de sódio obtida mediante um gerador de radionuclídeo.
Ultra-TeckneKow FM tem que ser eluído e a solução obtida pode ser utilizada tal como está ou para marcação radiativa de alguns equipamentos de reagentes particulares para a preparação de radiofármacos.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização:
Curium Pharma Spain S. A.
Avenida Doctor Severo Ochoa, nº 29, 3º-2
28100, Alcobendas, Madrid, Espanha
Responsável pela fabricação:
Curium Netherlands B.V.
Westerduinweg 3
1755 LE Petten
Países Baixos
Data da última revisão deste prospecto: abril 2017
Esta informação está destinada unicamente a médicos ou profissionais do sector sanitário:
É incluída a ficha técnica completa de Ultra-TechneKow FM como um documento separado no envase do produto, com o fim de facilitar aos médicos ou profissionais do sector sanitário informações científicas e informações práticas sobre a administração e uso deste radiofármaco.
Por favor, consulte a ficha técnica.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACOForma farmacêutica: RADIOFÁRMACO, 10-40 GBqSubstância ativa: technetium (99mTc) pertechnetateFabricante: Monrol Europe S.R.L.Requer receita médicaForma farmacêutica: RADIOFÁRMACO, 2/4/6/8/10/12/16/20/25/50 GBq DE TECNÉCIO-99MSubstância ativa: technetium (99mTc) pertechnetateFabricante: Curium Pharma Spain S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 37 MBq/mlSubstância ativa: sodium iodide (123I)Fabricante: Curium Pharma Spain S.A.Requer receita médica
Alternativas a ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO em Polónia
Alternativa a ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO em Ukraine
Médicos online para ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de ULTRA-TECHnekow FM 2,15-43,00 GBq GERADOR DE RADIOFÁRMACO – sujeita a avaliação médica e regras locais.











