COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO

Pergunte a um médico sobre a prescrição de COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO

Como usar COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO
Introdução
Prospecto: informação para o utilizador
COSOPT 20mg/ml + 5mg/ml colírio em solução
dorzolamida / timolol
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, embora tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é COSOPT colírio em solução e para que é utilizado
- O que necessita de saber antes de começar a usar COSOPT colírio em solução
- Como usar COSOPT colírio em solução
- Possíveis efeitos adversos
- Conservação de COSOPT colírio em solução
Conteúdo do envase e informação adicional
1. O que é Cosopt colírio em solução e para que é utilizado
COSOPT contém dois medicamentos: dorzolamida e timolol.
- Dorzolamida pertence a um grupo de medicamentos chamados "inibidores da anidrase carbónica".
- Timolol pertence a um grupo de medicamentos chamados "betabloqueantes".
Estes medicamentos diminuem a pressão no olho de diferentes maneiras.
COSOPT é prescrito para reduzir a pressão ocular elevada no tratamento do glaucoma quando o uso de um colírio betabloqueante em monoterapia não seja adequado.
2. O que necessita de saber antes de começar a usar Cosopt colírio em solução
Não use COSOPT
- se é alérgico a dorzolamida hidrocloruro, timolol maleato ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6).
- se tem agora ou teve no passado problemas respiratórios, como asma ou bronquite obstructiva crónica grave (doença do pulmão grave que pode causar sibilância, dificuldade na respiração e/ou tosse existente desde há muito tempo).
- se tem um ritmo cardíaco lento, insuficiência cardíaca ou alterações do ritmo cardíaco (batimentos irregulares do coração).
- se sofre de doença ou distúrbios renais graves, ou antecedentes de pedras nos rins.
- se tem excesso de acidez do sangue causada por um acúmulo de cloretos no sangue (acidose hipoclorémica).
Se não tiver certeza se deve usar este medicamento, consulte o seu médico ou farmacêutico.
Advertências e precauções
Consulte o seu médico antes de começar a usar COSOPT.
Informa ao seu médico de qualquer problema médico ou ocular atual ou passado:
- cardiopatia coronária (os sintomas podem incluir dor torácica ou opressão no peito, dificuldade ao respirar, ou ahogo), insuficiência cardíaca, pressão da sangue baixa.
- alterações do ritmo cardíaco, tais como diminuição do ritmo cardíaco.
- problemas respiratórios, asma ou doença pulmonar obstructiva crónica.
- doença da circulação do sangue pobre (tal como doença de Raynaud ou síndrome de Raynaud).
- diabetes, porque o timolol pode mascarar sinais e sintomas de açúcar no sangue baixo.
- sobreactividade da glândula da tiróide, porque o timolol pode mascarar sinais e sintomas.
Informa ao seu médico, antes de que tenha uma intervenção cirúrgica, que está usando COSOPT, porque o timolol pode alterar os efeitos de alguns medicamentos usados durante a anestesia.
Também, informa ao seu médico sobre qualquer alergia ou reações alérgicas, incluindo rash, inchaço da face, lábios, língua e/ou garganta, que pode causar dificuldade na respiração ou ao engolir.
Informa ao seu médico se padece de fraqueza muscular ou se lhe foi diagnosticada miastenia grave (fraqueza muscular).
Se desenvolver qualquer outra irritação ocular ou problema novo nos olhos, como vermelhidão dos olhos ou inchaço das pálpebras, consulte imediatamente o seu médico.
Se suspeita que COSOPT lhe está causando uma reação alérgica ou hipersensibilidade (por exemplo, erupção cutânea, reação cutânea grave ou vermelhidão e coceira nos olhos), pare de usar este medicamento e consulte imediatamente o seu médico.
Informa ao seu médico se ocorre uma infecção ocular, se sofre uma lesão no olho, se se submete a uma intervenção cirúrgica ocular ou se desenvolve uma reação que inclua novos sintomas ou agravamento dos existentes.
Quando COSOPT é instilado no olho, pode afetar todo o corpo.
Crianças
Existem dados clínicos limitados da administração em lactentes e em crianças.
Pacientes de idade avançada
Nos estudos com COSOPT, os efeitos deste medicamento foram semelhantes tanto nos pacientes de idade avançada como nos mais jovens.
Uso em pacientes com deterioração hepática
Informa ao seu médico se sofre ou sofreu problemas do fígado.
Uso de COSOPT com outros medicamentos
COSOPT pode afetar ou ser afetado por outros medicamentos que está a usar, incluindo outras gotas oculares para o tratamento do glaucoma. Informa ao seu médico se está a usar ou tem intenção de usar medicamentos para reduzir a pressão arterial, medicamentos para o coração ou medicamentos para tratar a diabetes. Informa ao seu médico ou farmacêutico se está utilizando, usou recentemente ou pode ter que usar qualquer outro medicamento. Isto é particularmente importante se está:
- toma medicamentos para reduzir a pressão arterial ou para tratar doenças cardíacas (tais como bloqueadores dos canais de cálcio, betabloqueantes ou digoxina).
- toma medicamentos para tratar uma alteração ou irregularidade do ritmo cardíaco, tais como bloqueadores dos canais de cálcio, betabloqueantes ou digoxina.
- usa outro colírio que contém betabloqueantes.
- toma outro inibidor da anidrase carbónica, tal como acetazolamida.
- toma inibidores da monoamino oxidase (IMAO).
- toma um fármaco parasimpaticomimético que possa ter sido prescrito para ajudar a eliminar urina. Os parasimpaticomiméticos são também um tipo particular de medicamento que, por vezes, é usado para ajudar a restaurar os movimentos normais através do intestino.
- toma narcóticos, tais como a morfina utilizada para tratar a dor moderada a aguda.
- toma medicamentos para tratar a diabetes.
- toma antidepressivos conhecidos como fluoxetina e paroxetina.
- toma uma sulfamida.
- toma quinidina (usada para tratar distúrbios do coração e alguns tipos de malária).
Uso em desportistas: Este medicamento contém timolol que pode produzir um resultado positivo nos testes de controlo de dopagem.
Gravidez e lactação
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de usar este medicamento.
Não use COSOPT se está grávida, a não ser que o seu médico o considere necessário.
Não use COSOPT se está a amamentar o seu filho. O timolol pode chegar ao leite materno. Peça ao seu médico conselho antes de tomar qualquer medicamento durante a lactação.
Condução e uso de máquinas
Não foram realizados estudos dos efeitos sobre a capacidade para conduzir ou utilizar máquinas. Há efeitos adversos associados a COSOPT, tais como visão borrosa, que pode afetar a sua capacidade para conduzir e/ou manejar máquinas. Não conduza ou maneje máquinas até que se sinta bem ou a sua visão seja clara.
COSOPT contém cloreto de benzalconio
Este medicamento contém aproximadamente 0,002 mg de cloreto de benzalconio em cada gota, equivalente a 0,075 mg/ml.
O cloreto de benzalconio pode ser absorvido pelas lentes de contacto macias, alterando a sua cor. Retire as lentes de contacto antes de usar este medicamento e espere 15 minutos antes de voltar a colocá-las.
O cloreto de benzalconio pode causar irritação ocular, especialmente se padece de olho seco ou outras doenças da córnea (camada transparente da zona frontal do olho). Consulte o seu médico se sentir uma sensação estranha, coceira ou dor no olho após usar este medicamento.
3. Como usar Cosopt colírio em solução
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico. O seu médico estabelecerá a posologia apropriada e a duração do tratamento.
A dose recomendada é de uma gota no olho ou olhos afetados pela manhã e à noite.
Se usar este medicamento ao mesmo tempo que outro colírio, as gotas devem ser aplicadas com pelo menos 10 minutos de diferença.
Não altere a dose do medicamento sem consultar o médico.
Não deixe que a ponta do envase toque os olhos ou as zonas que os rodeiam. Pode estar contaminada com bactérias capazes de causar infecções oculares que originem danos graves nos olhos, e até mesmo a perda da visão. Para evitar uma possível contaminação do envase, lave as mãos antes de usar este medicamento e evite que a ponta do envase entre em contacto com qualquer superfície. Se acredita que o seu medicamento pode estar contaminado, ou se desenvolve uma infecção ocular, consulte o seu médico imediatamente para saber se pode continuar a usar este envase.
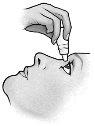
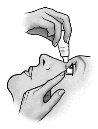
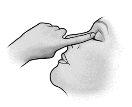
Instruções de uso:
Não use o envase se a tira de segurança de plástico ao redor do pescoço do envase não estiver ou se estiver quebrada. Quando abrir o envase pela primeira vez, arranque a tira de segurança de plástico.
Cada vez que usar COSOPT:
| |
| |
|
|
|
|
|
|
Se usar mais COSOPT do que deve
Se aplicar demasiadas gotas no olho ou engolir algo do conteúdo do envase, entre outros efeitos, pode sentir tontura, ter dificuldade em respirar ou notar que o coração lhe bate mais devagar.
Em caso de sobredosagem ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone: 91 562 04 20.
Se esquecer de usar COSOPT
É importante administrar este medicamento como lhe foi indicado pelo seu médico.
Se esquecer de aplicar uma dose, deve administrá-la o mais breve possível. No entanto, se for quase a hora da próxima dose, não administre a dose esquecida e continue com o programa de doses previsto normalmente.
Não use uma dose dupla para compensar as doses esquecidas.
Se interromper o tratamento com COSOPT
Se quiser interromper o tratamento com este medicamento, consulte primeiro o seu médico.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Efeitos adversos graves:
Se experimentar qualquer um dos seguintes efeitos adversos, pare de usar este medicamento e consulte imediatamente o seu médico, porque podem ser sinais de reação ao medicamento.
Reações generalizadas, incluindo inchaço debaixo da pele que podem ocorrer em áreas, tais como a face e membros, e podem obstruir as vias respiratórias, podendo causar dificuldade ao respirar, falta de ar, rash ou erupção com coceira, erupção generalizada e localizada, coceira, reação alérgica grave que de repente põe a vida em perigo.
Por regra, você pode continuar a usar as gotas, a menos que os efeitos sejam graves. Se está preocupado, consulte o médico ou farmacêutico. Não pare de usar COSOPT sem falar com o seu médico.
As seguintes reações adversas foram comunicadas com COSOPT ou com um dos seus componentes durante os ensaios clínicos ou após a comercialização:
Muito frequentes (podem afetar mais de 1 de cada 10 pessoas):
Queimadura e coceira dos olhos, alteração do sabor
Frequentes (podem afetar até 1 de cada 10 pessoas):
Vermelhidão em e ao redor do olho ou olhos, lagrimejo ou coceira ocular, erosão da córnea (dano na camada da frente do globo ocular), inflamação e/ou irritação em e ao redor do olho ou olhos, sensação de ter algo no olho, diminuição da sensibilidade da córnea (não aprecia que tem algo no olho e não sente dor), dor ocular, olhos secos, visão borrosa, dor de cabeça, sinusite (sensação de tensão ou congestão no nariz), náuseas, fraqueza/cansaço e fadiga.
Pouco frequentes (podem afetar até 1 de cada 100 pessoas):
Tonturas, depressão, inflamação do íris, alterações da visão, incluídas as modificações da refração (em alguns casos devido à suspensão da terapia miótica), diminuição dos batimentos cardíacos, desvanecimento, falta de ar, indigestão e pedras nos rins.
Raros (podem afetar até 1 de cada 1.000 pessoas):
Lúpus eritematoso sistémico (uma doença imune que pode causar uma inflamação dos órgãos internos), formigamento ou entorpecimento das mãos ou dos pés, insónia, pesadelos, perda de memória, um aumento nos sinais e sintomas de miastenia gravis (distúrbio muscular), diminuição do desejo sexual, acidente cerebrovascular, miopia transitória que remite ao cessar a terapia, desprendimento da camada inferior da retina que contém vasos sanguíneos após a cirurgia de filtração que pode causar alterações visuais, pálpebra caída (fazendo com que o olho permaneça meio fechado), visão dupla, crostas no pálpebra, inchaço da córnea (com sintomas de alterações visuais), pressão baixa no olho, sons de campainha no ouvido, pressão arterial baixa, alterações no ritmo ou velocidade com que bate o coração, insuficiência cardíaca congestiva (doença do coração com respiração entrecortada e inchaço de pés e pernas devido à acumulação de líquidos), edema (acumulação de líquidos), isquemia cerebral (chegada reduzida de sangue ao cérebro), dor no peito, batimentos cardíacos fortes que podem ser rápidos ou irregulares (palpitações), ataque cardíaco, fenómeno de Raynaud, mãos e pés inchados ou frios e diminuição da circulação nos seus braços e pernas, cãibras nas pernas e/ou dor de perna quando se caminha (claudicação), falta de respiração, deterioração da função pulmonar, gotejamento ou congestão de nariz, hemorragia nasal, constrição das vias respiratórias nos pulmões, tosse, irritação da garganta, secura de boca, diarreia, dermatite de contacto, perda de cabelo, erupção cutânea com aparência de cor branca prateada (erupção psoriasiforme), doença de Peyronie (que pode causar um encurvamento do pênis), reações de tipo alérgico, tais como erupção cutânea, rash, coceira, em raros casos possível inchaço dos lábios, olhos e boca, jadeamento, ou reações cutâneas graves (síndrome de Stevens-Johnson, necrólise epidérmica tóxica).
Como outros medicamentos que se aplicam aos olhos, o timolol é absorvido no sangue. Isto pode causar efeitos adversos semelhantes aos que aparecem com os agentes betabloqueantes orais. A incidência de efeitos adversos após a administração oftálmica tópica é mais baixa do que quando os medicamentos, por exemplo, são tomados pela boca ou são injetados. Os efeitos adversos adicionais listados incluem reações que aparecem dentro da classe de betabloqueantes quando se usam para tratar distúrbios oculares.
Não conhecida (a frequência não pode ser estimada a partir dos dados disponíveis):
Níveis de glicose no sangue baixos, insuficiência cardíaca, um tipo de alteração do ritmo do coração, dor abdominal, vómitos, dor muscular não causada por exercício, disfunção sexual, alucinações, sensação de corpo estranho no olho (sensação de ter algo no olho), aumento da frequência cardíaca e aumento da tensão arterial.
Comunicação de efeitos adversos:
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Cosopt colírio em solução
Mantenha este medicamento fora da vista e do alcance das crianças.
Não use este medicamento após a data de validade que aparece na etiqueta do envase e na caixa após CAD. A data de validade é o último dia do mês que se indica.
Este medicamento não requer nenhuma temperatura especial de conservação. Conserva o envase no embalagem exterior para protegê-lo da luz.
COSOPT deve ser usado num prazo não superior a 28 dias após a abertura inicial do envase.
Os medicamentos não devem ser jogados nos desagueiros nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de COSOPT
- Os princípios ativos são dorzolamida e timolol.
Cada ml contém 20 mg de dorzolamida (como 22,26 mg de dorzolamida hidrocloruro) e 5 mg de timolol (como 6,83 mg de timolol maleato).
- Os demais componentes são hidroxietil celulose, manitol, citrato de sódio, hidróxido de sódio e água para preparações inyectáveis. O cloruro de benzalconio é adicionado como conservante.
Aspecto do produto e conteúdo do envase
COSOPT é uma solução clara, incolor ou quase incolor, ligeiramente viscosa.
COSOPT é apresentado em um envase branco translúcido com 5 ml de solução. O envase de plástico é fechado com um tampão de rosca branco.
A tira de segurança que se encontra na etiqueta do envase fornece a evidência de que o medicamento não foi manipulado.
Tamanhos de envases:
1 x 5 ml (um envase de 5 ml)
3 x 5 ml (três envases de 5 ml)
6 x 5 ml (seis envases de 5 ml)
Pode ser que apenas alguns tamanhos de envases sejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
Santen Oy
Niittyhaankatu 20
33720 Tampere
Finlândia
Responsável pela fabricação
Santen Oy
Kelloportinkatu 1
33100 Tampere
Finlândia
Representante local
Santen Pharmaceutical Spain S.L.
Acanto, 22, 7º
28045 – Madrid
Espanha
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu e no Reino Unido (Irlanda do Norte) com os seguintes nomes:
Áustria, Bélgica, Dinamarca, Finlândia, França, Alemanha, Grécia, Irlanda, Itália, Luxemburgo, Países Baixos, Portugal, Espanha, Suécia e Reino Unido (Irlanda do Norte): COSOPT
Data da última revisão deste prospecto: 09/2023
A informação detalhada e atualizada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/

Quanto custa o COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO em Espanha em 2025?
O preço médio do COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO em dezembro de 2025 é de cerca de 12.11 EUR. Os valores podem variar consoante a região, a farmácia e a necessidade de receita. Confirme sempre com uma farmácia local ou fonte online para obter informações atualizadas.
- País de registo
- Preço médio em farmácia12.11 EUR
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃOForma farmacêutica: COLÍRIO, 10 mg/ml + 5 mg/mlSubstância ativa: timolol, combinationsFabricante: Novartis Europharm LimitedRequer receita médicaForma farmacêutica: COLÍRIO, 0,3 mg/ml + 5 mg/mlSubstância ativa: timolol, combinationsFabricante: Brill Pharma S.L.Requer receita médicaForma farmacêutica: COLÍRIO, 0,3 mg/ml + 5 mg/mlSubstância ativa: timolol, combinationsFabricante: Laboratorio Stada S.L.Requer receita médica
Alternativas a COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO em Poland
Alternativa a COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO em Ukraine
Médicos online para COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de COSOPT 20 mg/ml + 5 mg/ml COLÍRIO EM SOLUÇÃO – sujeita a avaliação médica e regras locais.