
BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO
Pergunte a um médico sobre a prescrição de BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO

Como usar BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO
Introdução
Prospecto: informação para o utilizador
Blizomit 10mg/ml + 5mg/ml colírio em suspensão
brinzolamida/timolol
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo. Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Blizomit e para que é utilizado
- O que necessita de saber antes de começar a usar Blizomit
- Como usar Blizomit
- Posíveis efeitos adversos
- Conservação de Blizomit
- Conteúdo do envase e informações adicionais
1. O que é Blizomit e para que é utilizado
Blizomit contém dois princípios ativos, brinzolamida e timolol, que actuam juntos para reduzir a pressão no interior do olho.
Este medicamento é utilizado para tratar a pressão elevada nos olhos, também chamada glaucoma ou hipertensão ocular, em doentes adultos com mais de 18 anos de idade e naqueles que não podem controlar eficazmente a pressão elevada nos olhos com um único medicamento.
2. O que necessita de saber antes de começar a usar Blizomit
Não use Blizomit
- Se é alérgico a brinzolamida, medicamentos chamados sulfonamidas (incluídos como exemplo medicamentos utilizados para tratar diabetes e infeções, também diuréticos (comprimidos para urinar)), timolol, betabloqueantes (medicamentos utilizados para diminuir a pressão sanguínea ou para tratar doenças cardíacas) ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- Se atualmente padece ou padeceu no passado problemas respiratórios como asma, bronquite obstructiva grave de longa duração (afeção do pulmão grave que pode causar sibilancias, dificuldade para respirar e/ou tosse persistente) ou outro tipo de problemas respiratórios.
- Se padece febre do feno grave.
- Se padece um ritmo cardíaco lento, insuficiência cardíaca ou distúrbios do ritmo cardíaco (latidos irregulares do coração).
- Se tem demasiada acidez no sangue (uma doença chamada acidose hiperclorémica).
- Se padece problemas graves de rim.
Advertências e precauções
Apenas utilize este medicamento no(s) seu(s) olho(s).
Se tiver sinais de hipersensibilidade ou reações graves, interrompa o uso deste medicamento e consulte o seu médico.
Consulte o seu médico ou farmacêutico antes de começar a usar este medicamento se padece ou padeceu no passado:
- doença cardíaca coronária (os sintomas podem incluir opressão ou dor no peito, falta de ar ou afogamento), insuficiência cardíaca, tensão arterial baixa,
- alterações do ritmo cardíaco, tais como latido lento do coração,
- problemas respiratórios, asma ou doença pulmonar obstructiva crónica,
- doença devida a má circulação sanguínea (tais como doença de Raynaud ou síndrome de Raynaud),
- diabetes, pois timolol pode mascarar os sinais e sintomas de açúcar baixo no sangue,
- hiperatividade da glândula da tiróide, pois timolol pode mascarar os sinais e sintomas de doença da tiróide,
- debilidade muscular (miastenia gravis),
- se está a ponto de se submeter a uma operação, informe o seu médico que está a utilizar este medicamento, pois timolol pode alterar os efeitos de alguns medicamentos que se utilizam durante a anestesia,
- se tem antecedentes de atopia (tendência a desenvolver uma reação alérgica) e reações alérgicas graves, pode ser mais sensível a sofrer uma reação alérgica enquanto está a utilizar este medicamento, e a adrenalina pode não ser tão eficaz para tratar uma reação alérgica. Quando receber qualquer outro tratamento, comunique ao médico ou enfermeiro que está a utilizar este medicamento,
- se tem problemas de fígado,
- se tem olhos secos ou problemas de córnea,
- se tem problemas de rim,
- se alguma vez desenvolveu uma erupção na pele grave ou descamação da pele, bolhas e/ou úlceras na boca após usar este medicamento ou outros medicamentos relacionados.
Tenha especial cuidado com este medicamento:
Foram notificadas reações de pele graves, incluindo o síndrome de Stevens-Johnson e necrólise epidérmica tóxica em associação com o tratamento de brinzolamida. Deixe de usar este medicamento e procure atenção médica imediatamente se notar algum dos sintomas relacionados com estas reações graves de pele descritas na secção 4.
Crianças e adolescentes
Não se recomenda este medicamento em crianças e adolescentes menores de 18 anos.
Outros medicamentos e Blizomit
Informa ao seu médico ou farmacêutico se está a utilizar, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento.
Este medicamento pode afetar, ou pode ser afetado por, outros medicamentos que está a utilizar, incluindo outros colírios para o tratamento do glaucoma. Consulte o seu médico se está a utilizar ou pensa utilizar medicamentos para diminuir a pressão sanguínea, tais como parasimpaticomiméticos e guanetidina, ou outros medicamentos para o coração, incluindo quinidina (utilizada para tratar afeções do coração e alguns tipos de malária), amiodarona ou outros medicamentos para tratar distúrbios do ritmo cardíaco e glucósidos para tratar insuficiência cardíaca. Consulte também o seu médico se está a utilizar ou pensa utilizar medicamentos para tratar a diabetes ou para tratar úlceras gástricas, medicamentos antifúngicos, antivirais ou antibióticos, ou antidepressivos, tais como fluoxetina e paroxetina.
Consulte o seu médico se está a utilizar outro inibidor da anidrase carbónica (acetazolamida ou dorzolamida).
Foi notificado ocasionalmente um aumento no tamanho da pupila quando se usa este medicamento junto com adrenalina (epinefrina).
Gravidez e amamentação
Se está grávida, acredita que possa estar grávida ou tem intenção de engravidar, não deve usar este medicamento a menos que o seu médico o considere necessário. Consulte o seu médico antes de utilizar este medicamento.
Não utilize este medicamento durante a amamentação, timolol pode passar para o leite materno. Consulte o seu médico antes de utilizar qualquer medicamento durante a amamentação.
Condução e uso de máquinas
Não conduza nem utilize máquinas até que a sua visão seja clara. Imediatamente após a aplicação deste medicamento, pode notar que a sua visão se torna borrosa durante um tempo.
Um dos componentes ativos pode piorar a capacidade de realizar tarefas que requeiram agudeza mental e/ou coordenação física. Se notar estes efeitos, tenha cuidado quando conduzir ou utilizar máquinas.
Blizomit contém cloreto de benzalconio
Este medicamento contém 1,7 µg de cloreto de benzalconio por gota (= 1 dose), equivalente a 0,1 mg/ml.
O cloreto de benzalconio pode ser absorvido pelas lentes de contacto macias e pode alterar a cor das lentes de contacto. Retire as lentes de contactoantes de usar este medicamento e espere 15 minutos antes de voltar a colocá-las. O cloreto de benzalconio pode causar irritação ocular, especialmente se padece de olho seco ou outras doenças da córnea (camada transparente da zona frontal do olho). Consulte o seu médico se sentir uma sensação estranha, comichão ou dor no olho após usar este medicamento.
3. Como usar Blizomit
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, consulte novamente o seu médico ou farmacêutico.
No caso de que este medicamento substitua um colírio anteriormente utilizado para o tratamento do glaucoma, interrompa o uso do medicamento anterior e comece a utilizar este medicamento no dia seguinte. Em caso de dúvida, consulte com o seu médico ou farmacêutico.
Para evitar uma possível contaminação da ponta do conta-gotas e da suspensão, deve ter a precaução de não tocar os párpados, ao redor dos mesmos ou outras superfícies com o conta-gotas. Deve manter o frasco bem fechado quando não estiver a utilizá-lo.
A instrução seguinte é útil para reduzir a quantidade de medicamento que passa para o sangue após a aplicação do colírio:
- Mantenha o párpado fechado ao mesmo tempo que pressiona com o dedo o bordo do olho junto à nariz durante pelo menos 2 minutos.
A dose recomendada é
Uma gota no olho ou olhos afetados, duas vezes ao dia.
Apenas deve aplicar este medicamento nos dois olhos se o seu médico assim o tiver recomendado. Siga o tratamento durante todo o período de tempo indicado pelo seu médico.
Como usar

1 2 3
- Pegue o frasco de Blizomit e coloque-se diante de um espelho.
- Lave as mãos.
- Agite bem antes de usar.
- Desrosqueie a tampa. Depois de remover a tampa, deve retirar o anel do lacre de segurança se estiver solto antes de utilizar este medicamento.
- Segure o frasco, boca para baixo, entre os dedos polegar e coração.
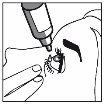
- Incline a cabeça para trás. Separe suavemente o párpado do olho com um dedo, até que se forme uma bolsa, na qual deve cair a gota (Figura 1).
- Aproxime a ponta do frasco do olho. Pode ajudar-se com o espelho.
- Não toque o olho, o párpado, zonas próximas nem outras superfícies com o conta-gotas, porque as gotas podem estar contaminadas.
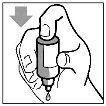
- Pressione suavemente a base do frasco para que caia uma gota de Blizomit cada vez.
- Não aperte o frasco:está projetado para que uma pressão suave sobre a base seja suficiente (Figura 2).
- Depois de utilizar Blizomit, pressione com o dedo o bordo do olho, junto à nariz, durante 2 minutos (Figura 3). Isso ajuda a evitar que Blizomit passe para o resto do corpo.
- Se aplicar gotas em ambos os olhos, repita todos os passos anteriores com o outro olho.
- Feche bem o frasco imediatamente após utilizar o produto.
- Utilize um único frasco antes de abrir o seguinte.
Se uma gota cair fora do olho, tente novamente.
Se está a utilizar outro colírio ou pomada oftálmica, espere pelo menos 5 minutos entre a aplicação de cada medicamento. As pomadas oftálmicas devem ser administradas por último.
Se usar mais Blizomit do que deve, pode eliminá-lo lavando os olhos com água morna. Não se aplique mais gotas até que seja a hora da próxima dose.
Pode experimentar uma diminuição do ritmo cardíaco, diminuição da pressão sanguínea, insuficiência cardíaca, dificuldade para respirar e afetação do sistema nervoso.
Em caso de sobredose ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone 91 562 04 20, indicando o medicamento e a quantidade utilizada.
Se esqueceu de usar Blizomit, continue com a próxima dose que estava prevista. Não se aplique uma dose dupla para compensar as doses esquecidas. Não se aplique mais de uma gota duas vezes ao dia no olho(s) afetado(s).
Se interromper o tratamento com Blizomitsem consultar o seu médico, a pressão no seu olho não estará controlada, o que pode provocar perda de visão.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Tal como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Deixe de usar Blizomit e procure atenção médica imediatamentese notar qualquer um dos seguintes sintomas:
- vermelhidão grave e picazão no olho, manchas vermelhas não elevadas, em forma de alvo ou circulares no tronco, frequentemente com bolhas centrais, descamação da pele, úlceras na boca, garganta, nariz, genitais e olhos. Estas erupções graves na pele podem ser precedidas de febre e sintomas semelhantes aos da gripe (síndrome de Stevens-Johnson, necrólise epidérmica tóxica).
A menos que os efeitos sejam graves, siga normalmente com o tratamento. Se estes efeitos o preocupam, consulte o seu médico ou farmacêutico. Não deixe de aplicar este medicamento sem consultar antes com o seu médico.
Efeitos adversos frequentes (podem afetar até 1 de cada 10 pessoas)
- Efeitos no olho:inflamação da superfície do olho, visão borrada, sinais e sintomas de irritação ocular (p. ex. queimadura, pontada, picazão, lacrimejamento, vermelhidão), dor ocular.
- Outros efeitos adversos:diminuição da frequência cardíaca, alterações do sabor.
Efeitos adversos pouco frequentes (podem afetar até 1 de cada 100 pessoas)
- Efeitos no olho:erosão da córnea (dano da camada anterior do globo ocular), inflamação da superfície do olho com a superfície danificada, inflamação dentro do olho, manchas corneais, sensação anormal nos olhos, secreção do olho, olho seco, vista cansada, picazão nos olhos, olho vermelho, vermelhidão da pálpebra.
- Outros efeitos adversos:contagem diminuída de leucócitos, descida da tensão arterial, tosse, sangue na urina presente, fraqueza corporal.
Efeitos adversos raros (podem afetar até 1 de cada 1.000 pessoas)
- Efeitos no olho:distúrbio da córnea, sensibilidade à luz, aumento da produção de lágrimas, crostas na pálpebra.
- Outros efeitos adversos:dificuldade para dormir (insônia), dor de garganta, coriza.
Frequência não conhecida (não pode ser estimada a partir dos dados disponíveis)
- Efeitos no olho:alergia ocular, alterações da visão, dano do nervo óptico, aumento da pressão ocular, depósitos na superfície do olho, percepção de estímulos diminuída no olho, inflamação ou infecção da conjuntiva (parte branca do olho), visão anormal, dupla ou reduzida, aumento da pigmentação do olho, bulto na superfície do olho, inchaço ocular, sensibilidade à luz, diminuição do crescimento ou número de pestanas, queda das pálpebras superiores (provocando que o olho fique meio fechado), inflamação da pálpebra e das glândulas das pálpebras, inflamação da córnea e desprendimento da camada de debaixo da retina que contém os vasos sanguíneos, os quais podem causar alterações da visão após operação de filtração, sensibilidade da córnea diminuída, erosão da córnea.
- Outros efeitos adversos:manchas vermelhas não elevadas, em forma de alvo ou circulares no tronco, frequentemente com bolhas centrais, descamação da pele, úlceras na boca, garganta, nariz, genitais e olhos que podem ser precedidas de febre e sintomas semelhantes aos da gripe. Estas erupções graves na pele podem ser potencialmente mortais (síndrome de Stevens-Johnson, necrólise epidérmica tóxica).
- Coração e circulação:alterações no ritmo ou frequência dos batimentos do coração, frequência cardíaca lenta, palpitações, tipo de distúrbio do ritmo cardíaco, aumento anormal da frequência cardíaca, dor no peito, função cardíaca reduzida, ataque cardíaco, aumento da tensão arterial, redução do fluxo sanguíneo ao cérebro, acidente cerebrovascular, edema (acumulação de líquido), insuficiência cardíaca congestiva (doença do coração com dificuldade para respirar e inchaço dos pés e pernas devido à acumulação de líquido), inchaço das extremidades, diminuição da tensão arterial, descoloração dos dedos das mãos e dos pés e, ocasionalmente, de outras partes do corpo (fenômeno de Raynaud), frio nos pés e mãos.
- Respiratório:constrição das vias respiratórias nos pulmões (predominantemente em pacientes com doença preexistente), falta de ar ou dificuldade para respirar, sintomas de resfriado, congestão no peito, infecção dos seios nasais (sinusite), espirros, nariz entupido, secura nasal, sangramentos nasais, asma, irritação de garganta.
- Sistema nervoso e distúrbios gerais:alucinações, depressão, pesadelos, perda de memória, dor de cabeça, nervosismo, irritabilidade, cansaço, tremor, sensação anormal, síncope, tontura, sonolência, fraqueza generalizada ou grave, sensações incomuns como formigamento.
- Gástrico:náuseas, vômitos, diarreia, gases intestinais ou desconforto abdominal, inflamação da garganta, sensação de boca seca ou anormal, dispepsia, dor de estômago.
- Sangue:valores anormais dos testes da função do fígado, aumento dos níveis sanguíneos de cloreto, ou diminuição da contagem celular dos glóbulos vermelhos nos exames de sangue.
- Alergia:aumento dos sintomas de alergia, reações alérgicas generalizadas, incluindo inchaço debaixo da pele que pode ocorrer em zonas como a face e extremidades e pode obstruir as vias respiratórias, podendo causar dificuldades para engolir ou respirar, urticária, erupção localizada e generalizada, picazão, reação alérgica repentina e grave que põe em risco a vida.
- Ouvido:zumbido nos ouvidos, sensação de tontura ou vertigem.
- Pele:erupção, vermelhidão ou inflamação da pele, sensação anormal ou diminuída na pele, perda de cabelo, erupção com aspecto branco prateado (erupção psoriasiforme) ou piora da psoríase.
- Muscular:dor muscular não causada por exercício, em articulações, costas ou generalizada, espasmos musculares, dor nas extremidades, fraqueza muscular/cansaço, aumento dos sinais e sintomas de miastenia gravis (distúrbio muscular).
- Rim:dor nos rins que se apresenta como dor na parte baixa das costas, urinar com frequência.
- Reprodução:disfunção sexual, desejo sexual diminuído, problemas sexuais masculinos.
- Metabolismo:níveis baixos de açúcar no sangue.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste folheto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Blizomit
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece no frasco e na caixa após “CAD”. A data de validade é o último dia do mês que se indica.
Este medicamento não requer condições especiais de conservação.
Para evitar infecções, deve descartar o frasco 4 semanas após a primeira abertura. Escreva a data de abertura no espaço fornecido na etiqueta do frasco e na caixa.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Deposite os recipientes e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos recipientes e dos medicamentos que já não precisa. Dessa forma, você ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição de Blizomit
- Os princípios ativos são brinzolamida e timolol. Um ml de suspensão contém 10 mg de brinzolamida e 5 mg de timolol (como maleato).
- Os demais componentes são cloreto de benzalconio (solução a 50 %) (ver seção 2 “Blizomit contém cloreto de benzalconio”), carbômero, edetato de dissódio, manitol (E421), água para preparações injetáveis, cloreto de sódio, poloxâmero, ácido clorídrico e/ou hidróxido de sódio.
São adicionadas quantidades muito pequenas de ácido clorídrico e/ou hidróxido de sódio para manter os níveis de acidez (níveis de pH) normais.
Aspecto do produto e conteúdo do envase
Frasco de plástico de 10 ml com ponta conta-gotas selada de LDPE branco e tampa de HDPE/LDPE branco com selo à prova de manipulações, que contém 5 ml de suspensão homogênea branca.
Estão disponíveis os seguintes tamanhos de envase: caixas de cartão que contêm 1 x 5 ml, 3 x 5 ml.
Pode ser que apenas alguns tamanhos de envases estejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
Pharmathen S.A.
Dervenakion 6
15351 Pallini, Attiki
Grécia
Responsável pela fabricação
Pharmathen S.A.
Dervenakion 6
15351 Pallini, Attiki
Grécia
Ou
Balkanpharma-Razgrad AD
68 Aprilsko vastanie Blvd.,
Razgrad, 7200,
Bulgária
Este medicamento está autorizado nos estados membros do Espaço Econômico Europeucom os seguintes nomes:
Alemanha | Blizomit 10 mg/ml + 5 mg/ml Augentropfensuspension |
França | BLIZOMIT 10 mg/5 mg par mL, collyre en suspension |
Espanha | Blizomit 10 mg/ml + 5 mg/ml colírio em suspensão |
Grécia | BLIZOMIT |
Países Baixos | BLIZOMIT |
Portugal | BLIZOMIT |
Itália | BLIZOMIT |
Data da última revisão destefolheto:setembro 2023
A informação detalhada deste medicamento está disponível na página web da agência
Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃOForma farmacêutica: COLÍRIO, 10 mg/ml + 5 mg/mlSubstância ativa: timolol, combinationsFabricante: Novartis Europharm LimitedRequer receita médicaForma farmacêutica: COLÍRIO, 0,3 mg/ml + 5 mg/mlSubstância ativa: timolol, combinationsFabricante: Brill Pharma S.L.Requer receita médicaForma farmacêutica: COLÍRIO, 0,3 mg/ml + 5 mg/mlSubstância ativa: timolol, combinationsFabricante: Laboratorio Stada S.L.Requer receita médica
Alternativas a BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO em Polonia
Alternativa a BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO em Ucrania
Médicos online para BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de BLIZOMIT 10 mg/mL + 5 mg/mL COLÍRIO EM SUSPENSÃO – sujeita a avaliação médica e regras locais.













