
Como usar Menopur
FOLHETO PARA O DOENTE
Folheto anexo ao embalagem: informação para o doente
MENOPUR, 75 IU FSH + 75 IU LH, pó e solvente para preparar solução para injeção
para injeções
Menotropina
Deve ler-se atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder reler caso necessário.
- Em caso de alguma dúvida, deve consultar o médico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico. Ver ponto 4.
Índice do folheto:
- 1. O que é MENOPUR e para que é utilizado
- 2. Informações importantes antes de tomar MENOPUR
- 3. Como tomar MENOPUR
- 4. Efeitos não desejados
- 5. Como conservar MENOPUR
- 6. Conteúdo do embalagem e outras informações
1. O que é MENOPUR e para que é utilizado
MENOPUR é um pó em forma de massa compacta que, antes da administração, deve ser dissolvido em líquido (solvente). O medicamento é administrado por injeção subcutânea ou intramuscular.
MENOPUR (menotropina de alta pureza obtida da urina de mulheres pós-menopáusicas) contém dois hormônios: hormônio folículo-estimulante (FSH) e hormônio luteinizante (LH).
FSH e LH são hormônios produzidos no organismo da mulher e do homem. Eles permitem o funcionamento normal dos órgãos do aparelho reprodutor.
MENOPUR é utilizado no tratamento da infertilidade nas seguintes situações:
em mulheres que não conseguem engravidar porque os ovários não produzem óvulos (também no caso da síndrome do ovário policístico). MENOPUR é utilizado em mulheres que, para o tratamento da infertilidade, já receberam citrato de clomifeno, mas este medicamento se revelou ineficaz;
em mulheres que participam em programas de reprodução assistida, tais como a fecundação in vitro e a transferência de embrião, a transferência de gameta para o oviduto e a injeção intracitoplasmática de espermatozoides no óvulo. MENOPUR estimula a produção, pelos ovários, de vários folículos ovarianos, nos quais os óvulos podem desenvolver-se (desenvolvimento de vários folículos ovarianos);
em homens, cujos testículos produzem uma quantidade insuficiente de espermatozoides devido à falta de gonadotropinas (hormônios produzidos pela hipófise e que influenciam os testículos).
2. Informações importantes antes de tomar MENOPUR
Antes de iniciar o tratamento com MENOPUR, é necessário que o médico avalie as causas da infertilidade em ambos os parceiros. É especialmente importante verificar se não existem doenças que requeiram um tratamento diferente:
hipotireoidismo e hipoadrenalismo;
níveis elevados de prolactina (hiperprolactinemia);
tumores da hipófise (glândula localizada na base do cérebro);
tumores do hipotálamo (área localizada sob a parte do cérebro chamada tálamo).
Se o doente tiver alguma das doenças mencionadas acima, deve informar o médico antes de iniciar o tratamento com MENOPUR.
Quando não tomar MENOPUR
Nas mulheres e homens:
se o doente for alérgico à menotropina ou a qualquer outro componente deste medicamento (listados no ponto 6);
se tiver sido detectado um tumor da hipófise ou do hipotálamo
Nas mulheres:
se a doente estiver grávida ou amamentando;
se a doente tiver cistos ovarianos ou aumento dos ovários não causado pela síndrome do ovário policístico;
se a doente apresentar sangramentos vaginais de causa desconhecida;
se a doente tiver tumores do útero, ovários ou seios;
se a doente tiver malformações dos órgãos genitais que impeçam o desenvolvimento da gravidez;
se a doente tiver miomas uterinos que impeçam o desenvolvimento da gravidez;
se a doente tiver menopausa precoce.
Nos homens:
se o doente tiver cancro da próstata;
se o doente tiver tumores dos testículos.
Precauções e advertências
Deve ter cuidado se a doente apresentar:
dor abdominal;
inchaço abdominal;
náuseas;
vômitos;
diarreia;
ganho de peso;
dificuldades respiratórias;
redução da frequência ou quantidade de urina eliminada.
Se algum desses sintomas ocorrer, deve informar imediatamente o médico, mesmo que apareçam alguns dias após a última dose do medicamento. Podem ser sintomas de hiperestimulação ovariana, que pode ter um curso grave.
Se esses sintomas piorarem, deve interromper o tratamento da infertilidade e iniciar o tratamento apropriado no hospital.
A observância da dose prescrita e a monitorização cuidadosa do tratamento reduzem a probabilidade de ocorrência desses sintomas.
Esses sintomas podem ocorrer também quando se interrompe o tratamento com MENOPUR. Se ocorrer algum desses sintomas, deve contactar imediatamente o médico.
Durante o tratamento com MENOPUR, o médico geralmente encaminha a doente para exames de ultrassom (com uso de ultrassom) e, por vezes, para exames de sangue para verificar a resposta ao tratamento.
O tratamento com hormônios como MENOPUR pode aumentar o risco de:
gravidez ectópica (fora do útero) em mulheres com doenças dos ovidutos previamente diagnosticadas;
aborto espontâneo;
gravidez múltipla (gémeos, trigémeos, etc.);
malformações congênitas (defeitos físicos presentes no bebê ao nascimento).
Em algumas mulheres submetidas a tratamento para infertilidade, desenvolveram-se cistos ovarianos ou tumores de outros órgãos do aparelho reprodutor. Até ao momento, não se sabe se isso foi causado pelo tratamento com hormônios como MENOPUR.
A probabilidade de ocorrência de tromboses nas veias ou artérias é maior em mulheres grávidas. O tratamento da infertilidade pode aumentar a probabilidade de tromboses, especialmente se a doente tiver excesso de peso ou se as tromboses ocorreram previamente na doente ou em algum familiar (parentes). A doente deve informar o médico se achar que isso a afeta.
MENOPUR, juntamente com o hormônio chamado gonadotropina coriônica humana (hCG), pode ser administrado no tratamento da infertilidade em homens.
Crianças e adolescentes
O uso do medicamento MENOPUR em crianças e adolescentes não é apropriado.
MENOPUR e outros medicamentos
Deve informar o médico sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar.
O citrato de clomifeno é outro medicamento utilizado no tratamento da infertilidade. Se MENOPUR for administrado ao mesmo tempo que o citrato de clomifeno, o efeito nos ovários pode ser aumentado.
MENOPUR pode ser utilizado em conjunto com o medicamento BRAVELLE. Ver ponto 3.
Gravidez e amamentação
O medicamento MENOPUR não deve ser utilizado durante a gravidez ou amamentação.
Condução de veículos e utilização de máquinas
É pouco provável que MENOPUR afete a capacidade de conduzir veículos ou utilizar máquinas.
MENOPUR contém cloreto de sódio
MENOPUR contém menos de 1 mmol de cloreto de sódio (23 mg) por dose, ou seja, o medicamento é considerado "livre de sódio".
3. Como tomar MENOPUR
Este medicamento deve ser sempre utilizado de acordo com as recomendações do médico. Em caso de dúvida, deve consultar o médico.
Mulheres que não ovulam (não produzem óvulos)
O tratamento deve ser iniciado dentro dos primeiros 7 dias do ciclo menstrual (o dia 1 é o primeiro dia da menstruação). O medicamento deve ser administrado diariamente durante pelo menos 7 dias.
A dose inicial é geralmente de 75 IU (unidades internacionais) de FSH + 75 IU de LH a 150 IU de FSH + 150 IU de LH (ou seja, de 1 a 2 ampolas de pó) por dia, mas pode ser ajustada de acordo com a resposta da doente até um máximo de 225 IU de FSH + 225 IU de LH (ou seja, 3 ampolas de pó) por dia. A dose prescrita deve ser administrada durante pelo menos 7 dias antes de qualquer ajuste da dose. Recomenda-se que, em cada ajuste, a dose seja aumentada em 37,5 IU de FSH + 37,5 IU de LH (ou seja, meia ampola de pó), mas não mais de 75 IU de FSH + 75 IU de LH (ou seja, 1 ampola de pó). O ciclo de tratamento deve ser interrompido se, após 4 semanas, não for detectada resposta.
Quando a resposta for satisfatória, no dia seguinte à última injeção de MENOPUR, deve ser administrada uma injeção única de outro hormônio - hCG em dose de 5000 IU a 10 000 IU.
Recomenda-se que a doente tenha relações sexuais no dia da administração e no dia seguinte à administração de hCG.
Alternativamente, pode ser realizada uma inseminação (introdução de sêmen diretamente no útero). A doente permanece sob vigilância cuidadosa do médico durante pelo menos 2 semanas após a administração de hCG.
O médico verificará os resultados do tratamento com MENOPUR. De acordo com o progresso do tratamento, o médico pode decidir interromper a administração de MENOPUR e não administrar hCG. Nesse caso, a doente será aconselhada a usar um método anticoncepcional mecânico (por exemplo, preservativo) ou a abster-se de relações sexuais até à próxima menstruação.
Mulheres que participam em programas de reprodução assistida
Se a doente também receber um tratamento com um agonista do GnRH (medicamento que ajuda a estimular a ação do hormônio que libera as gonadotropinas, GnRH), a administração de MENOPUR deve ser iniciada cerca de 2 semanas após o início do tratamento com o agonista do GnRH.
Se a doente também receber um tratamento com um antagonista do GnRH, a administração de MENOPUR deve ser iniciada no 2.º ou 3.º dia do ciclo menstrual (o dia 1 da menstruação é o primeiro dia do ciclo).
O medicamento deve ser administrado diariamente durante pelo menos 5 dias. A dose inicial de MENOPUR é geralmente de 150 IU de FSH + 150 IU de LH a 225 IU de FSH + 225 IU de LH (ou seja, de 2 a 3 ampolas de pó) por dia. De acordo com a resposta da doente ao tratamento, a dose pode ser aumentada até um máximo de 450 IU de FSH + 450 IU de LH (ou seja, 6 ampolas de pó) por dia. Não deve aumentar a dose de uma vez mais do que 150 IU de FSH + 150 IU de LH (ou seja, 2 ampolas de pó). Geralmente, o tratamento não deve durar mais de 20 dias.
Após a detecção de um número suficiente de folículos ovarianos de tamanho apropriado, a doente recebe uma injeção única de hCG em dose de até 10 000 IU para induzir a ovulação (libertação do óvulo).
A doente permanece sob vigilância cuidadosa do médico durante pelo menos 2 semanas após a administração de hCG.
O médico verificará os resultados do tratamento com MENOPUR. De acordo com o progresso do tratamento, o médico pode decidir interromper a administração de MENOPUR e não administrar hCG. Nesse caso, a doente será aconselhada a usar um método anticoncepcional mecânico (por exemplo, preservativo) ou a abster-se de relações sexuais até à próxima menstruação.
Homens:
O tratamento começa com a administração de hCG 3 vezes por semana em dose de 1000 IU a 3000 IU, até que se obtenha um nível adequado de testosterona no sangue. Em seguida, administra-se MENOPUR por via intramuscular em dose de 75 IU de FSH + 75 IU de LH a 150 IU de FSH + 150 IU de LH (ou seja, de 1 a 2 ampolas de pó) 3 vezes por semana durante vários meses.
INSTRUÇÕES PARA A ADMINISTRAÇÃO
Se o médico prescrever a autoadministração de MENOPUR, deve seguir todas as instruções fornecidas.
A primeira injeção de MENOPUR deve ser feita sob supervisão do médico.
RECONSTITUIÇÃO (DISSOLUÇÃO) DE MENOPUR:
MENOPUR é um pó e, antes da injeção, deve ser reconstituído (dissolvido). O líquido para dissolver o pó é fornecido com o pó. MENOPUR deve ser reconstituído imediatamente antes da administração. Para isso, deve:
- Colocar uma agulha grossa e longa na seringa (agulha para reconstituição).
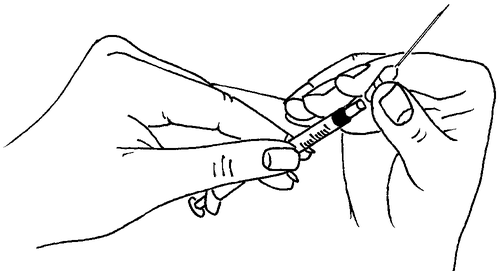
reconstituir.
- Quebrar a parte superior da ampola com o solvente no local indicado pelo ponto.
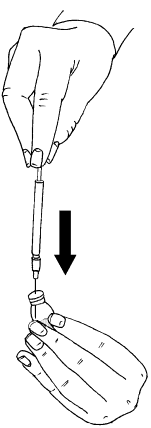
- Introduzir a agulha na ampola com o solvente.
- Retirar todo o líquido da ampola para a seringa.
- Introduzir a agulha através da tampa de borracha da ampola com o pó e, lentamente, injetar todo o líquido.
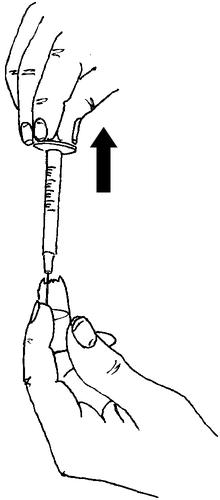
Visar a parede da ampola para evitar a formação de bolhas.
O pó deve dissolver-se rapidamente (em 2 minutos), formando uma solução transparente.
- Para facilitar a reconstituição do pó, pode-se agitar suavemente a ampola. Não deve agitar, pois isso pode causar a formação de bolhas.
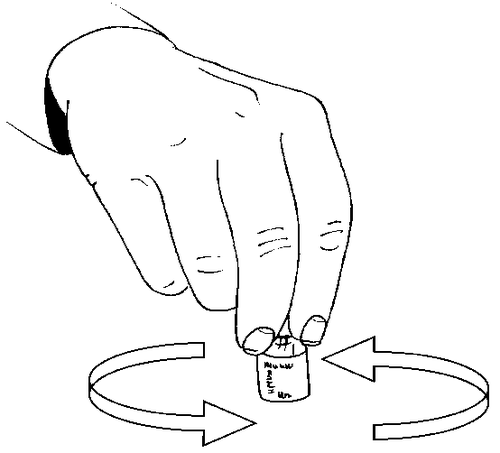
de ar. Se a solução não for transparente ou contiver partículas, não a deve usar.
- Retirar a solução de volta para a seringa.
Se o médico prescrever mais de uma ampola de MENOPUR por injeção, a solução obtida após a reconstituição do pó da primeira ampola pode ser injetada na segunda ampola com o pó. Esta operação pode ser repetida com as ampolas subsequentes com o pó - até um máximo de 3 ampolas com o pó -, mas apenas se o médico o tiver prescrito.
Se o médico prescrever o medicamento BRAVELLE juntamente com MENOPUR, pode misturar os dois medicamentos. Para isso, deve reconstituir MENOPUR, injetar lentamente a solução resultante na ampola com o medicamento BRAVELLE, esperar até que o medicamento BRAVELLE se dissolva, retirar a solução que contém os dois medicamentos para a seringa e injetar por via subcutânea. Este procedimento permite evitar a injeção de cada medicamento separadamente.
ADMINISTRAÇÃO DE MENOPUR:
- Após retirar a dose prescrita de MENOPUR para a seringa, deve trocar a agulha
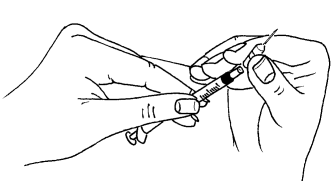
por uma agulha curta e fina (agulha para injeções).
- Posicionar a seringa com a agulha para cima e, com o dedo, bater suavemente na seringa para que as bolhas de ar subam para o topo. Pressionar suavemente o êmbolo da seringa até que uma primeira gota do líquido apareça na ponta da agulha.
- A doente é informada pelo médico ou pela enfermeira sobre onde injetar o medicamento (por exemplo, parte da frente da coxa, abdômen, etc.).
- Desinfetar (desinfectar) a pele no local da injeção.
- Para fazer a injeção, deve criar um dobra na pele com os dedos e, com um movimento rápido, introduzir a agulha a 90 graus (perpendicularmente). Injetar a solução, pressionando o êmbolo da seringa, e, em seguida, retirar a agulha.
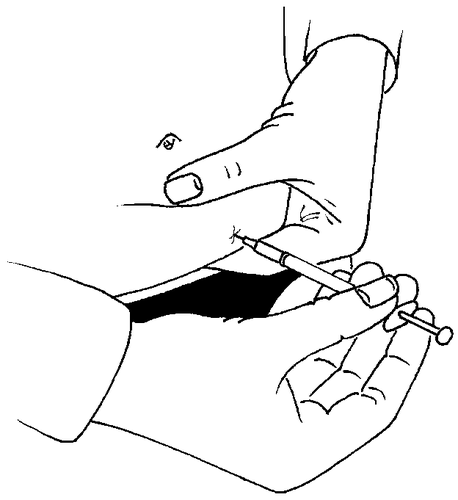
Após a retirada da agulha, pressionar o local da injeção para evitar sangramento. Uma massagem suave no local da injeção ajuda a espalhar a solução sob a pele.
- Os objetos usados não devem ser jogados fora nos contentores domésticos de resíduos, mas eliminados de forma apropriada.
Uso de uma dose maior do que a recomendada de MENOPUR
Em caso de uso de uma dose maior do que a recomendada de MENOPUR, deve informar o médico.
Omissão da administração de MENOPUR
Não deve tomar uma dose dupla para compensar a dose omitida. Em caso de omissão da administração de MENOPUR, deve informar o médico.
4. Efeitos não desejados
Como qualquer medicamento, MENOPUR pode causar efeitos não desejados, embora não todos os doentes os experimentem.
Os hormônios utilizados no tratamento da infertilidade, como MENOPUR, podem causar uma hiperestimulação ovariana, levando à ocorrência de uma doença chamada síndrome de hiperestimulação ovariana (OHSS), especialmente em mulheres com síndrome do ovário policístico. Os sintomas incluem: dor abdominal, inchaço abdominal, náuseas, vômitos, diarreia e ganho de peso. Em casos graves de OHSS, ocorreram complicações, tais como acúmulo de líquido na cavidade abdominal, na cavidade pélvica e (ou) na cavidade pleural, dificuldades respiratórias e redução da frequência ou quantidade de urina eliminada, formação de coágulos sanguíneos nos vasos sanguíneos (distúrbios tromboembólicos) e torção ovariana.
Se ocorrer algum desses sintomas, deve contactar imediatamente o médico, mesmo que apareçam alguns dias após a última dose do medicamento.
Durante o tratamento, podem ocorrer reações alérgicas (sensibilidade). Os sintomas dessas reações podem ser: erupções cutâneas, prurido, inchaço da garganta e dificuldades respiratórias. Se ocorrer algum desses sintomas, deve contactar imediatamente o médico.
Os seguintes efeitos não desejadossão frequentes, ou seja, ocorrem em 1 a 10 de cada 100 doentes tratados:
dor abdominal;
dor de cabeça;
náuseas;
inchaço abdominal;
dor pélvica;
estimulação ovariana excessiva, causando um nível alto de atividade (síndrome de hiperestimulação ovariana);
reações no local da injeção, tais como dor, vermelhidão, equimose, inchaço e (ou) prurido.
Os seguintes efeitos não desejadossão infrequentes, ou seja, ocorrem em 1 a 10 de cada 1000 doentes tratados:
vômitos;
distúrbios abdominais;
diarreia;
fadiga;
tontura;
bolhas com líquido nos ovários (cistos ovarianos);
distúrbios mamários, incluindo dor mamária, sensibilidade mamária, desconforto, dor nos mamilos e inchaço mamário;
ondas de calor.
Os seguintes efeitos não desejadossão raros, ou seja, ocorrem em 1 a 10 de cada 10 000 doentes tratados:
acne;
erupções cutâneas.
Além dos anteriormente mencionados, foram observados após a autorização do medicamento MENOPUR para a comercialização os seguintes efeitos não desejados, cuja frequênciade ocorrência é desconhecida:
distúrbios da visão;
febre;
mal-estar;
reações alérgicas;
aumento de peso;
dor muscular e articular (por exemplo, dor nas costas, dor no pescoço e dor nos braços e pernas);
torção ovariana, como complicação da hiperestimulação ovariana induzida pela estimulação excessiva;
prurido;
urticária;
coágulos sanguíneos, como complicação da hiperestimulação ovariana induzida pela estimulação excessiva.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Não Desejados de Medicamentos da Agência Reguladora de Medicamentos, Produtos Médicos e Produtos Biocidas {endereço atual ,número de telefone e fax do referido Departamento} e-mail: [email protected] .
A notificação de efeitos não desejados pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como conservar MENOPUR
O medicamento deve ser conservado em local não visível e inacessível às crianças.
Não conservar a uma temperatura superior a 25°C.
Conservar no embalagem original para proteger da luz.
Não usar este medicamento após o prazo de validade impresso na caixa e nas etiquetas da ampola e da ampola após a palavra EXP. O prazo de validade é o último dia do mês indicado.
Os medicamentos não devem ser jogados fora na canalização ou nos contentores domésticos de resíduos. Deve perguntar ao farmacêutico como eliminar os medicamentos de que já não precisa. Este procedimento ajudará a proteger o ambiente.
6. Conteúdo do embalagem e outras informações
O que contém MENOPUR
- A substância ativa do medicamento é menotropina de alta pureza (menotropina) (gonadotropina menopáusica humana, hMG) na quantidade equivalente a 75 IU de FSH (hormônio folículo-estimulante) e 75 IU de LH (hormônio luteinizante).
- Os outros componentes são:
- pó: lactose monoidratada, polissorbato 20, hidróxido de sódio, ácido clorídrico
- solvente: cloreto de sódio, água para injeções, ácido clorídrico 10%.
Como é MENOPUR e que conteúdo tem o embalagem
MENOPUR é um pó e solvente para preparar solução para injeção.
No embalagem de cartão, há 5 ou 10 ampolas de vidro incolor que contêm o pó.
No embalagem de cartão, há também o mesmo número de ampolas de vidro incolor que contêm o solvente.
Nem todos os tamanhos do embalagem podem estar disponíveis.
Responsável e fabricante:
Ferring GmbH
Wittland 11
D-24109 Kiel
Alemanha
Data da última atualização do folheto:
Para obter informações adicionais sobre o medicamento, deve contactar o representante do responsável:
Ferring Pharmaceuticals Portugal, Lda.
Rua do Pó, 5 - 1.º andar, 1200-453 Lisboa
Tel.: +351 213 122 400, Fax: +351 213 122 409
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorFerring GmbH
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a MenopurForma farmacêutica: Pó, 600 UI FSH + 600 UI LHSubstância ativa: human menopausal gonadotrophinRequer receita médicaForma farmacêutica: Pó, 1200 UI FSH + 1200 UI LHSubstância ativa: human menopausal gonadotrophinRequer receita médicaForma farmacêutica: Pó, 150 UI FSH + 150 UI LHSubstância ativa: human menopausal gonadotrophinFabricante: Ferring GmbHRequer receita médica
Alternativas a Menopur noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Menopur em Іспанія
Alternativa a Menopur em Україна
Médicos online para Menopur
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Menopur – sujeita a avaliação médica e regras locais.






