
Ikatibant Ranbaxi
Pergunte a um médico sobre a prescrição de Ikatibant Ranbaxi

Como usar Ikatibant Ranbaxi
1. O que é o medicamento Icatibanto Ranbaxy e para que é utilizado
O Icatibanto Ranbaxy contém a substância ativa icatibanto.
Este medicamento é utilizado para tratar os sintomas de angioedema hereditário (HAE) em doentes adultos e adolescentes e crianças com idade igual ou superior a 2 anos.
No decurso do HAE, ocorre um aumento do nível de uma substância no sangue chamada bradicinina, o que leva a sintomas como inchaço, dor, náuseas e diarreia.
O Icatibanto Ranbaxy bloqueia a actividade da bradicinina, interrompendo assim o desenvolvimento dos sintomas do ataque de HAE.
2. Informações importantes antes de tomar o medicamento Icatibanto Ranbaxy
Quando não tomar o medicamento Icatibanto Ranbaxy
- se o doente for alérgico ao icatibanto ou a qualquer outro componente deste medicamento (listados no ponto 6).
Precauções e advertências
Antes de começar a tomar o medicamento Icatibanto Ranbaxy, deve discutir com o médico:
- se o doente tiver angina de peito (fluxo sanguíneo reduzido para o músculo cardíaco);
- se o doente tiver tido recentemente um acidente vascular cerebral.
Os efeitos não desejados associados à utilização do medicamento Icatibanto Ranbaxy são semelhantes aos sintomas da doença.
Se o doente notar piora dos sintomas do ataque após a administração deste medicamento, deve informar imediatamente o médico.
DK/PT/3244/001/IA/003
Além disso:
- Antes de administrar uma injeção por si mesmo ou antes de um cuidador administrar o medicamento, o doente ou o cuidador deve ser treinado para realizar injeções subcutâneas.
- Se o doente tiver um ataque na garganta (obstrução das vias respiratórias superiores), que administra por si mesmo o Icatibanto Ranbaxy ou a quem um cuidador administra o Icatibanto Ranbaxy, deve procurar imediatamente ajuda médica num estabelecimento de saúde.
- Se, após uma injeção única por si mesmo ou após uma injeção única pelo cuidador, os sintomas não desaparecerem, o doente deve procurar ou o cuidador deve levar o doente ao médico para uma segunda injeção do medicamento Icatibanto Ranbaxy. Não se deve administrar mais de duas injeções adicionais em doentes adultos num período de 24 horas.
Crianças e adolescentes
Não se recomenda a utilização do medicamento Icatibanto Ranbaxy em crianças com menos de 2 anos ou com peso inferior a 12 kg, pois não foi estudado neste grupo etário.
Medicamento Icatibanto Ranbaxy e outros medicamentos
Deve informar o médico sobre todos os medicamentos que o doente está a tomar actualmente ou recentemente, bem como sobre os medicamentos que o doente planeia tomar.
Não são conhecidas interacções do medicamento Icatibanto Ranbaxy com outros medicamentos. Se o doente estiver a tomar um medicamento conhecido como inibidor da enzima conversora da angiotensina (inibidor da ECA) (por exemplo, captopril, enalapril, ramipril, quinapril, lisinopril), utilizado para reduzir a pressão arterial ou por qualquer outra razão, deve informar o médico antes de tomar este medicamento.
Gravidez e amamentação
Se a doente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planeiar ter um filho, deve consultar o médico antes de começar a tomar este medicamento.
A doente não deve amamentar durante 12 horas após a administração do medicamento Icatibanto Ranbaxy.
Condução de veículos e utilização de máquinas
Não deve conduzir veículos ou operar máquinas se o doente apresentar sensação de fadiga ou tonturas devido ao ataque de HAE ou após a administração do medicamento Icatibanto Ranbaxy.
Medicamento Icatibanto Ranbaxy contém sódio
O medicamento contém menos de 1 mmol (23 mg) de sódio por dose, ou seja, o medicamento é considerado "livre de sódio".
3. Como tomar o medicamento Icatibanto Ranbaxy
Este medicamento deve ser sempre tomado de acordo com as recomendações do médico. Em caso de dúvida, deve consultar o médico.
Se o doente estiver a tomar o Icatibanto Ranbaxy pela primeira vez, a primeira dose do medicamento é sempre administrada por um médico ou enfermeiro. O médico dirá ao doente quando pode sair em segurança para casa.
Após a conversa com o médico ou enfermeiro e o treinamento para realizar injeções subcutâneas, o doente pode administrar por si mesmo o Icatibanto Ranbaxy ou um cuidador pode administrar o medicamento ao doente, se o doente tiver um ataque de angioedema hereditário (HAE).
É importante que a injeção subcutânea do medicamento Icatibanto Ranbaxy seja administrada o mais rapidamente possível após a detecção do ataque de angioedema hereditário. O médico responsável ensinará ao doente e ao seu cuidador como administrar com segurança o medicamento de acordo com as instruções fornecidas no Folheto para o doente.
DK/PT/3244/001/IA/003
Quando e como frequentemente tomar o medicamento Icatibanto Ranbaxy
O médico determinará a dose exata do medicamento Icatibanto Ranbaxy e dirá ao doente como frequentemente o tomar.
Adultos
- A dose recomendada do medicamento Icatibanto Ranbaxy é de uma injeção (3 mL, 30 mg), administrada por via subcutânea imediatamente após a detecção do ataque de angioedema (por exemplo, inchaço cutâneo acentuado, especialmente na face e no pescoço, ou agravamento da dor abdominal).
- Se, após 6 horas, os sintomas não desaparecerem, deve procurar aconselhamento médico para uma segunda injeção do medicamento Icatibanto Ranbaxy. Não se deve administrar mais de duas injeções em doentes adultos num período de 24 horas.
- Não tomar mais de 3 injeções num período de 24 horas. Se o doente necessitar de mais de 8 injeções por mês, deve consultar o médico.
Crianças e adolescentes com idade entre 2 e 17 anos
- A dose recomendada do medicamento Icatibanto Ranbaxy é de uma injeção de 1 mL a 3 mL, dependendo do peso corporal, administrada por via subcutânea imediatamente após a detecção dos sintomas do ataque de angioedema (por exemplo, inchaço cutâneo acentuado, especialmente na face e no pescoço, ou agravamento da dor abdominal).
- Mais informações sobre a posologia encontram-se nas instruções
- Se o doente não tiver certeza sobre a dose a administrar, deve consultar o médico, farmacêutico ou enfermeiro.
Se os sintomas se agravarem ou não desaparecerem, deve procurar imediatamente ajuda médica.
Como administrar o medicamento Icatibanto Ranbaxy
O Icatibanto Ranbaxy é destinado a ser administrado por via subcutânea. Cada seringa deve ser utilizada apenas uma vez.
Este medicamento é administrado por injeção com uma agulha curta na gordura subcutânea da barriga.
Em caso de dúvidas adicionais sobre a utilização deste medicamento, deve consultar o médico ou farmacêutico.
A seguinte instrução detalhada aplica-se:
- -administração por si mesmo (adultos)
- -administração por um cuidador ou profissional de saúde a doentes adultos, adolescentes e crianças com idade superior a 2 anos (com peso corporal não inferior a 12 kg).
A instrução inclui os seguintes passos principais:
- 1) Informações gerais 2a) Preparação da seringa pré-cheia para crianças e adolescentes (2-17 anos) com peso corporal de 65 kg ou menos 2b) Preparação da seringa pré-cheia e agulha para injeção (todos os doentes)
- 3) Preparação do local da injeção
- 4) Injeção da solução
- 5) Remoção do material de injeção
DK/PT/3244/001/IA/003
Instruções detalhadas para a injeção
- 1) Informações gerais
- Antes de começar, deve limpar a superfície de trabalho.
- Lavar as mãos com água e sabão.
- Retirar a seringa pré-cheia do pacote.
- Remover a tampa da extremidade da seringa pré-cheia, desrosqueando-a
- Depois de desrosquear a tampa, colocar a seringa pré-cheia de lado
2a) Preparação da seringa pré-cheia para crianças e adolescentes (com idade entre 2 e 17 anos) com peso corporal de 65 kg ou menos:
Informações importantes para profissionais de saúde e cuidadores:
Se a dose for inferior a 30 mg (3 mL), para obter a dose correta a partir da seringa pré-cheia, serão necessários:
a) uma seringa pré-cheia com o medicamento Icatibanto Ranbaxy (contendo a solução de icatibanto)
b) um adaptador
c) uma seringa de 3 mL com graduações
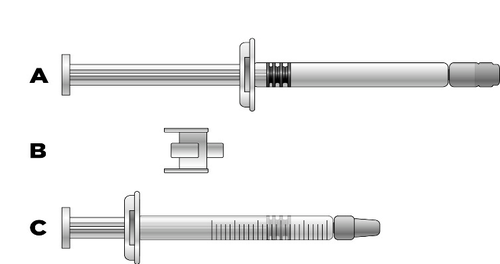
Deve retirar o volume da dose necessária em mililitros para uma seringa de 3 mL com graduações (ver tabela abaixo).
DK/PT/3244/001/IA/003
Tabela 1: Esquema de dosagem para crianças e adolescentes
| Peso corporal | Volume da solução |
| 12 kg a 25 kg | 1,0 mL |
| 26 kg a 40 kg | 1,5 mL |
| 41 kg a 50 kg | 2,0 mL |
| 51 kg a 65 kg | 2,5 mL |
Doentes com peso corporal superior a 65 kgdevem receber todo o conteúdo da seringa pré-cheia (3 mL).

Se o doente não tiver certeza sobre o volume da solução a retirar, deve consultar o médico, farmacêutico ou enfermeiro.
- 1) Retirar as capas da agulha do adaptador.

Deve evitar tocar na extremidade e na ponta do adaptador e da seringa para evitar contaminação.
- 2) Rosquear o adaptador na seringa pré-cheia.
- 3) Fixar a seringa com graduações à outra extremidade do adaptador, garantindo que as duas extremidades estejam bem conectadas.

Retirada da solução de icatibanto para a seringa com graduações:
- 1) Para retirar a dose da solução de icatibanto, deve pressionar o êmbolo da seringa pré-cheia (à esquerda na ilustração abaixo).
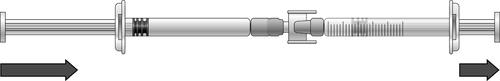
- 2) Se a solução de icatibanto não começar a fluir para a seringa com graduações, deve puxar suavemente o êmbolo da seringa até que a solução comece a fluir para dentro (ver ilustração abaixo).
DK/PT/3244/001/IA/003
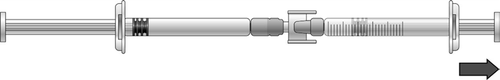
- 3) Deve continuar a pressionar o êmbolo da seringa pré-cheia até que o volume da dose necessário (ver tabela 1) flua para a seringa com graduações. Informações sobre a posologia encontram-se na tabela 1.
Se houver ar na seringa com graduações, deve:
- Girar as seringas conectadas de modo a que a seringa pré-cheia fique por cima (ver ilustração abaixo).
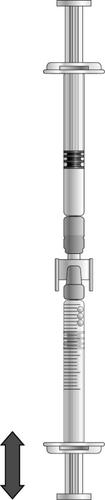
- Pressionar o êmbolo da seringa com graduações para que o ar retorne à seringa pré-cheia (pode ser necessário repetir este passo várias vezes).
- Retirar o volume necessário da solução de icatibanto.
- 4) Desconectar a seringa pré-cheia com o adaptador da seringa com graduações.
- 5) Colocar a seringa pré-cheia com o adaptador num recipiente especial para objetos perfurantes, destinado à eliminação de resíduos que possam causar lesões.
DK/PT/3244/001/IA/003
2b) Preparação da seringa pré-cheia e agulha para injeção:
Todos os doentes (adultos, crianças e adolescentes)
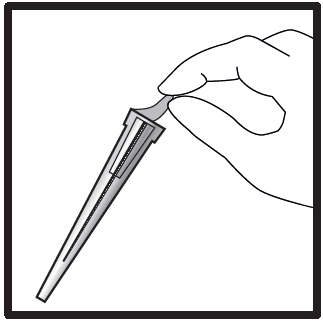
- Retirar a capa da agulha do pacote.
- Remover a camada de vedação da capa da agulha (a agulha deve permanecer na capa).
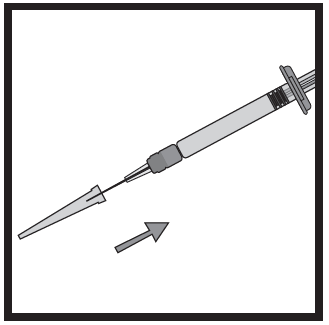
- Segurar firmemente a seringa. Colocar cuidadosamente a agulha na seringa que contém a solução incolor.
- Rosquear a seringa na agulha ainda fixada na capa.
- Retirar a agulha da capa, puxando pelo corpo da seringa. Não puxar pelo êmbolo da seringa.
- A seringa está agora pronta para a injeção .
- 3) Preparação do local da injeção
DK/PT/3244/001/IA/003
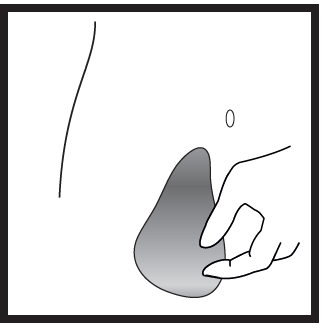
- Escolher o local da injeção. O local da injeção deve ser o dobro da pele da barriga, cerca de 5-10 cm abaixo do umbigo, de um dos lados. Esta área da pele deve estar a uma distância de pelo menos 5 cm de qualquer cicatriz. Não escolher uma área da pele com equimoses, inchaço ou dor.
- Limpar o local da injeção, esfregando com um disco de gaze embebido em álcool e deixar secar
- 4) Injeção da solução
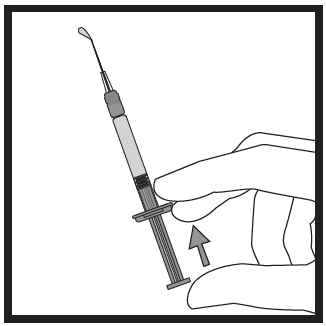
- Deve segurar a seringa com uma mão, entre dois dedos, com o polegar na extremidade do êmbolo.
- Certificar-se de que não há bolhas de ar na seringa, pressionando o êmbolo até que apareça a primeira gota na ponta da agulha.
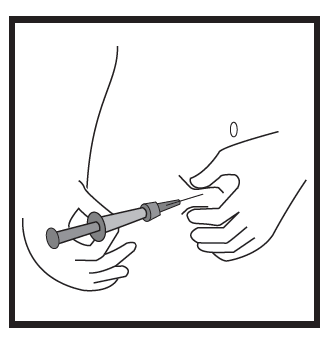
- Segurar a seringa num ângulo de 45-90 graus em relação à pele, com a agulha dirigida para a pele.
- Segurando a seringa com uma mão, com a outra mão segurar suavemente o dobro da pele no local que foi previamente desinfetado.
- Segurando o dobro da pele, aproximar a seringa da pele e introduzir rapidamente a agulha no dobro da pele.
DK/PT/3244/001/IA/003
- Pressionar lentamente o êmbolo da seringa, mantendo a mão imóvel, até que todo o líquido seja injetado na pele e a seringa esteja completamente esvaziada.
- Pressionar o êmbolo durante cerca de 30 segundos.
- Soltar o dobro da pele e retirar suavemente a agulha.
- 5) Remoção do material de injeção
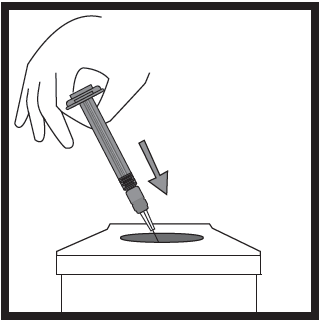
- Colocar a seringa, agulha e capa da agulha num recipiente para objetos perfurantes, destinado à eliminação de resíduos que possam causar lesões.
4. Efeitos não desejados
Como todos os medicamentos, este medicamento pode causar efeitos não desejados, embora não ocorram em todos.
Quase todos os doentes que tomam o Icatibanto Ranbaxy apresentam reação no local da injeção (irritação, inchaço, dor, coceira, vermelhidão da pele e sensação de queimadura). Estes efeitos são geralmente leves e desaparecem sem necessidade de tratamento adicional.
Deve informar imediatamente o médico se o doente notar agravamento dos sintomas do ataque após a administração deste medicamento.
Muito frequentes(podem ocorrer em mais de 1 doente em 10):
Reações adicionais no local da injeção (sensação de pressão, equimose, alteração da sensibilidade e/ou formigamento, coceira e erupção cutânea elevada e sensação de calor).
Frequentes(podem ocorrer em até 1 doente em 10):
Náuseas
Dores de cabeça
Tonturas
Febre
Coceira
Erupção cutânea
Vermelhidão da pele
Resultados anormais dos testes hepáticos
Frequência desconhecida(frequência não pode ser estimada com base nos dados disponíveis):
Urticária
DK/PT/3244/001/IA/003
Notificação de efeitos não desejados
Se ocorrerem efeitos não desejados, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou farmacêutico, ou enfermeiro.
Os efeitos não desejados podem ser notificados directamente para o Departamento de Monitorização de Efeitos Não Desejados de Medicamentos da Autoridade Central Nacional de Medicamentos e Produtos de Saúde
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Sítio web: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos não desejados permitirá reunir mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Icatibanto Ranbaxy
O medicamento deve ser conservado num local fora do alcance e da vista das crianças.
Não utilizar este medicamento após o prazo de validade impresso na etiqueta e na caixa.
O prazo de validade é o último dia do mês indicado.
Não conservar a uma temperatura superior a 25°C. Não congelar.
Não utilizar este medicamento se a seringa ou o pacote da agulha estiverem danificados ou se houver sinais visíveis de deterioração, como a solução estar turva, haver partículas sólidas ou a cor ter mudado.
Os medicamentos não devem ser eliminados na canalização ou em recipientes de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos que já não são utilizados. Este procedimento ajudará a proteger o ambiente.
6. Conteúdo do pacote e outras informações
O que contém o medicamento Icatibanto Ranbaxy
- A substância ativa é o icatibanto. Cada seringa pré-cheia contém 30 miligramas de icatibanto (na forma de octanoato). Cada mL da solução contém 10 mg de icatibanto.
- Os outros componentes são cloreto de sódio, ácido acético glacial, hidróxido de sódio (para ajustar o pH) e água para injeção (ver ponto 2).
Como é o medicamento Icatibanto Ranbaxy e que conteúdo tem o pacote
O Icatibanto Ranbaxy tem a forma de solução incolor para injeção em seringa pré-cheia de vidro com capacidade de 3 mL. O pacote inclui uma agulha para injeção subcutânea.
O Icatibanto Ranbaxy está disponível em embalagens individuais contendo uma seringa pré-cheia com uma agulha ou em embalagens coletivas contendo três seringas pré-cheias com três agulhas.
Nem todos os tamanhos de embalagem podem estar disponíveis no mercado.
DK/PT/3244/001/IA/003
Titular da autorização de comercialização
Ranbaxy (Poland) Sp. z o.o.
ul. Idzikowskiego 16
00-710 Warszawa
tel. 22 642 07 75
Fabricante/Importador
Terapia SA
Str. Fabricii nr. 124,
400632 Cluj Napoca
Romênia
Pharmadox Healthcare Ltd.
KW20A Kordin Industrial Park
PLA 3000 Paola
Malta
Eurofins PROXY Laboratories B.V.
Archimedesweg 25
2333 Leiden
Países Baixos
Este medicamento está autorizado para comercialização nos países membros da Área Económica Europeia e no Reino Unido (Irlanda do Norte) sob as seguintes denominações:
Dinamarca: Icatibant SUN
Romênia: Icatibant Terapia 30 mg soluţie injectabilă în seringă preumplută
Data da última actualização do folheto: 02.05.2023
- País de registo
- Substância ativa
- Requer receita médicaNão
- Fabricante
- ImportadorEurofins Proxy Laboratories BV Pharmadox Healthcare Ltd. Terapia S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Ikatibant RanbaxiForma farmacêutica: Solução, 30 mgSubstância ativa: icatibantFabricante: Fresenius Kabi Austria GmbHRequer receita médicaForma farmacêutica: Solução, 30 mgSubstância ativa: icatibantFabricante: Universal Farma, S.L.Requer receita médicaForma farmacêutica: Solução, 30 mgSubstância ativa: icatibantFabricante: Universal Farma, S.L.Requer receita médica
Alternativas a Ikatibant Ranbaxi noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Ikatibant Ranbaxi em Espanha
Alternativa a Ikatibant Ranbaxi em Ukraine
Médicos online para Ikatibant Ranbaxi
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Ikatibant Ranbaxi – sujeita a avaliação médica e regras locais.














