

Cordarone

Pergunte a um médico sobre a prescrição de Cordarone

Como usar Cordarone
Folheto informativo: informação para o doente
Cordarone
50 mg/ml, solução para injeção
Hidroclorido de amiodarona
{logo sanofi}
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico ou a enfermeira.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou a enfermeira. Ver ponto 4.
Índice do folheto
- 1. O que é Cordarone e para que é utilizado
- 2. Informações importantes antes de tomar Cordarone
- 3. Como tomar Cordarone
- 4. Efeitos não desejados
- 5. Como conservar Cordarone
- 6. Conteúdo da embalagem e outras informações
1. O que é Cordarone e para que é utilizado
O medicamento Cordarone é uma solução para injeção que contém a substância ativa
hidroclorido de amiodarona. A amiodarona é um medicamento antiarrítmico potente utilizado no tratamento da arritmia cardíaca.
A amiodarona é administrada por via intravenosa em situações em que é necessário obter uma ação rápida do medicamento
ou quando a administração oral do medicamento não é possível.
É utilizado no tratamento de distúrbios cardíacos graves:
- distúrbios do ritmo cardíaco na doença de Wolff-Parkinson-White
- fibrilhação e flutter auricular, taquiarritmias supraventriculares paroxísticas: taquicardia supraventricular e nodal, quando outros medicamentos não podem ser utilizados
- distúrbios do ritmo ventricular (taquicardia ventricular, fibrilhação ventricular), quando outros medicamentos antiarrítmicos são ineficazes.
2. Informações importantes antes de tomar Cordarone
Quando não tomar Cordarone:
- se o doente tiver alergia ao iodo, amiodarona ou a qualquer um dos outros componentes deste medicamento (listados no ponto 6); Em caso de ocorrência de sintomas de alergia, tais como erupção cutânea pruriginosa, dificuldade em engolir e respirar ou edema de lábios, face, garganta e língua, deve contactar imediatamente o médico;
- em doentes com doenças cardíacas: bradicardia sinusal, bloco sinoatrial e síndrome do nó sinoatrial, exceto em doentes com marca-passo implantado (risco de inibição da atividade do nó);
- em doentes com bloco atrioventricular de 2º ou 3º grau, exceto em doentes com marca-passo implantado;
- em doentes com bloco bi ou trifásico, exceto em doentes com desfibrilhador implantado ou com sistema de estimulação temporário implantado;
- em conjunto com medicamentos que podem causar distúrbios do ritmo cardíaco graves - do tipo torsade de pointes(ver: Cordarone e outros medicamentos);
- se o doente tiver doença da tiróide;
- se a doente estiver grávida ou a amamentar;
- em caso de colapso circulatório, hipotensão arterial grave;
- em caso de insuficiência respiratória grave;
- em doentes com cardiomiopatia congestiva ou insuficiência cardíaca.
As contraindicações acima não se aplicam se a amiodarona for utilizada na unidade de cuidados intensivos para ressuscitação cardiopulmonar em caso de parada cardíaca súbita devido a fibrilhação ventricular resistente à desfibrilhação.
Precauções e advertências
O Cordarone deve ser administrado por via intravenosa apenas na unidade de cuidados intensivos,
onde o estado clínico do doente é constantemente monitorizado (registo de ECG, valores de pressão arterial).
- O medicamento Cordarone causa alterações no registo de ECG - no entanto, isso não é um sinal de intoxicação pelo medicamento.
- O medicamento Cordarone pode causar distúrbios do ritmo cardíaco ou piorar os distúrbios do ritmo cardíaco existentes, especialmente devido à interação com alguns medicamentos (ver: Cordarone e outros medicamentos e ponto 4) e (ou) em caso de distúrbios eletrolíticos (diminuição dos níveis de potássio e (ou) magnésio no sangue). Não se deve permitir que o nível de potássio no organismo seja muito baixo (hipocalemia) e deve-se corrigir a deficiência.
- Não é recomendado o uso concomitante do medicamento Cordarone com os seguintes medicamentos: betabloqueadores, antagonistas dos canais de cálcio que diminuem a atividade cardíaca (verapamil, diltiazem), laxantes que podem causar hipocalemia (ver Cordarone e outros medicamentos).
- Antes de iniciar o tratamento com o medicamento Cordarone, deve discutir com o médico ou farmacêutico se o doente está atualmente tomando um medicamento que contenha sofosbuvir, utilizado no tratamento da hepatite C, pois isso pode causar uma bradicardia grave. O médico pode considerar métodos de tratamento alternativos. Se for necessário tratar com amiodarona e sofosbuvir, pode ser necessário um monitoramento adicional do ritmo cardíaco.
- Deve informar imediatamente o médico,se o doente estiver tomando um medicamento que contenha sofosbuvir, utilizado no tratamento da hepatite C, e se durante o tratamento ocorrerem:
- batimento cardíaco lento ou irregular ou distúrbios do ritmo cardíaco,
- dificuldade respiratória ou piora da dificuldade respiratória existente,
- dor no peito,
- tontura,
- palpitações,
- estado de nearca ou síncope.
- O medicamento Cordarone pode causar pneumonia intersticial. Os sintomas incluem dificuldade respiratória e tosse sem expectoração. Em caso de suspeita de pneumonia intersticial no doente, o médico realizará um exame radiológico do tórax e considerará o tratamento adicional com o medicamento Cordarone, pois a pneumonia intersticial geralmente melhora se a terapia com o medicamento for interrompida rapidamente. O médico também considerará o tratamento com corticosteroides.
- Foram observados casos muito raros de complicações respiratórias graves, por vezes fatais, geralmente no período imediatamente após a cirurgia (ver Cordarone e outros medicamentos e ponto 4).
- Antes da cirurgia, o anestesista deve ser informado de que o doente recebeu o medicamento Cordarone.
- Durante o tratamento com o medicamento Cordarone e dentro de 24 horas após a sua administração, podem ocorrer distúrbios agudos ou crônicos da função hepática que podem levar à morte. Por isso, desde o início do tratamento, o médico realizará regularmente exames da função hepática (determinação da atividade das aminotransferases no sangue). Em caso de distúrbios da função hepática, o médico considerará a redução da dose do medicamento ou a interrupção do tratamento.
- Deve interromper imediatamente o tratamento com o medicamento Cordarone se ocorrerem reações cutâneas graves (por exemplo, erupção cutânea progressiva com bolhas ou lesões na mucosa, febre e artralgia, doença grave que se manifesta por bolhas gigantes subcutâneas, úlceras extensas na pele, descamação de grandes placas de pele e febre - ver também ponto 4). Estes sintomas podem ser fatais para o doente.
- Em caso de visão turva ou piora da visão, deve realizar-se um exame ocular completo, incluindo um exame do fundo do olho. Em caso de detecção de lesões ou inflamação do nervo óptico, é necessário interromper o tratamento com o medicamento Cordarone devido ao risco de perda de visão.
- Para evitar a ação não desejada no local da injeção, o medicamento Cordarone deve ser administrado por via intravenosa através de um acesso venoso central.
- Se o doente estiver na lista de espera para um transplante cardíaco, o médico responsável pode alterar o tipo de tratamento antes do transplante. Isso se deve ao fato de que a administração de amiodarona antes do transplante cardíaco aumenta o risco de ocorrência de uma complicação fatal (disfunção primária do transplante), na qual o coração transplantado deixa de funcionar corretamente nas primeiras 24 horas após a operação.
Cordarone e outros medicamentos
Deve informar o médico sobre todos os medicamentos que o doente está atualmente tomando ou
tomou recentemente, bem como sobre os medicamentos que o doente planeia tomar.
Não se deve tomar o medicamento Cordarone em conjunto com medicamentos que possam causar distúrbios do ritmo cardíaco graves (do tipo torsade de pointes). Estes medicamentos incluem:
- medicamentos utilizados no tratamento da arritmia (batimento cardíaco irregular): quinidina, dizopiramida, procanamida, sotalol, bretilio, bepridil,
- eritromicina administrada por via intravenosa (antibiótico), cotrimoxazol (medicamento anti-infeccioso) ou medicamento anti-protozoário - pentamidina,
- medicamentos antipsicóticos, tais como: clorpromazina, tiordiazina, flufenazina, pimozida, haloperidol, amisulprida, sertindol,
- alguns medicamentos utilizados em outras doenças psiquiátricas: preparados de lítio e medicamentos antidepressivos tricíclicos, por exemplo, doksepina, amitriptilina,
- alguns medicamentos antihistamínicos utilizados no tratamento da alergia: terfenadina, astemizol, mizolastina,
- medicamentos anti-maláricos: quinina, clorquina, mefloquina, halofantrina,
- medicamento utilizado no tratamento de distúrbios da circulação cerebral, tonturas, zumbido, distúrbios da memória e do aprendizado, especialmente em idosos - vincamina,
- medicamentos neurolépticos,
- medicamento utilizado no tratamento da evacuação gástrica retardada - cisaprida.
Não se recomenda o uso concomitante do medicamento Cordarone com:
- fluorquinolonas - medicamentos anti-infecciosos: ciprofloxacina, ofloxacina, levofloxacina,
- betabloqueadores - medicamentos utilizados em doenças cardíacas, por exemplo, propranolol,
- medicamentos da classe dos antagonistas dos canais de cálcio que diminuem o ritmo cardíaco - utilizados na angina de peito (doença cardíaca) ou na hipertensão arterial (pressão arterial muito alta): verapamil, diltiazem,
- medicamentos antivirais utilizados no tratamento da hepatite C, por exemplo, sofosbuvir, daclatasvir, simeprevir ou ledipasvir, devido ao risco de bradicardia (frequência cardíaca lenta),
- alguns laxantes (medicamentos utilizados no tratamento da constipação) que podem causar hipocalemia (baixo nível de potássio no sangue): bisacodil, senna,
- medicamentos que reduzem o nível de colesterol - estatinas, por exemplo, simvastatina, atorvastatina, lovastatina. Deve-se ter cuidado ao usar os seguintes medicamentos em conjunto com o Cordarone:
- diuréticos, por exemplo, furosemida,
- medicamentos anti-inflamatórios - corticosteroides administrados por via sistêmica, por exemplo, hidrocortisona, prednisolona,
- tetracosactida - medicamento utilizado no exame de certas doenças hormonais,
- medicamento antifúngico - anfotericina B administrada por via intravenosa,
- substâncias utilizadas na anestesia geral ou altas concentrações de oxigênio administradas durante as operações cirúrgicas (ver Precauções e advertências no ponto 2 e ponto 4). Antes da operação cirúrgica, deve-se informar o anestesista sobre o uso do medicamento Cordarone,
- fenitoína - utilizada no tratamento de convulsões: deve-se realizar um monitoramento rigoroso do doente e, assim que ocorram sintomas de superdose, reduzir a dose de fenitoína e determinar o nível de fenitoína no sangue,
- glicosídeos digitálicos, por exemplo, digoxina - utilizados em doenças cardíacas: o médico prescreverá exames para determinar o nível de digoxina no sangue e realizar um exame de ECG e ajustar a dose do glicosídeo digital; o doente deve ser monitorizado para detectar sinais de intoxicação por glicosídeos digitálicos,
- medicamentos anticoagulantes - warfarina, dabigatrana: será necessário realizar exames regulares da coagulação do sangue para ajustar as doses orais de medicamentos anticoagulantes, tanto durante o tratamento como após a interrupção do tratamento com o medicamento Cordarone; pode ser necessário ajustar a dose de dabigatrana,
- medicamentos utilizados para prevenir a rejeição de transplantes - ciclosporina, tacrolimo e sirolimo,
- flecainida - utilizada no tratamento da arritmia: o tratamento será realizado sob controle rigoroso do médico; o médico ajustará a dose de flecainida,
- fentanil - medicamento analgésico potente,
- lidocaína - medicamento anestésico,
- sildenafila - utilizada no tratamento da impotência,
- midazolam - utilizada em estados de ansiedade e para sedação antes das operações cirúrgicas,
- triazolam - utilizada no tratamento da insônia,
- dihidroergotamina e ergotamina - medicamentos anti-migraña,
- colchicina - utilizada no tratamento da gota aguda.
Cordarone com alimentos e bebidas
Recomenda-se evitar o consumo de suco de toranja durante o tratamento com o medicamento Cordarone.
Gravidez, amamentação e fertilidade
Se a doente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planejar ter um filho, deve consultar o médico antes de tomar este medicamento.
Gravidez
Devido ao efeito do Cordarone na tiróide do feto, o uso do medicamento durante a gravidez é
contraindicado. Antes de tomar o medicamento, deve consultar o médico.
Amamentação
O uso do medicamento Cordarone durante a amamentação é contraindicado. Antes de tomar o
medicamento, deve consultar o médico.
Fertilidade
Não há dados sobre o efeito da amiodarona na fertilidade humana.
Condução de veículos e uso de máquinas
Com base nos dados de segurança do uso da amiodarona, o medicamento não afeta a capacidade de
conduzir veículos ou operar máquinas.
Cordarone contém álcool benzílico
O Cordarone contém 60 mg de álcool benzílico em cada ampola (o que corresponde a 20 mg/ml) como
conservante.
O álcool benzílico pode causar reações alérgicas.
A administração de álcool benzílico a crianças pequenas está associada ao risco de efeitos não
desejados graves, incluindo distúrbios respiratórios (síndrome de "gasping").
Este medicamento não deve ser administrado a recém-nascidos (até 4 semanas de vida) sem
recomendação médica.
Este medicamento não deve ser administrado a crianças pequenas (com menos de 3 anos de idade) por
mais de uma semana sem recomendação médica ou farmacêutica.
As mulheres grávidas ou que amamentam devem consultar o médico ou farmacêutico antes de tomar o
medicamento, pois uma grande quantidade de álcool benzílico pode se acumular no seu organismo e
causar efeitos não desejados (acidose metabólica).
Os doentes com doenças hepáticas ou renais devem consultar o médico ou farmacêutico antes de tomar o
medicamento, pois uma grande quantidade de álcool benzílico pode se acumular no seu organismo e
causar efeitos não desejados (acidose metabólica).
3. Como tomar Cordarone
O medicamento é administrado por um médico ou enfermeira de acordo com as instruções do médico.
Em caso de dúvidas, deve consultar o médico.
O medicamento deve ser administrado por via intravenosa, com controle constante do estado do doente
(registo de ECG, medição da pressão arterial).
O medicamento Cordarone é diluído antes da administração ao doente.
O médico escolhe a dose adequada para cada doente com base no peso corporal e na doença.
Geralmente, são utilizadas as seguintes doses:
Adultos:
Infusão intravenosa
Dose de carga: 5 mg/kg de peso corporal, administrada em 250 ml de solução de glicose a 5% em infusão que dura de 20 minutos a 2 horas. A infusão pode ser repetida 2 a 3 vezes ao dia. A velocidade da infusão deve ser ajustada com base no efeito terapêutico obtido.
Dose de manutenção: 10-20 mg/kg de peso corporal por dia (geralmente 600 a 800 mg/24 horas, até uma dose de 1200 mg/24 horas) em infusão em 250 ml de solução de glicose a 5% por vários dias.
Quando o efeito terapêutico desejado for alcançado, o médico prescreverá a administração concomitante de amiodarona por via oral na dose usual de carga (3 x 200 mg por dia). A dose administrada por via intravenosa deve ser reduzida gradualmente.
Dosagem em situações de emergência: 150-300 mg de amiodarona em 10-20 ml de solução de glicose a 5% em injeção lenta, que dura pelo menos 3 minutos.
Uma segunda injeção pode ser repetida não antes de 15 minutos, mesmo que na primeira injeção tenha sido administrada apenas a solução de uma ampola (150 mg), devido ao risco de colapso circulatório. Se for necessário administrar doses adicionais de amiodarona, elas devem ser administradas em infusão intravenosa.
Resuscitação cardiopulmonar
Em caso de ressuscitação cardiopulmonar de um doente com fibrilhação ventricular resistente à desfibrilhação, a primeira dose de 300 mg (ou 5 mg/kg) de amiodarona, diluída em 20 ml de solução de glicose a 5%, é administrada em bolus intravenoso. Em caso de persistência da fibrilhação ventricular, pode-se considerar a administração de uma segunda dose intravenosa de amiodarona de 150 mg (ou 2,5 mg/kg).
Não se deve misturar outros medicamentos com a amiodarona na mesma seringa.
Não se deve injetar outros medicamentos no mesmo acesso venoso.
Em caso de suspeita de que a ação do medicamento Cordarone é muito forte ou muito fraca, deve consultar o médico.
Uso em doentes idosos
Não há dados detalhados sobre a dosagem em doentes idosos.
Em doentes idosos, deve-se ter cuidado especial.
Uso em crianças e adolescentes
Deve-se ter cuidado ao administrar medicamentos por via intravenosa que contenham álcool benzílico a crianças com menos de 3 anos de idade (ver também "Cordarone contém álcool benzílico").
Uso de dose maior do que a recomendada de Cordarone
Como o medicamento será administrado ao doente durante a estadia no hospital, é pouco provável que seja administrada uma dose muito pequena ou muito grande do medicamento, mas se o doente tiver alguma dúvida, deve informar o médico ou a enfermeira.
Omissão da dose de Cordarone
Medicamento utilizado em ambiente hospitalar.
Interrupção do tratamento com Cordarone
Em caso de dúvidas adicionais sobre o uso deste medicamento, deve consultar o médico ou a enfermeira.
4. Efeitos não desejados
Como qualquer medicamento, o Cordarone pode causar efeitos não desejados, embora não todos os doentes os experimentem.
Deve interromper o tratamento com o Cordarone e procurar aconselhamento médico imediatamente se ocorrerem:
Frequência desconhecida (não pode ser estimada com base nos dados disponíveis):
- edema de Quincke - reação alérgica grave que causa edema na face, dificuldade em respirar e engolir;
- reação cutânea que pode ser fatal, caracterizada por erupção cutânea, bolhas, descamação da pele e dor [nekrolise epidérmica tóxica (TEN), síndrome de Stevens-Johnson (SJS), pênfigo bolhoso, reação medicamentosa com eosinofilia e sintomas generalizados (DRESS)].
- batimento cardíaco irregular, que pode ser um sinal de arritmia do tipo torsade de pointes(ver Precauções e advertências e Cordarone e outros medicamentos no ponto 2);
- visão turva ou piora da visão; podem ser sintomas de lesão do nervo óptico, que pode levar à perda de visão (ver Precauções e advertências no ponto 2);
- ver, ouvir ou sentir coisas que não existem (alucinações);
- pode ocorrer um aumento do número de infecções. Isso pode ser devido à diminuição do número de glóbulos brancos (neutropenia);
- diminuição grave do número de glóbulos brancos, o que aumenta o risco de infecções (agranulocitose). Muito raro (ocorre em menos de 1 em 10.000 doentes):
- choque anafilático (conjunto de sintomas clínicos que ocorrem quando os mecanismos de autorregulação do organismo não são capazes de garantir um fluxo sanguíneo adequado para os órgãos e tecidos vitais, causado por uma reação alérgica grave) caracterizado por confusão, fraqueza, síncope
- tontura, fadiga e falta de ar; podem ser sintomas de bradicardia grave, parada sinusal, especialmente em doentes com distúrbio da atividade sinusal e (ou) em doentes idosos, ocorrência de um novo tipo de distúrbio do ritmo cardíaco ou piora dos distúrbios do ritmo cardíaco existentes, por vezes com parada cardíaca;
- icterícia e dor abdominal, perda de apetite, fadiga, febre, alta atividade das aminotransferases nos exames de sangue; são sintomas de insuficiência hepática grave ou falha hepática aguda;
- dificuldade respiratória e tosse sem expectoração; podem ser sintomas de pneumonia intersticial ou fibrose pulmonar (ver Precauções e advertências no ponto 2) ou ocorrência de espasmo brônquico e (ou) apneia em caso de insuficiência respiratória grave e especialmente em doentes com asma brônquica;
- dor de cabeça que piora pela manhã ou após esforço, náusea, convulsões, síncope, distúrbios da visão ou desorientação, podem ser sintomas de distúrbios da função cerebral devido à hipertensão intracraniana (pseudotumor cerebral).
Outros efeitos não desejados do medicamento Cordarone podem ocorrer com a seguinte frequência:
Comum (ocorre em 1 a 10 em cada 100 doentes):
- bradicardia, geralmente moderada;
- reações no local da injeção do medicamento, tais como dor, rubor, edema, necrose, equimose, infiltrado, inflamação, endurecimento, tromboflebite, flebite, inflamação do tecido conjuntivo, infecção, alterações da pigmentação da pele;
- hipotensão, geralmente moderada e transitória, caracterizada por tontura, desorientação e síncope. Foram relatados casos de hipotensão arterial grave ou colapso circulatório após a superdose do medicamento ou administração muito rápida do medicamento;
- erupção cutânea pruriginosa (exantema);
- diminuição da libido. Muito raro (ocorre em menos de 1 em 10.000 doentes):
- mau estar, sensação de desorientação ou fraqueza, náusea (enjoo), perda de apetite, irritabilidade. Isso pode indicar uma doença chamada "síndrome de secreção inadequada do hormônio antidiurético (SIADH)";
- náusea;
- aumento da atividade das aminotransferases nos exames de sangue, que geralmente é moderado (1,5 a 3 vezes acima do limite superior normal), ocorre no início do tratamento. Essas anormalidades podem retornar aos valores normais após a redução da dose do medicamento ou espontaneamente;
- dor de cabeça;
- suor;
- rubor súbito do rosto.
Frequência desconhecida (não pode ser estimada com base nos dados disponíveis):
- dor nas costas;
- urticária;
- hipertireoidismo caracterizado por agitação, perda de peso, aumento da sudorese;
- pancreatite aguda ou pancreatite grave;
- diminuição da libido;
- delírio (incluindo confusão), alucinações;
- complicação fatal pós-transplante cardíaco (disfunção primária do transplante), na qual o coração transplantado deixa de funcionar corretamente (ver Precauções e advertências no ponto 2).
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados
neste folheto, deve informar o médico ou a enfermeira. Os efeitos não desejados podem ser notificados
diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Medicamentos do Instituto
de Saúde Animal e Medicamentos de Uso Humano,
Rua Jerozolimskie, 181C, 02-222 Varsóvia, telefone: +48 22 49 21 301, fax: +48 22 49 21 309,
Site: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização ou ao
seu representante na Polônia.
A notificação de efeitos não desejados pode ajudar a obter mais informações sobre a segurança do
medicamento.
5. Como conservar Cordarone
Manter o medicamento em temperatura abaixo de 25°C.
Manter o medicamento em local não visível e inacessível às crianças.
Não usar o medicamento após o prazo de validade impresso na caixa após "EXP". O prazo de validade
refere-se ao último dia do mês indicado.
6. Conteúdo da embalagem e outras informações
O que contém Cordarone
- A substância ativa do medicamento é hidroclorido de amiodarona 1 ampola contém 150 mg de hidroclorido de amiodarona
- Os outros componentes são: álcool benzílico, polissorbato 80, água para injeção.
Como é Cordarone e o que o embalagem contém
A embalagem contém 6 ampolas de 3 ml.
Titular da autorização de comercialização:
Sanofi Winthrop Industrie
Rua Raspail, 82
94250 Gentilly
França
Fabricante:
Sanofi-Winthrop Industrie
Rua da Virgem, 1
33440 Ambares
França
Delpharm Dijon
Boulevard da Europa, 6
21800 Quetigny
França
Sanofi S.r.l.
Via Valcanello, 4
03012 Anagni (FR)
Itália
Para obter informações mais detalhadas, deve contactar o representante do titular da autorização de comercialização na Polônia:
Sanofi Sp. z o.o.
Rua Marcin Kasprzak, 6
01-211 Varsóvia
telefone: +48 22 280 00 00
Data da última atualização do folheto:
-------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico especializado: Para obter informações completas sobre o medicamento, deve consultar a Característica do Produto(ChPL).
Dosagem e modo de administração
O Cordarone, solução para injeção, deve ser utilizado apenas em unidades de cuidados intensivos
com capacidade de monitoramento cardíaco, desfibrilhação e estimulação cardíaca. O medicamento
deve ser utilizado em infusão intravenosa. Em caso de infusão contínua ou repetida, a amiodarona
deve ser administrada por meio de um acesso venoso central para evitar reações não desejadas no
local da injeção (ver ponto 4.8).
Devido ao risco de ocorrência de hipotensão arterial grave e colapso circulatório, a amiodarona em
injeção intravenosa só pode ser administrada em situações de emergência, quando outros medicamentos
são ineficazes, apenas na unidade de cuidados intensivos, com monitoramento eletrocardiográfico
contínuo. A dose utilizada é de aproximadamente 5 mg/kg de peso corporal. Exceto em casos de
ressuscitação cardiopulmonar de doentes com fibrilhação ventricular resistente à desfibrilhação, a
injeção da dose de amiodarona deve durar pelo menos 3 minutos.
O produto Cordarone, solução para injeção, é incompatível com a solução fisiológica de cloreto de
sódio e pode ser utilizado apenas com solução de glicose a 5%. A solução de amiodarona com
concentração inferior a 300 mg (2 ampolas) em 500 ml de solução de glicose a 5% não é estável e
não deve ser utilizada.
Infusão intravenosa
Dose de carga: geralmente, a dose de carga é de 5 mg/kg de peso corporal, administrada em 250 ml de solução de glicose a 5% em infusão que dura de 20 minutos a 2 horas. A infusão pode ser repetida 2 a 3 vezes ao dia. A velocidade da infusão deve ser ajustada com base no efeito terapêutico obtido.
O efeito terapêutico ocorre nos primeiros minutos e, em seguida, diminui gradualmente, por isso, para prolongá-lo, é necessário continuar a administração do medicamento em infusão.
Dose de manutenção: 10-20 mg/kg de peso corporal por dia (geralmente 600 a 800 mg/24 horas, até uma dose de 1200 mg/24 horas) em infusão em 250 ml de solução de glicose a 5% por vários dias. Em cada caso, deve-se tentar administrar a dose mínima eficaz.
Transição da administração intravenosa para oral: quando o efeito terapêutico desejado for alcançado, deve-se iniciar a administração concomitante de amiodarona por via oral na dose usual de carga (3 x 200 mg por dia). A dose administrada por via intravenosa deve ser reduzida gradualmente.
Dosagem em situações de emergência:150-300 mg de amiodarona em 10-20 ml de solução de glicose a 5% em injeção lenta, que dura pelo menos 3 minutos.
Uma segunda injeção pode ser repetida não antes de 15 minutos, mesmo que na primeira injeção tenha sido administrada apenas a solução de uma ampola (150 mg), devido ao risco de colapso circulatório. Se for necessário administrar doses adicionais de amiodarona, elas devem ser administradas em infusão intravenosa.
Resuscitação cardiopulmonar
Em caso de ressuscitação cardiopulmonar de um doente com fibrilhação ventricular resistente à desfibrilhação, a primeira dose de 300 mg (ou 5 mg/kg) de amiodarona, diluída em 20 ml de solução de glicose a 5%, é administrada em bolus intravenoso. Em caso de persistência da fibrilhação ventricular, pode-se considerar a administração de uma segunda dose intravenosa de amiodarona de 150 mg (ou 2,5 mg/kg).
Não se deve misturar outros medicamentos com a amiodarona na mesma seringa.
Não se deve injetar outros medicamentos no mesmo acesso venoso.
Uso em doentes idosos
Não há dados detalhados sobre a dosagem em doentes idosos.
No entanto, em doentes idosos, deve-se ter cuidado especial devido ao risco de ocorrência de bradicardia grave ou distúrbios da condução.
Crianças e adolescentes
Não foi estabelecida a segurança e eficácia da amiodarona em crianças. Os dados disponíveis são descritos nos pontos 5.1 e 5.2 da ChPL
Devido à presença de álcool benzílico, deve-se ter cuidado ao administrar amiodarona por via intravenosa a recém-nascidos, lactentes e crianças com menos de 3 anos de idade (ver ponto 4.4).
Método de abertura da ampola:
A ampola deve ser segurada de modo que o ponto colorido esteja voltado para a pessoa que a segura (figura 1). A parte superior da ampola deve ser colocada entre o polegar e o dedo indicador (o polegar deve ser colocado no ponto colorido), e, em seguida, a ampola deve ser pressionada por trás (figura 2 e
- 3).
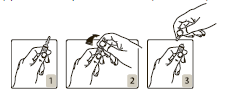
Incompatibilidades farmacêuticas
O uso de materiais médicos de plástico que contenham DEHP (ftalato de di(2-etilhexila)) em conjunto com a solução de amiodarona para injeção intravenosa pode levar à liberação de DEHP. Para minimizar a exposição do doente ao DEHP, recomenda-se realizar a diluição final da amiodarona antes da infusão e administrar o medicamento usando conjuntos que não contenham DEHP.
O produto Cordarone para injeção intravenosa também é incompatível com a solução fisiológica de cloreto de sódio e pode ser utilizado apenas com solução de glicose a 5%. A solução de amiodarona com concentração inferior a 300 mg (2 ampolas) em 500 ml de solução de glicose a 5% não é estável e não deve ser utilizada.
Precauções e advertências especiais para uso
A amiodarona pode ser administrada por via intravenosa apenas na unidade de cuidados intensivos,onde
o estado clínico do doente é constantemente monitorizado (registo de ECG, valores de pressão arterial).
Se possível, a amiodarona em forma de injeção intravenosa deve ser administrada por meio de um acesso venoso central para evitar reações não desejadas no local da injeção (ver ponto 4.8).
Deve-se prestar atenção a qualquer sinal de hipotensão, insuficiência respiratória grave, insuficiência cardíaca não controlada ou grave.
Informações detalhadas sobre injeções intravenosas
Devido ao risco de distúrbios hemodinâmicos (hipotensão grave, colapso circulatório) a injeção intravenosa não é recomendada rotineiramente. Em situações em que isso é possível, a infusão intravenosa é preferida. Amiodarona pode ser administrada por injeção intravenosaapenas em situações de emergência, quando outros medicamentos são ineficazes, exclusivamente na unidade de terapia intensiva, onde o paciente é continuamente monitorizado (registro de ECG, valores de pressão arterial). A dose é de aproximadamente 5 mg/kg de peso corporal. Amiodarona deve ser administrada por injeção intravenosa com duração de pelo menos 3 minutos, exceto em casos de ressuscitação cardiorespiratória relacionada à fibrilação ventricular, quando a desfibrilhação não é eficaz. A próxima injeção pode ser repetida não antes de 15 minutos, mesmo que na primeira injeção tenha sido administrado apenas o conteúdo de uma ampola (150 mg), devido ao risco de ocorrência de colapso circulatório irreversível. Se for necessário administrar doses adicionais de amiodarona, elas devem ser administradas na forma de infusão intravenosa. Não se deve misturar outros medicamentos com amiodarona na mesma seringa. Não se deve injetar outros medicamentos no mesmo acesso venoso. Distúrbios da função cardíaca (ver seção 4.8 do RCP) A ação farmacológica da amiodarona causa alterações no exame de ECG: prolongamento do intervalo QT (relacionado ao prolongamento do período de repolarização) com possível formação de onda U. No entanto, essas alterações não indicam toxicidade da amiodarona. Foram relatados casos de ocorrência de um novo tipo de distúrbio do ritmo cardíaco ou piora de distúrbios do ritmo cardíaco já tratados, às vezes levando à morte. É importante, mas difícil de distinguir se isso se deve à falta de eficácia do medicamento, que tem ação proarritmica, ou se está relacionado à gravidade dos distúrbios do ritmo cardíaco. Menos frequentemente, foram relatados casos de ação proarritmica da amiodarona do que com outros medicamentos antiarritmicos. A ação proarritmica da amiodarona ocorre especialmente como resultado da interação com medicamentos que prolongam o intervalo QT e (ou) em caso de distúrbios eletrolíticos (ver seções 4.5 e 4.8). Independentemente do prolongamento do intervalo QT, a amiodarona tem baixa atividade de indução de distúrbios do ritmo cardíaco do tipo torsade de pointes. Bradicardia grave e bloqueio cardíaco Durante o uso de esquemas que incluem sofosbuvir em conjunto com amiodarona, foram observados casos graves e potencialmente fatais de bradicardia e bloqueio cardíaco. A bradicardia ocorreu geralmente dentro de algumas horas a dias, mas também foram observados casos em que esse tempo foi mais longo, geralmente até 2 semanas após o início do tratamento para HCV. Pacientes que recebem um esquema que inclui sofosbuvir devem receber amiodarona apenas quando o uso de outros medicamentos antiarritmicos alternativos é contraindicado ou não é tolerado. Se o uso concomitante de amiodarona for necessário, é recomendado monitorar a função cardíaca dos pacientes em condições hospitalares durante as primeiras 48 horas após o início da administração concomitante; e, subsequentemente, a frequência cardíaca deve ser monitorada em condições ambulatoriais ou pelo próprio paciente, diariamente, por pelo menos 2 semanas de tratamento. Devido ao longo período de meia-vida da amiodarona, também é recomendado monitorar a função cardíaca, como descrito acima, em pacientes que interromperam o uso de amiodarona nos últimos meses e irão iniciar um esquema que inclui sofosbuvir. Todos os pacientes que recebem amiodarona em conjunto com um esquema que inclui sofosbuvir devem ser informados sobre o risco de ocorrência de sintomas de bradicardia e bloqueio cardíaco e sobre a necessidade de procurar ajuda médica imediatamente se esses sintomas ocorrerem. Distúrbios do sistema respiratório (ver seção 4.8 do RCP) A ocorrência de falta de ar e tosse não produtiva pode estar relacionada à toxicidade pulmonar, como a ocorrência de pneumonia intersticial. Foram relatados casos muito raros de pneumonia intersticial após o uso de amiodarona por via intravenosa. Se houver suspeita de tal diagnóstico em um paciente que apresentou falta de ar durante o esforço, tanto como único sintoma quanto associada à piora do estado geral do paciente (fadiga, perda de peso, febre), deve ser realizado um exame radiológico do tórax. Nesse caso, deve ser reavaliada a necessidade de continuar o tratamento com amiodarona, pois a pneumonia intersticial é geralmente reversível após a interrupção precoce da amiodarona (sintomas clínicos geralmente desaparecem após 3 a 4 semanas, com subsequente melhora gradual dos resultados dos exames radiológicos e funcionais pulmonares, em um período de vários meses). Também deve ser considerada a introdução de tratamento com corticosteroides. Foram relatados alguns casos muito raros de complicações respiratórias graves, às vezes fatais, que ocorreram geralmente logo após uma cirurgia (síndrome de insuficiência respiratória aguda do adulto). Isso pode estar relacionado à interação com oxigênio administrado em alta concentração (ver seções 4.5 e 4.8). Distúrbios da função hepática (ver seção 4.8 do RCP) É recomendado monitorar regularmente e de perto a função hepática (dosagem de aminotransferases) durante o tratamento com amiodarona, começando no momento em que o tratamento é iniciado. A dosagem de amiodarona deve ser reduzida ou o tratamento interrompido se a atividade de aminotransferases aumentar três vezes acima do limite superior da faixa normal, o que pode indicar a ocorrência de distúrbios hepáticos agudos graves (incluindo insuficiência grave das células hepáticas ou insuficiência hepática, às vezes levando à morte) ou distúrbios hepáticos crônicos. Esses distúrbios podem ocorrer durante o uso de amiodarona tanto por via oral quanto intravenosa e dentro de 24 horas após a administração intravenosa de amiodarona. Os sintomas clínicos e biológicos de distúrbios hepáticos crônicos podem ser de gravidade leve (possível aumento do tamanho do fígado, aumento da atividade de aminotransferases 1,5 a 5 vezes acima do limite superior da faixa normal). Essas anormalidades geralmente desaparecem após a interrupção do tratamento com amiodarona. No entanto, foram relatados casos fatais. Reações cutâneas graves O tratamento com amiodarona deve ser interrompido imediatamente se ocorrerem reações cutâneas que possam indicar a ocorrência do síndrome de Stevens-Johnson (erupção cutânea progressiva com bolhas ou lesões nas mucosas, febre e dor nas articulações) ou necrólise epidérmica tóxica (doença grave e aguda caracterizada por bolhas gigantes subepidérmicas, úlceras extensas na pele, descamação de grandes placas de pele e febre), erupção bolhosa, reação medicamentosa com eosinofilia e sintomas generalizados (DRESS). Esses sintomas podem ser fatais para o paciente. Distúrbios oculares (ver seção 4.8) Se ocorrer visão turva ou piora da visão, deve ser realizado imediatamente um exame oftalmológico completo, incluindo um exame do fundo do olho com oftalmoscópio. A constatação de neuropatia do nervo óptico e (ou) neurite óptica exige a interrupção do tratamento com amiodarona devido ao risco de progressão para perda de visão. Interacções com outros medicamentos (ver seção 4.5 do RCP) Não é recomendado o uso concomitante de amiodarona com os seguintes medicamentos: medicamentos beta-adrenolíticos, antagonistas dos canais de cálcio que reduzem o ritmo cardíaco (verapamil, diltiazem), laxantes estimulantes que podem causar hipocalemia, medicamentos antivirais usados no tratamento da hepatite C, como sofosbuvir, daclatasvir, simeprevir ou ledipasvir, devido ao risco de ocorrência de bradicardia grave. O uso concomitante de amiodarona com esquemas que incluem sofosbuvir pode levar a bradicardia grave e sintomática. Se não for possível evitar o uso concomitante de amiodarona com esquemas que incluem sofosbuvir, é recomendado monitorar a função cardíaca do paciente (ver seção 4.4). Antes da cirurgia, o anestesista deve ser informado sobre o uso de amiodarona pelo paciente. Crianças e adolescentes A segurança e eficácia de amiodarona em crianças não foram estabelecidas. Os dados disponíveis são descritos nas seções 5.1 e 5.2. O produto Cordarone na forma de solução para injeção contém benzoato de bencilo na concentração de 20 mg/ml (ver seção 6.1). O benzoato de bencilo em recém-nascidos, lactentes e crianças com até 3 anos de idade pode causar reações tóxicas e alérgicas. Após a administração intravenosa de soluções que contêm esse conservante, foram relatados casos de "síndrome de distúrbios respiratórios fatais" (em inglês, "gasping syndrome"), com resultado fatal em recém-nascidos (crianças antes de completar o primeiro mês de vida). Os sintomas incluem ocorrência súbita de "síndrome de distúrbios respiratórios fatais", hipotensão, bradicardia e colapso cardiovasculares. Mais advertências especiais sobre o uso prolongado de amiodarona estão disponíveis na bula do medicamento Cordarone, comprimidos, 200 mg.
Sobredosagem
Não há dados disponíveis sobre a sobredosagem de amiodarona administrada por via intravenosa. Existem poucos relatos sobre a sobredosagem de amiodarona administrada por via oral. Pode ocorrer bradicardia sinusal, bloqueio atrioventricular, taquicardia ventricular, distúrbios do ritmo cardíaco do tipo torsade de pointes, insuficiência circulatória, bem como hipotensão e lesão hepática. Tanto a amiodarona quanto seus metabólitos não são removidos durante a diálise. A sobredosagem do medicamento requer assistência médica especializada; o tratamento é sintomático.
- País de registo
- Substância ativa
- Requer receita médicaNão
- ImportadorDelpharm Dijon Sanofi S.r.l. Sanofi Winthrop Industrie
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a CordaroneForma farmacêutica: Concentrado, 30 mg/mlSubstância ativa: amiodaroneNão requer receita médicaForma farmacêutica: Concentrado, 50 mg/mlSubstância ativa: amiodaroneFabricante: hameln rds s.r.o. HBM Pharma s.r.o.Não requer receita médicaForma farmacêutica: Solução, 50 mg/mlSubstância ativa: amiodaroneFabricante: Krka, d.d., Novo mestoNão requer receita médica
Alternativas a Cordarone noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Cordarone em Ukraine
Alternativa a Cordarone em Espanha
Médicos online para Cordarone
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Cordarone – sujeita a avaliação médica e regras locais.










