
Ваксігріптетра

Запитайте лікаря про рецепт на Ваксігріптетра

Інструкція із застосування Ваксігріптетра
Укладена інструкція: інформація для пацієнта
VaxigripTetra, суспензія для ін'єкцій в шприці-ампулі
Чотирьохвалентна вакцина проти грипу (розщеплений віріон), інактивована
Перш ніж використовувати вакцину, уважно ознайомтеся з цією інструкцією, оскільки вона містить важливу інформацію для дорослих пацієнтів або дітей.
- Збережіть цю інструкцію, щоб у разі потреби знову її прочитати.
- Якщо у вас виникли будь-які сумніви, зверніться до лікаря, фармацевта або медсестри.
- Цю вакцину призначено конкретній особі. Не передавайте її іншим.
- Якщо у дорослого пацієнта або дитини з'являються будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перераховані в цій інструкції, повідомте про це лікаря, фармацевта або медсестру. Див. пункт 4.
Зміст інструкції
- 1. Що таке VaxigripTetra і для чого вона використовується
- 2. Інформація, яка повинна бути відомою перед застосуванням вакцини VaxigripTetra
- 3. Як застосовувати VaxigripTetra
- 4. Можливі побічні ефекти
- 5. Як зберігати вакцину VaxigripTetra
- 6. Зміст упаковки і інші відомості
1. Що таке VaxigripTetra і для чого вона використовується
VaxigripTetra - вакцина. Ця вакцина допомагає дорослим і дітям від 6 місяців захищатися від грипу.
Після введення вакцини VaxigripTetra імунна система (природна система захисту організму)
виробляє власний захист проти захворювання (антитіла). Вакцина, введена під час вагітності,
допомагає захищати вагітних жінок, а також дітей від народження до 6 місяців, передаючи захист від матері до дитини під час вагітності (див. також пункти 2 і 3).
Ніхто з компонентів вакцини не може викликати грип.
Вакцина VaxigripTetra повинна застосовуватися згідно з офіційними рекомендаціями.
Грип - це захворювання, яке може швидко поширюватися і викликатися багатьма різними штамами вірусу, які можуть змінюватися щороку. Через цю можливу щорічну зміну циркулюючих штамів, а також через тривалість захисту, забезпеченого вакциною, рекомендується щорічне щеплення. Найбільше ризик захворювання на грип спостерігається під час зимових місяців між жовтнем і березнем. У разі дорослих і дітей, які не були щеплені восени, все ще є підстави для щеплення до весни, оскільки до цього часу існує ризик захворювання на грип. Лікар зможе порадити найкращий час для щеплення.
Вакцина VaxigripTetra призначена для захисту дорослих і дітей від чотирьох штамів вірусу, які входять до складу вакцини, приблизно через 2-3 тижні після щеплення. Оскільки інкубаційний період грипу становить кілька днів, у разі контакту з вірусом грипу безпосередньо перед або після щеплення все ще можливо захворювання.
Вакцина не захищає від застуди, хоча деякі її симптоми схожі на грип.
2. Інформація, яка повинна бути відомою перед застосуванням вакцини VaxigripTetra
Повідомте лікаря або фармацевта, якщо будь-яке з нижченаведених тверджень стосується дорослого пацієнта або дитини, якій призначено вакцину VaxigripTetra. Якщо щось незрозуміле, попросіть лікаря або фармацевта пояснити.
Коли не застосовувати вакцину VaxigripTetra:
- Якщо у дорослого пацієнта або дитини є алергія на:
- Активні речовини, або
- Будь-який з інших компонентів цієї вакцини (перелічених у пункті 6), або
- Будь-який компонент, який може бути присутнім у дуже малих кількостях, такий як залишки яєць (альбумін яєць курей, білок курей), неоміцин, формальдегід або октоксинол-9,
- Якщо у дорослого пацієнта або дитини виявлено захворювання, яке супроводжується високою або помірною температурою або гострим захворюванням, щеплення повинно бути відкладено до одужання.
Попередження та обережність
Перед застосуванням вакцини VaxigripTetra необхідно поговорити з лікарем, фармацевтом або медсестрою.
Перед щепленням необхідно повідомити лікаря, якщо у дорослого пацієнта або дитини спостерігаються:
- Ослаблення імунної відповіді (спричинене дефіцитом імунітету або прийомом ліків, які впливають на імунну систему),
- Кровотечі або схильність до синяків. Лікар вирішить, чи повинен дорослий пацієнт або дитина прийняти вакцину.
Омдлення може трапитися (особливо у підлітків) після або навіть перед будь-яким уколом.
Тому необхідно повідомити лікаря або медсестру, якщо пацієнт або його дитина мали омдлення при попередніх ін'єкціях.
Як і у випадку з будь-якою вакциною, VaxigripTetra може не забезпечити повний захист усім щепленим особам.
Не всі діти до 6 місяців, народжені жінками, щепленими під час вагітності, будуть захищені.
Повідомте лікаря, якщо у дорослого пацієнта або дитини планується аналіз крові через кілька днів після щеплення проти грипу, через спостережувані хибно-позитивні результати аналізу крові у деяких пацієнтів, яким раніше було зроблено щеплення.
Діти
Застосування вакцини VaxigripTetra не рекомендується дітям до 6 місяців.
VaxigripTetra та інші ліки
Повідомте лікаря або фармацевта про всі ліки або вакцини, які приймає дорослий пацієнт або дитина зараз або останнім часом, а також про ліки або вакцини, які планують приймати.
- Вакцина VaxigripTetra може бути введена одночасно з іншими вакцинами, але в різні кінцівки.
- При застосуванні ліків, які знижують імунітет, таких як кортикостероїди, цитотоксичні ліки або радіотерапія, імунна відповідь на щеплення може бути знижена.
Вагітність і годування грудьми
Якщо пацієнтка вагітна або годує грудьми, підозрює, що може бути вагітна, повинна проконсультуватися з лікарем або фармацевтом перед застосуванням цієї вакцини.
Вакцина VaxigripTetra може бути введена в усіх періодах вагітності.
Вакцина VaxigripTetra може бути застосована під час годування грудьми.
Лікар вирішить про можливість введення вакцини VaxigripTetra.
Водіння транспортних засобів і використання техніки
Вакцина VaxigripTetra не має впливу або має незначний вплив на здатність водіння транспортних засобів і використання техніки.
VaxigripTetra містить калій і натрій
Цей препарат містить менше 1 ммоль калію (39 мг) і менше 1 ммоль натрію (23 мг) на дозу, тобто фактично є "вільним від калію" і "вільним від натрію".
3. Як застосовувати VaxigripTetra
Дозування
Дорослі отримують одну дозу 0,5 мл.
Застосування у дітей
Діти від 6 місяців до 17 років отримують одну дозу 0,5 мл.
Дітям до 9 років, які раніше не були щеплені проти грипу, необхідно вводити другу дозу 0,5 мл через не менше 4 тижнів.
У разі вагітних жінок одна доза 0,5 мл, введена під час вагітності, може захищати дитину від народження до 6 місяців. Для отримання додаткової інформації зверніться до лікаря або фармацевта.
Як приймати VaxigripTetra
Лікар або медсестра введе рекомендовану дозу вакцини у вигляді ін'єкції в м'яз або під шкіру.
Застосування більшої, ніж рекомендована, дози вакцини VaxigripTetra
У деяких випадках випадково вводили більшу дозу, ніж рекомендована.
У цих випадках, коли повідомлялися побічні ефекти, вони були такими ж, як і після введення рекомендованої дози (див. пункт 4).
У разі будь-яких подальших сумнівів, пов'язаних з застосуванням цієї вакцини, зверніться до лікаря або фармацевта.
4. Можливі побічні ефекти
Як і будь-який лік, ця вакцина може викликати побічні ефекти, хоча вони не виникнуть у всіх.
Алергічні реакції
Негайно зверніться до лікаря або медичного працівника, або зверніться до найближчої приймальної, якщо у дорослого пацієнта або дитини виникнуть алергічні реакції (згідно з повідомленнями: можуть виникнути у до 1 з 1000 осіб), які можуть загрожувати життю.
Симптоми можуть включати висип, свербіж, кропив'янку, червоність, труднощі з диханням, задишку, набряк обличчя, губ, горла або язика, холодну, вологу шкіру, серцебиття, головокружіння, слабкість або омдлення.
Інші побічні ефекти, повідомлені у дорослих і старших осіб
Дуже часто (можуть виникнути у понад 1 з 10 осіб)
- Головний біль, біль у м'язах, загальне погане самопочуття, біль у місці ін'єкції. Часто у старших осіб Часто (можуть виникнути у до 1 з 10 осіб)
- Гарячка, озноб, реакції в місці ін'єкції: червоність, набряк, твердість. Не дуже часто у старших осіб Не дуже часто (можуть виникнути у до 1 з 100 осіб)
- Головокружіння, діарея, нудота, втома, реакції в місці ін'єкції: синяки, свербіж і теплота. Рідко у дорослих Рідко у старших осіб
- Удари гарячки: спостерігалися тільки у старших осіб.
- Збільшення лімфатичних вузлів у області шиї, паху або пахвин (лімфаденопатія): спостерігалися тільки у дорослих.
Рідко (можуть виникнути у до 1 з 1000 осіб)
- Порушення відчуття дотику, болю, тепла і холоду (парестезія), сонливість, надмірна потливість, нетипова втома або слабкість (астенія), симптоми грипоподібні.
- Біль у суглобах, дискомфорт у місці ін'єкції: спостерігалися тільки у дорослих.
Інші побічні ефекти, повідомлені у дітей від 3 до 17 років
Дуже часто (можуть виникнути у понад 1 з 10 осіб)
- Головний біль, біль у м'язах, загальне погане самопочуття, озноб, реакції в місці ін'єкції: біль, набряк, червоність, твердість. Часто у дітей від 9 до 17 років Часто (можуть виникнути у до 1 з 10 осіб)
- Гарячка, синяк у місці ін'єкції.
Не дуже часто (можуть виникнути у до 1 з 100 осіб) у дітей від 3 до 8 років
- Тимчасове зниження кількості певних типів клітин у крові, званих тромбоцитами; їх низький рівень може викликати надмірне утворення синяків або кровотечу (транзиторна тромбоцитопенія): повідомлялося у одного дитини 3 років.
- Сварливість, неспокій.
- Головокружіння, діарея, блювання, біль у животі, біль у суглобах, втома, теплота у місці ін'єкції.
Не дуже часто (можуть виникнути у до 1 з 100 осіб) у дітей від 9 до 17 років
- Діарея, свербіж у місці ін'єкції.
Інші побічні ефекти, повідомлені у дітей від 6 місяців до 35 місяців
Дуже часто (можуть виникнути у понад 1 з 10 осіб):
- Блювання, біль у м'язах, сварливість, втрата апетиту, загальне погане самопочуття, гарячка. Не дуже часто у дітей від 24 місяців до 35 місяців Рідко у дітей до 24 місяців Рідко у дітей від 24 місяців до 35 місяців
- Реакції в місці ін'єкції: біль/чутливість, червоність.
- Головний біль: спостерігався тільки у дітей до 24 місяців.
- Сонливість, нетиповий плач: спостерігалися тільки у дітей до 24 місяців.
Часто (можуть виникнути у до 1 з 10 осіб):
- Озноб: спостерігався тільки у дітей від 24 місяців.
- Реакції в місці ін'єкції: твердість, набряк, синяк у місці ін'єкції.
Не дуже часто (можуть виникнути у до 1 з 100 осіб):
- Діарея, надчутливість.
Рідко (можуть виникнути у до 1 з 1000 осіб):
- Грипоподібне захворювання, реакції в місці ін'єкції: висип, свербіж.
У дітей від 6 місяців до 8 років, які отримують 2 дози, побічні ефекти після першої і після другої дози схожі. Менше побічних ефектів може виникнути після введення другої дози у дітей від 6 місяців до 35 місяців.
Спостережувані побічні ефекти зазвичай виникали протягом перших 3 днів після щеплення і проходили самостійно протягом 1-3 днів після виникнення. Спостережувані побічні ефекти мали легкий характер.
Загалом побічні ефекти виникали рідше у старших осіб, ніж у дорослих і дітей.
Нижче перелічені побічні ефекти повідомлялися після введення вакцини Vaxigrip. Вони можуть виникнути після введення вакцини VaxigripTetra:
- Біль, відчутний уздовж нервів (нейралгія), напади (конвульсії), неврологічні розлади, які можуть викликати шийний спазм, дезорієнтацію, оніміння, біль і слабкість кінцівок, втрату рівноваги, втрату рефлексів, параліч частини або всього тіла (енцефаліт і менінгіт, неврит, синдром Гієна-Барре).
- Васкуліт, який може призвести до висипів на шкірі та в дуже рідких випадках до тимчасових порушень функції нирок.
- Транзиторна тромбоцитопенія, лімфаденопатія, парестезія у вікових групах, інших ніж перелічені вище для цих побічних ефектів.
Повідомлення про побічні ефекти
Якщо у дорослого пацієнта або дитини виникнуть будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перераховані в цій інструкції, повідомте про це лікаря, фармацевта або медсестру. Побічні ефекти можна повідомляти безпосередньо до Департаменту моніторингу небажаних дій лікарських засобів Міністерства охорони здоров'я України
вул. Миколи Амосова, 7
03041 Київ
Телефон: +38 (044) 206 23 24
Факс: +38 (044) 206 23 24
Веб-сайт: https://www.moz.gov.ua
Побічні ефекти також можна повідомляти відповідальному суб'єкту.
Повідомлення про побічні ефекти дозволить зібрати більше інформації про безпеку застосування ліків.
5. Як зберігати вакцину VaxigripTetra
Вакцину необхідно зберігати в місці, недоступному для дітей.
Не застосовуйте цю вакцину після закінчення терміну придатності, вказаного на етикетці та упаковці після «Термін придатності (EXP)». Термін придатності означає останній день вказаного місяця.
Зберігайте у холодильнику (2 °C – 8 °C). Не заморожуйте. Зберігайте шприц-ампулу в зовнішній упаковці для захисту від світла.
Ліки не слід викидати у каналізацію або домашні контейнери для відходів. Зверніться до фармацевта, щоб дізнатися, як видалити ліки, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище.
6. Зміст упаковки і інші відомості
Що містить VaxigripTetra
- Активними речовинами є: Вірус грипу (інактивований, розщеплений) наступних штамів*:
A/Victoria/4897/2022 (H1N1)pdm09-подібний штам (A/Victoria/4897/2022, IVR-238)
............................................................................................................................. 15 мкг HA**
A/Croatia/10136RV/2023 (H3N2)-подібний штам (A/Croatia/10136RV/2023, X-425A)
…………………………………………………………………………………. 15 мкг HA**
B/Austria/1359417/2021-подібний штам (B/Michigan/01/2021, тип дикого)
............................................................................................................................. 15 мкг HA**
B/Phuket/3073/2013-подібний штам (B/Phuket/3073/2013, тип дикого)
............................................................................................................................. 15 мкг HA**
у дозі 0,5 мл
* вирощені в курячих ембріонах, отриманих від здорових стад
** гемаглютинін
Вакцина відповідає рекомендаціям Всесвітньої організації охорони здоров'я (WHO) для північної півкулі та рекомендаціям Європейського Союзу на сезон 2025/2026.
- Інші компоненти: буферний розчин, який містить хлорид натрію, хлорид калію, дигідрофосфат натрію, дигідрофосфат калію та воду для ін'єкцій.
Деякі компоненти, такі як яйця (альбумін яєць курей, білок курей), неоміцин, формальдегід або октоксинол-9, можуть бути присутні у дуже малих кількостях (див. пункт 2).
Як виглядає VaxigripTetra і що містить упаковка
Після легкого встрясання вакцина являє собою безбарвну, опалесцентну рідину.
VaxigripTetra - суспензія для ін'єкцій у шприці-ампулі по 0,5 мл, з прикріпленою голкою або без голки (в упаковці по 1, 10 або 20) або з окремою голкою в захисній оболонці (в упаковці по 1 або 10). Не всі розміри упаковок повинні бути в обігу.
Відповідальний суб'єкт і виробник
Відповідальним суб'єктом в Україні є:
Санофі Вінтроп Індустрі
82 Avenue Raspail
94250 Gentilly, Франція
Виробником є:
Санофі Вінтроп Індустрі - 1541 avenue Marcel Mérieux - 69280 Marcy l’Etoile - Франція
Санофі Вінтроп Індустрі - Voie de l’Institut - Parc Industriel d’Incarville – B.P 101 - 27100 Val de
Reuil - Франція>
<Санофі Авертіс Зрт. - Campona utca 1. (Harbor Park) - 1225 Будапешт - Угорщина>
Цей лікарський засіб дозволений до обігу в країнах-членах Європейського економічного простору під наступними назвами:
Австрія: VaxigripTetra Injektionssuspension in einer Fertigspritze.
Литва: VaxigripTetra injekcinė suspensija užpildytame švirkšte.
Болгарія, Хорватія, Кіпр, Естонія, Фінляндія, Франція, Греція, Ісландія, Латвія, Мальта, Польща, Португалія, Румунія, Словенія, Швеція, Нідерланди: VaxigripTetra.
Данія, Норвегія: Vaxigriptetra.
Бельгія, Люксембург: Vaxigrip Tetra suspension injectable en seringue préremplie.
Німеччина, Італія, Іспанія, Чехія, Словаччина, Угорщина: Vaxigrip Tetra.
Ірландія, Велика Британія (Північна Ірландія): Quadrivalent influenza vaccine (split virion, inactivated).
Дата останньої актуалізації інструкції:травень 2025
Інші джерела інформації
Поточна затверджена інформація про цей продукт доступна після сканування коду QR на пачці туби або за наступною адресою URL: https://vaxigriptetra-nh.info.sanofi
-----------------------------------------------------------------------------------------------------------------------
Інформація, призначена виключно для медичного персоналу:
Як і у випадку з усіма вакцинами, які вводяться ін'єкціями, необхідно забезпечити належне лікування і медичний нагляд на випадок виникнення анафілактичної реакції після введення вакцини.
Перед введенням вакцина повинна досягти кімнатної температури.
Встрясайте перед застосуванням. Перевірте візуально перед введенням.
Вакцини не слід застосовувати у разі наявності в суспензії твердих частинок.
Вакцини не слід змішувати з іншими лікарськими засобами в одному шприці.
Вакцини не слід вводити безпосередньо в кровоносні судини.
Див. також пункт 3. Як застосовувати VaxigripTetra
| <Підготовка до застосування | |
| Інструкція щодо використання голки з захисною оболонкою з шприцем-ампулою з кінчиком Luer | |
| Lock: | |
Рисунок А: Голка з захисною оболонкою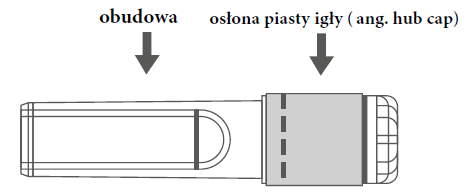 | Рисунок Б: Елементи захисної оболонки голки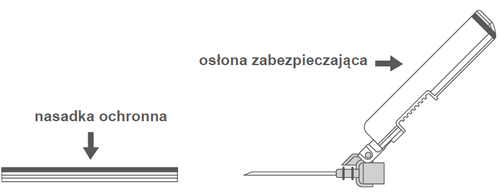 |
| Крок 1: Для кріплення голки до шприца необхідно зняти захисну оболонку голки (англ. hub cap), щоб відкрити голку, і ніжно вкрутити голку в адаптер Luer Lock шприца до відчуття легкого опору. | ||
| Крок 2: Зняти обудову голки. Голка захищена захисною оболонкою і захисною насадкою. | ||
| Крок 3: А: Відсуньте захисну оболонку від голки у напрямку корпусу шприца під показаним кутом. Б: Зняти захисну насадку. | 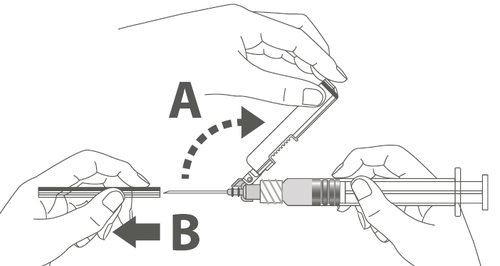 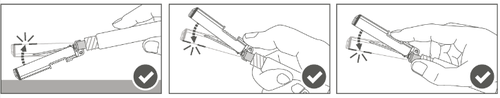 | |
| Крок 4: Після ін'єкції заблокуйте (активуйте) захисну оболонку, застосовуючи одну з трьох (3) показаних технік обробки однією рукою: активація на плоскій поверхні, великим пальцем або вказівним пальцем. Увага: Активація підтверджується чутним і (або) відчутним "кліком". | ||
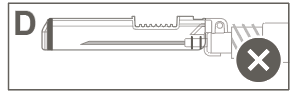
| Крок 5: Перевірте візуально роботу захисної оболонки. Захисна оболонка повинна бути повністю заблокована (активована), як показано на рисунку С. Рисунок Д показує, що захисна оболонка НЕ є повністю заблокованою (не активованою). | ||
Попередження: Не слід намагатися розблокувати (деактивувати) пристрій захисту після виштовхування голки з захисної оболонки.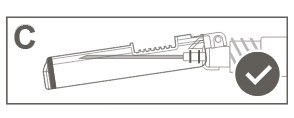 | ||
 | ||
| Всі невикористані залишки лікарського засобу або його відходи слід видалити згідно з місцевими правилами. Зверніться до фармацевта, щоб дізнатися, як видалити ліки, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище. | ||
| > | ||
- Країна реєстрації
- Діючі речовини
- Потрібен рецептТак
- ІмпортерSanofi Winthrop Industrie Sanofi Winthrop Industrie Sanofi-Aventis Zrt.
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до ВаксігріптетраФорма випуску: Суспензія, 60 мкг HA/штам, 1 доза (0,7 мл)Діючі речовини: influenza, inactivated, split virus or surface antigenПотрібен рецептФорма випуску: Суспензія, 60 мкг HA/штам, 1 доза (0,5 мл)Діючі речовини: influenza, inactivated, split virus or surface antigenПотрібен рецептФорма випуску: Суспензія, 1 доза (0,5 мл)Діючі речовини: influenza, inactivated, split virus or surface antigenПотрібен рецепт
Аналоги Ваксігріптетра в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Ваксігріптетра у Spain
Аналог Ваксігріптетра у Ukraine
Лікарі онлайн щодо Ваксігріптетра
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Ваксігріптетра – за рішенням лікаря та згідно з місцевими правилами.














