
Ефлуелда Тетра

Запитайте лікаря про рецепт на Ефлуелда Тетра

Інструкція із застосування Ефлуелда Тетра
УПОСТЕРІЖНИЙ ЛИСТ ДЛЯ ПАЦІЄНТА
Упаковка з інформацією для користувача
Efluelda Tetra, суспензія для ін'єкцій в ампуло-шприці
Чотирьохвалентна вакцина проти грипу (розщеплений віріон, інактивована),
60 мкг HA/доза
Цей лікарський засіб буде додатково моніторитися. Це дозволить швидко
визначити нову інформацію про безпеку. Користувач препарату також може допомогти,
повідомляючи про будь-які побічні дії, які виникли після застосування препарату. Щоб дізнатися,
як повідомляти про побічні дії – див. пункт 4.
Перед застосуванням вакцини необхідно ретельно ознайомитися з вмістом упаковки, оскільки вона містить важливу інформацію для дорослого пацієнта чи дитини.
- Зберігайте цю упаковку, щоб у разі потреби знову її прочитати.
- У разі будь-яких сумнівів зверніться до лікаря, фармацевта або медсестри.
- Цю вакцину призначено конкретній особі. Не передавайте її іншим.
- Якщо в пацієнта виникнуть будь-які побічні дії, включаючи ті, які не перелічені в цій упаковці, повідоміть про це лікаря, фармацевта або медсестру. Див. пункт 4.
Зміст упаковки
- 1. Що таке Efluelda Tetra і для чого вона застосовується
- 2. Важлива інформація перед застосуванням вакцини Efluelda Tetra
- 3. Як застосовувати вакцину Efluelda Tetra
- 4. Можливі побічні дії
- 5. Як зберігати вакцину Efluelda Tetra
- 6. Зміст упаковки та інші відомості
1. Що таке Efluelda Tetra і для чого вона застосовується
Efluelda Tetra – вакцина. Ця вакцина допомагає захистити осіб у віці 60 років і старше від
грипу. Застосування вакцини Efluelda Tetra повинно базуватися на офіційних рекомендаціях
щодо щеплень проти грипу.
Після введення вакцини Efluelda Tetra імунна система (природний захист організму)
виробляє власний захист проти захворювання (антитіла). Жоден з компонентів вакцини не може
спричинити грип.
Грип – це інфекційне захворювання дихальної системи, яке викликається вірусами грипу, з насильством від легкого до важкого і може призвести до серйозних ускладнень, таких як пневмонія, яке може потребувати госпіталізації, а甚至 смерті. Грип – це захворювання, яке може швидко поширюватися і викликатися багатьма різними штамами вірусу, які можуть змінюватися
кожного року. Через цю можливу щорічну зміну циркулюючих штамів, а також через тривалість дії захисту, забезпеченого вакциною, рекомендується проводити щеплення кожного року. Найбільше ризик захворювання на грип спостерігається під час холодних місяців між
жовтнем і березнем. У разі осіб, які не були щеплені восени, все ще є підстава для щеплення
в період до весни, оскільки до цього часу існує ризик захворювання на грип. Лікар буде能够 порекомендувати найкращий час для щеплення.
Вакцина Efluelda Tetra призначена для захисту проти чотирьох штамів вірусу, які входять до складу вакцини, приблизно через 2-3 тижні після щеплення. Оскільки інкубаційний період для грипу становить кілька днів, у разі контакту з вірусом грипу безпосередньо перед або після щеплення, все ще можливо захворювання.

Вакцина не захищає від застуди, хоча деякі її симптоми схожі на грип.
2. Важлива інформація перед застосуванням вакцини Efluelda Tetra
Повідоміть лікаря або фармацевта, якщо будь-яке з нижченаведених тверджень стосується особи, якій призначено вакцину Efluelda Tetra. Якщо щось незрозуміле, попросіть лікаря або фармацевта пояснити.
Коли не застосовувати вакцину Efluelda Tetra:
- Якщо особа має алергію на:
- активні речовини, або
- будь-який з інших компонентів цієї вакцини (перелічених у пункті 6), або
- будь-який компонент, який може бути присутнім у дуже малих кількостях, такий як залишки яєць (альбумін яєць курей, білки курей) і формальдегід.
Попередження та обережність
Перед застосуванням вакцини Efluelda Tetra необхідно поговорити з лікарем, фармацевтом або
медсестрою.
Перед щепленням повідоміть лікаря, якщо в пацієнта спостерігається:
- ослаблення імунної відповіді (спричинене дефіцитом імунітету або прийомом ліків, які впливають на імунну систему),
- кровотечі або схильність до синяків,
- перебіг синдрому Гієна-Барре (GBS) (важке м'язове ослаблення) після отримання вакцини проти грипу,
- хвороба, яка перебігає з високою або помірною температурою або гостра хвороба. Щеплення повинно бути відкладено до часу одужання. Лікар вирішить, чи слід приймати вакцину.
Омдленіння може виникнути після, або навіть перед будь-яким уколом. Тому необхідно повідомити лікаря або медсестру, якщо особа пережила омдленіння при попередніх ін'єкціях.
Як і у випадку з будь-якою вакциною, Efluelda Tetra може не забезпечити повний захист усім
щепленим особам.
Повідоміть лікаря, якщо в пацієнта протягом кількох днів після щеплення проти грипу планується аналіз крові, через спостережувані хибно-позитивні результати аналізу крові у деяких пацієнтів, які раніше були щеплені.
Діти
Цю вакцину не слід застосовувати у дітей. Застосування цієї вакцини рекомендується у осіб дорослого віку у віці 60 років і старше.
Вакцина Efluelda Tetra та інші ліки
Повідоміть лікаря або фармацевта про всі ліки або вакцини, які приймає пацієнт зараз або нещодавно, а також про ліки або вакцини, які планує приймати.
- У разі введення вакцини Efluelda Tetra в одночасному режимі з іншими вакцинами, ці вакцини повинні бути введені в різні кінцівки.
- Відзначено, що побічні дії можуть бути посилені при одночасному введенні вакцин.
- У разі застосування ліків, які знижують імунітет, таких як кортикостероїди, цитотоксичні ліки або радіотерапія, імунна відповідь на щеплення може бути ослабленою.
Вагітність і годування грудьми
Вакцина Efluelda Tetra призначена для застосування виключно у осіб дорослого віку у віці 60 років і старше.
Якщо пацієнтка вагітна або годує грудьми, підозрює, що може бути вагітною або планує мати дитину,
повинна проконсультуватися з лікарем або фармацевтом перед застосуванням цієї вакцини. Лікар або фармацевт допоможуть вирішити, чи повинна пацієнтка отримати вакцину Efluelda Tetra.
Проведення транспортних засобів і обслуговування машин
Вакцина Efluelda Tetra не має впливу або має незначний вплив на здатність керувати транспортними засобами та обслуговувати машини.
Вакцина Efluelda Tetra містить калій і натрій
Ця вакцина містить менше 1 ммоль натрію (23 мг) на дозу, тобто практично «вільна від натрію».
3. Як застосовувати вакцину Efluelda Tetra
Дорослі у віці 60 років і старше отримують одну дозу 0,7 мл.
Як приймати вакцину Efluelda Tetra
Лікар або медсестра введуть рекомендовану дозу вакцини у вигляді ін'єкції в м'яз або під шкіру.
У разі будь-яких подальших сумнівів, пов'язаних з застосуванням цієї вакцини, зверніться до лікаря або фармацевта.
4. Можливі побічні дії
Як і будь-який лік, ця вакцина може спричинити побічні дії, хоча не у всіх вони виникнуть.
Алергічні реакції
Відразу ж зверніться до лікаря, якщо в пацієнта виникнуть:
- Важкі алергічні реакції:
- можуть вимагати медичної допомоги, з низьким артеріальним тиском, задишкою, свистом у легенях або проблемами з диханням, швидким пульсом і слабким пульсом, холодною, вологою шкірою, головокружінням, яке може призвести до втрати свідомості (анafilaksія [в тому числі ангіоневротичний набряк тобто набряк, найбільш помітний на голові та шиї, включаючи обличчя, губи, язик, горло чи інші частини тіла, який може викликати труднощі з ковтанням або диханням]).
Зверніться до лікаря, якщо в пацієнта виникнуть:
- Алергічні реакції, такі як шкірні реакції, які можуть охоплювати все тіло, включаючи свербіж, кропив'янку, висипку. Ці побічні дії рідкі (можуть спостерігатися у до 1 з 1000 осіб).
Інші побічні дії
Нижченаведені побічні дії були повідомлені у дорослих у віці 60 років і старше.
Дуже часто (можуть виникнути у більше ніж 1 з 10 осіб):
- Реакції в місці ін'єкції: біль, червоність (еритема)
- Загальне погане самопочуття (втома), головний біль, біль у м'язах
Часто (можуть виникнути у максимум 1 з 10 осіб):
- Реакції в місці ін'єкції: опухання, синяк, загустіння
- Гарячка, озноб
Не дуже часто (можуть виникнути у максимум 1 з 100 осіб):
- Реакції в місці ін'єкції: свербіж
- Втома, сонливість, нудота, блювота, діарея
- Кашель, м'язова слабкість, нудота, фарингіт (біль у ротоглотці)
Рідко (можуть виникнути у максимум 1 з 1000 осіб):
- Брак енергії (слабкість), червоність, біль у суглобах, головокружіння центрального походження, нічні поти, висипка, оніміння або відчуття поколювання (парестезії), риніт (гайморит), головокружіння (забурення рівноваги), надмірна кров у білку ока (гіперемія ока)
- Біль у кінцівках
Частота невідома: частота не може бути визначена на основі доступних даних
- Зниження кількості певних типів клітин у крові, званих тромбоцитами; їх низький рівень може спричинити надмірне утворення синяків або кровотечу (тромбоцитопенія)
- Збільшення лімфатичних вузлів у області шиї, паху або пахвинної області (лімфаденопатія)
- Нейрологічні розлади, які можуть спричинити шийне м'язове ослаблення, дезорієнтацію, оніміння, біль і м'язову слабкість кінцівок, втрату рівноваги, втрату рефлексів, параліч частини або всього тіла (менінгіт і мієліт, неврит плечового сплетення, синдром Гієна-Барре), параліч обличчя (параліч Белла), розлади зору, спричинені дисфункцією зорових нервів (неврит зорового нерва/нейропатія), судоми (в тому числі фебрильні судоми), омдленіння безпосередньо після щеплення
- Васкуліт, який може призвести до шкірних висипів, а в дуже рідких випадках – до тимчасових порушень функції нирок, розширення кровоносних судин
- Біль у грудній клітці
- Свистящий дихання, стиск у горлі, труднощі з диханням (задишка)
Більшість побічних дій виникла зазвичай протягом 3 днів після щеплення і проходила протягом 3 днів. Насильство цих побічних дій було легким до помірного.
Звітність про побічні дії
Якщо виникнуть будь-які побічні дії, включаючи ті, які не перелічені в цій упаковці, повідоміть про це лікаря, фармацевта або медсестру. Побічні дії можна повідомляти безпосередньо до Департаменту моніторингу небажаних дій лікарських засобів Міністерства охорони здоров'я
вул. Джерельна, 4
03110 Київ
Телефон: +380 44 279 64 04
Факс: +380 44 279 64 04
Веб-сайт: https://www.moz.gov.ua/
Побічні дії також можна повідомляти відповідальному суб'єкту.
Звітність про побічні дії дозволить зібрати більше інформації про безпеку застосування ліків.
5. Як зберігати вакцину Efluelda Tetra
Вакцину необхідно зберігати в місці, недоступному для дітей.
Не застосовуйте цю вакцину після закінчення терміну придатності, вказаного на етикетці та упаковці
після «Термін придатності (EXP)». Термін придатності позначає останній день вказаного місяця.
Зберігайте у холодильнику (2 ° C – 8 ° C). Не заморожуйте. Зберігайте ампуло-шприц у
зовнішній упаковці для захисту від світла.
Ліки не слід викидати у каналізацію чи домашні контейнери для відходів. Зверніться до фармацевта, щоб дізнатися, як видалити ліки, які вже не використовуються. Таке поводження допоможе захистити
довкілля.
6. Зміст упаковки та інші відомості
Що містить вакцина Efluelda Tetra
- Активними речовинами є: Вірус грипу (інактивований, розщеплений) наступних штамів*:
A/Victoria/4897/2022 (H1N1)pdm09-подібний штам (A/Victoria/4897/2022, IVR-238)
.............................................................................................................................. 60 мкг HA**
A/Croatia/10136RV/2023 (H3N2)-подібний штам (A/Croatia/10136RV/2023, X-425A)
.............................................................................................................................. 60 мкг HA**
B/Austria/1359417/2021-подібний штам (B/Michigan/01/2021, дикий тип)
……………………………………….. ................................................................ 60 мкг HA**
B/Phuket/3073/2013-подібний штам (B/Phuket/3073/2013, дикий тип)
….…………………………………….. .............................................................. 60 мкг HA**
у дозі 0,7 мл
*
вирощений у курячих ембріонах
**
гемаглютинін
Вакцина відповідає рекомендаціям Всесвітньої організації охорони здоров'я (World Health Organization, WHO) для північної півкулі та рекомендаціям Європейського Союзу на сезон 2025/2026.
Інші компоненти: буферний розчин, який містить хлорид натрію, моногідрофосфат натрію, дигідрофосфат натрію, вода для ін'єкцій і октилоксинол-9 .
Деякі компоненти, такі як залишки яєць (альбумін яєць курей, білки курей) або формальдегід, можуть бути присутні у дуже малих кількостях (див. пункт 2).
Як виглядає вакцина Efluelda Tetra і що містить упаковка
Після легкого встрясання вакцина являє собою безбарвну, опалескуючу рідину.
Efluelda Tetra – суспензія для ін'єкцій в ампуло-шприці по 0,7 мл, з голкою або без голки
(в упаковці по 1, 5 або 10) або з голкою в захисній оболонці (в упаковці по 1 або 10).
Не всі розміри упаковок повинні бути в обігу.
Відповідальний суб'єкт та імпортер
Відповідальний суб'єкт:
Sanofi Winthrop Industrie
82 Avenue Raspail
94250 Gentilly, Франція
Імпортер:
Sanofi Winthrop Industrie
Voie de l’Institut - Parc Industriel d'Incarville
B.P 101
27100 Val de Reuil, Франція
Цей лікарський засіб дозволений до обігу в країнах-членах Європейського
Економічного простору під наступними назвами:
Дата останньої актуалізації упаковки:липень 2025
Інші джерела інформації
Поточна затверджена інформація про цей продукт доступна після сканування смартфоном коду QR
на паперовій упаковці або за наступною адресою URL:
https://eflueldatetra-nh.info.sanofi/
Інформація, призначена виключно для фахового медичного персоналу:
Як і у випадку з усіма вакцинами, які вводяться ін'єкціями, необхідно забезпечити належне лікування та медичний нагляд на випадок виникнення анафілактичної реакції після введення вакцини.
Перед введенням вакцина повинна досягти кімнатної температури.
Встряхніть перед застосуванням. Перевірте візуально перед введенням.
Вакцини не слід застосовувати у разі наявності в суспензії твердих частинок.
Вакцини не слід змішувати з іншими лікарськими засобами в тому самому шприці.
Вакцини не слід вводити безпосередньо в кровоносні судини.
Див. також пункт 3. Як застосовувати вакцину Efluelda Tetra
| Австрія, Бельгія, Болгарія, Кіпр, Чехія, Німеччина, Данія, Греція, Фінляндія, Франція, Хорватія, Угорщина, Ірландія, Італія, Латвія, Нідерланди, Норвегія, Польща, Португалія, Румунія, Швеція, Словенія, Словаччина, Іспанія | Efluelda Tetra |
| Велика Британія (Північна Ірландія) | Чотирьохвалентна вакцина проти грипу (розщеплений віріон, інактивована) високої дози |
Підготовка до застосування
Інструкція щодо використання голки з захисною оболонкою з ампуло-шприцем з кінцівкою Luer Lock:
| Рисунок А: Голка з захисною оболонкою (в обудові) | Рисунок Б: Елементи захисної оболонки голки (підготовлені до застосування) |
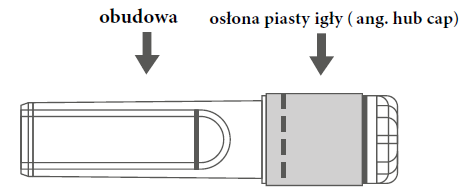 | 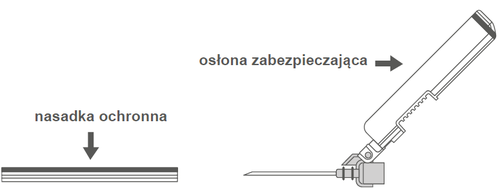 |
| Крок 1: Для прикріплення голки до шприца необхідно зняти захисний ковпачок голки (анг. hub cap), щоб відкрити голку, і легенько вкрутити голку в адаптер Luer Lock шприца до появи легкого опору. | |
Крок 2: Зняти обудову голки. Голка захищена захисною оболонкою і захисним ковпачком.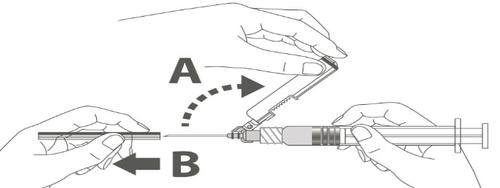 | |
| Kрок 3: A: Відсунути захисну оболонку від голки у бік корпусу шприца під показаним кутом. B: Зняти захисний ковпачок. | |
| Kрок 4: Після ін'єкції заблокувати (активувати) захисну оболонку, застосовуючи одну з трьох (3) представлених технік обслуговування однією рукою: активування на плоскій поверхні, великим пальцем або вказівним пальцем. Зауваження: Активування підтверджується чутним і (або) відчутним «кліком». | 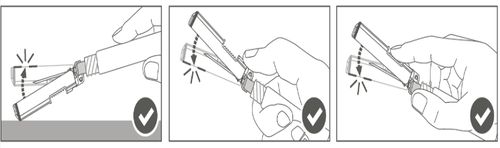 |
| Крок 5: Перевірити візуально роботу захисної оболонки. Захисна оболонка повинна бути повністю заблокована (активована), як показано на рисунку С. Рисунок D показує, що захисна оболонка НЕ є повністю заблокованою (не активованою). | 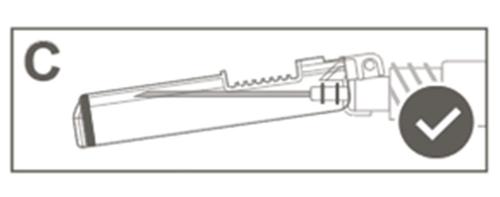 |
Попередження: Не слід намагатися розблокувати (деактивувати) захисне пристосування шляхом висування голки з захисної оболонки.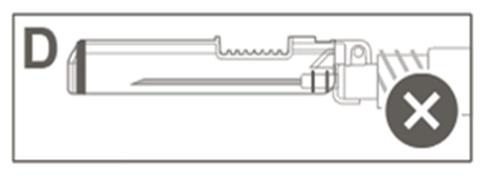 | |
Будь-які невикористані залишки лікарського засобу або його відходи слід видалити згідно з місцевими правилами.>
- Країна реєстрації
- Діючі речовини
- Потрібен рецептТак
- ІмпортерSanofi Winthrop Industrie
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до Ефлуелда ТетраФорма випуску: Суспензія, 60 мкг HA/штам, 1 доза (0,5 мл)Діючі речовини: influenza, inactivated, split virus or surface antigenПотрібен рецептФорма випуску: Суспензія, 1 доза (0,5 мл)Діючі речовини: influenza, inactivated, split virus or surface antigenПотрібен рецептФорма випуску: Суспензія, 1 доза (0,5 мл)Діючі речовини: influenza, inactivated, split virus or surface antigenПотрібен рецепт
Аналоги Ефлуелда Тетра в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Ефлуелда Тетра у Испания
Аналог Ефлуелда Тетра у Украина
Лікарі онлайн щодо Ефлуелда Тетра
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Ефлуелда Тетра – за рішенням лікаря та згідно з місцевими правилами.














