

Пріорікс

Запитайте лікаря про рецепт на Пріорікс

Інструкція із застосування Пріорікс
УПОКОРІСТЬОВУЙ ТАБЛИЧКА ДЛЯ ПАЦІЄНТА
Упаковочна вкладка: інформація для користувача
Priorix,порошок і розчинник для приготування розчину для ін'єкцій
Вакцина проти кору, епідемічного паротиту та краснухи, жива
Перед застосуванням вакцини необхідно ретельно ознайомитися з вмістом вкладки, оскільки вона містить важливу інформацію для пацієнта.
- Необхідно зберегти цю вкладку, щоб у разі потреби мати можливість знову її прочитати.
- У разі виникнення будь-яких сумнівів необхідно звернутися до лікаря або фармацевта.
- Вакцину призначено строго визначеній особі. Не слід її передавати іншим.
- Якщо у пацієнта виникнуть будь-які побічні ефекти, включаючи всі побічні ефекти, не перелічені в цій вкладці, необхідно повідомити про це лікаря або фармацевта. Див. пункт 4. Вміст цієї вкладки сформульовано з урахуванням того, що вона буде читана особою, якій призначено вакцину. Однак оскільки ця вакцина може бути призначена дорослим і дітям, можливо, що з вмістом вкладки ознайомиться буде батько чи опікун дитини.
Зміст вкладки:
- 1. Що таке вакцина Priorix і для чого вона призначена
- 2. Важливі відомості перед застосуванням вакцини Priorix
- 3. Як застосовувати вакцину Priorix
- 4. Можливі побічні ефекти
- 5. Як зберігати вакцину Priorix
- 6. Зміст упаковки та інші відомості
1. Що таке вакцина Priorix і для чого вона призначена
Priorix є вакциною, яка застосовується у дітей після досягнення 9 місяців життя, у підлітків та дорослих з метою профілактики кору, епідемічного паротиту та краснухи.
Як діє Priorix
Імунна система (природна система захисту організму) особи, якій введено вакцину Priorix, буде виробляти антитіла, завдяки чому пацієнт буде захищений від інфекції вірусами кору, епідемічного паротиту та краснухи.
Незважаючи на те, що вакцина Priorix містить живі віруси, вони надто слабкі, щоб спричинити захворювання на кору, епідемічний паротит та краснуху у здорових осіб.
2. Важливі відомості перед застосуванням вакцини Priorix
Коли не застосовувати вакцину Priorix:
- якщо раніше виникла алергічна реакція на будь-який компонент цієї вакцини (перелічений у пункті 6). Серед симптомів алергії слід назвати свербіж шкіри, труднощі з диханням, набряк обличчя або язика,
- якщо раніше виникла алергічна реакція на нейоміцин (антібіотик). Контактне дерматит, викликаний нейоміцином (шкірний висип у ситуації, коли відбувається прямий контакт з алергеном, таким як нейоміцин), не є протипоказанням до застосування вакцини, але необхідно повідомити про це лікаря,
- якщо існує гостра і тяжка хвороба, яка перебігає з гарячкою. У такому випадку щеплення буде відкладено до часу одужання. Легка інфекція, така як, наприклад, застуда, не повинна бути протипоказанням до щеплення, але необхідно попередньо обговорити це з лікарем,
- якщо існує будь-яка хвороба (наприклад, інфекція, викликана вірусом імунодефіциту людини (ВІЛ) або синдром набутого імунодефіциту (СНІД)) або якщо пацієнт приймає препарати, які можуть ослабити імунну систему. Те, чи отримає пацієнт вакцину, залежатиме від рівня імунітету,
- якщо встановлено вагітність. Крім того, необхідно уникати вагітності протягом 1 місяця після щеплення.
Попередження та заходи обережності
Перед введенням вакцини Priorix необхідно обговорити це з лікарем або фармацевтом, якщо:
- пацієнт страждає від розладів центральної нервової системи, судом з високою гарячкою або якщо в його родині раніше виникли судоми. У разі виникнення високої гарячки після щеплення необхідно негайно проконсультуватися з лікарем,
- у пацієнта раніше виникла тяжка алергічна реакція на білок курячого яйця,
- у пацієнта виникли побічні ефекти після щеплення проти кору, епідемічного паротиту або краснухи, які включали легке утворення синяків або кровотечу триваліше ніж зазвичай (див. пункт 4),
- пацієнт має ослаблену імунну систему (наприклад, у разі інфекції вірусом ВІЛ). Пацієнта необхідно піддати ретельному спостереженню з урахуванням того, що реакція на вакцину може не бути достатньою для забезпечення захисту від хвороби (див. пункт 2 «Коли не застосовувати вакцину Priorix»).
Після або навіть перед введенням кожної вакцини у вигляді ін'єкції може виникнути синкопе (особливо у підлітків). У зв'язку з цим необхідно повідомити лікаря або медсестру, якщо у пацієнта раніше виникло синкопе під час введення ін'єкції.
Якщо пацієнт буде щеплений у термін 72 годин після контакту з особою, хворою на кору, вакцина Priorix може забезпечити певний рівень захисту від захворювання.
Діти віком до 12 місяців
Діти, щеплені у перший рік життя, можуть не бути повністю захищені. Якщо необхідно буде введення додаткових доз вакцини, лікар призначить їх введення.
Як і у випадку з усіма вакцинами, вакцина Priorix може не забезпечувати повний захист усіх щеплених осіб.
Вакцина Priorix та інші препарати
Необхідно повідомити лікаря про всі щеплення та препарати, які приймає пацієнт зараз або раніше, а також про препарати або вакцини, які пацієнт планує приймати.
Вакцина Priorix може бути введена одночасно з іншими вакцинами, такими як:
вакцина проти дифтерії, тетуану, коклюшу (безкомпонентна), вакцина проти інфекції Haemophilus influenzae типу b, пероральна або інактивована вакцина проти поліомієліту, вакцина проти вірусного гепатиту типу А, вакцина проти вірусного гепатиту типу Б, вакцина проти вітряної віспи, вакцина проти менінгококу групи Б, а також кон'югована вакцина проти менінгококу серогрупи С, вакцина кон'югована проти менінгококу груп А, С, W135 і Y, а також кон'югована вакцина проти пневмококу. Для отримання додаткової інформації необхідно звернутися до лікаря або медсестри.
Кожна вакцина повинна бути введена в інше місце.
Якщо Priorix не може бути введено одночасно з іншими вакцинами, які містять живі, атenuовані віруси, необхідно дотримуватися інтервалу не менше одного місяця між щепленнями.
Щеплення може бути відкладено на термін не менше 3 місяців, якщо пацієнт раніше мав переливання крові або отримав людську імуноглобулін.
Якщо у пацієнта необхідно провести туберкуліновий тест (шкірне дослідження на туберкульоз), необхідно провести його до або одночасно з введенням вакцини чи через 6 тижнів після щеплення.
Вагітність, годування грудьми та вплив на фертильність
Вакцини Priorix не слід вводити вагітним жінкам .
Якщо пацієнтка вагітна або годує грудьми, підозрює, що може бути вагітною або планує мати дитину, вона повинна проконсультуватися з лікарем або фармацевтом перед застосуванням цієї вакцини.
Крім того, важливо, щоб протягом місяця після щеплення пацієнтка не стала вагітною. У цей період необхідно застосовувати ефективний метод контрацепції для уникнення вагітності.
Непередбачене введення вакцини Priorix вагітній жінці не повинно бути причиною переривання вагітності.
Priorix містить сорбітол, пара-амінобензойну кислоту, фенілаланін, натрій і калій
Ця вакцина містить 9 мг сорбітолу в кожній дозі.
Priorix містить пара-амінобензойну кислоту. Вона може викликати алергічні реакції (можливі реакції типу пізнього) та виключно бронхоспазм.
Вакцина містить 334 мкг фенілаланіну в кожній дозі. Фенілаланін може бути шкідливим для пацієнтів з фенілкетонурією (ФКУ), рідкісною генетичною хворобою, при якій фенілаланін накопичується в організмі, оскільки організм не усуває її належним чином.
Ця вакцина містить менше 1 ммоль (23 мг) натрію на дозу, тобто вакцину вважають «вільною від натрію».
Ця вакцина містить калій, менше 1 ммоль (39 мг) калію на дозу, тобто вакцину вважають «вільною від калію».
3. Як застосовувати вакцину Priorix
Вакцину Priorix вводять підшкірно або внутрішньом'язово, у верхню частину плеча або зовнішню частину стегна.
Priorix призначено для застосування у дітей після досягнення 9 місяців життя, підлітків та дорослих.
Відповідний момент щеплення та кількість введених доз визначається лікарем на основі офіційних рекомендацій.
Вакцини не слід вводити внутрішньовенно.
4. Можливі побічні ефекти
Як і будь-який препарат, ця вакцина може викликати побічні ефекти, хоча не у всіх вони виникнуть.
Після введення вакцини Priorix під час клінічних досліджень виникли наступні побічні ефекти:
♦ Дуже часто (можуть виникнути частіше ніж 1 на 10 доз вакцини):
- Червоність у місці введення
- Гарячка (38°C або вище)
♦ Часто (можуть виникнути рідше ніж 1 на 10 доз вакцини):
- Біль і набряк у місці введення
- Гарячка (вище 39,5°C)
- Висип
- Інфекція верхніх дихальних шляхів
♦ Не дуже часто (можуть виникнути рідше ніж 1 на 100 доз вакцини):
- Воспалення середнього вуха
- Збільшення лімфатичних вузлів (вузли в області шиї, паху або пахвин)
- Втрата апетиту
- Нервозність
- Нетиповий плач
- Безсоння
- Червоність, подразнення або сльозотеча очей (кон'юнктивіт)
- Воспалення бронхів
- Кашель
- Набряк слинних залоз біля вух (лімфатичні вузли в області щоки)
- Діарея
- Вомітування
♦ Рідко (можуть виникнути рідше ніж 1 на 1000 доз вакцини):
- Судоми з високою температурою
- Алергічні реакції
Після введення вакцини до обігу дуже рідко повідомлялося про виникнення наступних побічних ефектів:
- Біль у суглобах і м'язах
- Кровотеча або легше утворення синяків через зниження кількості тромбоцитів
- Нагальні алергічні реакції, які загрожують життю
- Інфекція або запалення мозку, спинного мозку та периферійних нервів, які призводять до тимчасових труднощів з ходьбою (хитання) та/або тимчасової втрати координації руху, запалення деяких нервів з можливим відчуттям оніміння або втрати чутливості чи порушення руху (синдром Гієна-Барре)
- Зуження або блокування кровоносних судин
- Віспоподібний висип (симптомами є червоні, часто сверблячі точки, подібні до висипу, який виникає при кору, які з'являються спочатку на кінцівках та іноді на обличчі та інших частинах тіла)
- Симптоми, подібні до кору та епідемічного паротиту (у тому числі тимчасовий, болючий набряк яєчок та набряклі залози на шиї)
Звітність про побічні ефекти
Якщо виникнуть будь-які побічні ефекти, включаючи всі побічні ефекти, не перелічені у цій вкладці, необхідно повідомити про це лікаря або фармацевта. Побічні ефекти можна повідомляти безпосередньо до Департаменту моніторингу непередбачених дій лікарських засобів Управління реєстрації лікарських засобів, медичних виробів та біоцидів:
Ал. Єрусалимські 181С
02-222 Варшава
Тел.: 22 49 21 301
Факс: 22 49 21 309
Сайт: https://smz.ezdrowie.gov.pl
Побічні ефекти також можна повідомляти відповідальному суб'єкту.
Звітність про побічні ефекти дозволить зібрати більше інформації про безпеку застосування препарату.
5. Як зберігати вакцину Priorix
Вакцину необхідно зберігати в місці, недоступному для дітей.
Не слід застосовувати цю вакцину після закінчення терміну придатності, вказаного на зовнішній упаковці.
Зберігати і перевозити у охолодженому стані (2°C – 8°C).
Не заморожувати.
Зберігати в оригінальній упаковці для захисту від світла.
Після реконструкції вакцину необхідно негайно ввести. Якщо це не можливо, вона повинна бути збережена в холодильнику (2°C – 8°C) та використана протягом 8 годин після реконструкції.
Лікарських засобів не слід викидати у каналізацію чи домашні контейнери для відходів. Необхідно запитати у фармацевта, як усунути лікарські засоби, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище.
6. Зміст упаковки та інші відомості
Що містить вакцина Priorix
Активними речовинами вакцини є живі атenuовані віруси: кору, епідемічного паротиту та краснухи.
Інші компоненти вакцини:
Порошок: амінокислоти (у тому числі фенілаланін), лактоза (безводна), мананіт (Е 421), сорбітол (Е 420),
середа 199 (у тому числі фенілаланін, пара-амінобензойна кислота, натрій і калій).
Розчинник: вода для ін'єкцій.
Як виглядає вакцина Priorix і що містить упаковка
Вакцина Priorix випускається у вигляді порошку та розчинника для приготування розчину для ін'єкцій (порошок у однодозовій флаконі та розчинник у ампуло-стрижці (0,5 мл)) у наступних розмірах упаковок:
- із 2 окремими голками: упаковки по 1 або 10 штук,
- без голок: упаковки по 1 або 10 штук.
Priorix поставляється у вигляді білуватого до легкого рожевого порошку, частина якого може бути жовтуватою до легкого помаранчевого, та прозорого, безбарвного розчинника (вода для ін'єкцій). Ці компоненти після реконструкції утворюють вакцину.
Не всі типи упаковок повинні бути в обігу.
Відповідальний суб'єкт і виробник
GlaxoSmithKline Biologicals S.A.
вул. Інститутська 89
1330 Ріксансарт, Бельгія
Дата останньої актуалізації вкладки:07/2025
Інші джерела інформації
Детальна інформація про цей препарат доступна на сайті Управління реєстрації лікарських засобів, медичних виробів та біоцидів .
------------------------------------------------------------------------------------------------------------------------
Інформація, призначена виключно для фахового медичного персоналу:
Аналогічно до всіх вакцин, які вводяться ін'єкційно, існує можливість виникнення рідкої анафілактичної реакції, тому необхідно забезпечити можливість фахової медичної допомоги безпосередньо після щеплення.
Алкоголь, а також інші дезінфікуючі засоби повинні випаруватися зі шкіри перед введенням вакцини, оскільки вони можуть викликати інактивацію атenuованих вірусів, які містяться у вакцині.
Вакцина Priorix у жодному разі не повинна вводитися внутрішньовенно.
У зв'язку з відсутністю досліджень сумісності вакцина не повинна змішуватися з іншими лікарськими засобами.
Розчинник та вакцину після реконструкції необхідно візуально оцінити перед реконструкцією та перед введенням щодо наявності сторонніх частинок та (або) фізичних змін. У разі виявлення порушень у зовнішньому вигляді не слід використовувати розчинник або підготовану вакцину.
Вакцину необхідно піддати реконструкції шляхом додавання всього розчинника з ампуло-стрижки до флакону з порошком.
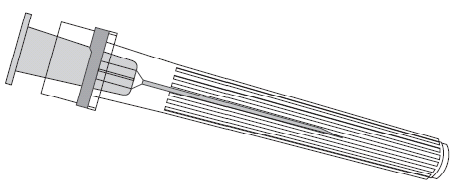
Для прикріплення голки до ампуло-стрижки необхідно ретельно ознайомитися з інструкцією, представленою на малюнках 1 і 2. Ампуло-стрижка, поставляється з вакциною PRIORIX, може відрізнятися незначно від зображеної на малюнку (може не мати різьби для вкручування голки). У такому випадку голка повинна бути закріплена без вкручування.
Голка
Ампуло-стрижка
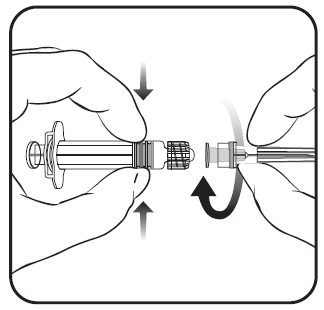
Необхідно завжди тримати ампуло-стрижку за її корпус, а не за поршень чи адаптер Luer Lock (англ. Luer Lock Adaptor, LLA), а голку необхідно утримувати в осі ампуло-стрижки (як показано на малюнку 2). Не слідування цим рекомендаціям може призвести до перекосу адаптера LLA та витоку з ампуло-стрижки.
Якщо під час прикріплення голки до ампуло-стрижки відбувається від'єднання адаптера LLA, необхідно використовувати нову дозу вакцини (нову ампуло-стрижку і флакон).
Малюнок 1. Малюнок 2.
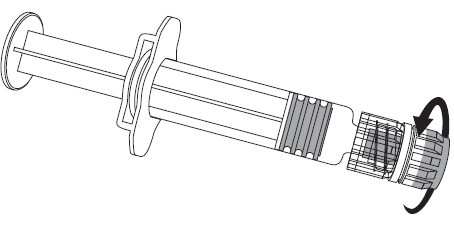
- 1. Необхідно відкрутити насадку ампуло-стрижки шляхом обертання її у напрямку, протилежному до руху годинникової стрілки (як показано на малюнку 1).
Незалежно від того, чи обертатиметься адаптер LLA, чи ні, необхідно слідувати наступним інструкціям:
- 2. Необхідно прикріпити голку до ампуло-стрижки шляхом деликатного прикріплення насадки голки до адаптера LLA та обертання її на чверть обертання у напрямку, збігальному з рухом годинникової стрілки, до тих пір, поки не відчутиться блокування голки (як показано на малюнку 2).
- 3. Необхідно зняти захисний кожух голки, який може чинити опір.
- 4. Необхідно додати розчинник до порошку. Після цього необхідно енергійно встряхнути до моменту повного розчинення порошку.
Залежно від незначних коливань pH, вакцина після реконструкції може набувати колір від персикового до рожевого з відтінком фуксії, що не впливає на її ефективність.
- 5. Необхідно витягнути всю вміст флакону.
- 6. Для введення вакцини необхідно використовувати нову голку. Для цього необхідно відкрутити голку від ампуло-стрижки та прикріпити голку для ін'єкцій, слідуючи опису, представленому в пункті 2.
Після реконструкції вакцину необхідно негайно ввести. Якщо це не можливо, вона повинна бути збережена в холодильнику (2°C – 8°C) та використана протягом 8 годин після реконструкції.
Всі залишки незастосованого продукту або його відходи необхідно усунути у спосіб, що відповідає місцевим правилам.
- Країна реєстрації
- Діючі речовини
- Потрібен рецептТак
- Виробник
- ІмпортерGlaxoSmithKline Biologicals S.A.
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до ПріоріксФорма випуску: Порошок, -Потрібен рецептФорма випуску: Порошок, -Виробник: GlaxoSmithKline Biologicals S.A.Потрібен рецептФорма випуску: Суспензія, 160 антигенних одиниць ELISA вірусу гепатиту A, штам GBM/0,5 мл; 1 доза (0,5 мл)Діючі речовини: hepatitis A, inactivated, whole virusПотрібен рецепт
Аналоги Пріорікс в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Пріорікс у Іспанія
Аналог Пріорікс у Україна
Лікарі онлайн щодо Пріорікс
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Пріорікс – за рішенням лікаря та згідно з місцевими правилами.














