
Мівацуріум Калцекс
Запитайте лікаря про рецепт на Мівацуріум Калцекс

Інструкція із застосування Мівацуріум Калцекс
Упаковка з інструкцією: інформація для пацієнта
Mivacurium Kalceks, 2 мг/мл, розчин для ін'єкцій/інфузій
Mivacurium
Перш ніж використовувати препарат, уважно ознайомтеся з вмістом цієї інструкції, оскільки вона містить важливу інформацію для пацієнта.
- Збережіть цю інструкцію, щоб у разі потреби ви могли її знову прочитати.
- Якщо у вас виникли будь-які сумніви, зверніться до лікаря або медсестри.
- Якщо в пацієнта з'явилися будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цій інструкції, повідомте про це лікаря або медсестру. Див. пункт 4.
Зміст інструкції
- 1. Що таке препарат Mivacurium Kalceks і для чого він використовується
- 2. Інформація, яку потрібно знати до використання препарату Mivacurium Kalceks
- 3. Як використовувати препарат Mivacurium Kalceks
- 4. Можливі побічні ефекти
- 5. Як зберігати препарат Mivacurium Kalceks
- 6. Зміст упаковки і інші відомості
1. Що таке препарат Mivacurium Kalceks і для чого він використовується
Mivacurium Kalceks містить активну речовину під назвою мівакурій. Ця речовина належить до групи м'язових релаксантів.
Цей препарат використовується:
- для м'язової релаксації під час операцій у дорослих, підлітків і дітей віком від 2 місяців і старше, включаючи операції на серці;
- для полегшення інтубації трахеї (введення трубки в трахею), якщо пацієнту потрібна допомога з диханням.
Для отримання більшої кількості інформації про цей препарат зверніться до лікаря.
2. Інформація, яку потрібно знати до використання препарату Mivacurium Kalceks
Коли не використовувати препарат Mivacurium Kalceks
- якщо пацієнт має алергію на мівакурій або будь-який інший компонент цього препарату (перелічені в пункті 6);
- якщо в пацієнта виявлена генетична аномалія холінестерази;
- якщо пацієнт або його родина раніше мали погану реакцію на анестетики.
Якщо пацієнт не впевнений, чи стосується він однієї з вищезазначених ситуацій, він повинен обговорити це з лікарем або медсестрою перед використанням цього препарату.
Попередження та обережність
Перш ніж почати використовувати препарат, пацієнт повинен обговорити це з лікарем або медсестрою, якщо:
- в пацієнта спостерігається м'язова слабкість, втома або труднощі з координацією рухів (міастенія);
- пацієнт має опіки, які потребують медичного лікування;
- в пацієнта раніше спостерігалася алергічна реакція на будь-який м'язовий релаксант, який вводився під час операції;
- пацієнт чутливий до зниження артеріального тиску;
- пацієнт пройшов процедуру плазмаферезу;
- пацієнт отримав донорську плазму;
- пацієнт пройшов операцію на серці з використанням апарату штучного кровообігу;
- пацієнт має знижену кількість крові (гіповолемія);
- пацієнт має порушення кислотно-лужного балансу;
- пацієнт має порушення рівня натрію, калію або кальцію;
- пацієнтка була вагітна або народила дитину протягом останніх 6 тижнів;
- пацієнт має генетичну аномалію холінестерази;
- пацієнт чутливий до гістаміну або має бронхіальну астму.
Перш ніж використовувати цей препарат, пацієнт повинен обговорити з лікарем, якщо в нього спостерігаються або раніше спостерігалися будь-які з нижчезазначених станів:
- тетанія;
- важкі або тривалі інфекції, такі як туберкульоз;
- будь-яка тривала хвороба, після якої пацієнт залишається ослабленим;
- пухлина;
- анемія (зниження кількості червоних кров'яних тілець);
- гіповітаміноз;
- гіпотиреоз;
- серцеві захворювання;
- виразка шлунка;
- опіки;
- хвороби печінки або нирок;
- колагенові захворювання (колагенози або захворювання сполучної тканини).
Якщо пацієнт не впевнений, чи стосується він однієї з вищезазначених ситуацій, він повинен обговорити це з лікарем або медсестрою перед використанням цього препарату.
Діти
Препарат не слід застосовувати у дітей віком до 2 місяців.
Mivacurium Kalceks та інші препарати
Пацієнт повинен повідомити лікаря або медсестру про всі препарати, які він зараз приймає, або планує приймати. Це стосується також препаратів, які видаються без рецепта, включаючи рослинні препарати. Це потрібно тому, що ці препарати можуть впливати на ефективність дії препарату Mivacurium Kalceks або спричиняти побічні ефекти.
Особливо пацієнт повинен повідомити лікаря або медсестру, якщо він приймає будь-який з нижчезазначених препаратів:
- анестетики, такі як кетамін, енфлуран, ізофлуран, севофлуран і галотан (використовуються для зменшення чутливості та болю під час хірургічних процедур);
- м'язові релаксанти, такі як суksametonій хлорид і панкуроній;
- антибіотики, такі як аміноглікозиди, поліміксини, спектиноміцин, тетрацикліни, лінкоміцин і кліндаміцин (використовуються для лікування інфекцій);
- препарати для лікування аритмій, такі як пропранолол (також використовується для лікування високого артеріального тиску), лідокаїн, прокаїнамід, хінідин і блокатори кальцієвих каналів (препарати проти аритмій);
- мочогінні препарати, такі як фуросемід, тіазиди, манітол і ацетазоламід;
- препарати для лікування ревматизму, такі як хлорохін або Д-пеніциламін;
- стероїди;
- препарати для лікування епілепсії, такі як фенітоїн;
- препарати, використовувані для лікування психічних захворювань, таких як літій, інгібітори моноамінооксидази (МАО), селективні інгібітори зворотного захоплення серотоніну або хлорпромазин (який також може використовуватися для лікування нудоти);
- препарати, що містять магній, такі як препарати для лікування нудоти та диспепсії;
- препарати, що блокують нервові вузли, такі як триметафан і гексаметоній;
- препарати для лікування болю в грудній клітці (стенокардія), такі як окспренолол (також використовується для лікування високого артеріального тиску);
- бамбутерол (використовується для лікування астми);
- препарати, які можуть знижувати рівень холінестерази в крові, такі як протипухлинні препарати, йодек eкotioфат, фосфороорганічні сполуки, інгібітори холінестерази та деякі гормони.
Вагітність і годування грудьми
Якщо пацієнтка вагітна або годує грудьми, підозрює вагітність або планує мати дитину, вона повинна проконсультуватися з лікарем перед використанням цього препарату.
Водіння транспортних засобів і робота з механізмами
Водіння транспортних засобів або робота з механізмами одразу після операції може бути небезпечною. Лікар повідомить пацієнта, як довго йому потрібно чекати, перш ніж він зможе водити транспортні засоби та працювати з механізмами.
3. Як використовувати препарат Mivacurium Kalceks
Пацієнт ніколи не повинен самостійно вводити цей препарат. Його завжди вводить кваліфікована особа.
Цей препарат може вводитися:
- як єдина ін'єкція в вену (введення в вену болюсно);
- у вигляді тривалого внутрішньовенного введення. Препарат вводиться повільно протягом тривалого періоду часу.
Лікар вирішує, яким способом вводити цей препарат і яку дозу отримує пацієнт. Вона залежить від:
- маси тіла пацієнта;
- необхідного рівня і тривалості м'язової релаксації;
- очікуваної реакції пацієнта на препарат.
Цього препарату не слід застосовувати у дітей віком до 2 місяців.
Введення більшої, ніж рекомендована, дози препарату Mivacurium Kalceks
Цей препарат повинен завжди вводитися під суворо контрольованими умовами. Однак, якщо пацієнт вважає, що введена доза препарату більша, ніж рекомендована, він повинен негайно повідомити про це лікаря або медсестру.
4. Можливі побічні ефекти
Як і будь-який препарат, цей препарат може спричиняти побічні ефекти, хоча вони не спостерігаються у всіх пацієнтів.
Алергічні реакції (можуть спостерігатися не частіше, ніж у 1 з 10 000 пацієнтів)
Якщо в пацієнта спостерігається алергічна реакція, він повинен негайно повідомити про це лікаря або медсестру. Симптоми можуть включати:
- наглий свистячий дихання, біль у грудній клітці або стиск у грудній клітці
- опухання повік, обличчя, губ, рота або мови
- грудкова висипка на шкірі або кропив'янка в будь-якому місці на тілі
- запілля (нагальна негодність кровообігу)
Пацієнт повинен повідомити лікаря або медсестру, якщо він помічає будь-який з нижчезазначених симптомів:
Дуже часто (можуть спостерігатися частіше, ніж у 1 з 10 пацієнтів)
- червоність шкіри
Не дуже часто (можуть спостерігатися не частіше, ніж у 1 з 100 пацієнтів)
- підвищена частота серцевих скорочень
- зниження артеріального тиску
- свистячий дихання або кашель
- висипка або кропив'янка (грудкова висипка на шкірі або "кропив'янка" в будь-якому місці на тілі)
Звітність про побічні ефекти
Якщо спостерігаються будь-які побічні ефекти, включаючи будь-які побічні ефекти, не перелічені в цій інструкції, пацієнт повинен повідомити про це лікаря або фармацевта. Побічні ефекти можна повідомляти безпосередньо до Департаменту моніторингу небажаних дій лікарських засобів Міністерства охорони здоров'я України
вул. Миколи Амосова, 7
04053, м. Київ
Телефон: +38 (044) 206 27 30
Факс: +38 (044) 206 27 31
Веб-сайт: https://www.moz.gov.ua/
Побічні ефекти також можна повідомляти відповідальному суб'єкту.
Звітність про побічні ефекти дозволить зібрати більше інформації про безпеку використання препарату.
5. Як зберігати препарат Mivacurium Kalceks
Препарат слід зберігати в місці, недоступному для дітей.
Не слід використовувати цей препарат після закінчення терміну його дії, вказаного на пачці з картону після слів "Термін дії" і на ампулі після слів "EXP". Термін дії означає останній день вказаного місяця.
Зберігати в холодильнику (2°C – 8°C).
Стабільність після розведення
Показано хімічну і фізичну стабільність протягом 48 годин при температурі 30°C і 2 до 8°C після розведення з розчинами для інфузії (переліченими нижче) у концентрації 0,5 мг/мл.
З мікробіологічної точки зору, розведений розчин слід використовувати негайно. Якщо він не буде використаний негайно, відповідальність за час і умови зберігання перед використанням лежить на користувачі. Час зберігання розчину зазвичай не повинен перевищувати 24 години при температурі від 2 до 8°C, якщо тільки розведення не відбулося в контрольованих і валідованих асеptyчних умовах.
Ліки не слід викидати в каналізацію або домашні контейнери для відходів. Пацієнт повинен запитати у фармацевта, як видалити ліки, які вже не використовуються. Таке поводження допоможе захистити навколишнє середовище.
6. Зміст упаковки і інші відомості
Що містить препарат Mivacurium Kalceks
- Активна речовина - мівакурій. 1 мл розчину містить 2 мг мівакурію (Mivacurium) у вигляді мівакурій хлориду. Кожна ампула об'ємом 5 мл містить 10 мг мівакурію (у вигляді мівакурій хлориду). Кожна ампула об'ємом 10 мл містить 20 мг мівакурію (у вигляді мівакурій хлориду).
- Інший компонент - вода для ін'єкцій.
Як виглядає препарат Mivacurium Kalceks і що містить упаковка
Прозорий, безбарвний або світло-жовтий розчин, вільний від видимих частинок.
5 мл або 10 мл розчину в ампулах з безбарвного скла типу I, з одним пунктом розриву.
Ампули упаковані в обгортку. Обгортки упаковані в картонну коробку.
Варіанти упаковки:
5 або 10 ампул по 5 мл
5 або 10 ампул по 10 мл
Не всі варіанти упаковки повинні бути в обігу.
Відповідальний суб'єкт і виробник
AS KALCEKS
Кrustpils iela 71E
LV-1057 Рига
Латвія
Телефон: +371 67083320
Електронна пошта: [email protected]
Цей препарат дозволений до обігу в країнах-членах Європейського економічного простору під наступними назвами:
Латвія
Mivacurium Kalceks 2 мг/мл розчин для ін'єкцій/інфузій
Німеччина
Mivacurium Kalceks 2 мг/мл ін'єкційний/інфузійний розчин
Польща
Mivacurium Kalceks
Дата останньої актуалізації інструкції:
---------------------------------------------------------------------------------------------------------------------------
Інформація, призначена лише для фахівців медицини:
Дозування
- Введення болюсно у дорослих
Mivacurium Kalceks вводиться внутрішньовенно. Середня доза, необхідна для досягнення 95% гальмування одиночної реакції скорочення великого пальця на стимуляцію ліктьового нерва (ED), становить 0,07 мг/кг маси тіла. (діапазон від 0,06 до 0,09 мг/кг маси тіла) у дорослих, анестезованих наркотичними анальгетиками.
Для інтубації трахеї рекомендується наступна схема дозування:
а)
Доза 0,2 мг/кг маси тіла, введена протягом 30 секунд, забезпечує хороші або відмінні умови для інтубації трахеї протягом 2-2,5 хвилин.
б)
Доза 0,25 мг/кг маси тіла, введена у вигляді роздільної дози (0,15 мг/кг маси тіла, а потім через 30 секунд 0,1 мг/кг маси тіла), забезпечує хороші або відмінні умови для інтубації трахеї протягом 1,5-2,0 хвилин після закінчення введення першої частини дози.
У здорових дорослих рекомендується діапазон доз, введених болюсно, від 0,07 до 0,25 мг/кг маси тіла. Час дії блокади нервово-м'язової провідності залежить від дози. Дози 0,07 мг/кг маси тіла, 0,15 мг/кг маси тіла, 0,20 мг/кг маси тіла і 0,25 мг/кг маси тіла викликають клінічно ефективну блокаду, яка триває приблизно 13, 16, 20 і 23 хвилини відповідно.
Дози до 0,15 мг/кг маси тіла можна вводити протягом 5-15 секунд. Більші дози слід вводити протягом 30 секунд або у вигляді роздільних доз, щоб мінімізувати можливість появи порушень з боку серцево-судинної системи.
Повну блокаду можна продовжити шляхом введення підтримуючих доз мівакурію. Кожна доза 0,1 мг/кг маси тіла, введена під час анестезії, викликаної наркотичними анальгетиками, продовжує клінічно ефективну блокаду на приблизно 15 хвилин. Наступні додаткові дози не викликають кумулятивного ефекту блокади нервово-м'язової провідності.
Ефект блокади нервово-м'язової провідності мівакурію посилюється при одночасному застосуванні інгалаційних анестетиків. Клінічні дослідження показали, що під час застосування ізофлурану або енфлурану рекомендується зменшити початкову дозу мівакурію навіть на 25%. Під час стабільної анестезії, викликаної ізофлураном або енфлураном, рекомендується зменшити швидкість інфузії мівакурію навіть на 40%. Клінічні дослідження показали, що при одночасному застосуванні севофлурану швидкість інфузії мівакурію слід зменшити навіть на 50%. При застосуванні галотану потреба в обмеженні швидкості інфузії може бути меншою.
Самостійне закінчення блокади нервово-м'язової провідності після застосування мівакурію триває приблизно 15 хвилин, незалежно від величини введеної дози мівакурію.
Блокаду нервово-м'язової провідності, викликану застосуванням мівакурію, можна зняти шляхом введення стандартних доз інгібіторів холінестерази. Однак, оскільки самостійне закінчення блокади нервово-м'язової провідності після застосування мівакурію відбувається швидко, у звичайній практиці зняття блокади може не бути необхідним, оскільки воно скорочує час до закінчення блокади лише на 5-6 хвилин.
- Введення інфузією у дорослих
Для підтримання блокади нервово-м'язової провідності мівакурій можна застосовувати у вигляді тривалої інфузії. Після появи перших ознак самостійного закінчення блокади після введення початкової дози мівакурію рекомендується швидкість інфузії 8-10 мкг/кг маси тіла/хв (0,5-0,6 мг/кг маси тіла/год).
Початкова швидкість інфузії повинна бути встановлена на основі реакції пацієнта на стимуляцію периферичних нервів і клінічних критеріїв.
Швидкість інфузії слід регулювати шляхом поступового зміни введеної дози на приблизно 1 мкг/кг маси тіла/хв (0,06 мг/кг маси тіла/год). Зазвичай рекомендується підтримувати задану швидкість інфузії протягом至少 3 хвилин перед її зміною.
У дорослих, анестезованих наркотичними анальгетиками, середня швидкість інфузії в діапазоні 6-7 мкг/кг маси тіла/хв дозволяє підтримувати тривалу блокаду нервово-м'язової провідності на рівні 89-99%. Під час стабільної анестезії, викликаної ізофлураном або енфлураном, рекомендується зменшити швидкість інфузії мівакурію навіть на 40%. Клінічні дослідження показали, що при одночасному застосуванні севофлурану швидкість інфузії мівакурію слід зменшити навіть на 50%. При застосуванні галотану потреба в обмеженні швидкості інфузії може бути меншою.
Самостійне закінчення блокади нервово-м'язової провідності після застосування мівакурію у вигляді інфузії не залежить від тривалості інфузії і є порівнюванним з закінченням блокади після введення одиночних доз.
Застосування мівакурію у вигляді тривалої інфузії не було пов'язано з розвитком тахіфілаксії або кумулятивного ефекту блокади нервово-м'язової провідності.
Особливі групи пацієнтів
Педіатрична популяція
Немовлята і діти віком від 7 місяців до 12 років
Mivacurium має вищу дозу ED (близько 0,1 мг/кг маси тіла), початок дії препарату відбувається швидше, час дії клінічно ефективної блокади є коротшим, а самостійне закінчення дії є швидшим у немовлят і дітей віком від 7 місяців до 12 років порівняно з дорослими.
Діапазон рекомендуємої дози, введеної у вигляді болюсу, у дітей віком від 7 місяців до 12 років становить від 0,1 до 0,2 мг/кг маси тіла, введеної протягом 5-15 секунд. Доза 0,2 мг/кг маси тіла, введена під час стабільної анестезії, викликаної наркотичними анальгетиками або галотаном, викликає клінічно ефективну блокаду нервово-м'язової провідності протягом приблизно 9 хвилин.
Для виконання інтубації трахеї у немовлят і дітей віком від 7 місяців до 12 років рекомендується введення мівакурію у дозі 0,2 мг/кг маси тіла. Максимальна блокада нервово-м'язової провідності спостерігається зазвичай протягом 2 хвилин після введення цієї дози і протягом цього часу повинно бути можливим виконання інтубації.
У немовлят і дітей підтримуючі дози зазвичай слід вводити частіше, ніж у дорослих.
З наявних даних випливає, що підтримуюча доза 0,1 мг/кг маси тіла продовжує клінічно ефективну блокаду на приблизно 6-9 хвилин під час анестезії, викликаної наркотичними анальгетиками або галотаном.
Немовлята і діти зазвичай потребують вищої швидкості інфузії порівняно з дорослими.
Під час анестезії галотаном середня швидкість інфузії, необхідна для підтримання блокади нервово-м'язової провідності на рівні 89-99% у пацієнтів віком від 7 до 23 місяців, становить приблизно 11 мкг/кг маси тіла/хв (близько 0,7 мг/кг маси тіла/год) [діапазон: від 3 до 26 мкг/кг маси тіла/хв (близько 0,2-1,6 мг/кг маси тіла/год)].
У дітей віком від 2 до 12 років еквівалентна середня швидкість інфузії становить приблизно 13-14 мкг/кг маси тіла/хв (близько 0,8 мг/кг маси тіла/год) [діапазон: 5-31 мкг/кг маси тіла/хв (близько 0,3-1,9 мг/кг маси тіла/год)] під час анестезії галотаном або наркотичними анальгетиками.
Блокада нервово-м'язової провідності, викликану застосуванням мівакурію, посилюється при одночасному застосуванні інгалаційних анестетиків. Клінічні дослідження показали, що у дітей віком від 2 до 12 років під час застосування севофлурану швидкість інфузії мівакурію слід зменшити навіть на 70%.
Від початку самостійного закінчення блокади нервово-м'язової провідності до повного закінчення цього процесу минає приблизно 10 хвилин.
Немовлята віком від 2 до 6 місяців
Mivacurium має подібну дозу ED порівняно з дорослими (0,07 мг/кг маси тіла), але початок дії препарату відбувається швидше, час дії клінічно ефективної блокади є коротшим, а самостійне закінчення дії є швидшим у немовлят віком від 2 до 6 місяців.
Рекомендований діапазон доз, введених у вигляді болюсу, у немовлят віком від 2 до 6 місяців становить 0,1-0,15 мг/кг маси тіла, введеної протягом 5-15 секунд. Доза 0,15 мг/кг маси тіла, введена під час стабільної анестезії галотаном, викликає клінічно ефективну блокаду нервово-м'язової провідності, яка триває приблизно 9 хвилин.
Доза мівакурію 0,15 мг/кг маси тіла рекомендується для виконання інтубації трахеї у немовлят віком від 2 до 6 місяців. Максимальна блокада нервово-м'язової провідності спостерігається після приблизно 1,4 хвилини після введення цієї дози і протягом цього часу повинно бути можливим виконання інтубації.
У немовлят віком від 2 до 6 місяців підтримуючі дози зазвичай слід вводити частіше, ніж у дорослих. З наявних даних випливає, що підтримуюча доза 0,1 мг/кг маси тіла продовжує клінічно ефективну блокаду на приблизно 7 хвилин під час анестезії галотаном.
Немовлята віком від 2 до 6 місяців зазвичай потребують вищої швидкості інфузії порівняно з дорослими. Середня швидкість інфузії, необхідна для підтримання блокади нервово-м'язової провідності на рівні 89-99% під час анестезії галотаном, становить приблизно 11 мкг/кг маси тіла/хв (близько 0,7 мг/кг маси тіла/год) [діапазон: від 4 до 24 мкг/кг маси тіла/хв (близько 0,2-1,5 мг/кг маси тіла/год)].
Від початку самостійного закінчення блокади нервово-м'язової провідності до повного закінчення цього процесу минає приблизно 10 хвилин.
Новонароджені та немовлята віком до 2 місяців
Безпека і ефективність застосування мівакурію хлориду у новонароджених та немовлят віком до 2 місяців не встановлені. Не можна сформулювати рекомендації щодо дозування.
Пацієнти похилого віку
У пацієнтів похилого віку, які отримують одиночну дозу мівакурію у вигляді швидкого внутрішньовенного введення, період часу від введення препарату до появи його дії та тривалості і швидкості закінчення блокади можуть бути збільшені на 20-30% порівняно з молодшими пацієнтами. Пацієнти похилого віку можуть потребувати повільнішої інфузії або рідшого введення підтримуючих доз при швидкому внутрішньовенному введенні.
Пацієнти з серцево-судинними захворюваннями
Пацієнтам з клінічно значимими проявами серцево-судинних захворювань початкову дозу мівакурію слід вводити протягом至少 60 секунд. Мівакурій, введений у такий спосіб, викликав мінімальні зміни гемодинаміки у пацієнтів, які піддавалися кардіохірургічним операціям.
Пацієнти з нирковою недостатністю
У пацієнтів з термінальною нирковою недостатністю клінічно ефективна блокада, викликана застосуванням мівакурію у дозі 0,15 мг/кг маси тіла, триває приблизно в 1,5 раза довше, ніж у пацієнтів з нормальною функцією нирок. Тому дозу препарату слід коригувати залежно від індивідуальної клінічної реакції пацієнта.
Продовжена і посилена блокада нервово-м'язової провідності також може спостерігатися у пацієнтів з гострою або хронічною нирковою недостатністю внаслідок зниження активності холінестерази крові.
Пацієнти з печінковою недостатністю
У пацієнтів з термінальною печінковою недостатністю клінічно ефективна блокада, викликана застосуванням мівакурію у дозі 0,15 мг/кг маси тіла, триває приблизно в 3 раза довше, ніж у пацієнтів з нормальною функцією печінки. Продовження цього часу дії пов'язано з спостережуваним у цих пацієнтів значним зниженням активності холінестерази крові. Тому дозу слід коригувати залежно від індивідуальної клінічної реакції пацієнта.
Пацієнти з зниженою активністю холінестерази крові
Mivacurium метаболізується холінестеразою крові. Активність холінестерази крові може бути знижена при генетичних аномаліях холінестерази крові (наприклад, у пацієнтів, які є гетерозиготами або гомозиготами щодо атипового гена холінестерази крові) та при різних патологічних станах або після застосування деяких препаратів. У пацієнтів з зниженою активністю холінестерази крові слід очікувати можливості продовження часу дії блокади нервово-м'язової провідності після застосування мівакурію. Незначне зниження активності цього ферменту (тобто до 20% порівняно з нижньою межею нормальних значень) не має клінічно значимого впливу на тривалість блокади.
Пацієнти з надмірною масою тіла
У пацієнтів з надмірною масою тіла (які перевищують належну для зросту масу тіла на 30% або більше), початкову дозу мівакурію слід розрахувати для належної, а не реальної маси тіла.
Моніторинг пацієнтів
Аналогічно до всіх препаратів, які блокують нервово-м'язову провідність, під час застосування мівакурію рекомендується моніторинг нервово-м'язової діяльності для індивідуалізації вимог до дозування.
При застосуванні мівакурію не спостерігається значного зниження реакції скорочення м'язів, виміряної методом чотириімпульсного стимулювання (train-of-four). Часто можливо виконання інтубації трахеї до повного гальмування реакції скорочення м'яза-приводника великого пальця на стимуляцію методом чотириімпульсного стимулювання.
Спосіб застосування
Для внутрішньовенного введення.
Цей продукт не містить бактеріостатичних консервантів і призначений для застосування у одного пацієнта.
Mivacurium Kalceks (2 мг/мл) можна застосовувати для інфузії у вигляді нерозведеного розчину.
Передозування
Симптоми і ознаки
Надмірно тривале паралітичне作用 і його наслідки є основними симптомами передозування препаратів, які блокують нервово-м'язову провідність. Однак існує підвищене ризик появи гемодинамічних побічних ефектів, зокрема зниження артеріального тиску.
Поведінка
До моменту відновлення самостійної ефективної дихальної діяльності необхідно підтримувати прохідність дихальних шляхів та застосовувати вентиляцію з позитивним тиском вдиху.
Слід застосувати препарати, які викликають повне знеболення, оскільки свідомість після застосування мівакурію не порушується.
Введення інгібіторів ацетилхолінестерази разом з атропіном або глікопіронієм на момент появи ознак самостійного відновлення нервово-м'язової провідності може прискорити це відновлення.
Відповідне положення пацієнта та введення за необхідності рідини або препаратів, які викликають звуження судин, можуть підтримати діяльність серцево-судинної системи.
Несумісність
Mivacurium, розчин, має кислотний pH (близько 4,5) і не повинен змішуватися з сильними лугами, наприклад, з барбітуратами.
Не слід змішувати цей лікарський засіб з іншими лікарськими засобами, крім перелічених нижче.
Інструкції щодо використання та видалення
Тільки для одноразового використання.
Ампула повинна бути перевірена візуально перед застосуванням. Слід застосовувати тільки прозорі та вільні від частинок розчини.
Після відкриття лікарського засобу його слід застосувати негайно.
Через те, що препарат не містить бактеріостатичних консервантів, розчин мівакурію слід застосовувати в умовах повної асептики, а будь-яке розведення слід проводити безпосередньо перед застосуванням. Будь-які невикористані залишки розчину в відкритих ампулах слід видалити.
Показано, що мівакурій можна змішувати з деякими препаратами, які зазвичай застосовуються під час операції, які існують у вигляді кислотних розчинів. Коли через одну і ту ж вставлену голку або канюлю вводяться мівакурій та інші анестетики, а не показано можливість їх змішування, після введення кожного препарату слід кожен раз промивати систему ізотонічним розчином хлориду натрію.
Mivacurium Kalceks є сумісним з наступними розчинами для інфузії:
- 9 мг/мл (0,9%) розчин хлориду натрію
- 50 мг/мл (5%) внутрішньовенний розчин глюкози
- 1,8 мг/мл (0,18%) розчин хлориду натрію та 40 мг/мл (4%) розчин глюкози
- р-н Рінгера з лактатом
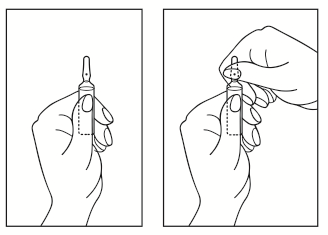
Інструкція з відкриття ампули
- 1) Оберніть ампулу кольоровим пунктом вгору. Якщо у верхній частині ампули знаходиться розчин, необхідно легонько постукати пальцем, щоб перенести весь розчин у нижню частину ампули.
- 2) Використовуйте обидві руки, щоб відкрити ампулу; тримаючи нижню частину ампули в одній руці, другою рукою відламайте верхню частину ампули в бік від кольорового пункту (див. малюнок нижче).
- Країна реєстрації
- Діючі речовини
- Потрібен рецептНі
- ІмпортерAS Kalceks
- Інформація є довідковою і не є медичною порадою. Перед прийомом будь-яких препаратів обов'язково проконсультуйтеся з лікарем. Oladoctor не несе відповідальності за медичні рішення, прийняті на основі цього контенту.
- Альтернативи до Мівацуріум КалцексФорма випуску: Розчин, 2 мг/млДіючі речовини: mivacurium chlorideНе потрібен рецептФорма випуску: Порошок, 4 мгДіючі речовини: pipecuronium bromideВиробник: Gedeon Richter Plc.Не потрібен рецептФорма випуску: Розчин, 10 мг/млДіючі речовини: atracuriumВиробник: Akciju sabiedriba "Kalceks"Не потрібен рецепт
Аналоги Мівацуріум Калцекс в інших країнах
Найкращі аналоги з тією самою діючою речовиною та терапевтичним ефектом.
Аналог Мівацуріум Калцекс у Espanha
Лікарі онлайн щодо Мівацуріум Калцекс
Консультація щодо дозування, побічних ефектів, взаємодій, протипоказань та поновлення рецепта на Мівацуріум Калцекс – за рішенням лікаря та згідно з місцевими правилами.














