

Ваксигрип

Спросите врача о рецепте на Ваксигрип

Инструкция по применению Ваксигрип
ЛИСТОВКА, ПРИЛАГАЕМАЯ К УПАКОВКЕ: ИНФОРМАЦИЯ ДЛЯ ПОЛЬЗОВАТЕЛЯ
Vaxigrip, суспензия для инъекций в шприце-ампуле
Трехвалентная вакцина против гриппа (расщепленный вирион), инактивированная
Необходимо внимательно ознакомиться с содержанием листовки перед применением вакцины, поскольку она содержит важную информацию для взрослого пациента или ребенка.
- Необходимо сохранить эту листовку, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу, фармацевту или медсестре.
- Эту вакцину назначили строго определённому человеку. Ее не следует передавать другим.
- Если у взрослого пациента или ребенка出现ят любые нежелательные реакции, включая любые нежелательные реакции, не указанные в этой листовке, необходимо сообщить об этом врачу, фармацевту или медсестре. См. пункт 4.
Содержание листовки
- 1. Что такое Vaxigrip и для чего она используется
- 2. Важные сведения перед применением вакцины Vaxigrip
- 3. Как применять вакцину Vaxigrip
- 4. Возможные нежелательные реакции
- 5. Как хранить вакцину Vaxigrip
- 6. Содержание упаковки и другие сведения
1. Что такое Vaxigrip и для чего она используется
Vaxigrip является вакциной.
Эта вакцина, вводимая взрослым и детям от 6 месяцев, помогает
защитить от заболевания гриппом.
После введения вакцины Vaxigrip иммунная система (естественная защитная система организма)
производит собственную защиту от заболевания (антитела). Вакцина, введенная во время беременности,
помогает защитить беременных женщин, а также детей от рождения до 6 месяцев,
переносимую защиту от матери к ребенку во время беременности (см. также пункты 2 и 3).
Ни один из компонентов вакцины не может вызвать грипп.
Применение вакцины Vaxigrip должно быть в соответствии с официальными рекомендациями.
Грипп является заболеванием, которое может быстро распространяться и вызывается множеством различных
штаммов вируса, которые могут меняться каждый год. Из-за этой возможной ежегодной смены
циркулирующих штаммов, а также с учетом периода сохранения защиты, обеспечиваемой вакциной, рекомендуется
проводить вакцинацию каждый год. Наибольшая опасность заболевания гриппом возникает во время холодных месяцев между октябрем и марцем. В случае взрослых и детей, которые не были привиты осенью, все еще оправдано провести вакцинацию в период до весны, поскольку до этого времени существует риск заболевания гриппом. Врач сможет порекомендовать лучшее время для вакцинации.
Вакцина Vaxigrip предназначена для защиты взрослых и детей от трех штаммов
вируса, содержащихся в вакцине, через примерно 2-3 недели после вакцинации.
Поскольку инкубационный период для гриппа составляет несколько дней, в случае воздействия взрослого или ребенка
на вирус гриппа непосредственно перед или после вакцинации, все еще возможно заболеть.
Вакцина не защищает от простуды, хотя некоторые ее симптомы похожи на грипп.
2. Важные сведения перед применением вакцины Vaxigrip
Необходимо проинформировать врача или фармацевта, если любое из следующих утверждений относится
к взрослому пациенту или ребенку, которым должна быть введена вакцина Vaxigrip. Если что-либо неясно, необходимо попросить врача или фармацевта объяснить.
Когда не применять вакцину Vaxigrip
- Если у взрослого пациента или ребенка есть аллергия на:
- Активные вещества, или
- Любой из остальных компонентов этой вакцины (перечисленных в пункте 6), или
- Любой компонент, который может присутствовать в очень небольших количествах, такой как остаток яйца (альбумин яичный, белок куринный), неомицин, формальдегид или октил-9.
Предостережения и меры предосторожности
Перед применением вакцины Vaxigrip необходимо поговорить с врачом, фармацевтом или
медсестрой.
Перед вакцинацией необходимо проинформировать врача, если у взрослого пациента или ребенка наблюдаются:
- Ослабление иммунного ответа (вызванный дефицитом иммунитета или приемом препаратов, влияющих на иммунную систему),
- Кровотечения или склонность к образованию синяков. Если у взрослого пациента или ребенка выявлена острая болезнь, протекающая с лихорадкой, вакцинация должна быть отложена до тех пор, пока лихорадка не пройдет. Врач решит, должен ли взрослый пациент или ребенок получить вакцину. Обморок может возникнуть (особенно у подростков) после, или даже до, любого укола. Поэтому необходимо проинформировать врача или медсестру, если пациент или его ребенок испытывал обмороки при предыдущих инъекциях.
Как и в случае с любой вакциной, вакцина Vaxigrip может не обеспечить полную защиту
всем привитым людям.
Не все дети в возрасте до 6 месяцев, родившиеся у вакцинированных во время беременности женщин,
будут защищены.
Дети
Применение вакцины Vaxigrip не рекомендуется у детей в возрасте до 6 месяцев.
Вакцина Vaxigrip и другие препараты
Необходимо сообщить врачу или фармацевту о всех препаратах или вакцинах, принимаемых
взрослым пациентом или ребенком в настоящее время или недавно, а также о препаратах или вакцинах, которые
планируется применять.
- Вакцина Vaxigrip может быть введена одновременно с другими вакцинами, но в разные конечности.
- При применении препаратов или терапии, снижающих иммунитет, таких как кортикостероиды, цитотоксические препараты или радиотерапия, иммунный ответ на вакцинацию может быть ослаблен.
Беременность и кормление грудью
Если пациентка беременна или кормит грудью, предполагает, что может быть беременной, должна
проконсультироваться с врачом или фармацевтом перед применением этой вакцины.
Вакцина Vaxigrip может быть введена во всех периодах беременности.
Вакцина Vaxigrip может быть применена во время кормления грудью.
Врач/фармацевт решает возможность введения вакцины Vaxigrip.
Вождение транспортных средств и управление механизмами
Вакцина Vaxigrip не влияет или оказывает незначительное влияние на способность управлять
транспортными средствами и механизмами.
Вакцина Vaxigrip содержит калий и натрий
Этот препарат содержит менее 1 ммоль калия (39 мг) и менее 1 ммоль натрия (23 мг) на дозу, то есть
препарат считается «свободным от калия» и «свободным от натрия».
3. Как применять вакцину Vaxigrip
Дозировка
Взрослые получают одну дозу 0,5 мл.
Применение у детей и подростков
Дети от 6 месяцев до 17 лет получают одну дозу 0,5 мл.
Детям до 9 лет, которые ранее не были привиты против гриппа, необходимо ввести вторую дозу 0,5 мл через не менее 4 недель.
В случае беременных женщин одна доза 0,5 мл, введенная во время беременности, может защитить ребенка от
рождения до 6 месяцев. Для получения дополнительной информации необходимо обратиться к врачу или фармацевту.
Как вводить вакцину Vaxigrip
Врач или медсестра введет рекомендуемую дозу вакцины в виде инъекции в мышцу или под
кожу.
Применение большей, чем рекомендуемая, дозы вакцины Vaxigrip
В некоторых случаях случайно вводилась большая доза, чем рекомендуемая.
В этих случаях, когда сообщались нежелательные реакции, они были аналогичны тем, которые описаны после
введения рекомендуемой дозы (см. пункт 4).
В случае любых дальнейших сомнений, связанных с применением этой вакцины, необходимо обратиться к врачу или фармацевту.
4. Возможные нежелательные реакции
Как и любой препарат, эта вакцина может вызывать нежелательные реакции, хотя они не возникают у
каждого.
Необходимо немедленно обратиться к врачу или медицинскому работнику, или пойти в ближайшую приемную, если возникает аллергическая реакция.
Аллергические реакции
Могут возникнуть сразу после введения вакцины и могут угрожать жизни.
Симптомы могут включать:
- сыпь, зуд (зуд), трудности с дыханием, одышка, отек (отек) лица, губ, горла или языка, низкое кровяное давление, учащенное сердцебиение и слабый пульс, холодная, влажная кожа, головокружение, слабость или обморок (анafilактическая реакция, ангиоэдем, шок).
Другие симптомы могут включать:
- области зудящей, покрасневшей, отечной (отечной) и треснувшей кожи (атопический дерматит), внезапное покраснение кожи, удары тепла, кровь в белке глаза (гиперемия глаза), покраснение и раздражение глаза (конъюнктивит), раздражение горла, боль в горле, раздражение внутри носа, насморк, чихание, заложенность носа, пазух или горла, онемение или ощущение покалывания во рту (парестезии во рту), сыпь во рту (высыпания на слизистой оболочке рта), астму.
Эти аллергические реакции были зарегистрированы как возникающие не очень часто (могут возникать у до 1 из 100 человек) или редко (могут возникать у до 1 из 1000 человек).Дополнительные нежелательные реакции у взрослых и пожилых людей
Очень часто (могут возникать более чем у 1 из 10 человек):
- головная боль, боль в мышцах, общее плохое самочувствие, боль в месте инъекции.
Часто (могут возникать реже чем у 1 из 10 человек):
- лихорадка, озноб, реакции в месте инъекции: покраснение (гиперемия), индурация, отек.
Не очень часто (могут возникать у до 1 из 100 человек):
- увеличение лимфатических узлов в области шеи, подмышек или паха (лимфаденопатия), необычная слабость, ощущение усталости, сонливость, головокружение, чрезмерное потоотделение, боль в суставах, диарея, ощущение тошноты (тошнота), реакции в месте инъекции: синяки (гематома), зуд, тепло, дискомфорт.
Редко (могут возникать у до 1 из 1000 человек):
- ощущение онемения или покалывания (парестезии), рвота, снижение аппетита, симптомы, подобные гриппу.
- ослабление чувствительности (гипестезия), боль в животе, аллергия в месте инъекции: наблюдалась только у взрослых.
- отслоение кожи в месте инъекции: наблюдалась только у взрослых.
Дополнительные нежелательные реакции, возникающие у детей в возрасте от 3 до 17 лет
Очень часто (могут возникать более чем у 1 из 10 человек):
- головная боль, боль в мышцах, общее плохое самочувствие, озноб, реакции в месте инъекции: боль, покраснение, отек, индурация.
Часто (могут возникать реже чем у 1 из 10 человек):
- лихорадка, синяк (гематома) в месте инъекции. Не очень часто (могут возникать у до 1 из 100 человек):
- ощущение усталости, головокружение, диарея, реакции в месте инъекции: зуд, тепло.
- увеличение лимфатических узлов в области шеи, подмышек или паха, боль в животе, рвота, беспокойство, капризность, боль в суставах, плач: наблюдалась только у детей в возрасте от 3 до 8 лет.
- снижение количества определенных типов клеток крови, называемых тромбоцитами; их небольшое количество может вызывать чрезмерное образование синяков или кровотечение (тромбоцитопения): наблюдалась только у одного ребенка в возрасте 3 лет.
- необычная слабость, дискомфорт в месте инъекции: наблюдалась только у детей в возрасте от 9 до 17 лет.
Дополнительные нежелательные реакции, зарегистрированные у детей от 6 месяцев до 35 месяцев
Очень часто (могут возникать более чем у 1 из 10 человек):
- раздражительность, рвота, боль в мышцах, общее плохое самочувствие, лихорадка, снижение аппетита, реакции в месте инъекции: болезненность, покраснение.
- необычный плач, сонливость: наблюдалась только у детей до 24 месяцев.
- головная боль: наблюдалась только у детей после 24 месяцев.
Часто (могут возникать реже чем у 1 из 10 человек):
- диарея, реакции в месте инъекции: индурация, гематома, отек.
- озноб: наблюдалась только у детей после 24 месяцев. Редко (могут возникать у до 1 из 1000 человек):
- симптомы, подобные гриппу, реакции в месте инъекции: зуд, сыпь. У детей в возрасте от 6 месяцев до 8 лет, получающих 2 дозы, нежелательные реакции после первой и после второй дозы подобны. Меньше нежелательных реакций может возникнуть после введения второй дозы у детей в возрасте от 6 месяцев до 35 месяцев. Большинство нежелательных реакций возникали обычно в течение 3 дней после вакцинации и проходили без лечения в течение 1-3 дней после возникновения. Степень большинства этих нежелательных реакций была легкой или умеренной.
Частота возникновения следующих нежелательных реакций неизвестна (не может быть определена
на основе доступных данных) в целой популяции, за исключением популяции, для которой указанная нежелательная реакция
упоминается выше:- увеличение лимфатических узлов в области шеи, подмышек или паха.
- ощущение онемения или покалывания (парестезии), боль, ощущаемая вдоль нервов (нейралгия), приступы ( судороги), неврологические расстройства, которые могут вызывать жесткость шеи, дезориентацию, онемение, боль и слабость конечностей, потерю равновесия, потерю рефлексов, паралич части или всего тела (воспаление мозга и спинного мозга, воспаление нерва, синдром Гийена-Барре).
- воспаление кровеносных сосудов, которое может привести к кожным высыпаниям и в очень редких случаях к временным нарушениям функции почек.
- временное снижение количества определенных типов клеток крови, называемых тромбоцитами; их небольшое количество может вызывать чрезмерное образование синяков или кровотечение (временная тромбоцитопения).
Сообщение о нежелательных реакциях
Если у взрослого пациента или ребенка возникают любые нежелательные реакции, включая любые нежелательные реакции, не указанные в листовке, необходимо сообщить об этом врачу, фармацевту или медсестре. Нежелательные реакции можно сообщать напрямую в Департамент мониторинга нежелательных реакций лекарственных препаратов Управления по регистрации лекарственных препаратов, медицинских изделий и биоцидных препаратов
ул. Аллея Ерозолимских, 181С
02-222 Варшава
Тел.: + 48 22 49 21 301
Факс: + 48 22 49 21 309
Сайт: https://smz.ezdrowie.gov.pl
Нежелательные реакции также можно сообщать ответственному лицу.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности применения препарата.5. Как хранить вакцину Vaxigrip
Вакцину необходимо хранить в месте, недоступном для детей.
Не применять эту вакцину после истечения срока годности, указанного на этикетке и упаковке
после «Срок годности (EXP)». Срок годности обозначает последний день указанного месяца.
Хранить в холодильнике (2 ° C–8 ° C). Не замораживать. Хранить шприц-ампулу
в наружной упаковке для защиты от света.
Лекарства не следует выбрасывать в канализацию или домашние мусорные контейнеры. Необходимо спросить
фармацевта, как утилизировать лекарства, которые больше не используются. Такое поведение поможет защитить
окружающую среду.6. Содержание упаковки и другие сведения
Что содержит вакцина Vaxigrip
Активными веществами являются: Вирус гриппа (инактивированный, расщепленный) следующих штаммов*:
A/Victoria/4897/2022 (H1N1)pdm09-подобный штамм (A/Victoria/4897/2022, IVR-238)
............................................................................................................. 15 микрограммов HA**
A/Croatia/10136RV/2023 (H3N2)-podobный штамм (A/Croatia/10136RV/2023, X-425A)
............................................................................................................. 15 микрограммов HA**
B/Austria/1359417/2021-подобный штамм (B/Michigan/01/2021, тип дикого)
............................................................................................................. 15 микрограммов HA**
в дозе 0,5 мл
*выращенный в куриных эмбрионах, полученных из здоровых стад
**гемагглютинин
Вакцина соответствует рекомендациям Всемирной организации здравоохранения (World Health Organization, WHO) для северного полушария и рекомендациям Европейского Союза на сезон 2025/2026.
Остальные компоненты: буферный раствор, содержащий хлорид натрия, хлорид калия, дигидрофосфат натрия, диводородфосфат калия, вода для инъекций.
Некоторые компоненты, такие как яйца (альбумин яичный, белок куринный), неомицин, формальдегид или октил-9, могут присутствовать в очень небольших количествах (см. пункт 2).Как выглядит вакцина Vaxigrip и что содержит упаковка
После легкого встряхивания вакцина представляет собой бесцветную, опалесцирующую жидкость.
Вакцина Vaxigrip является суспензией для инъекций в шприце-ампуле по 0,5 мл, с приложенной
иглой, с отдельной иглой или без иглы или с отдельной иглой в защитной оболочке, в упаковке по 1 или
10, все в картонной коробке. Не все размеры упаковок могут находиться в обороте.Ответственное лицо и производитель
Ответственное лицо:
Sanofi Winthrop Industrie
82 avenue Raspail
94250 Gentilly, Франция
Производитель:
Sanofi Winthrop Industrie, 1541 avenue Marcel Mérieux, 69280 Marcy l'Etoile, Франция
Sanofi Winthrop Industrie, Voie de l’Institut - Parc Industriel d'Incarville, B.P. 101, 27100 Val de
Reuil, Франция
Sanofi-Aventis Zrt., Budynek Dc5, Campona Utca 1, Budapest XXII,1225, ВенгрияЭтот лекарственный препарат разрешен к обращению в странах-членах Европейского
Экономического пространства под следующими названиями:
Страна-член Название Австрия, Бельгия, Болгария, Хорватия, Чехия, Дания, Эстония, Финляндия, Франция, Испания, Нидерланды, Ирландия, Исландия, Литва, Люксембург, Латвия, Мальта, Германия, Норвегия, Польша, Португалия, Румыния, Словакия, Словения, Швеция, Венгрия, Италия Vaxigrip Кипр, Греция Vaxigrip TIV Дата последнего обновления листовки:июнь 2025
Другие источники информации
Текущие утвержденные сведения о этом продукте доступны <после сканирования смартфоном QR-кода, указанного на картонной коробке или> по следующему URL-адресу: https://vaxigrip-nh.info.sanofi
---------------------------------------------------------------------------------------------------------------------Сведения, предназначенные только для медицинского персонала:
Как и при всех вакцинах, вводимых в виде инъекций, необходимо обеспечить надлежащее лечение и медицинский надзор на случай возникновения анафилактической реакции после введения вакцины.
Перед введением вакцину необходимо привести к комнатной температуре.
Встряхнуть перед использованием. Проверить визуально перед введением.
Вакцину не следует применять в случае присутствия твердых частиц в суспензии.
Вакцину не следует смешивать с другими лекарственными препаратами в одном шприце.
Вакцину не следует вводить непосредственно в кровеносные сосуды.
См. также пункт 3. Как применять вакцину Vaxigrip<Подготовка к введению Инструкция по использованию иглы с защитной оболочкой с шприцем-ампулой с концом Luer Замок: 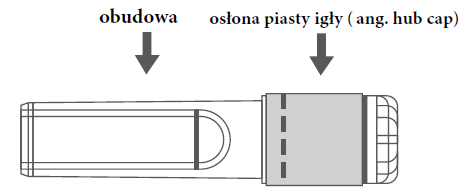
Рисунок А: Игла с защитной оболочкой (в корпусе) Рисунок Б: Элементы защитной оболочки иглы (приготовлены для использования) 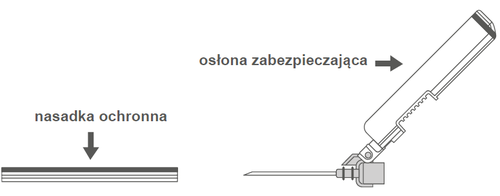
Шаг 1: Чтобы прикрепить иглу к шприцу, необходимо снять защитную оболочку иглы (анг. hub cap), чтобы открыть корпус иглы, и осторожно вкрутить иглу в адаптер Luer Lock шприца до ощущения легкого сопротивления. Шаг 2: Снять корпус иглы. Игла защищена защитной оболочкой и защитным наконечником. 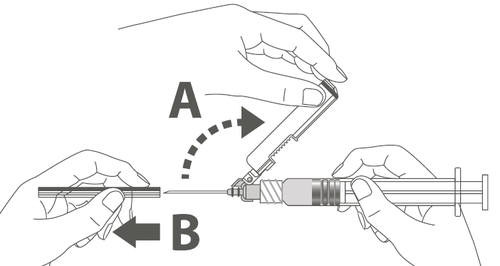
Шаг 3: А: Отодвинуть защитную оболочку от иглы в направлении корпуса шприца под указанным углом. Б: Снять защитный наконечник. 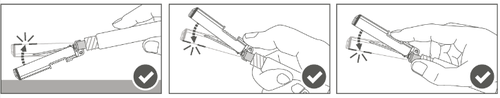
Шаг 4: После инъекции необходимо заблокировать (активировать) защитную оболочку, используя одну из трех (3) представленных техник обращения одной рукой: активация на плоской поверхности, большим пальцем или указательным пальцем. Примечание: Активация подтверждается слышимым и (или) ощутимым «щелчком». Шаг 5: Проверить визуально работу защитной оболочки. Защитная оболочка должна быть полностью заблокирована (активирована), как показано на рисунке С. Рисунок D показывает, что защитная оболочка НЕ полностью заблокирована (не активирована). 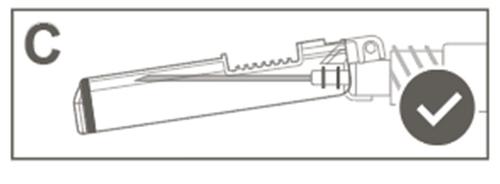
Предупреждение: Не следует пытаться разблокировать (деактивировать) защитное устройство путем выталкивания иглы из защитной оболочки. 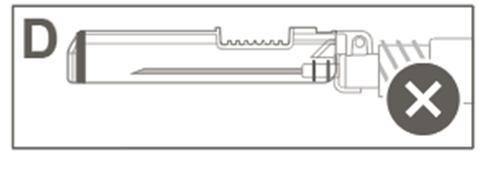
Все неиспользованные остатки лекарственного препарата или его отходы необходимо утилизировать в соответствии с местными правилами.
- Страна регистрации
- Активное вещество
- Требуется рецептДа
- ИмпортерSanofi Winthrop Industrie Sanofi Winthrop Industrie Sanofi-Aventis Zrt.
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги ВаксигрипФорма выпуска: Суспензия, 60 мкг HA/штамм, 1 доза (0,7 мл)Активное вещество: influenza, inactivated, split virus or surface antigenТребуется рецептФорма выпуска: Суспензия, 60 мкг HA/штамм, 1 доза (0,5 мл)Активное вещество: influenza, inactivated, split virus or surface antigenТребуется рецептФорма выпуска: Суспензия, 1 доза (0,5 мл)Активное вещество: influenza, inactivated, split virus or surface antigenТребуется рецепт
Аналоги Ваксигрип в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Ваксигрип в Испания
Аналог Ваксигрип в Украина
Врачи онлайн по Ваксигрип
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Ваксигрип – по решению врача и с учетом местных правил.














