
Антитгромбин Иии Нф Такеда

Спросите врача о рецепте на Антитгромбин Иии Нф Такеда

Инструкция по применению Антитгромбин Иии Нф Такеда
Инструкция, прилагаемая к упаковке: информация для пользователя
АнтиТромбин III NF Takeda, 50 МЕ/мл, порошок и растворитель для приготовления раствора для
инфузии
человеческий антиТромбин III, полученный из плазмы крови
Необходимо внимательно ознакомиться с содержанием инструкции перед использованием препарата, поскольку она содержит важную информацию для пациента.
- Необходимо сохранить эту инструкцию, чтобы в случае необходимости можно было ее повторно прочитать.
- В случае любых сомнений необходимо обратиться к врачу или фармацевту.
- Если у пациента出现ят любые нежелательные реакции, включая все нежелательные реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу или фармацевту. См. пункт 4.
Содержание инструкции
- 1. Что такое препарат АнтиТромбин III NF Takeda и для чего он используется
- 2. Важные сведения перед использованием АнтиТромбина III NF Takeda
- 3. Как использовать АнтиТромбин III NF Takeda
- 4. Возможные нежелательные реакции
- 5. Как хранить АнтиТромбин III NF Takeda
- 6. Содержание упаковки и другие сведения
1. Что такое препарат АнтиТромбин III NF Takeda и для чего он используется
АнтиТромбин III NF Takeda выпускается в виде порошка или порошка светло-желтого до светло-зеленого цвета с прилагаемым растворителем для приготовления раствора для инфузии.
АнтиТромбин III NF Takeda доступен в упаковках, содержащих:
- 500 МЕ антиТромбина III и 10 мл растворителя или
- 1000 МЕ антиТромбина III и 20 мл растворителя
АнтиТромбин III NF Takeda относится к фармакотерапевтической группе, называемой антикоагулянтами.
АнтиТромбин III NF Takeda используется для лечения врожденного или приобретенного дефицита антиТромбина III, при котором дефицит может возникать при различных клинических состояниях.
2. Важные сведения перед использованием АнтиТромбина III NF Takeda
Когда не использовать АнтиТромбин III NF Takeda
- если пациент имеет аллергическую реакцию на антиТромбин III или любой другой компонент этого препарата (перечисленный в пункте 6)
- у пациентов с тромбоцитопенией, индуцированной гепарином (т.е. снижением количества тромбоцитов) в анамнезе
Предостережения и меры предосторожности
Идентифицируемость
Для улучшения идентифицируемости биологических лекарственных препаратов необходимо четко записать название и номер серии вводимого препарата.
- Необходимо проинформировать лечащего врача, если出现ят первые симптомы аллергической реакции (например, крапивница, включая генерализованную, чувство сдавления в груди, свистящее дыхание, снижение артериального давления и анафилактический шок). Тяжелые симптомы могут потребовать введения экстренной помощи.
- Необходимо проинформировать врача, если пациент принимает или принимал recently препараты, содержащие гепарин (например, для лечения тромбоза), поскольку действие антиТромбина усиливается гепарином.
- АнтиТромбин III NF Takeda производится из человеческой плазмы крови. При введении препаратов, полученных из человеческой крови или плазмы крови, нельзя полностью исключить передачу инфекционных агентов. Это относится также к патогенам, которые еще не известны. Однако риск передачи инфекционных агентов снижается за счет тщательного отбора доноров и плазмы крови, а также процедур инактивации/удаления вирусов.
Дети
Не использовать этот препарат у детей в возрасте до 6 лет, поскольку не определена безопасность и эффективность его использования в этой возрастной группе.
АнтиТромбин III NF Takeda и другие препараты
Необходимо сообщить врачу о всех препаратах, которые пациент принимает в настоящее время или принимал recently, а также о препаратах, которые пациент планирует принимать.
Необходимо сообщить врачу о препаратах, которые пациент принимает в настоящее время или принимал recently, содержащих гепарин (например, для лечения тромбоза), поскольку действие антиТромбина усиливается гепарином.
Беременность, грудное вскармливание и влияние на фертильность
Необходимо сообщить врачу, если пациентка беременна или кормит грудью. Врач решит, можно ли использовать АнтиТромбин III NF Takeda во время беременности или грудного вскармливания.
Если пациентка беременна или кормит грудью, предполагает, что может быть беременна или планирует иметь ребенка, она должна проконсультироваться с врачом или фармацевтом перед использованием этого препарата.
Вождение транспортных средств и эксплуатация машин
Хотя не наблюдалось влияния на способность управлять транспортными средствами и эксплуатировать машины, такое влияние не может быть исключено. Поэтому рекомендуется, чтобы пациент не управлял транспортными средствами и не эксплуатировал машины без предварительной консультации с врачом.
АнтиТромбин III NF Takeda содержит натрий
500 МЕ/10 мл
Препарат содержит 37,7 мг натрия (основного компонента поваренной соли) в каждой ампуле. Это соответствует 1,9% рекомендуемой ВОЗ максимальной суточной дозы натрия для взрослых.
1000 МЕ/20 мл
Препарат содержит 75,5 мг натрия (основного компонента поваренной соли) в каждой ампуле. Это соответствует 3,8% рекомендуемой ВОЗ максимальной суточной дозы натрия для взрослых.
3. Как использовать АнтиТромбин III NF Takeda
АнтиТромбин III NF Takeda будет вводиться только под медицинским наблюдением. Доза будет зависеть от массы тела и индивидуальных потребностей пациента. Лечащий врач определит дозу, которая должна быть введена. АнтиТромбин III NF Takeda будет вводиться в виде инфузии в вену.
Использование большей, чем рекомендуемая, дозы АнтиТромбина III NF Takeda
Не сообщалось о симптомах передозировки антиТромбина.
Пропуск использования АнтиТромбина III NF Takeda
Не применимо.
Прекращение использования АнтиТромбина III NF Takeda
Не применимо.
4. Возможные нежелательные реакции
Как и любой препарат, этот препарат может вызывать нежелательные реакции, хотя они не возникают у каждого пациента.
Нежелательные реакции, наблюдаемые после введения АнтиТромбина III NF Takeda, включают повышенную чувствительность, анафилактическую реакцию, дрожь и приливы жара.
- Повышенная чувствительность или аллергические реакции, такие как: ангиоэдем, жжение и покалывание в месте введения инфузии, озноб, приливы жара, генерализованная крапивница, головная боль, зудящая сыпь, снижение артериального давления, сонливость, тошнота, тревога, учащенное сердцебиение, чувство сдавления в груди, онемение, рвота, свистящее дыхание, были отмечены редко, но могут в некоторых случаях перейти в тяжелую анафилактическую реакцию (включая анафилактический шок).
- В редких случаях наблюдалась лихорадка.
- В редких случаях может возникнуть тромбоцитопения (т.е. снижение количества тромбоцитов), которая является медиатором, индуцированным гепарином. Наблюдалось снижение количества тромбоцитов ниже 100 000/μл или снижение количества тромбоцитов на 50%.
Если любой из симптомов нежелательной реакции ухудшится или если возникнут какие-либо симптомы нежелательной реакции, не указанные в этой инструкции, необходимо сообщить об этом врачу.
Сообщение о нежелательных реакциях
Если возникнут какие-либо симптомы нежелательной реакции, включая все симптомы нежелательной реакции, не указанные в инструкции, необходимо сообщить об этом врачу или фармацевту. Нежелательные реакции можно сообщать trực tiếp в Департамент мониторинга нежелательных реакций лекарственных препаратов Управления регистрации лекарственных препаратов, медицинских изделий и биоцидных продуктов:
Ал. Ерозолимских 181С
02-222 Варшава
Тел.: + 48 22 49 21 301
Факс: + 48 22 49 21 309
Сайт: https://smz.ezdrowie.gov.pl
Нежелательные реакции можно сообщать также ответственному лицу.
Благодаря сообщению о нежелательных реакциях можно будет собрать больше информации о безопасности использования препарата.
5. Как хранить АнтиТромбин III NF Takeda
Препарат хранить в месте, недоступном для детей.
Хранить в холодильнике (2°C до 8°C). Не замораживать.
Хранить в оригинальной упаковке для защиты от света.
Не использовать этот препарат после истечения срока годности, указанного на этикетке и упаковке после EXP. Срок годности указывает последний день указанного месяца.
Не использовать этот препарат, если раствор мутный или содержит осадки.
Препараты не следует выбрасывать в канализацию или домашние контейнеры для мусора. Необходимо спросить у фармацевта, как утилизировать препараты, которые больше не используются. Такое поведение поможет защитить окружающую среду.
6. Содержание упаковки и другие сведения
Что содержит АнтиТромбин III NF Takeda
- Активным веществом препарата является человеческий антиТромбин III, полученный из плазмы крови
- Другими компонентами являются глюкоза, хлорид натрия, цитрат натрия двузамещенный и трис(гидроксиметил)аминометан
Как выглядит АнтиТромбин III NF Takeda и что содержит упаковка
АнтиТромбин III NF Takeda выпускается в виде порошка для приготовления раствора для инфузии, содержащего номинально 500 МЕ (или 1000 МЕ) антиТромбина, полученного из человеческой плазмы крови, в ампуле и растворителе.
500 МЕ/10 мл
После реконституции в 10 мл стерильной воды для инъекций препарат содержит примерно 50 МЕ/мл (500 МЕ/10 мл) человеческого антиТромбина III из плазмы крови.
1000 МЕ/20 мл
После реконституции в 20 мл стерильной воды для инъекций препарат содержит примерно 50 МЕ/мл (1000 МЕ/20 мл) человеческого антиТромбина III из плазмы крови.
АнтиТромбин III NF Takeda является лиофилизированным светло-желтым или светло-зеленым порошком.
Каждая упаковка также содержит:
- 1 переносяющую иглу
- 1 иглу с фильтром
- 1 иглу для удаления воздуха
- 1 иглу для одноразового использования
- 1 набор для инфузии
Ответственное лицо и производитель
Ответственное лицо
Takeda Pharma Sp. z o.o.
ул. Проста 68
00-838 Варшава
Производитель
Takeda Manufacturing Austria AG
Industriestrasse 67
1221 Вена, Австрия
Дата последнего обновления инструкции: ------------------------------------------------------------------------------------------------------------------------
Информация, предназначенная только для медицинского персонала:
Дозировка и способ введения
Лечение должно проводиться под наблюдением врача с опытом лечения пациентов с дефицитом антиТромбина.
Дозировка
При врожденном дефиците антиТромбина доза должна быть индивидуально подобрана для каждого пациента и учитывать семейный анамнез в отношении тромбоэмболических осложнений, текущие факторы риска и результаты лабораторных исследований.
Дозировка и продолжительность терапии замены при приобретенном дефиците зависят от уровня антиТромбина в плазме крови, наличия симптомов повышенного потребления, причины расстройства и тяжести клинического состояния пациента. В каждом случае размер дозы и частота ее введения должны быть определены на основе лабораторных результатов и оценки клинического состояния пациента и реакции на лечение.
Количество вводимых единиц антиТромбина выражается в международных единицах (МЕ), которые относятся к текущему стандарту ВОЗ для антиТромбина. Активность антиТромбина в плазме крови выражается в процентах (относительно нормальной человеческой плазмы крови) или в международных единицах (относящихся к Международному стандарту антиТромбина в плазме крови).
Активность одной международной единицы (МЕ) антиТромбина соответствует количеству антиТромбина в 1 мл нормальной человеческой плазмы крови. Расчет необходимой дозы антиТромбина основан на данных, что введение 1 МЕ антиТромбина на килограмм массы тела вызывает увеличение активности антиТромбина в плазме крови на примерно 2%.
Первоначальная доза рассчитывается по следующей формуле:
Необходимое количество единиц = масса тела (кг) x (Целевой уровень – текущая активность антиТромбина [%]) x 0,5
Первоначальный целевой уровень антиТромбина в плазме крови зависит от оценки клинического состояния пациента.
После установления показаний для замены антиТромбина одна доза должна обеспечить достижение целевого уровня антиТромбина в плазме крови и затем поддержание его нормального уровня. Размер дозы должен быть определен и контролироваться на основе измерений активности антиТромбина, которые должны проводиться не менее двух раз в день до стабилизации состояния пациента, а затем один раз в день, желательно незадолго до следующей инфузии. Коррекция дозы должна учитывать как повышенное потребление антиТромбина, так и лабораторные результаты и клинические симптомы. Во время лечения активность антиТромбина должна поддерживаться на уровне выше 80%, если клинические показания не требуют другого, эффективного уровня.
Средняя первоначальная доза при врожденном дефиците составляет 30-50 МЕ/кг массы тела.
Затем доза и частота введения, а также продолжительность лечения должны быть скорректированы в зависимости от лабораторных результатов и клинического состояния пациента.
Дети и подростки
Не определена безопасность и эффективность использования препарата АнтиТромбин III NF Takeda у детей в возрасте до 6 лет. Поэтому не рекомендуется использовать препарат в этой возрастной группе.
Способ введения
Вводить внутривенно. Максимальная скорость инфузии составляет 5 мл/мин.
Специальные меры предосторожности при удалении и подготовке препарата к использованию
АнтиТромбин III NF Takeda должен быть реконституирован непосредственно перед введением, поскольку продукт не содержит консервантов.
Необходимо использовать только прилагаемый набор для инфузии. Во время подготовки раствора необходимо соблюдать асептические техники. Готовый раствор должен быть использован немедленно после подготовки.
Перед введением необходимо проверить, что реконституированный препарат не содержит нерастворимых частиц и не изменил цвет. Раствор должен быть прозрачным или слегка опалесцирующим. Не использовать растворы, которые являются мутными или содержат осадки.
Не хранить в холодильнике после реконституции.
Приготовление раствора:
- 1. Довести закрытую ампулу, содержащую растворитель (воду для инъекций), до комнатной температуры (макс. 37°C).
- 2. Снять защитные колпачки с ампул, содержащих порошок и растворитель (рис. А), и продезинфицировать резиновые пробки обеих ампул.
- 3. Снять защитный колпачок с одного конца переносящей иглы, повернув и потянув (рис. Б). Вставить открытый конец иглы в резиновую пробку ампулы с растворителем (рис. В).
- 4. Снять защитный колпачок с другого конца переносящей иглы, обращая внимание на то, чтобы не прикоснуться к открытой части.
- 5. Перевернуть ампулу с растворителем вверх дном и вставить свободный конец переносящей иглы в резиновую пробку ампулы с порошком (рис. Д). Растворитель будет всосан в ампулу с порошком на основе вакуума.
- 6. Отделить обе ампулы, вынув иглу из ампулы с порошком (рис. Е). Аккуратно встряхнуть ампулу, чтобы ускорить растворение.
- 7. После полного растворения порошка вставить прилагаемую иглу для удаления воздуха (рис. Ф), и образовавшаяся пена осядет. Удалить иглу для удаления воздуха.
Введение:
- 8. Удалить защитный колпачок с прилагаемой иглы с фильтром, повернув и потянув, и надеть ее на стерильную одноразовую шприц. Взять раствор в шприц (рис. Г).
- 9. Отделить иглу с фильтром от шприца и, надев прилагаемую иглу для одноразового использования (или прилагаемый набор для инфузии), медленно ввести раствор внутривенно (максимальная скорость введения 5 мл/мин).
Если препарат не был отфильтрован во время растворения, необходимо использовать одноразовый набор для инфузии с соответствующим фильтром (максимальная скорость инфузии: 5 мл/мин).
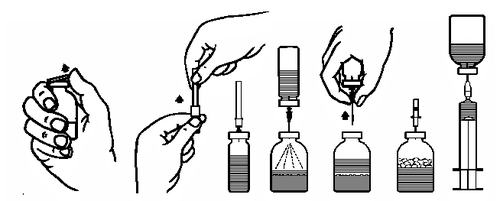
рис. А рис. Б
рис. В рис. Г
рис. Д рис. Е рис. Ж
Все неиспользованные остатки препарата или его отходы должны быть удалены в соответствии с местными правилами.
Фармацевтическая несовместимость
Препарат не должен смешиваться с другими препаратами.
Специальные предостережения и меры предосторожности при использовании
Как и в случае с другими препаратами, содержащими белки, используемыми для внутривенных инфузий, введение АнтиТромбина III NF Takeda может вызвать аллергические реакции.
Аллергические реакции и анафилактические реакции были зарегистрированы после введения препарата АнтиТромбин III NF Takeda. В некоторых случаях они могут перейти в тяжелую анафилактическую реакцию (включая анафилактический шок).
Во время инфузии пациенты должны быть тщательно наблюдаемы и внимательно отслеживаться на предмет возникновения любых нежелательных реакций. Необходимо проинформировать пациента о ранних симптомах аллергической реакции, таких как зудящая сыпь, генерализованная крапивница, чувство сдавления в груди, свистящее дыхание, снижение артериального давления и анафилактический шок. Если эти симптомы возникают после введения препарата, пациент должен обратиться к лечащему врачу.
В случае анафилактического шока необходимо применить стандартное лечение.
Takeda является зарегистрированным товарным знаком Takeda Pharmaceutical Company Limited.
- Страна регистрации
- Активное вещество
- Требуется рецептНет
- Производитель
- ИмпортерTakeda Manufacturing Austria AG
- Информация носит справочный характер и не является медицинской рекомендацией. Перед приемом любых препаратов проконсультируйтесь с врачом. Oladoctor не несет ответственности за медицинские решения, принятые на основе этого контента.
- Аналоги Антитгромбин Иии Нф ТакедаФорма выпуска: Порошок, 500 МЕАктивное вещество: Антитромбин IIIПроизводитель: Instituto Grifols S.A.Не требуется рецептФорма выпуска: Порошок, 1000 МЕАктивное вещество: Антитромбин IIIПроизводитель: Instituto Grifols S.A.Не требуется рецептФорма выпуска: Порошок, 50 МЕ/млАктивное вещество: Антитромбин IIIПроизводитель: Takeda Manufacturing Austria AGНе требуется рецепт
Аналоги Антитгромбин Иии Нф Такеда в других странах
Лучшие аналоги с тем же действующим веществом и терапевтическим эффектом.
Аналог Антитгромбин Иии Нф Такеда в Украина
Аналог Антитгромбин Иии Нф Такеда в Испания
Врачи онлайн по Антитгромбин Иии Нф Такеда
Консультация по дозировке, побочным эффектам, взаимодействиям, противопоказаниям и продлению рецепта на Антитгромбин Иии Нф Такеда – по решению врача и с учетом местных правил.














