

TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS

Pergunte a um médico sobre a prescrição de TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS

Como usar TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS
Introdução
Prospecto: informação para o utilizador
Toshedra 35 mg Xarope em sobres
Extracto seco de Hedera helix L. (hiedra)
Leia todo o prospecto detenidamente antes de começar a tomar este medicamento porque contém informações importantes para si.
Siga exactamente as instruções de administração do medicamento contidas neste prospecto ou as indicadas pelo seu médico ou farmacêutico.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se necessitar de conselho ou mais informações, consulte o seu farmacêutico.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
- Deve consultar um médico se piorar ou se não melhorar após 7 dias.
Conteúdo do prospecto
- O que é Toshedra e para que é utilizado
- O que necessita de saber antes de começar a tomar Toshedra
- Como tomar Toshedra
- Possíveis efeitos adversos
- Conservação de Toshedra
- Conteúdo do envase e informação adicional
1. O que é Toshedra e para que é utilizado
Toshedra é um expectorante.
Toshedra é um medicamento à base de plantas utilizado como expectorante para a tos produtiva que acompanha afecções bronquiais benignas. Facilita a eliminação da mucosidade.
Toshedra está indicado em adultos, adolescentes e crianças maiores de 6 anos.
2. O que necessita de saber antes de começar a tomar Toshedra
Não tome Toshedra:
- Se é alérgico à hiedra (Hedera helix L.), a plantas da família das Araliáceas ou a algum dos outros componentes deste medicamento (incluídos na secção 6).
- Não administrar a crianças menores de 2 anos, pois existe o risco de que se agravem os sintomas respiratórios.
Advertências e precauções:
Consulte o seu médico ou farmacêutico antes de começar a tomar Toshedra.
Deve consultar com o médico ou farmacêutico nos casos de dispnéia (dificuldade para respirar), febre ou escarros purulentos.
Não se recomenda o uso concomitante com outros antitussígenos como a codeína ou dextrometorfano sem prévia consulta médica.
Recomenda-se precaução em pacientes com gastrite ou úlcera gástrica.
Este medicamento não deve ser administrado a crianças de 2 a 5 anos, pois não pode ser dosificado adequadamente; existem outras formulações mais adequadas para este grupo de idade.
Em caso de agravamento dos sintomas ou se não se produzir melhoria após 7 dias de iniciar o tratamento, este deve ser interrompido e deve-se consultar com o médico.
Toma de Toshedra com outros medicamentos:
Informa ao seu médico ou farmacêutico se está a tomar, tomou recentemente ou pudesse ter que tomar qualquer outro medicamento.
Gravidez, lactação e fertilidade:
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
Gravidez:
Não há estudos adequados e bem controlados em mulheres grávidas, pelo que não se recomenda a sua administração.
Lactação:
Não existe informação do passo dos componentes deste medicamento para o leite materno, pelo que não se recomenda a sua administração a mulheres durante o período de lactação.
Fertilidade:
Não existem dados disponíveis sobre fertilidade.
Consulte o seu médico ou farmacêutico antes de utilizar qualquer medicamento.
Condução e uso de máquinas
Não se realizaram estudos dos efeitos sobre a capacidade para conduzir e utilizar máquinas.
Toshedra contém sorbitol.
Este medicamento contém 1,925 mg de sorbitol em cada sobre de 5 ml (385 mg por cada ml).
O sorbitol é uma fonte de frutose. Se o seu médico lhe indicou que você (ou o seu filho) padece de uma intolerância a certos açúcares, ou lhe foi diagnosticada intolerância hereditária à frutose (IHF), uma doença genética rara, na qual o paciente não pode descompor a frutose, consulte você (ou o seu filho) com o seu médico antes de tomar este medicamento.
O sorbitol pode provocar malestar gastrointestinal e um ligeiro efeito laxante.
3. Como tomar Toshedra
Siga exactamente as instruções de administração deste medicamento contidas neste prospecto ou as indicadas pelo seu médico ou farmacêutico. Em caso de dúvida, pergunte ao seu médico ou farmacêutico.
A dose recomendada é:
- Adultos e adolescentes maiores de 12 anos: 5 ml de xarope (1 sobre), 3 vezes ao dia, (equivalente a 105 mg diários de extracto seco de folhas de hiedra).
- Crianças entre 6 e 12 anos de idade:5 ml de xarope (1 sobre), 2 vezes ao dia, (equivalente a 70 mg diários de extracto seco de folhas de hiedra).
Se estima que a acção de Toshedra é demasiado forte ou débil, comunique-o ao seu médico ou farmacêutico.
Toshedra é tomado por via oral.
Para mais detalhes do uso dos sobres, siga os diagramas seguintes:
Pressione suavemente o sobre antes de usá-lo, como se mostra.
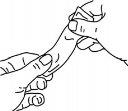
Segure firmemente o sobre e rasgue o sobre por onde indicam as riscas.
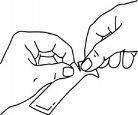
Engula o medicamento, apertando o sobre até que fique vazio.
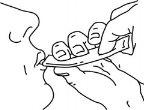
Deve consultar um médico se piorar ou não melhorar após uma semana de tratamento.
Se tomar mais Toshedra do que deve
No caso de que se tenha tomado mais Toshedra do que devia ou em caso de sobredose ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone 915 620 420, indicando o medicamento e a quantidade ingerida.
Não exceda a dose diária recomendada. A ingestão de quantidades significativamente mais altas (mais de três vezes a dose diária) pode provocar náuseas, vómitos e diarreia.
Neste caso, deve consultar o seu médico.
Se esquecer de tomar Toshedra:
Não tome uma dose dupla para compensar a dose esquecida.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora não todas as pessoas os sofram.
Frequentes (podem afetar entre 1 e 10 de cada 100 pacientes): foram notificadas reações do sistema gastrointestinal como náuseas, vómitos ou diarreia.
Pouco frequentes (podem afetar entre 1 e 10 de cada 1.000 pacientes): foram notificadas reações alérgicas como urticária, erupções cutâneas, dificuldade para respirar (dispnéia).
Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto.
Se notar sintomas de alergia (hipersensibilidade), interrompa a tomada de Toshedra.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Toshedra
Mantenha este medicamento fora da vista e do alcance das crianças.
Não requer condições especiais de conservação.
Não utilize este medicamento após a data de caducidade que aparece no envase, após “CAD”. A data de caducidade é o último dia do mês que se indica.
Os medicamentos não devem ser deitados fora pelos desgotos nem para o lixo. Deposite os envases e os medicamentos que não necessita no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não necessita. Deste modo, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Toshedra 35 mg xarope em sobres:
O princípio ativo é: extracto seco de folha de Hedera helix. 5 ml de Toshedra contêm 35 mg de extracto seco de folha de Hedera helix L. (hiedra) (4-8:1), dissolvente de extracção: etanol 30% (m/m). Os outros componentes são: água purificada, sorbato de potássio, ácido cítrico, sorbitol líquido não cristalizável (E-420), goma xantana e essência de cereja.
Aspecto do produto e conteúdo do envase:
Toshedra 35 mg xarope apresenta-se em sobres unidose de fácil abertura, de 5 ml cada um, formados por uma lâmina complexa de alumínio (PET/Alu/PE/PET/PE).
Envase com 20 sobres.
Titular da autorização de comercialização e responsável pela fabricação:
Kern Pharma, S.L.
Vênus, 72 – Pol. Ind. Colón II
08228 Terrassa – Barcelona
Espanha
Data da última revisão deste prospecto: Novembro 2023
A informação detalhada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
- País de registo
- Substância ativa
- Requer receita médicaNão
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉSForma farmacêutica: SOLUÇÃO/SUSPENSÃO ORAL, 7 mg/mlSubstância ativa: Hederae helicis foliumFabricante: Engelhard Arzneimittel Gmbh & Co. KgNão requer receita médicaForma farmacêutica: SOLUÇÃO/SUSPENSÃO ORAL, 35 mgSubstância ativa: Hederae helicis foliumFabricante: Adventia Pharma S.L.Não requer receita médicaForma farmacêutica: SOLUÇÃO/SUSPENSÃO ORAL, 7 mg/mlSubstância ativa: Hederae helicis foliumFabricante: Adventia Pharma S.L.Não requer receita médica
Alternativas a TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS em Poland
Alternativa a TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS em Ukraine
Médicos online para TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de TOSHEDRA 35 MG PÓ PARA SOLUÇÃO ORAL EM SACHÉS – sujeita a avaliação médica e regras locais.














