
SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO

Pergunte a um médico sobre a prescrição de SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO

Como usar SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO
Introdução
Prospecto: informação para o utilizador
SmofKabiven extra Nitrogénio sem eletrólitos emulsão para perfusão
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é SmofKabiven extra Nitrogénio sem eletrólitos e para que é utilizado
- O que precisa saber antes de começar a usar SmofKabiven extra Nitrogénio sem eletrólitos
- Como usar SmofKabiven extra Nitrogénio sem eletrólitos
- Efeitos adversos possíveis
- Conservação de SmofKabiven extra Nitrogénio sem eletrólitos
- Conteúdo do envase e informação adicional
1. O que é SmofKabiven extra Nitrogénio sem eletrólitos e para que é utilizado
SmofKabiven extra Nitrogénio sem eletrólitos é uma emulsão para perfusão que é administrada na sua sangue mediante um gotejador (perfusão intravenosa). O produto contém aminoácidos (componentes utilizados na formação de proteínas), glicose (carboidratos) e lípidos (gordura), em uma bolsa de plástico e pode ser administrado a adultos e crianças a partir de 2 anos de idade.
Um profissional de saúde irá administrar SmofKabiven extra Nitrogénio sem eletrólitos quando outras formas de alimentação não forem suficientemente boas ou não forem possíveis.
2. O que precisa saber antes de começar a usar SmofKabiven extra Nitrogénio sem eletrólitos
Não use SmofKabiven extra Nitrogénio sem eletrólitos:
- se é alérgico (hipersensível) aos princípios ativos ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6)
- se é alérgico ao peixe ou ao ovo
- se é alérgico aos amendoins ou à soja, não deve utilizar este produto. SmofKabiven extra Nitrogénio sem eletrólitos contém óleo de soja
- se tem demasiados lípidos no sangue (hiperlipidemia)
- se padece uma alteração hepática grave
- se sofre problemas de coagulação do sangue (alterações da coagulação)
- se o seu organismo apresenta problemas para a utilização dos aminoácidos
- se sofre doença renal grave sem possibilidade de diálise
- se se encontra em choque agudo
- se tem demasiado açúcar no sangue (hiperglicemia), que não está controlada
- se tem líquido nos pulmões (edema pulmonar agudo)
- se tem demasiado líquido no organismo (hiperhidratado)
- se apresenta insuficiência cardíaca que não está em tratamento
- se tem um defeito no sistema de coagulação do sangue (síndrome hemofagocitótico)
- se se encontra em uma situação instável, como após um trauma grave, diabetes mellitus não controlada, ataque cardíaco agudo, derrame cerebral, coágulo de sangue, acidose metabólica (uma alteração que dá lugar a demasiado ácido no sangue), infecção grave (sepsis grave), coma, e se não tem suficiente líquido no organismo (deshidratação hipotónica).
- em crianças recém-nascidas ou menores de 2 anos
Advertências e precauções
Consulte o seu médico antes de começar a usar SmofKabiven extra Nitrogénio sem eletrólitos se tiver:
- problemas renais
- diabetes mellitus
- pancreatite (inflamação do pâncreas)
- problemas hepáticos
- hipotireoidismo (problemas da tiróide)
- sepsis (infecção grave)
Se durante a perfusão aparecer febre, erupção cutânea, inchaço, dificuldade para respirar, arrepios, suor, náuseas ou vómitos, informe o seu profissional de saúde imediatamente, porque estes sintomas poderiam ser causados por uma reação alérgica, ou porque está a receber demasiada quantidade do medicamento.
O seu médico necessitará controlar regularmente o seu sangue, por meio de análises da função hepática e outros valores.
Crianças e adolescentes
SmofKabiven extra Nitrogénio sem eletrólitos não é destinado a crianças recém-nascidas nem crianças com menos de 2 anos de idade.
SmofKabiven extra Nitrogénio sem eletrólitos pode ser administrado a crianças de 2 a 16/18 anos de idade.
Uso de SmofKabiven extra Nitrogénio sem eletrólitos com outros medicamentos
Informa o seu médico se está a tomar, tomou recentemente ou poderia ter que tomar qualquer outro medicamento, mesmo os adquiridos sem receita.
Gravidez e amamentação
Não existe informação sobre o uso de SmofKabiven extra Nitrogénio sem eletrólitos durante a gravidez ou no período de amamentação. Por isso, SmofKabiven extra Nitrogénio sem eletrólitos deve ser administrado a mulheres grávidas ou em período de amamentação, apenas se o médico o considerar necessário. No entanto, o uso de SmofKabiven extra Nitrogénio sem eletrólitos pode ser considerado na gravidez e na amamentação, se o seu médico o aconselhar.
Condução e uso de máquinas
Não é relevante, uma vez que este medicamento é administrado no hospital.
3. Como usar SmofKabiven extra Nitrogénio sem eletrólitos
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte de novo o seu médico.
O seu médico decidirá a dose para si de forma individual, dependendo do seu peso corporal e da sua situação. SmofKabiven extra Nitrogénio sem eletrólitos será administrado por um profissional de saúde.
Se usar mais SmofKabiven extra Nitrogénio sem eletrólitos do que deve
É muito pouco provável que receba demasiada quantidade do medicamento, uma vez que SmofKabiven extra Nitrogénio sem eletrólitos será administrado por um profissional de saúde.
4. Efeitos adversos possíveis
Assim como todos os medicamentos, SmofKabiven extra Nitrogénio sem eletrólitos pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Frequentes(podem afetar até 1 de cada 10 doentes): um ligeiro aumento da temperatura corporal.
Pouco frequentes(podem afetar até 1 de cada 100 doentes): níveis elevados no sangue (plasma) de componentes hepáticos, ausência de apetite, náuseas, vómitos, arrepios, tonturas e dor de cabeça.
Raros(podem afetar até 1 de cada 1000 doentes): pressão sanguínea baixa ou elevada, dificuldade para respirar, frequência cardíaca rápida (taquicardia). Reações de hipersensibilidade (que podem dar sintomas como inchaço, febre, descida da pressão sanguínea, erupções cutâneas, zonas vermelhas inchadas, rubor, dor de cabeça). Sensações de frio e calor. Palidez. Lábios e pele com coloração azulada (devido à falta de oxigénio no sangue). Dor no pescoço, nas costas, nos ossos, no peito e na zona lombar.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los directamente através do Sistema Español de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de SmofKabiven extra Nitrogénio sem eletrólitos
Mantenha este medicamento fora da vista e do alcance das crianças.
Mantenha na sobrebolsa. Não conserve a temperatura superior a 25º C. Não congele.
Não utilize este medicamento após a data de validade que aparece na bolsa e na caixa. A data de validade é o último dia do mês que se indica.
6. Conteúdo do envase e informação adicional
SmofKabiven extra Nitrogênio sem eletrólitos contém
As substâncias ativas são | g por 1000 ml |
Alanina | 9,2 |
Arginina | 7,9 |
Glicina | 7,2 |
Histidina | 2,0 |
Isoluecina | 3,3 |
Leucina | 4,8 |
Lisina (como acetato) | 4,3 |
Metionina | 2,8 |
Fenilalanina | 3,3 |
Prolina | 7,3 |
Serina | 4,3 |
Taurina | 0,65 |
Treonina | 2,9 |
Triptófano | 1,3 |
Tirosina | 0,26 |
Valina | 4,1 |
Glucosa (como monohidrato) | 85 |
Azeite de soja, refinado | 8,7 |
Triglicerídeos de cadeia média | 8,7 |
Azeite de oliva, refinado | 7,2 |
Azeite de peixe, rico em ácidos graxos ômega-3 | 4,3 |
Os demais componentes são: glicerol, fosfolipídios de ovo purificados, todo-rac-α-tocoferol, hidróxido sódio (ajuste pH), oleato sódio, ácido acético glacial (ajuste pH), ácido clorídrico (ajuste pH) e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
As soluções de glucosa e aminoácidos são transparentes, incolores ou ligeiramente amareladas e livres de partículas. A emulsão lipídica é branca e homogênea.
Tamanhos de envase:
1 x 506 ml, 6 x 506 ml
1 x 1012 ml, 4 x 1012 ml
1 x 1518 ml, 4 x 1518 ml
1 x 2025 ml, 4 x 2025 ml
1 x 2531 ml, 3 x 2531 ml
Título da autorização de comercialização e responsável pela fabricação
Título da autorização de comercialização
Fresenius Kabi España S.A.U.
C/ Marina 16-18.
08005 Barcelona (Espanha)
Responsável pela fabricação
Fresenius Kabi AB, SE-751 74 Uppsala, Suécia
Data da última revisão deste prospecto: Março 2023
A informação detalhada e atualizada deste medicamento está disponível na página Web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
------------------------------------------------------------------------------------------------------------------------
Esta informação está destinada unicamente a profissionais do setor sanitário:
Advertências e precauções especiais de uso
Para evitar os riscos associados a velocidades de perfusão demasiado rápidas, recomenda-se o uso de uma perfusão contínua e bem controlada, se possível mediante o uso de uma bomba de perfusão.
Como o uso de uma veia central está associado a um elevado risco de infecção, devem ser tomadas precauções assépticas estritas para evitar qualquer contaminação durante a inserção do catéter e a manipulação.
Devem ser monitorizados a glucosa sérica, os eletrólitos e a osmolaridade, assim como o balanço hídrico, o equilíbrio ácido-base e os níveis de enzimas hepáticos.
Ante qualquer sinal ou sintoma de reação anafiláctica (como febre, tremores, erupção cutânea ou dispneia) deve interromper-se imediatamente a perfusão.
SmofKabiven extra Nitrogênio sem eletrólitos não deve ser administrado simultaneamente com sangue no mesmo equipamento de perfusão, devido ao risco de pseudoaglutinação.
Forma de administração
Via intravenosa, perfusão em uma veia central.
Para proporcionar uma nutrição parenteral completa, devem ser adicionados a SmofKabiven extra Nitrogênio sem eletrólitos oligoelementos e vitaminas, de acordo com as necessidades do paciente.
Posologia
Adultos
Dosagem:
A faixa de doses de 13-31 ml SmofKabiven extra Nitrogênio sem eletrólitos/kg pc/dia aportará 0,14 – 0,32 g de nitrogênio/kg pc/dia (correspondentes a 0,85 – 2,0 g aminoácidos/kg pc/dia) e 12 – 28 kcal/kg pc/dia de energia total (8 – 19 kcal/kg pc/dia de energia não-proteica).
Velocidade de perfusão
A velocidade de perfusão máxima usual para glucosa é 0,25 g/kg pc/h, para os aminoácidos 0,1 g/kg pc/h, e para lípidos 0,15 g/kg pc/h.
A velocidade de perfusão não deve exceder 1,5 ml/kg pc/hora (correspondente a 0,13 g de glucosa, 0,10 g de aminoácidos e 0,04 g de lípidos/kg pc/h). O período de perfusão recomendado é de 14 – 24 horas.
Nutrição parenteral intradiálise (NPID)
A velocidade máxima de infusão para a nutrição parenteral intradiálitica (NPID) em pacientes adultos estáveis em tratamento renal sustitutivo crônico é de 3,0 ml/kg/h (correspondente a 0,20 g de aminoácidos/kg/h, 0,25 g de glucosa/kg/h e 0,09 g de lípidos/kg/h). O volume de infusão na NPID deve ser guiado pela diferença entre a ingestão de alimentos por via oral e as ingestas de nutrientes recomendadas, as perdas de nutrientes inevitáveis causadas pela terapia de substituição renal, assim como pela tolerância metabólica individual do paciente. O tempo de infusão habitual para seu uso na NPID é de 3 a 5 horas, dependendo das necessidades do paciente e da duração prevista da sessão de terapia de substituição renal. A dose diária máxima recomendada não se modifica.
Dose máxima diária:
A dose máxima diária varia com a situação clínica do paciente e pode mesmo mudar de um dia para outro. A dose máxima diária recomendada é de 31 ml/kg pc/dia.
População pediátrica
Crianças (2-11 anos)
Dosagem:
A dose de até 31 ml/kg pc/dia deve ser ajustada regularmente de acordo com os requisitos do paciente pediátrico que variam mais do que nos pacientes adultos.
Velocidade de perfusão:
A velocidade máxima de perfusão é de 1,8 ml/kg pc/h (correspondente a 0,12 g de aminoácidos/kg/h, 0,15 g/glucosa/kg/h e 0,05 g lípidos/kg/h). Na velocidade de perfusão máxima recomendada, não usar períodos de perfusão maiores de 17 horas, exceto em casos excepcionais e sob estreita monitorização.
O período de perfusão recomendado é de 12 – 24 horas.
Dose máxima diária:
A dose máxima diária varia com a condição clínica do paciente e pode mesmo mudar de dia a dia. A dose máxima diária é de 31 ml/kg pc/dia.
Adolescentes (12-16/18 anos)
SmofKabiven extra Nitrogênio sem eletrólitos pode ser usado em adolescentes da mesma forma que em adultos.
Precauções de eliminação
Não utilizar se o envase estiver deteriorado.
Utilizar apenas se as soluções de aminoácidos e glucosa forem transparentes e incolores ou ligeiramente amareladas, e se a emulsão lipídica for branca e homogênea. Deve misturar-se o conteúdo das três câmaras separadas antes de utilizar, e antes de realizar qualquer adição através do puerto de aditivos. Depois da abertura das soldaduras tipo peel, a bolsa deve ser invertida várias vezes com o fim de garantir uma mistura homogênea, que não mostre evidência de uma separação de fases.
Para um único uso. Deve descartar-se qualquer mistura sobrante após a perfusão.
Compatibilidade
Estão disponíveis dados de compatibilidade com os produtos de marca Dipeptiven 200 mg/ml, Supliven, Glycophos 216 mg/ml, Vitalipid Adultos/Infantil e Soluvit liofilizado em quantidades definidas e com soluções com eletrólitos em concentrações definidas. Ao adicionar os eletrólitos, devem ser consideradas as quantidades já presentes na bolsa de acordo com as necessidades clínicas do paciente. Os dados gerados respaldam adições à bolsa ativada de acordo com a tabela seguinte:
Intervalo de compatibilidade estabelecido durante 7 dias, ou seja, 6 dias de armazenamento a 2-8ºC seguido de 24 horas a 20-25ºC.
Unidades | Conteúdo total máximo | |||||
Tamanho da bolsa de SmofKabiven Extra Nitrogênio Sem Eletrólitos | ml | 506 | 1012 | 1518 | 2025 | 2531 |
Aditivo | Volume | |||||
Dipeptiven | ml | 0-150 | 0 - 300 | 0 - 300 | 0 - 300 | 0 - 300 |
Supliven | ml | 0 - 10 | 0 - 20 | 0 - 20 | 0 - 20 | 0 - 20 |
Soluvit | vial | 0 - 1 | 0 - 2 | 0 - 2 | 0 - 2 | 0 - 2 |
Vitalipid Adultos/Infantil | ml | 0 - 10 | 0 - 20 | 0 - 20 | 0 - 20 | 0 - 20 |
Límites dos eletrólitos1 | Concentração | |||||
Sódio | mmol | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 |
Potássio | mmol | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 | ≤ 150 |
Cálcio | mmol | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 |
Magnésio | mmol | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 | ≤ 5 |
Fosfato orgânico (Glycophos) | mmol | ≤ 30 | ≤ 30 | ≤ 30 | ≤ 30 | ≤ 30 |
Zinco | mmol | ≤ 0,2 | ≤ 0,2 | ≤ 0,2 | ≤ 0,2 | ≤ 0,2 |
Selênio | µmol | ≤ 2 | ≤ 2 | ≤ 2 | ≤ 2 | ≤ 2 |
1inclui as quantidades de todos os produtos.
Nota: Esta tabela indica a compatibilidade. Não é uma diretriz de dosagem.
No caso dos produtos com nome comercial, antes de prescrevê-los, consulte a ficha técnica aprovada.
Existem dados sobre a compatibilidade com outros aditivos e o tempo de conservação das diferentes misturas, disponíveis sob solicitação.
As adições devem ser realizadas assépticamente.
Período de validade após a mistura das câmaras da bolsa
Foi demonstrada a estabilidade física e química da bolsa de três câmaras misturada durante 48 horas a 20-25°C. Desde um ponto de vista microbiológico, o produto deve ser utilizado imediatamente. Se não for utilizado imediatamente, o tempo de conservação até seu uso e as condições prévias ao seu uso são responsabilidade do usuário e normalmente não devem ser superiores a 24 horas a 2-8º C, a menos que a mistura tenha sido realizada em condições assépticas controladas e validadas.
Período de validade após a mistura com aditivos
Foi demonstrada estabilidade físico-química no uso da bolsa mista de três câmaras com aditivos (ver apartado 6.6) até 7 dias, ou seja, 6 dias a 2-8ºC seguidos de 24 horas a 20-25ºC, incluindo a duração da administração. Desde um ponto de vista microbiológico, o produto deve ser utilizado imediatamente após realizar as adições. Se não for utilizado imediatamente, o tempo de conservação até seu uso e as condições prévias ao seu uso são responsabilidade do usuário. O tempo de conservação normalmente não deve ser superior a 24 horas a 2-8º C, a menos que a adição dos suplementos tenha sido realizada em condições assépticas controladas e validadas.
Instruções para o uso de SmofKabiven extra Nitrogênio sem eletrólitos
A bolsa
506 ml, 1012 ml, 1518 ml, 2025 ml, 2531 ml
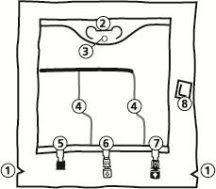
- Cortes na sobrebolsa
- Alça
- Orifício para pendurar a bolsa
- Selos rompíveis
- Porto cego (utilizado apenas durante a fabricação)
- Porto de adição
- Porto de perfusão
- Absorvente de oxigênio
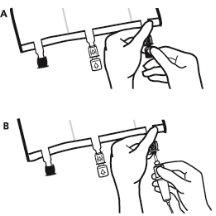
- Abertura da sobrebolsa
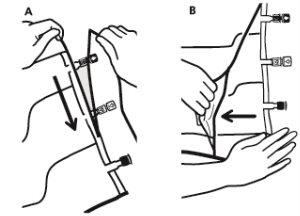
- Para extrair a sobrebolsa, segurá-la em posição horizontal e rasgar pela corte até os portos ao longo do bordo superior (A)
- Então, simplesmente rasgar ao longo do envase; separar a sobrebolsa e descartá-la junto com o absorvente de oxigênio (B).
- Mistura
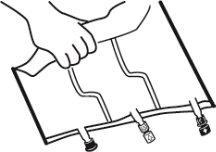
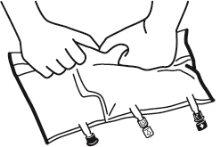
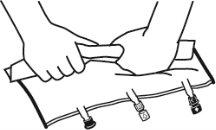
- Colocar a bolsa em uma superfície plana.
- Enrolar a bolsa desde a parte do pendurador até a parte dos portos, primeiro com a mão direita e a seguir aplicando uma pressão constante com a mão esquerda até que as soldaduras verticais se abram. As soldaduras peel verticais se abrem devido à pressão do líquido.
As soldaduras peel também podem ser abertas antes de retirar a sobrebolsa.
Nota:os líquidos se misturam facilmente embora a soldadura horizontal permaneça fechada.
506 ml, 1012 ml, 1518 ml, 2025 ml, 2531 ml
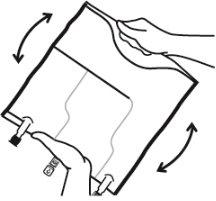
- Misturar os conteúdos das três câmaras invertendo a bolsa três vezes até que os componentes estejam completamente misturados.
- Finalização da preparação:
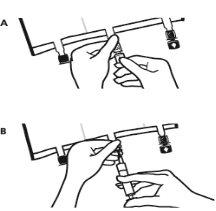
- Colocar a bolsa de novo sobre uma superfície plana. Pouco antes de injetar os aditivos, romper o porto de adição branco pela marca em forma de seta (A).
Nota:A membrana do porto de aditivos é estéril.
- Segurar a base do porto de aditivos. Inserir a agulha, injetar os aditivos (de compatibilidade conhecida) pelo centro do ponto de injeção (B).
- Misturar completamente entre cada adição, invertendo a bolsa três vezes. Utilizar seringas com agulhas de calibre 18-23 e uma longitude máxima de 40 mm.
- Pouco antes de inserir o conjunto de perfusão, romper o porto de perfusão azul pela marca em forma de seta (A).
Nota:A membrana do porto de perfusão é estéril.
- Usar um equipamento de perfusão não ventilado ou fechar a entrada do ar do equipamento ventilado.
- Segurar a base do porto de perfusão.
- Introduzir o punção através do porto de perfusão. O punção deve estar totalmente inserido para assegurar sua retenção.
Nota:A parte interna do porto de perfusão é estéril.
- Pendurado da bolsa
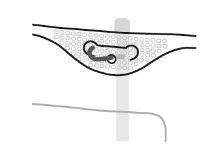
- Pendurar a bolsa pela alça que há sob o pendurador
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃOForma farmacêutica: PERFURAÇÃO INJETÁVEL, 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 4,76 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 g / 3,5 g / 200 gSubstância ativa: combinationsFabricante: Baxter S.L.Requer receita médicaForma farmacêutica: SOLUÇÃO INJETÁVEL PARA PERFUSÃO, 3,5 g / 200 g / 5,22 g / 1,88 g / 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 662 mg / 1,02 g / 4,76 g / 5,15 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 gSubstância ativa: combinationsFabricante: Baxter S.L.Requer receita médicaForma farmacêutica: PERFURAÇÃO INJETÁVEL, 4,25 g / 300 g / 5,22 g / 1,54 g / 4,76 g / 1,53 g / 8,76 g / 4,08 g / 5,1 g / 6,2 g / 3,57 g / 3,4 g / 662 mg / 1,02 g / 5,78 g / 5,94 g / 6,16 g / 4,93 g / 17,6 g / 0,34 g / 9,78 gSubstância ativa: combinationsFabricante: Baxter S.L.Requer receita médica
Alternativas a SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO em Polónia
Alternativa a SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO em Ukraine
Médicos online para SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de SMOFKABIVEN EXTRA NITROGEN SEM ELETRÓLITOS EMULSÃO PARA PERFUSÃO – sujeita a avaliação médica e regras locais.














