
Olimel N12e

Pergunte a um médico sobre a prescrição de Olimel N12e

Como usar Olimel N12e
Folheto para o doente: Informação para o utilizador
OLIMEL N12E, emulsão para infusão
Deve ler atentamente o conteúdo do folheto antes de administrar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto, para que possa relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico ou enfermeiro.
- Se o doente apresentar algum efeito indesejado, incluindo qualquer efeito indesejado não listado no folheto, deve informar o médico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento OLIMEL N12E, emulsão para infusão e para que é utilizado
- 2. Informações importantes antes de administrar o medicamento OLIMEL N12E, emulsão para infusão
- 3. Como usar o medicamento OLIMEL N12E, emulsão para infusão
- 4. Efeitos indesejados
- 5. Como armazenar o medicamento OLIMEL N12E, emulsão para infusão
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento OLIMEL N12E, emulsão para infusão e para que é utilizado
OLIMEL N12E é uma emulsão para infusão. O medicamento é fornecido em um saco de três câmaras.
Na primeira câmara, há uma solução de glicose com cálcio, na segunda - uma emulsão lipídica, e na
terceira - uma solução de aminoácidos com outros eletrólitos.
OLIMEL N12E é utilizado para nutrição parenteral por via intravenosa em adultos e crianças com mais de
2 anos de idade, quando a nutrição oral não é adequada.
OLIMEL N12E só pode ser utilizado sob controle médico.
2. Informações importantes antes de administrar o medicamento OLIMEL N12E, emulsão para infusão
Quando não usar o medicamento OLIMEL N12E, emulsão para infusão:
- em prematuros, recém-nascidos e crianças com menos de 2 anos de idade;
- se o doente tiver alergia a ovos, soja, proteínas de amendoim, milho/produtos que contenham milho (ver também o ponto "Precauções e advertências" abaixo) ou a qualquer um dos outros componentes do medicamento (listados no ponto 6);
- se a administração de alguns aminoácidos causar uma reação anormal no organismo do doente;
- se o doente tiver um nível muito alto de lipídios no sangue;
- se o doente tiver hiperglicemia (nível muito alto de açúcar no sangue);
- se o doente tiver um nível anormalmente alto de qualquer um dos eletrólitos (sódio, potássio, magnésio, cálcio e/ou fósforo) no sangue.
Em cada caso, o médico tomará a decisão de administrar o medicamento com base em fatores como idade,
peso corporal do doente e seu estado de saúde, incluindo os resultados dos exames realizados.
Precauções e advertências
Antes de iniciar a administração do medicamento OLIMEL N12E, deve discutir com o médico ou enfermeiro.
A administração excessivamente rápida de soluções para nutrição parenteral total pode resultar em lesão
ou morte do doente.
Se ocorrerem sinais ou sintomas atípicos de reação alérgica (como suor, febre, calafrios, dor de cabeça,
erupção cutânea ou problemas respiratórios), deve interromper imediatamente a infusão. O medicamento
contém óleo de soja e fosfolipídios de ovo. As proteínas de soja e ovo podem causar reações de hipersensibilidade.
Foram observadas reações alérgicas cruzadas entre as proteínas de soja e amendoim.
O medicamento OLIMEL N12E contém glicose derivada do milho, que pode causar reações de hipersensibilidade,
se o doente tiver alergia ao milho ou produtos que contenham milho (ver ponto "Quando não usar o medicamento
OLIMEL N12E, emulsão para infusão" acima).
Dificuldades respiratórias também podem ser um sinal de que pequenas partículas bloquearam os vasos sanguíneos
nos pulmões (depósitos nos vasos pulmonares). Se ocorrerem dificuldades respiratórias, deve informar o médico
ou enfermeiro. Eles decidirão sobre a ação apropriada.
O antibiótico ceftriaxon não deve ser misturado ou administrado simultaneamente com qualquer solução que contenha
cálcio (incluindo o medicamento OLIMEL N12E) por via intravenosa.
Esses medicamentos não devem ser administrados simultaneamente, mesmo por diferentes linhas de infusão ou locais de infusão.
No entanto, o medicamento OLIMEL N12E e a ceftriaxon podem ser administrados sequencialmente, se as linhas de infusão forem inseridas em locais diferentes ou forem trocadas ou limpas com solução fisiológica de cloreto de sódio entre as infusões, para evitar a formação de depósitos (precipitação de sais de cálcio da ceftriaxon).
Devido ao risco de precipitação, o medicamento OLIMEL N12E não deve ser administrado pela mesma linha de infusão
ou adicionado ao antibiótico amplicilina ou ao medicamento anticonvulsivante fosfenitoína.
O óleo e o óleo de soja presentes no medicamento OLIMEL N12E contêm vitamina K. Normalmente, isso não afeta
a ação de medicamentos anticoagulantes (como a cumarina). No entanto, se o doente estiver tomando medicamentos
anticoagulantes, deve informar o médico.
Os lipídios presentes na emulsão podem interferir nos resultados de alguns exames laboratoriais, se a amostra de sangue
for coletada antes que os lipídios sejam eliminados do sangue do doente (isso ocorre após 5 a 6 horas após a administração
dos lipídios).
O medicamento OLIMEL N12E contém potássio. Deve haver precaução especial em doentes que estejam tomando
medicamentos diuréticos, inibidores da enzima conversora de angiotensina (ECA), antagonistas do receptor de angiotensina
II (medicamentos usados no tratamento da hipertensão) ou medicamentos imunossupressores. Esses medicamentos podem
causar um aumento nos níveis de potássio no sangue.
Gravidez, amamentação e fertilidade
Se a paciente estiver grávida ou amamentando, achar que pode estar grávida ou planejar ter um filho, deve consultar
o médico antes de administrar este medicamento.
Falta de experiência adequada sobre o uso do medicamento OLIMEL N12E em mulheres grávidas ou amamentando.
Se necessário, pode ser considerada a administração do medicamento OLIMEL N12E durante a gravidez e amamentação.
O medicamento OLIMEL N12E deve ser administrado a mulheres grávidas ou amamentando apenas após uma avaliação cuidadosa.
Fertilidade
Falta de dados adequados.
Condução de veículos e uso de máquinas
Não se aplica.
3. Como usar o medicamento OLIMEL N12E, emulsão para infusão
Dosagem
OLIMEL N12E deve ser usado apenas em adultos e crianças com mais de 2 anos de idade.
O medicamento tem a forma de emulsão para infusão administrada por via intravenosa.
Antes de usar, OLIMEL N12E deve estar à temperatura ambiente.
OLIMEL N12E é destinado apenas para uso único.
A infusão de 1 saco geralmente dura de 12 a 24 horas.
Dosagem - Adultos
A velocidade de administração, de acordo com as necessidades e o estado clínico do doente, será determinada
pelo médico.
O medicamento pode ser usado por tanto tempo quanto necessário, dependendo do estado clínico do doente.
Dosagem - Crianças com mais de 2 anos de idade e adolescentes
A dose do medicamento e o período de administração são determinados pelo médico. Isso depende da idade, peso,
altura, estado de saúde e capacidade do organismo de decompor e utilizar os componentes do medicamento
OLIMEL N12E.
Uso de dose maior do que a recomendada do medicamento OLIMEL N12E, emulsão para infusão
Se o doente receber uma dose excessiva do medicamento ou uma infusão muito rápida, os aminoácidos presentes
podem contribuir para um aumento da acidez do sangue e ocorrência de sintomas de hipervolemia (aumento do volume
sanguíneo). Pode ocorrer um aumento nos níveis de glicose no sangue e na urina, e pode desenvolver-se um quadro
de hiperosmolaridade (aumento da viscosidade do sangue), e os lipídios presentes na emulsão podem aumentar os níveis
de triglicerídeos no sangue. A administração de uma infusão com velocidade excessiva ou volume excessivo do medicamento
OLIMEL N12E pode causar náuseas, vômitos, calafrios, dor de cabeça, ondas de calor, suor excessivo (hiperidrose)
e distúrbios eletrolíticos. Nesse caso, deve interromper imediatamente a infusão.
Em alguns casos, em casos graves, o médico pode precisar submeter o doente a diálise renal por um período para ajudar
os rins a eliminar o excesso do medicamento.
Para evitar essas situações, o médico monitora regularmente o estado do doente e verifica os parâmetros sanguíneos.
Em caso de dúvidas sobre o uso do medicamento, deve consultar o médico.
4. Efeitos indesejados
Como qualquer medicamento, este medicamento pode causar efeitos indesejados, embora não ocorram em todos.
Se ocorrerem alterações no bem-estar durante ou após o tratamento, deve informar imediatamente o médico ou enfermeiro.
Os exames realizados pelo médico durante a administração do medicamento ao doente devem minimizar o risco de efeitos
indesejados.
Se ocorrerem sinais ou sintomas atípicos de reação alérgica, como suor excessivo, febre, calafrios, dor de cabeça, erupção
cutânea ou dificuldades respiratórias, deve interromper imediatamente a infusão.
Durante o uso do medicamento OLIMEL, foram relatados os seguintes efeitos indesejados:
Frequência - Frequente: pode afetar até 1 em 10 doentes
- taquicardia (batimento cardíaco acelerado);
- perda de apetite;
- aumento dos níveis de lipídios no sangue (hipertrigliceridemia);
- dor abdominal;
- diarreia;
- náuseas;
- aumento da pressão arterial (hipertensão).
Frequência - Desconhecida: frequência não pode ser estimada com base nos dados disponíveis
- reações de hipersensibilidade, incluindo suor, febre, calafrios, dor de cabeça, erupção cutânea (eritematosa, papulosa, pustulosa, maculosa, erupção generalizada), prurido, ondas de calor, dificuldades respiratórias;
- infusão extravasada (vazamento da infusão para os tecidos circundantes) pode causar dor, irritação, inchaço/edema, vermelhidão (eritema)/aquecimento, necrose da pele ou bolhas/pústulas, inflamação, espessamento ou tensão da pele no local da infusão;
- vômitos.
Durante o uso de medicamentos semelhantes para nutrição parenteral, foram relatados os seguintes efeitos indesejados:
Frequência - Muito raro: pode afetar até 1 em 10.000 doentes
- diminuição da capacidade de eliminação de lipídios (síndrome de sobrecarga lipídica) relacionada a um piora súbito do estado de saúde do doente. Os sintomas da síndrome de sobrecarga lipídica geralmente desaparecem após a interrupção da infusão da emulsão lipídica:
- febre;
- diminuição do número de glóbulos vermelhos, que pode causar palidez e fraqueza ou falta de ar (anemia);
- baixo número de glóbulos brancos, que pode aumentar o risco de infecções (leucopenia);
- baixo número de plaquetas, que pode aumentar o risco de hematomas e/ou sangramentos (trombocitopenia);
- distúrbios da coagulação, que afetam a capacidade de coagulação do sangue;
- acúmulo de lipídios no fígado (hepatomegalia);
- piora da função hepática;
- sintomas do sistema nervoso central (por exemplo, coma).
Frequência — Desconhecida:frequência não pode ser estimada com base nos dados disponíveis
- reações alérgicas;
- resultados anormais de exames de sangue para função hepática;
- dificuldade de eliminação da bile (colestase);
- aumento do tamanho do fígado (hepatomegalia);
- doenças hepáticas relacionadas à nutrição parenteral (ver "Precauções e advertências" no ponto 2);
- icterícia;
- diminuição do número de plaquetas (trombocitopenia);
- aumento dos níveis de azoto no sangue (azotemia);
- aumento da atividade de enzimas hepáticas;
- formação de pequenas partículas que podem causar obstrução dos vasos sanguíneos nos pulmões (depósitos nos vasos pulmonares), levando a embolia pulmonar e dificuldades respiratórias (insuficiência respiratória).
Notificação de efeitos indesejados
Se ocorrerem efeitos indesejados, incluindo qualquer efeito indesejado não listado no folheto, deve informar o médico
ou enfermeiro. Efeitos indesejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos
Indesejados de Medicamentos da Agência Nacional de Vigilância Sanitária
Rua Alexandre Herculano, 58
1250-008 Lisboa
Telefone: +351 21 798 73 00
Fax: +351 21 798 73 99
Sítio na Internet: https://www.infarmed.pt/
Efeitos indesejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos indesejados pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como armazenar o medicamento OLIMEL N12E, emulsão para infusão
O medicamento deve ser armazenado em local não visível e inacessível a crianças.
Não use este medicamento após a data de validade impressa na embalagem e no rótulo do frasco, após (MM/AAAA).
A data de validade é o último dia do mês indicado.
Não congelar.
Armazenar na embalagem protetora.
Medicamentos não devem ser jogados na rede de esgotos ou lixeiras domésticas. Deve perguntar ao farmacêutico como eliminar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento OLIMEL N12E, emulsão para infusão
Os princípios ativos em cada um dos sacos da emulsão pronta para uso são: 14,2% (correspondente a 14,2 g/100 ml)
solução de L-aminoácidos (alanina, arginina, glicina, histidina, isoleucina, leucina, lisina (na forma de lisina acetato),
metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina, ácido aspártico, ácido glutâmico) com eletrólitos (sódio, potássio, magnésio, fosfatos, acetatos, cloretos),
17,5% (correspondente a 17,5 g/100 ml) emulsão lipídica (óleo de oliva refinado e óleo de soja refinado) e 27,5% (correspondente
a 27,5 g/100 ml) solução de glicose (na forma de glicose monohidratada) com cálcio.
Os outros componentes são:
| Câmara contendo emulsão lipídica | Câmara contendo solução de aminoácidos | Câmara contendo solução de glicose |
| Fosfolipídios de ovo refinados, glicerol, oleato de sódio, hidróxido de sódio (para ajuste do pH), água para injeção | Ácido acético glacial (para ajuste do pH), água para injeção | Ácido clorídrico (para ajuste do pH), água para injeção |
Como é o medicamento OLIMEL N12E emulsão para infusão e o que contém a embalagem
OLIMEL N12E é uma emulsão para infusão fornecida em um saco de três câmaras. A primeira câmara contém
a emulsão lipídica, a segunda câmara contém a solução de aminoácidos com eletrólitos, e a terceira câmara contém
a solução de glicose com cálcio. As câmaras são separadas por selos não permeáveis.
Antes da administração, o conteúdo das câmaras deve ser misturado girando o saco em direção a si mesmo, começando
pela parte superior do saco, até que os selos se abram.
Aspeto antes da mistura:
- As soluções de aminoácidos e glicose são transparentes, incolores ou ligeiramente amareladas.
- A emulsão lipídica é homogênea com aspeto leitoso.
Aspeto após a mistura: emulsão homogênea com aspeto leitoso.
O saco de três câmaras é um saco plástico multicamada. A camada interna (de contato) do saco é compatível com os componentes
e aditivos permitidos.
Para evitar o contato com o oxigênio do ar, o saco é embalado em uma embalagem protetora que protege contra a entrada
de oxigênio, com um sachê que absorve oxigênio.
Tamanhos da embalagem
saco de 650 ml: 1 caixa de cartão com 10 sacos
saco de 1000 ml: 1 caixa de cartão com 6 sacos
saco de 1500 ml: 1 caixa de cartão com 4 sacos; 1 caixa de cartão com 5 sacos
saco de 2000 ml: 1 caixa de cartão com 4 sacos; 1 caixa de cartão com 5 sacos
1 saco com capacidade de 650 ml, 1000 ml, 1500 ml e 2000 ml.
Nem todos os tamanhos de embalagem podem estar disponíveis.
Responsável e fabricante
Responsável
Baxter Portugal, Lda.
Rua da Cidade, 12
1200-781 Lisboa
Fabricante
BAXTER S.A.
Boulevard René Branquart 80
7860 Lessines
Bélgica
Este medicamento está autorizado para comercialização nos países membros da Área Econômica Europeia sob as seguintes denominações:
Área Econômica Europeia
Bélgica, Bulgária, Croácia, Chipre, República Checa, Estônia, França, Grécia, Hungria, Itália, Letônia, Lituânia,
Luxemburgo, Holanda, Romênia, Eslovênia, Eslováquia, Espanha: OLIMEL N12E
Áustria: ZentroOLIMEL 7,6 % com eletrólitos
Alemanha: Olimel 7,6 % E
Dinamarca, Islândia, Suécia, Noruega, Finlândia, Polônia, Portugal: Olimel N12E
Irlanda, Malta, Reino Unido: TRIOMEL 12 g/l nitrogênio 950 kcal/l com eletrólitos
Data da última atualização do folheto abril 2025
-------------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico especializado:
A. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
OLIMEL N12E tem a forma de um saco de três câmaras.
Cada saco contém uma solução de glicose com cálcio, uma emulsão lipídica e uma solução de aminoácidos com outros
eletrólitos.
| Conteúdo por saco | ||||
| 650 ml | 1000 ml | 1500 ml | 2000 ml | |
| 27,5% solução de glicose (correspondente a 27,5 g/100 ml) | 173 ml | 267 ml | 400 ml | 533 ml |
| 14,2% solução de aminoácidos (correspondente a 14,2 g/100 ml) | 347 ml | 533 ml | 800 ml | 1067 ml |
| 17,5% emulsão lipídica (correspondente a 17,5 g/100 ml) | 130 ml | 200 ml | 300 ml | 400 ml |
A composição da emulsão pronta para uso após a mistura do conteúdo das três câmaras:
| Princípios ativos | 650 ml | 1000 ml | 1500 ml | 2000 ml |
| Óleo de oliva refinado + óleo de soja refinado | 22,75 g | 35,00 g | 52,50 g | 70,00 g |
| Alanina | 7,14 g | 10,99 g | 16,48 g | 21,97 g |
| Arginina | 4,84 g | 7,44 g | 11,16 g | 14,88 g |
| Ácido aspártico | 1,43 g | 2,20 g | 3,30 g | 4,39 g |
| Ácido glutâmico | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Glicina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| Histidina | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| Isoleucina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Leucina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| Lisina (correspondente a lisina acetato) | 3,88 g (5,48 g) | 5,97 g (8,43 g) | 8,96 g (12,64 g) | 11,95 g (16,85 g) |
| Metionina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Fenilalanina | 3,42 g | 5,26 g | 7,90 g | 10,53 g |
| Prolina | 2,94 g | 4,53 g | 6,79 g | 9,06 g |
| Serina | 1,95 g | 3,00 g | 4,50 g | 5,99 g |
| Treonina | 2,46 g | 3,79 g | 5,69 g | 7,58 g |
| Triptofano | 0,82 g | 1,26 g | 1,90 g | 2,53 g |
| Tirosina | 0,13 g | 0,20 g | 0,30 g | 0,39 g |
| Valina | 3,16 g | 4,86 g | 7,29 g | 9,72 g |
| Octanato de sódio tri-hidratado | 0,97 g | 1,5 g | 2,24 g | 2,99 g |
| Glicerofosfato de sódio di-hidratado | 2,39 g | 3,67 g | 5,51 g | 7,34 g |
| Cloruro de potássio | 1,45 g | 2,24 g | 3,35 g | 4,47 g |
| Cloruro de magnésio hexa-hidratado | 0,53 g | 0,81 g | 1,22 g | 1,62 g |
| Cloruro de cálcio di-hidratado | 0,34 g | 0,52 g | 0,77 g | 1,03 g |
| Glicose (correspondente a glicose monohidratada) | 47,67 g (52,43 g) | 73,33 g (80,67 g) | 110,00 g (121,00 g) | 146,67 g (161,33 g) |
Os excipientes são:
| Câmara contendo emulsão lipídica | Câmara contendo solução de aminoácidos com eletrólitos | Câmara contendo solução de glicose com cálcio |
| Fosfolipídios de ovo refinados, glicerol, oleato de sódio, hidróxido de sódio (para ajuste do pH), água para injeção | Ácido acético glacial (para ajuste do pH), água para injeção | Ácido clorídrico (para ajuste do pH), água para injeção |
Os valores nutricionais da emulsão pronta para uso, de acordo com o tamanho do saco:
| 650 ml | 1000 ml | 1500 ml | 2000 ml | |
| Lipídios | 22,8 g | 35,0 g | 52,5 g | 70,0 g |
| Aminoácidos | 49,4 g | 75,9 g | 113,9 g | 151,9 g |
| Azoto | 7,8 g | 12,0 g | 18,0 g | 24,0 g |
| Glicose | 47,7 g | 73,3 g | 110,0 g | 146,7 g |
| Valor energético: | ||||
| Valor energético total aproximado | 620 kcal | 950 kcal | 1420 kcal | 1900 kcal |
| Valor energético não proteico | 420 kcal | 640 kcal | 960 kcal | 1280 kcal |
| Valor energético da glicose | 190 kcal | 290 kcal | 430 kcal | 580 kcal |
| Valor energético dos lipídios | 230 kcal | 350 kcal | 520 kcal | 700 kcal |
| Relação: valor energético não proteico/azoto | 53 kcal/g | 53 kcal/g | 53 kcal/g | 53 kcal/g |
| Relação: valor energético da glicose/lipídios | 45/55 | 45/55 | 45/55 | 45/55 |
| Lipídios/valor energético total | 37% | 37% | 37% | 37% |
| Eletrólitos: | ||||
| Sódio | 22,8 mmol | 35,0 mmol | 52,5 mmol | 70,0 mmol |
| Potássio | 19,5 mmol | 30,0 mmol | 45,0 mmol | 60,0 mmol |
| Magnésio | 2,6 mmol | 4,0 mmol | 6,0 mmol | 8,0 mmol |
| Cálcio | 2,3 mmol | 3,5 mmol | 5,3 mmol | 7,0 mmol |
| Fosfatos | 9,5 mmol | 15,0 mmol | 21,9 mmol | 29,2 mmol |
| Acetatos | 46 mmol | 70 mmol | 105 mmol | 140 mmol |
| Cloruros | 30 mmol | 45 mmol | 68 mmol | 90 mmol |
| pH | 6,4 | 6,4 | 6,4 | 6,4 |
| Osmolalidade aproximada | 1270 mOsm/l | 1270 mOsm/l | 1270 mOsm/l | 1270 mOsm/l |
B. DOSAGEM E MODO DE ADMINISTRAÇÃO
Dosagem
OLIMEL N12E não é recomendado para uso em crianças com menos de 2 anos de idade, devido à composição e volume
inadequados (ver pontos 4.4; 5.1 e 5.2 do RCM).
Não ultrapassar a dose diária máxima recomendada. Devido à composição fixa do saco de três câmaras, pode não ser
possível atender às necessidades nutricionais do doente simultaneamente. Pode haver situações clínicas em que os doentes
precisam de quantidades diferentes de nutrientes do que as encontradas no saco de composição fixa. Nesses casos, qualquer
mudança no volume (dose) deve levar em conta o efeito sobre a dosagem de todos os outros nutrientes do medicamento
OLIMEL N12E. Nesses casos, o pessoal médico especializado pode considerar ajustar o volume (dose) do medicamento
OLIMEL N12E para atender às necessidades aumentadas.
Adultos
A dosagem depende do gasto energético do doente, estado clínico, peso corporal e capacidade de metabolizar os componentes
do medicamento OLIMEL N12E, bem como dos nutrientes energéticos ou proteicos adicionais administrados por via oral/enteral,
portanto, é necessário escolher o tamanho do saco apropriado.
A necessidade diária média é:
- 0,16 a 0,35 g de azoto/kg de peso corporal (1 a 2 g de aminoácidos/kg), dependendo do estado nutricional do doente e do grau de catabolismo. Populações específicas podem requerer até 0,4 g de azoto/kg de peso corporal (2,5 g de aminoácidos/kg).
- 20 a 40 kcal/kg,
- 20 a 40 ml de líquido/kg ou 1 a 1,5 ml por kcal consumida.
Para o medicamento OLIMEL N12E, a dose diária máxima é determinada com base na ingestão de aminoácidos, 26 ml/kg
corresponde a 2,0 g de aminoácidos/kg, 1,9 g de glicose/kg, 0,9 g de lipídios/kg. Para um doente com 70 kg de peso corporal,
isso corresponde a 1820 ml do medicamento OLIMEL N12E por dia, o que significa a ingestão de 138 g de aminoácidos, 133 g
de glicose e 64 g de lipídios (ou seja, 1171 kcal não proteicas e um total de 1723 kcal).
Na terapia de substituição renal contínua (CRRT):Para o medicamento OLIMEL N12E, a dose diária máxima é determinada
com base na ingestão de aminoácidos, 33 ml/kg corresponde a 2,5 g de aminoácidos/kg, 2,4 g de glicose/kg, 1,2 g de lipídios/kg.
Para um doente com 70 kg de peso corporal, isso corresponde a 2310 ml do medicamento OLIMEL N12E por dia, o que significa
a ingestão de 175 g de aminoácidos, 169 g de glicose e 81 g de lipídios (ou seja, 1486 kcal não proteicas e um total de 2187 kcal).
Em doentes com obesidade mórbida: A dose deve ser calculada com base no peso corporal ideal (em inglês, ideal body weight - IBW).
Para o medicamento OLIMEL N12E, a dose diária máxima é determinada com base na ingestão de aminoácidos, 33 ml/kg
IBW corresponde a 2,5 g de aminoácidos/kg, 2,4 g de glicose/kg, 1,2 g de lipídios/kg. Para um doente com 70 kg de peso corporal,
isso corresponde a 2310 ml do medicamento OLIMEL N12E por dia, o que significa a ingestão de 175 g de aminoácidos, 169 g
de glicose e 81 g de lipídios (ou seja, 1486 kcal não proteicas e um total de 2187 kcal).
Geralmente, a velocidade de administração deve ser aumentada gradualmente durante a primeira hora, e em seguida, a velocidade
de infusão deve ser ajustada de acordo com a dose, volume diário do medicamento administrado e duração da infusão.
Para o medicamento OLIMEL N12E, a velocidade máxima de infusão é de 1,3 ml/kg/h, o que corresponde a 0,10 g de aminoácidos/kg/h,
0,10 g de glicose/kg/h e 0,05 g de lipídios/kg/h.
Crianças com mais de 2 anos de idade e adolescentes
Não foram realizados estudos nessa população pediátrica.
A dosagem depende do gasto energético do doente, estado clínico, peso corporal e capacidade de metabolizar os componentes
do medicamento OLIMEL N12E, bem como dos nutrientes energéticos ou proteicos adicionais administrados por via oral/enteral;
portanto, é necessário escolher o tamanho do saco apropriado. Além disso, a necessidade diária de líquidos, azoto e energia diminui
com a idade. Foram considerados dois grupos, de 2 a 11 anos e de 12 a 18 anos.
Para o medicamento OLIMEL N12E, no grupo etário de 2 a 11 anos, os fatores limitantes para a dose diária são as concentrações
de aminoácidos e magnésio. Nesse grupo etário, o fator limitante para a velocidade de administração por hora é a concentração
de aminoácidos. No grupo etário de 12 a 18 anos, os fatores limitantes para a dose diária são as concentrações de aminoácidos e magnésio.
Nesse grupo etário, o fator limitante para a velocidade de administração por hora é a concentração de aminoácidos. Os valores resultantes
são apresentados abaixo:
| Componente | 2 a 11 anos | 12 a 18 anos | ||
| Recomendado | Volume máximo de OLIMEL N12E | Recomendado | Volume máximo de OLIMEL N12E | |
| Dose diária máxima | ||||
| Líquidos (ml/kg/dia) |
| 33 |
| 26 |
| Aminoácidos (g/kg/dia) |
| 2,5 |
| 2 |
| Glicose (g/kg/dia) | 1,4 – 8,6 | 2,4 | 0,7 - 5,8 | 1,9 |
| Lipídios (g/kg/dia) | 0,5 - 3 | 1,2 | 0,5 - 2 (até 3) | 0,9 |
| Valor energético total (kcal/kg/dia) |
| 31,4 |
| 24,7 |
| Velocidade máxima de administração por hora | ||||
| OLIMEL N12E (ml/kg/h) | 2,6 | 1,6 | ||
| Aminoácidos (g/kg/h) | 0,20 | 0,20 | 0,12 | 0,12 |
| Glicose (g/kg/h) | 0,36 | 0,19 | 0,24 | 0,12 |
| Lipídios (g/kg/h) | 0,13 | 0,09 | 0,13 | 0,06 |
Geralmente, a velocidade de administração deve ser aumentada gradualmente durante a primeira hora, e em seguida, a velocidade
de infusão deve ser ajustada de acordo com a dose, volume diário do medicamento administrado e duração da infusão.
Em geral, em crianças pequenas, é recomendado iniciar a infusão com uma dose diária baixa e aumentá-la gradualmente até
a dose máxima (ver acima).
A velocidade máxima de administração em crianças de 2 a 11 anos é de 2,6 ml/kg/h, e em crianças de 12 a 18 anos é de 1,6 ml/kg/h.
Modo de administração
Apenas para uso único.
Recomenda-se que, após a abertura, o conteúdo do saco seja usado imediatamente e não armazenado para uma infusão posterior.
Após a mistura, obtém-se uma mistura homogênea com aspeto leitoso.
As instruções para a preparação e administração da emulsão para infusão estão no ponto 6.6 do RCM.
Devido à alta osmolalidade do OLIMEL N12E, deve ser administrado apenas por via intravenosa central.
O tempo de administração recomendado para o saco de nutrição parenteral é de 12 a 24 horas.
O tratamento com nutrição parenteral pode ser continuado por tanto tempo quanto necessário, dependendo do estado clínico do doente.
C. INCOMPATIBILIDADES FARMACÊUTICAS
Não adicionar nenhum medicamento ou substância a qualquer um dos componentes do saco ou à emulsão pronta para uso sem
confirmar previamente a compatibilidade e estabilidade do produto resultante (especialmente a estabilidade da emulsão lipídica).
Incompatibilidades podem ocorrer devido à acidez excessiva (pH baixo) ou teor inadequado de cátions divalentes (Ca e Mg), que podem
desestabilizar a emulsão lipídica.
Assim como na preparação de outras misturas para nutrição parenteral, deve-se considerar a relação entre o teor de cálcio e fosfatos.
Um excesso de cálcio e fosfato, especialmente na forma de sais inorgânicos, pode causar a formação de depósitos de fosfato de cálcio.
OLIMEL N12E contém íons de cálcio, o que aumenta o risco de formação de coágulos em preparados de sangue ou componentes sanguíneos
com citrato como anticoagulante/conservante.
Não misturar ou administrar ceftriaxon simultaneamente com soluções intravenosas que contenham cálcio, incluindo o medicamento
OLIMEL N12E, pela mesma linha de infusão (por exemplo, por um conector em forma de Y) devido ao risco de formação de sais de cálcio
da ceftriaxon (ver pontos 4.4 e 4.5 do RCM). Ceftriaxon e soluções que contenham cálcio podem ser administrados sequencialmente,
se as linhas de infusão forem inseridas em locais diferentes ou forem trocadas ou limpas com solução fisiológica de cloreto de sódio entre
as infusões, para evitar a formação de depósitos.
Devido ao risco de formação de depósitos, o medicamento OLIMEL N12E não deve ser administrado pela mesma linha de infusão
ou adicionado ao antibiótico amplicilina ou ao medicamento anticonvulsivante fosfenitoína.
Deve verificar a compatibilidade com soluções administradas simultaneamente pela mesma linha de infusão, cateter ou cânula.
Devido ao risco de pseudoaglutinação, não deve administrar este medicamento antes, durante ou após a administração de sangue pela
mesma linha de infusão.
D. PRECAUÇÕES ESPECIAIS PARA ELIMINAÇÃO E PREPARO DO MEDICAMENTO PARA USO
Revisão dos estágios de preparo do OLIMEL N12E antes da administração está apresentada na Figura 1.
Abertura
Remover o saco protetor.
Descartar o sachê que absorve oxigênio.
Certificar-se de que o saco ou selos não estão danificados. Use apenas se o saco estiver não danificado e os selos estiverem
intactos (ou seja, o conteúdo das 3 câmaras não foi misturado), as soluções de aminoácidos e glicose são transparentes, incolores
ou ligeiramente amareladas, praticamente livres de partículas visíveis e a emulsão lipídica é homogênea com aspeto leitoso.
Mistura das soluções e emulsões
Antes de romper os selos, certificar-se de que o medicamento está à temperatura ambiente.
Iniciar a partir da parte superior do saco (perto da alça), girar o saco com as duas mãos. Os selos desaparecerão a partir da
parte dos portos. Continuar a girar o saco até que os selos se abram até metade de sua extensão.
Misturar, girando o saco pelo menos 3 vezes.
Após a mistura, o medicamento tem a forma de uma emulsão homogênea com aspeto leitoso.
Componentes adicionais
A capacidade do saco é suficiente para permitir a adição de vitaminas, eletrólitos e oligoelementos.
Todos os aditivos (incluindo vitaminas) devem ser introduzidos na emulsão pronta (após a ruptura das soldas e após a mistura do conteúdo das 3 câmaras).
As vitaminas também podem ser adicionadas à câmara que contém glicose antes da preparação da emulsão pronta (antes da ruptura das soldas e antes da mistura do conteúdo das três câmaras).
Os componentes adicionais devem ser introduzidos por pessoal qualificado em condições assépticas.
Para o produto OLIMEL N12E, podem ser adicionados eletrólitos, fosfatos inorgânicos/orgânicos e produtos multivitamínicos disponíveis no mercado (como Cernevit) e produtos que contenham vários oligoelementos (como Nutryelt). A concentração total máxima dos componentes adicionais listados na tabela abaixo foi determinada com base em dados de estabilidade e não deve ser considerada como recomendação de dosagem. A suplementação deve ser ditada pelas necessidades clínicas do paciente e não deve exceder as diretrizes nutricionais. Ao alcançar a concentração total máxima, deve-se considerar a quantidade de eletrólitos já presentes no saco.
A compatibilidade com produtos de diferentes fontes pode variar, e os profissionais de saúde devem realizar controles adequados ao misturar o produto OLIMEL N12E com outras soluções para administração parenteral.
| Componentes adicionais possíveis por 1000 ml do produto OLIMEL N12E (para crianças e adolescentes) | |||
| Conteúdo | Aditivo máximo | Conteúdo máximo | |
| Sódio | 35 mmol | 115 mmol | 150 mmol |
| Potássio | 30 mmol | 120 mmol | 150 mmol |
| Magésio | 4,0 mmol | 1,6 mmol | 5,6 mmol |
| Cálcio | 3,5 mmol | 1,5 mmol | 5,0 mmol |
| Fosfatos inorgânicos | 0 mmol | 10 mmol Pi ou 10 mmol Po | 10 mmol Pi + 15 mmol Po ou 25 mmol Poa,b |
| Fosfatos orgânicos | 15 mmola | ||
| Outros componentes adicionais (oligoelementos, vitaminas, selênio e zinco)c | |||
| Oligoelementos – Nutryelt Pediátricod | 1 frasco por saco (10 ml de solução concentrada) | ||
| Vitaminas e | 1 frasco (liofilizado) | ||
| Selênio | 60 µg por saco | ||
| Zinco | 3 mg por saco | ||
| Componentes adicionais possíveis por 1000 ml do produto OLIMEL N12E (para adultos) | |||
| Conteúdo | Aditivo máximo | Conteúdo máximo | |
| Sódio | 35 mmol | 115 mmol | 150 mmol |
| Potássio | 30 mmol | 120 mmol | 150 mmol |
| Magésio | 4,0 mmol | 1,6 mmol | 5,6 mmol |
| Cálcio | 3,5 mmol | 1,5 mmol | 5,0 mmol |
| Fosfatos inorgânicos | 0 mmol | 10 mmol Pi ou 10 mmol Po | 10 mmol Pi + 15 mmol Po ou 25 mmol Poa,b |
| Fosfatos orgânicos | 15 mmola | ||
| Outros componentes adicionais (oligoelementos, vitaminas, selênio e zinco)c | |||
| Oligoelementos - Nutryelt d | 2 frascos por saco (10 ml de solução concentrada) | ||
| Vitaminas - Cernevite | 1 frasco (5 ml de liofilizado) | ||
| Selênio | 500 µg por saco | ||
| Zinco | 20 mg por saco | ||
Ao introduzir componentes adicionais, deve-se:
- controlar as condições assépticas,
- preparar o local de injeção no saco,
- perfurar o local de injeção e injetar os componentes adicionais usando uma agulha para injeção ou um dispositivo para preparar o produto medicinal,
- misturar o conteúdo do saco com os componentes adicionais.
Prazo de validade após mistura
Foi demonstrada a estabilidade química e física durante o uso por 7 dias a uma temperatura de 2°C a 8°C e subsequentemente por 48 horas de armazenamento a uma temperatura não superior a 30°C.
Do ponto de vista microbiológico, o produto deve ser usado imediatamente. Se o produto não for usado imediatamente, durante o uso, o tempo e as condições de armazenamento até o momento de uso são de responsabilidade do usuário, e o armazenamento não deve durar mais de 24 horas a uma temperatura de 2°C a 8°C, a menos que a reconstituição tenha ocorrido em condições assépticas controladas e validadas.
Prazo de validade após adição de componentes adicionais
Após a adição de componentes adicionais, foi demonstrada a estabilidade química e física durante o uso por 7 dias a uma temperatura de 2°C a 8°C e subsequentemente por 48 horas de armazenamento a uma temperatura não superior a 30°C.
Do ponto de vista microbiológico, o produto deve ser usado imediatamente. Se o produto não for usado imediatamente, durante o uso, o tempo e as condições de armazenamento até o momento de uso são de responsabilidade do usuário, e o armazenamento não deve durar mais de 24 horas a uma temperatura de 2°C a 8°C, a menos que a adição de componentes adicionais tenha ocorrido em condições assépticas controladas e validadas.
Preparação da infusão
Controlar as condições assépticas.
Suspender o saco.
Remover o protetor plástico do porto de administração do produto medicinal.
Introduzir firmemente a agulha do conjunto de infusão no porto de administração do produto medicinal.
Figura 1. Etapas de preparação do produto OLIMEL para administração


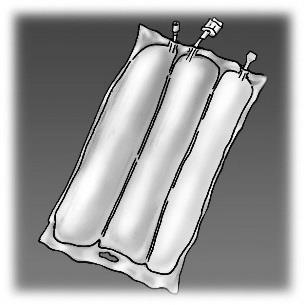
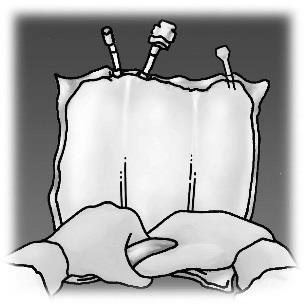
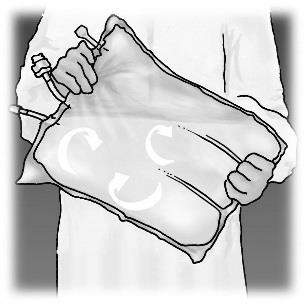
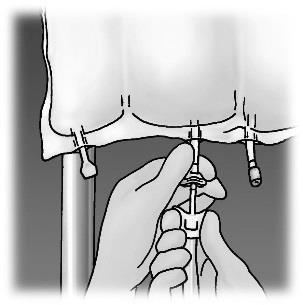
Administração
Apenas para uso único.
Administrar o produto apenas após a ruptura das soldas que separam as 3 câmaras e após a mistura do conteúdo delas.
Deve-se garantir que na emulsão pronta para infusão não ocorra a separação de fases.
Após a abertura do saco, o conteúdo deve ser utilizado imediatamente. Não é permitido armazenar o saco aberto para a próxima infusão. Não reconectar sacos parcialmente usados.
Para evitar a possibilidade de formação de embolias aéreas causadas pela presença de gás no primeiro saco, não conectar sacos em série.
Qualquer resíduo do produto não utilizado ou seus resíduos e todo o conjunto de infusão devem ser destruídos.
Extravasação
O local de inserção do cateter deve ser monitorado regularmente para sinais de extravasação.
Em caso de extravasação, a administração do produto deve ser interrompida imediatamente, deixando o cateter ou a cânula no local para iniciar o tratamento imediatamente. Se possível, antes de remover o cateter/cânula, deve-se realizar uma aspiração do líquido através do cateter/cânula para reduzir a quantidade de líquido nos tecidos.
Dependendo do tipo de produto extravasado (incluindo o produto(s) misturado(s) com o produto OLIMEL N12E, se aplicável) e do grau/extentão do possível dano, devem ser tomadas medidas apropriadas.
Opções de tratamento podem incluir tratamento não farmacológico, farmacológico e (ou) intervenção cirúrgica. Em caso de extravasação significativa, deve-se consultar um cirurgião plástico dentro de 72 horas.
O local de extravasação deve ser monitorado a cada 4 horas durante as primeiras 24 horas e, subsequentemente, uma vez ao dia.
Não deve-se reiniciar a infusão na mesma veia central.
Baxter e Olimel são marcas registradas da Baxter International Inc.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorBaxter S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Olimel N12eForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médica
Alternativas a Olimel N12e noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Olimel N12e em Espanha
Alternativa a Olimel N12e em Ukraine
Médicos online para Olimel N12e
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Olimel N12e – sujeita a avaliação médica e regras locais.














