
Smofkabiven Nutribase

Pergunte a um médico sobre a prescrição de Smofkabiven Nutribase

Como usar Smofkabiven Nutribase
Folheto informativo: informação para o utilizador
SmofKabiven Nutribase, emulsão para infusão
Deve ler atentamente o conteúdo do folheto antes de usar o medicamento, pois contém
informações importantes para o doente.
- Deve conservar este folheto para o poder reler se necessário.
- Em caso de dúvidas, deve consultar o médico, farmacêutico ou enfermeiro.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é SmofKabiven Nutribase e para que é usado
- 2. Informações importantes antes de usar SmofKabiven Nutribase
- 3. Como usar SmofKabiven Nutribase
- 4. Efeitos não desejados
- 5. Como conservar SmofKabiven Nutribase
- 6. Conteúdo do pacote e outras informações
1. O que é SmofKabiven Nutribase e para que é usado
SmofKabiven Nutribase é uma emulsão para infusão, administrada ao doente por via intravenosa (infusão).
O pacote do medicamento é um saco plástico que contém aminoácidos (componentes necessários para a produção
de proteínas), glicose (carboidratos), gorduras (lípidos) e sais (eletrólitos). O medicamento pode ser usado em doentes adultos
e crianças com 2 anos de idade ou mais.
O pessoal médico qualificado administra SmofKabiven Nutribase quando outras formas de nutrição são
insuficientes ou impossíveis.
2. Informações importantes antes de usar SmofKabiven Nutribase
Não use SmofKabiven Nutribase se o doente tiver:
- alergia às substâncias ativas ou a qualquer um dos outros componentes do medicamento (listados no ponto 6);
- alergia a proteínas de peixe ou ovos;
- alergia a amendoins ou soja (SmofKabiven Nutribase contém óleo de soja);
- níveis de gordura no sangue muito altos (hiperlipidemia);
- problemas graves de fígado;
- problemas graves de coagulação do sangue (problemas graves de coagulação);
- doenças metabólicas congénitas de aminoácidos;
- doenças renais graves, sem possibilidade de diálise ou hemofiltração;
- choque agudo (problemas graves de circulação do sangue);
- níveis de glicose no sangue não controlados (hiperglicemia);
- níveis elevados no sangue (soro) de qualquer um dos eletrólitos presentes no medicamento SmofKabiven Nutribase;
- líquido nos pulmões (edema pulmonar agudo);
- excesso de líquido no organismo (sobrecarga de líquido);
- insuficiência cardíaca não tratada;
- problemas de coagulação do sangue (síndrome hemofagocitária);
- estado geral instável, por exemplo, estado pós-traumático grave, diabetes não controlada, ataque cardíaco agudo, acidente vascular cerebral, trombose, acidose metabólica (problema devido a uma quantidade excessiva de substâncias ácidas no sangue), infecção grave (sepse grave), coma, desidratação (desidratação hipotónica).
Não use SmofKabiven Nutribase em recém-nascidos e crianças com menos de 2 anos de idade.
Precauções e advertências
Antes de iniciar o tratamento com SmofKabiven Nutribase, deve discutir com o médico se o doente tiver:
- doenças renais;
- diabetes;
- pancreatite;
- doenças do fígado;
- problemas da tiróide (problemas da tiróide);
- sepse (infecção grave).
Se durante a infusão ocorrer febre, erupção cutânea, inchaço, dificuldade em respirar, arrepios, suor, náuseas ou vómitos, deve informar imediatamente o pessoal médico qualificado, pois esses sintomas podem ser causados por uma reação alérgica ou por uma dose excessiva do medicamento.
O médico pode recomendar exames de sangue regulares para verificar as funções do fígado e outros
parâmetros.
Crianças e adolescentes
SmofKabiven Nutribase não é destinado a recém-nascidos ou crianças com menos de 2 anos de idade. SmofKabiven Nutribase pode ser administrado a crianças e adolescentes com 2 a 18 anos de idade.
SmofKabiven Nutribase e outros medicamentos
Deve informar o médico sobre todos os medicamentos que o doente está a tomar atualmente ou recentemente, bem como sobre os medicamentos que o doente planeia tomar, incluindo os que são vendidos sem receita médica.
Gravidez e amamentação
Se a doente estiver grávida, suspeitar que possa estar grávida ou planeiar ter um filho, deve consultar o médico antes de usar este medicamento.
Não há dados sobre o uso do medicamento SmofKabiven Nutribase durante a gravidez. SmofKabiven Nutribase é administrado a mulheres grávidas apenas quando o médico considera que é necessário. SmofKabiven Nutribase pode ser administrado durante a gravidez sob prescrição médica.
Não há dados disponíveis sobre o uso do medicamento SmofKabiven Nutribase em mulheres que amamentam.
Os componentes e metabólitos da nutrição parenteral, como SmofKabiven Nutribase, passam para o leite materno. A nutrição parenteral pode ser necessária durante a amamentação. SmofKabiven Nutribase pode ser administrado a mulheres que amamentam apenas após uma avaliação cuidadosa do risco e benefício pelo médico.
Condução de veículos e utilização de máquinas
Não se aplica, pois SmofKabiven Nutribase é usado em ambiente hospitalar.
3. Como usar SmofKabiven Nutribase
Este medicamento deve ser sempre usado de acordo com as recomendações do médico. Em caso de dúvida, deve consultar o médico.
O médico escolhe a dose individual com base no peso e estado clínico do doente. SmofKabiven Nutribase é administrado por pessoal médico qualificado.
Uso de uma dose maior do que a recomendada de SmofKabiven Nutribase
É pouco provável que o doente receba uma dose excessiva de SmofKabiven Nutribase, pois o medicamento é administrado por pessoal médico qualificado.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não ocorram em todos.
Efeitos não desejados frequentes(podem ocorrer em até 1 em cada 10 doentes):
leve aumento da temperatura corporal.
Efeitos não desejados menos frequentes(podem ocorrer em até 1 em cada 100 doentes): aumento significativo das enzimas hepáticas no sangue, perda de apetite, náuseas, vómitos, arrepios, tontura e dor de cabeça.
Efeitos não desejados raros(podem ocorrer em até 1 em cada 1000 doentes): pressão arterial baixa ou alta, dificuldade em respirar, ritmo cardíaco acelerado (taquicardia).
Reações de hipersensibilidade (que podem causar sintomas como inchaço, febre, queda da pressão arterial, erupção cutânea, bolhas, vermelhidão, dor de cabeça). Sensação de calor e frio. Palidez. Leve cianose dos lábios e pele (relacionada à desoxigenação do sangue). Dor no pescoço, nas costas, nos ossos, no peito e na região lombar.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Não Desejados de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos Médicos e Produtos Biocidas
Al. Jerozolimskie 181C, 02-222 Varsóvia
telefone: +48 22 49 21 301, fax: +48 22 49 21 309
site: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao responsável pelo medicamento.
A notificação de efeitos não desejados permite reunir mais informações sobre a segurança do medicamento.
5. Como conservar SmofKabiven Nutribase
O medicamento deve ser conservado em local não visível e inacessível a crianças.
Não conservar a uma temperatura superior a 25°C. Não congelar. Conservar no saco exterior.
Não use este medicamento após a data de validade impressa no saco e na caixa de cartão.
A data de validade é o último dia do mês indicado.
6. Conteúdo do pacote e outras informações
O que contém SmofKabiven Nutribase
As substâncias ativas do medicamento são:
g por 1000 ml
| alanina | 4,7 |
| arginina | 4,1 |
| glicina | 3,7 |
| histidina | 1,0 |
| isoleucina | 1,7 |
| leucina | 2,5 |
| lisina (como acetato) | 2,2 |
| metionina | 1,5 |
| fenilalanina | 1,7 |
| prolina | 3,8 |
| serina | 2,2 |
| taurina | 0,34 |
| treonina | 1,5 |
| triptofano | 0,68 |
| tirosina | 0,14 |
| valina | 2,1 |
| cloreto de cálcio (na forma de composto di-hidratado) | 0,19 |
| glicerofosfato de sódio (na forma de composto hidratado) | 1,4 |
| sulfato de magnésio (na forma de composto heptahidratado) | 0,41 |
| cloreto de potássio | 1,5 |
| acetato de sódio (na forma de composto tri-hidratado) | 1,1 |
| sulfato de zinco (na forma de composto heptahidratado) | 0,0044 |
| glicose (na forma de composto monohidratado) | 89 |
| óleo de soja purificado | 12 |
| triglicerídeos de ácidos graxos saturados de cadeia média | 12 |
| óleo de oliva purificado | 9,8 |
| óleo de peixe rico em ácidos graxos ômega-3 | 5,9 |
Os outros componentes (substâncias auxiliares) são: glicerol, fosfolipídios purificados de ovo de galinha, alfa-tocoferol, hidróxido de sódio (para ajustar o pH), oleato de sódio, ácido acético glacial (para ajustar o pH) e água para injeção.
Como é SmofKabiven Nutribase e o que o pacote contém
SmofKabiven Nutribase, emulsão para infusão, está disponível em sacos tricômora, nos quais uma
compartimento contém solução de glicose, o outro aminoácidos e o terceiro emulsão lipídica. As soluções de glicose
e aminoácidos são transparentes, incolores a ligeiramente amareladas, sem partículas sólidas. A emulsão lipídica é branca e homogênea.
Tamanhos do pacote:
1 x 1026 ml, 4 x 1026 ml
1 x 1539 ml, 4 x 1539 ml
1 x 2052 ml, 4 x 2052 ml
1 x 2565 ml, 3 x 2565 ml
Nem todos os tamanhos do pacote precisam estar disponíveis.
Responsável pelo medicamento e fabricante
Fresenius Kabi AB
Rapsgatan 7
751 74 Uppsala
Suécia
Para obter informações mais detalhadas, deve contactar o representante do responsável pelo medicamento:
Fresenius Kabi Portugal, Lda.
Rua do Centro Empresarial do Aeroporto, n.º 31, 3.º andar, sala 2
4470-177 Maia
telefone: +351 229 435 610
Este medicamento está autorizado para comercialização nos estados membros do Espaço Económico Europeu sob as seguintes denominações:
Áustria
em curso
Bélgica
SmofKabiven Nutribase, emulsão para infusão
SmofKabiven Nutribase, émulsion pour perfusion
SmofKabiven Nutribase, Emulsion zur Infusion
Bulgária
СмофКабивен Централ Нутрибейз инфузионна емулсия
Croácia
SmofKabiven Nutribase, emulsija za infuziju
Chipre
SmofKabiven Nutribase
Dinamarca
SmofKabiven Nutribase
Estónia
SmofKabiven Nutribase
Finlândia
SmofKabiven Nutribase
França
SmofKabiven Nutribase, émulsion pour perfusion
Grécia
em curso
Espanha
SmofKabiven Nutribase, emulsión para perfusión
Países Baixos
SmofKabiven Nutribase, emulsie voor infusie
Irlanda
SmofKabiven Nutribase
Islândia
SmofKabiven Nutribase, innrennslislyf, fleyti
Lituânia
em curso
Luxemburgo
em curso
Letónia
SmofKabiven Nutribase, emulsija infūzijām
Alemanha
em curso
Noruega
SmofKabiven Nutribase, infusjonsvæske, emulsjon
Polónia
SmofKabiven Nutribase
Portugal
SmofKabiven Nutribase
República Checa
SmofKabiven Nutribase
Roménia
SmofKabiven Nutribase, emulsie perfuzabilă
Eslováquia
SmofKabiven Nutribase
Eslovénia
SmofKabiven Nutribase, emulzija za infundiranje
Suécia
SmofKabiven Nutribase
Hungria
SmofKabiven Nutribase, emulziós infúzió
Reino Unido
SmofKabiven Nutribase
Data da última revisão do folheto:
---------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas a profissionais de saúde (para obter mais informações, consulte a Característica do Produto Farmacêutico).
Precauções e advertências para a administração
Para evitar riscos associados à infusão a uma velocidade maior do que a recomendada, recomenda-se que seja realizada de forma contínua e controlada, sempre que possível com o uso de uma bomba de volume.
Como o uso de uma veia central para a infusão está associado a um risco aumentado de infecção, durante a colocação e manuseio do cateter, é recomendado seguir estritamente as normas de procedimento asséptico para evitar qualquer infecção.
Recomenda-se controlar os níveis de glicose e eletrólitos no soro, osmolalidade e o balanço de líquidos e equilíbrio ácido-básico, bem como realizar testes enzimáticos do fígado.
Em caso de ocorrerem sinais ou sintomas de reação anafilática (como febre, arrepios, erupção cutânea ou dificuldade em respirar), a infusão deve ser interrompida imediatamente.
Não se deve administrar SmofKabiven Nutribase juntamente com sangue no mesmo conjunto de infusão, devido ao risco de pseudoaglutinação.
Método de administração
Administração intravenosa, infusão em veia central.
Para garantir a nutrição parenteral completa, deve adicionar micronutrientes, vitaminas e, se necessário, eletrólitos (considerando os eletrólitos já presentes no medicamento SmofKabiven Nutribase), de acordo com as necessidades do doente. A mistura de componentes dentro do saco SmofKabiven Nutribase só deve ser feita se a compatibilidade for comprovada, ver ponto: Precauções especiais para a eliminação e preparação do medicamento para uso.
Posologia
Doentes adultos
Dose recomendada
O intervalo de dose é de 18 a 40 ml de SmofKabiven Nutribase/kg de peso corporal/dia, o que fornece de 0,10 a 0,22 g de nitrogênio/kg de peso corporal/dia (de 0,6 a 1,4 g de aminoácidos/kg de peso corporal/dia) e de 16 a 35 kcal/kg de peso corporal/dia de energia total (de 13 a 30 kcal/kg de peso corporal/dia de energia não proteica).
Velocidade de infusão
A velocidade máxima de infusão de glicose é de 0,25 g/kg de peso corporal/hora, de aminoácidos 0,1 g/kg de peso corporal/hora e de gorduras 0,15 g/kg de peso corporal/hora.
A velocidade de infusão não deve exceder 2,8 ml/kg de peso corporal/hora (o que corresponde a 0,25 g de glicose, 0,09 g de aminoácidos e 0,11 g de gorduras/kg de peso corporal/hora).
O tempo de infusão recomendado é de 6,5 a 24 horas.
Dose diária máxima
A dose diária máxima depende do estado clínico do doente e pode variar mesmo de um dia para o outro.
A dose diária máxima recomendada é de 40 ml/kg de peso corporal/dia.
Crianças e adolescentes
Crianças de 2 a 11 anos de idade
Dose recomendada
A dose de até 40 ml/kg de peso corporal/dia deve ser ajustada regularmente às necessidades do doente pediátrico, que variam muito mais do que nos doentes adultos.
Velocidade de infusão
A velocidade de infusão não deve exceder 3,4 ml/kg de peso corporal/hora (o que corresponde a 0,30 g de glicose/kg de peso corporal/hora, 0,12 g de aminoácidos/kg de peso corporal/hora e 0,13 g de gorduras/kg de peso corporal/hora).
O tempo de infusão recomendado é de 5 a 24 horas. Além de situações especiais e com monitorização cuidadosa, quando a velocidade máxima de infusão recomendada for usada, o tempo de infusão não deve exceder 11 horas e 45 minutos.
Dose diária máxima
A dose diária máxima é variável dependendo do estado clínico do doente e pode mudar mesmo de um dia para o outro. A dose diária máxima recomendada é de 40 ml/kg de peso corporal/dia.
Adolescentes de 12 a 18 anos de idade
Em adolescentes, SmofKabiven Nutribase pode ser administrado como em doentes adultos.
Precauções especiais para a eliminação e preparação do medicamento para uso
Não use se o pacote estiver danificado.
Use apenas se as soluções de aminoácidos e glicose forem transparentes, incolores a ligeiramente amareladas, e a emulsão lipídica for branca e homogênea .O conteúdo das três câmaras separadas deve ser misturado antes do uso e, se necessário, antes de adicionar outros componentes através do porto designado para esse fim.
Após a remoção das proteções, deve girar o saco três vezes para misturar completamente todos os componentes do medicamento e obter uma mistura homogênea, na qual não devem ser visíveis sinais de separação de fases.
Para uso único. Qualquer medicamento não utilizado ou resíduos devem ser destruídos.
Qualquer medicamento não utilizado ou resíduos devem ser eliminados de acordo com as regulamentações locais.
Compatibilidade
A tabela de compatibilidade a seguir apresenta as possibilidades de adicionar medicamentos Dipeptiven, Supliven, Vitalipid N Adult/Infant e Soluvit N (em pó). Os dados disponíveis confirmam a possibilidade de adicionar esses medicamentos ao saco ativado, de acordo com a tabela abaixo:
Nota: esta tabela tem como objetivo apresentar a compatibilidade. Não constitui diretrizes para a posologia.
Qualquer aditivo deve ser misturado com o medicamento em condições assépticas.
Validade após a mistura
Foi demonstrada a estabilidade física e química do conteúdo misturado do saco tricômora por 36 horas a 25°C. Do ponto de vista microbiológico, o medicamento deve ser usado imediatamente. Caso contrário, o período de validade durante o uso e as condições de armazenamento antes da administração são da responsabilidade do utilizador. Este período não deve exceder 24 horas a 2-8°C.
| Conteúdo máximo total | |
| SmofKabiven Nutribase | 1026 ml, 1539 ml, 2052 ml e 2565 ml |
| Produto adicionado | Volume |
| Dipeptiven |
|
| Supliven |
|
| Soluvit N |
|
| Vitalipid N Adult/Infant |
|
Validade após a mistura com aditivos
Do ponto de vista microbiológico, o medicamento deve ser usado imediatamente após a adição de outros componentes.
SmofKabiven Nutribase Instruções para a preparação do saco para uso
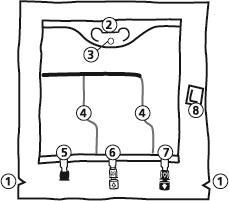
- 1. Corte no saco exterior
- 2. Alça do saco
- 3. Orifício de suspensão do saco
- 4. Soldas que separam as câmaras do saco
- 5. Porto cego (usado apenas na produção)
- 6. Porto para adicionar substâncias
- 7. Porto de infusão
- 8. Absorvedor de oxigênio
1. Remoção do saco exterior
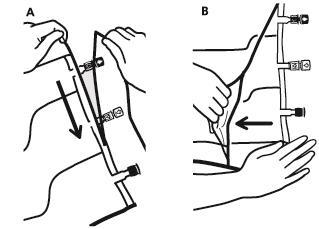
- Para remover o saco exterior, deve colocá-lo na horizontal e, começando pelo corte que se encontra perto dos portos, rasgar ao longo da borda superior (A).
- Em seguida, rasgar o saco exterior ao longo da borda longa, remover e descartar juntamente com o absorvedor de oxigênio (B).
2. Mistura
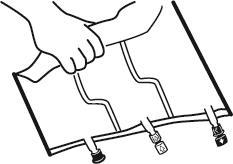
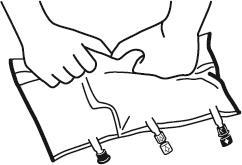
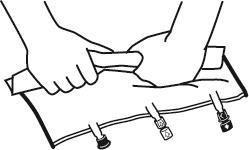
- Colocar o saco sobre uma superfície plana.
- Iniciar a partir da alça, enrolar firmemente o saco na direção dos portos, primeiro com a mão direita e, em seguida, aplicando pressão constante com a mão esquerda, até que as soldas verticais se abram. Elas se abrem sob a pressão do líquido. As soldas também podem ser abertas antes de remover o saco exterior. Nota: o líquido mistura-se facilmente, mesmo que a solda horizontal permaneça intacta.
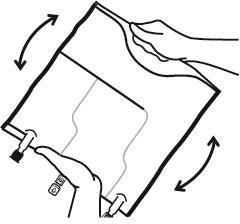
- Misturar o conteúdo das três câmaras virando o saco três vezes, o que deve garantir a mistura completa dos componentes.
3. Preparativos finais
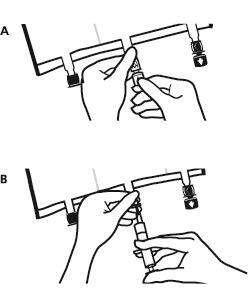
- Colocar o saco novamente sobre uma superfície plana e nivelada. Imediatamente antes de adicionar substâncias, remover a tampa de uso único que protege o porto branco para adicionar substâncias (A). Nota: a membrana do porto para adicionar substâncias é estéril.
- Segurar a base do porto para adicionar substâncias. Introduzir a agulha e injetar as substâncias adicionais (com compatibilidade conhecida) através do centro do local de injeção (B).
- Misturar cuidadosamente o conteúdo do saco após cada adição de componentes, virando o saco três vezes após cada adição. Use seringas com agulhas de diâmetro 18 a 23 G e comprimento máximo de 40 mm.
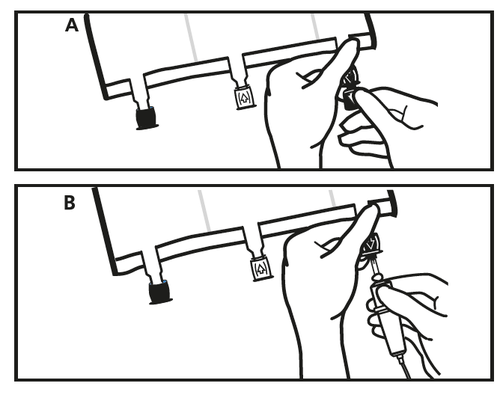
- Imediatamente antes de conectar o conjunto de infusão, remover a tampa de uso único que protege o porto azul de infusão (A). Nota: a membrana do porto de infusão é estéril.
- Use conjuntos de infusão sem dispositivo de ar ou feche o dispositivo de ar.
- Segurar a base do porto de infusão.
- Introduzir a agulha do conjunto de infusão no porto de infusão. Para garantir uma fixação segura da agulha, deve introduzir toda a sua extensão. Nota: a superfície interna do porto de infusão é estéril.
4. Suspensão do saco
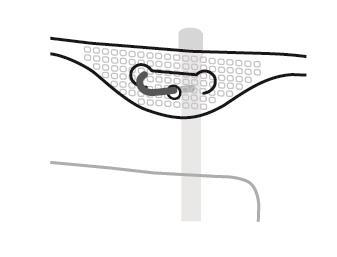
- Suspender o saco usando o orifício localizado abaixo da alça.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorFresenius Kabi AB
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Smofkabiven NutribaseForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médicaForma farmacêutica: Solução, -Substância ativa: combinationsNão requer receita médica
Alternativas a Smofkabiven Nutribase noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Smofkabiven Nutribase em Espanha
Alternativa a Smofkabiven Nutribase em Ukraine
Médicos online para Smofkabiven Nutribase
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Smofkabiven Nutribase – sujeita a avaliação médica e regras locais.














