

INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO

Pergunte a um médico sobre a prescrição de INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO

Como usar INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO
Introdução
Prospecto: informação para o utilizador
INTRALIPID 200 mg/ml emulsão para perfusão
Aceite de soja purificado
Leia todo o prospecto detenidamente antes de começar a usar o medicamento:
Se considera que algum dos efeitos adversos que sofre é grave ou se apercebe de qualquer efeito adverso não mencionado neste prospecto, informe o seu médico ou farmacêutico.
|
Neste prospecto:
- O que é INTRALIPID 200 mg/ml e para que é utilizado
- Antes de usar INTRALIPID 200 mg/ml
- Como usar INTRALIPID 200 mg/ml
- Possíveis efeitos adversos
- Conservação de INTRALIPID 200 mg/ml
- Informação adicional para o profissional de saúde
1. O que é INTRALIPID 200 mg/ml e para que é utilizado
INTRALIPID 200 mg/ml é uma emulsão lipídica para perfusão intravenosa. Apresenta-se em bolsas de plástico com sobrebolsa de 100 ml, 250 ml e 500 ml. Pertence ao grupo de medicamentos chamado soluções intravenosas para nutrição parenteral.
INTRALIPID está indicado em pacientes que necessitam de nutrição intravenosa para o aporte de energia e de ácidos graxos essenciais. INTRALIPID também está indicado em pacientes com deficiência de ácidos graxos essenciais (EFAD) que não podem manter ou restaurar um padrão normal de ácidos graxos essenciais mediante o aporte oral.
2. ANTES DE USAR INTRALIPID 200 mg/ml
Não use INTRALIPID 200 mg/ml:
INTRALIPID está contraindicado em pacientes com choque agudo e em pacientes com hiperlipemia severa. Insuficiência hepática grave. Síndrome hemofagocitótico.
Hipersensibilidade (alergia) à proteína de ovo, de soja ou de amendoim ou a qualquer um dos princípios ativos ou excipientes.
Tenha especial cuidado com INTRALIPID 200 mg/ml:
INTRALIPID deve ser administrado com precaução nos casos de alterações do metabolismo lipídico como insuficiência renal, na diabetes mellitus descompensada, pancreatite, alteração da função hepática, hipotireoidismo (se houver hipertrigliceridemia) e sepsis. Se for administrado INTRALIPID a pacientes nestas situações, é obrigatório realizar um controlo estrito da concentração de triglicéridos no soro.
Este produto contém aceite de soja e fosfolípidos de ovo, que muito raramente podem causar reações alérgicas. Foram observadas reações alérgicas cruzadas entre a soja e o amendoim.
INTRALIPID deve ser administrado com precaução a neonatos e prematuros com hiperbilirrubinemia e em casos de possível hipertensão pulmonar. Em neonatos, e particularmente em prematuros, com nutrição parenteral de longa duração, deve monitorizar-se o recuento plaquetário, o teste hepático e a concentração de triglicéridos no soro.
INTRALIPID pode interferir com certas determinações de laboratório (bilirrubina, lactato desidrogenase, saturação de oxigênio, Hb, etc), se a amostra de sangue for tomada antes de os lípidos terem sido adequadamente eliminados do fluxo sanguíneo. Os lípidos são eliminados após um período livre de lípidos de 5-6 horas, na maioria dos pacientes.
Quando for utilizado em recém-nascidos e crianças menores de 2 anos, a solução (nas bolsas e equipamentos de administração) deve ser protegida da exposição à luz até que termine a administração. A exposição de INTRALIPID à luz ambiental, em especial após misturar com oligoelementos ou vitaminas, gera peróxidos e outros produtos de degradação que podem ser reduzidos se o produto for protegido da exposição à luz.
Uso de outros medicamentos:
Alguns fármacos, como a insulina, podem interferir sobre o sistema corporal da lipase. No entanto, este tipo de interação tem apenas uma importância clínica menor.
A heparina, a doses terapêuticas, produz um aumento transitório da lipólise plasmática, o que dá lugar a um descenso transitório do aclaramento de triglicéridos devido a uma depleção da lipoproteína lipase.
O aceite de soja contém vitamina K1, o que deve ser tido em conta nos pacientes em tratamento com derivados cumarínicos, pois estes interferem com a vitamina K1.
Este medicamento não deve ser misturado com outros produtos, se não existirem dados de compatibilidade disponíveis.
Informar o seu médico ou farmacêutico se está utilizando ou utilizou recentemente qualquer outro medicamento, mesmo os adquiridos sem receita.
Gravidez e lactação:
Consulte o seu médico ou farmacêutico antes de utilizar qualquer medicamento.
Não foram reportados efeitos adversos durante a gravidez e a lactação.
Condução e uso de máquinas:
Não são de esperar efeitos sobre a capacidade para conduzir e utilizar máquinas.
3. Como USAR INTRALIPID 200 mg/ml
Siga exatamente as instruções de administração de Intralipid 200 mg/ml indicadas pelo seu médico. Consulte o seu médico ou farmacêutico se tiver dúvidas.
Devido ao risco de contaminação microbiológica, um envase aberto deve ser infundido num prazo máximo de 24 horas.
Quando for utilizado em recém-nascidos e crianças menores de 2 anos, a solução (nas bolsas e equipamentos de administração) deve ser protegida da exposição à luz até que termine a administração (ver seção 2).
Posologia e método de administração
A capacidade para eliminar INTRALIPID deve determinar a dosagem e a velocidade de perfusão. Ver posteriormente, Eliminação de lípidos.
DOSAGEM
1 g de triglicéridos corresponde a 5 ml de INTRALIPID 200 mg/ml.
Adultos. A dose máxima recomendada é 3 g de triglicéridos/ kg peso corporal/dia. Administrando este limite superior, INTRALIPID aporta um 70% dos requerimentos de energia, mesmo em pacientes com requerimentos energéticos altamente incrementados. A taxa de perfusão para INTRALIPID não deve exceder 500 ml em 5 horas.
Neonatos e crianças. O intervalo de doses recomendado em neonatos e crianças é 0,5-4 g de triglicéridos/ kg peso corporal/ dia. A taxa de perfusão não deve exceder 0,17 g de triglicéridos/ kg peso corporal/ hora (4 g em 24 horas). Em prematuros e em neonatos de baixo peso, INTRALIPID deve ser perfundido preferencialmente de forma contínua durante 24 horas. A dose inicial deve ser de 0,5-1 g/ kg pc/dia seguido por um aumento sucessivo de 0,5-1 g/ kg pc/ dia até 2 g/ kg pc/ dia. A dose pode ser incrementada até 4 g/ kg pc/ dia, apenas sob uma estreita monitorização da concentração de triglicéridos no soro, dos testes da função hepática e da saturação de oxigênio. As taxas indicadas são as taxas máximas e não devem ser excedidas com o fim de compensar doses não administradas.
Deficiência de ácidos graxos essenciais (EFAD). Para prevenir ou corrigir uma deficiência de ácidos graxos essenciais, deve ser aportado um 4-8% de energia não proteica como INTRALIPID com o fim de proporcionar quantidades suficientes de ácido linoleico e linolênico. Se uma EFAD está associada a estresse, a quantidade de INTRALIPID requerida para corrigir a deficiência pode ser substancialmente superior.
ELIMINAÇÃO DE LÍPIDOS
Adultos. A capacidade para eliminar lípidos deve ser estreitamente monitorizada em pacientes com as condições mencionadas na seção “ANTES DE USAR INTRALIPID 200 mg/ml”, e em pacientes que recebem INTRALIPID durante mais de uma semana. Isso é feito recolhendo uma amostra de sangue após um período de aclaramiento livre de lípidos de 5-6 horas. As células sanguíneas são então separadas do plasma mediante centrifugação. Se o plasma for opalescente, a perfusão deve ser adiada. A sensibilidade deste método pode ocasionar que uma hipertrigliceridemia passe despercebida. Por isso, é recomendado que se determinem as concentrações de triglicéridos no soro em pacientes que provavelmente apresentem uma tolerância a lípidos alterada.
Neonatos e crianças. A capacidade para eliminar lípidos deve ser controlada com regularidade em neonatos e em crianças. A determinação dos níveis de triglicéridos no soro é o único método fiável.
Se usar mais INTRALIPID 200 mg/ml do que devia:
Ver o apartado “POSSÍVEIS EFEITOS ADVERSOS”, “Síndrome de sobrecarga lipídica”. A sobredosagem severa de emulsões lipídicas contendo triglicéridos pode, especialmente se não forem administrados carboidratos simultaneamente, dar lugar a acidose.
Se tiver alguma outra dúvida sobre o uso deste produto, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, INTRALIPID pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
A perfusão de INTRALIPID pode causar um aumento da temperatura corporal e, com menor frequência, calafrios, tremores e náuseas/vômitos (incidência < 1%).
Os relatórios sobre outras reações adversas em relação às infusões de INTRALIPID são extremamente raros, menos de um relatório adverso por um milhão de infusões.
Classificação de sistemas de órgãos segundo a OMS | Frequência | Sintoma |
Alterações gerais a nível corporal | Pouco frequentes (mais de 1 entre 1.000, menos de 1 entre 100) Muito raras (menos de 1 entre 10.000) | Cefaleia (dor de cabeça), aumento da temperatura corporal, calafrios, tremores, cansaço Reação anafiláctica (reação alérgica) |
Alterações cardiovasculares | Muito raras (menos de 1 entre 10.000) | Efeitos circulatórios, p. ex. hipertensão/hipotensão (tensão arterial elevada ou baixa) |
Alterações gastrointestinais | Pouco frequentes (mais de 1 entre 1.000, menos de 1 entre 100) | Dor anormal, Náuseas, vômitos |
Alterações do sistema hepático e biliar | Muito raras (menos de 1 entre 10.000) | Incremento transitório dos ensaios da função hepática |
Alterações musculoesqueléticas, do tecido conjuntivo e ósseas | Muito raras (menos de 1 entre 10.000) | Dor abdominal |
Alterações de plaquetas, hemorragia e coagulação | Muito raras (menos de 1 entre 10.000) | Trombocitopenia (diminuição da quantidade de plaquetas) |
Alterações dos glóbulos vermelhos | Muito raras (menos de 1 entre 10.000) | Henólise (rotura de glóbulos vermelhos), reticulocitose (aumento de reticulócitos) |
Alterações do sistema reprodutor, masculino | Muito raras (menos de 1 entre 10.000) | Priapismo (ereção contínua do pênis) |
Alterações da pele | Muito raras (menos de 1 entre 10.000) | Rash (erupção cutânea), urticária |
Foi relatada trombocitopenia associada a tratamentos prolongados com INTRALIPID em crianças. Também foi detectado um aumento transitório dos testes da função hepática após a nutrição intravenosa prolongada com ou sem INTRALIPID. Foi observado colesterol incrementado em crianças após tratamento prolongado com INTRALIPID. As razões não são claras atualmente.
Síndrome de sobrecarga lipídica. Uma capacidade alterada para eliminar INTRALIPID pode dar lugar a um síndrome de sobrecarga lipídica como resultado de uma sobredosagem. No entanto, este síndrome pode aparecer também às taxas recomendadas de perfusão associado a mudanças repentinas na situação clínica do paciente, como alteração da função renal ou infecção. O síndrome de sobrecarga lipídica é caracterizado por hiperlipemia, febre, infiltração lipídica, alterações em vários órgãos e coma. Todos os sintomas são geralmente reversíveis se a perfusão de INTRALIPID for interrompida.
Se considera que algum dos efeitos adversos que sofre é grave ou se apercebe de qualquer efeito adverso não mencionado neste prospecto, informe o seu médico ou farmacêutico.
5. Conservação de INTRALIPID 200 mg/ml
Conservar a uma temperatura inferior a 25º C. Não congelar.
Mantenha fora do alcance e da vista das crianças.
Não utilize INTRALIPID após a data de validade que aparece no envase após as siglas CAD. A data de validade é o último dia do mês que se indica.
Não utilize INTRALIPID se observar que o envase está deteriorado. Para a bolsa: após a inspeção do indicador de integridade, deve retirar-se a sobrebolsa.
Os medicamentos não devem ser jogados nos deságues nem na lixeira. Pergunte ao seu médico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
Quando for utilizado em recém-nascidos e crianças menores de 2 anos, a solução (nas bolsas e equipamentos de administração) deve ser protegida da exposição à luz até que termine a administração (ver seção 2).
6. INFORMAÇÃO ADICIONAL
Composição de INTRALIPID 200 mg/ml
1 ml de emulsão contém:
O princípio ativo é:
Óleo de soja purificado 200 mg
Os outros componentes são: fosfolipídios de ovo purificados, glicerol (anidro), água para
preparações injetáveis.
Aspecto do produto e conteúdo do envase
Bolsa para perfusão: a bolsa consiste em uma bolsa interna (acondicionamento primário) com uma sobrebolsa. Entre a bolsa interna e a sobrebolsa se coloca um absorbente de oxigênio e um indicador de integridade (Oxalert)
A sobrebolsa, o absorbente de oxigênio e o indicador de integridade devem ser descartados após abrir a sobrebolsa. O indicador de integridade (OxalertTM) reage com o oxigênio livre e muda de cor em caso de alteração da sobrebolsa.
Tamanhos de envase: bolsas de 100 ml, 250 ml e 500 ml.
10 bolsas de 250 ml
12 bolsas de 500 ml
Pode ser que apenas alguns tipos ou tamanhos de envase sejam comercializados.
Todos os componentes dos materiais de acondicionamento estão livres de látex e de
PVC.
Título da autorização de comercialização e responsável pela fabricação
Título: Fresenius Kabi España S.A.U
C/ Marina 16-18, Torre Mapfre 08005 Barcelona
Responsável pela fabricação:
Fresenius Kabi AB
Rapsgatan 7, 751 82 Uppsala
Suécia
Este prospecto foi aprovado em outubro de 2019.
A informação detalhada e atualizada deste medicamento está disponível na página web da
Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es
--------------------------------------------------------------------------------------------------------------------
Esta informação está destinada unicamente a médicos ou profissionais do setor sanitário
Instruções de uso/manipulação
Utilizar unicamente se o envase permanecer intacto. Para a bolsa: após a inspeção do indicador de integridade, deve retirar-se a sobrebolsa.
As adições devem ser realizadas assepticamente. Não deve levar-se a cabo a adição isolada de soluções de eletrólitos a INTRALIPID. Somente podem ser adicionadas diretamente as soluções medicinais, nutricionais ou de eletrólitos, cuja compatibilidade tenha sido documentada. Existem dados de compatibilidade disponíveis por parte do fabricante, para várias misturas. O conteúdo sobrante das bolsas abertas, deve ser descartado e não ser conservado para uso posterior.
Quando se utilizar em recém-nascidos e crianças menores de 2 anos, a solução (nas bolsas e equipamentos de administração) se deve proteger da exposição à luz até que finalize a administração.
Precauções especiais de conservação
Após a adição de outros elementos nutricionais
Mistura em bolsa de plástico (filme livre de ftalato): as misturas preparadas assepticamente em uma área asseptica controlada e validada, devem utilizar-se nos 7 dias seguintes após a preparação. As misturas podem ser conservadas até 6 dias sob refrigeração (2-8°C), seguido de um período de perfusão máximo de 24 horas.
A exposição à luz das soluções para nutrição parenteral por via intravenosa, em especial após misturá-las com oligoelementos ou vitaminas, pode ter efeitos adversos no desfecho clínico dos recém-nascidos devido à geração de peróxidos e outros produtos de degradação. Quando se utilizar em recém-nascidos e crianças menores de 2 anos, INTRALIPID se deve proteger da luz ambiental até que finalize a administração.
Precauções especiais de eliminação e outras manipulações:
Quando se utilizar em recém-nascidos e crianças menores de 2 anos, deve proteger-se da exposição à luz até que finalize a administração. A exposição de INTRALIPID à luz ambiental, em especial após misturá-lo com oligoelementos ou vitaminas, gera peróxidos e outros produtos de degradação que podem reduzir-se se se proteger o produto da exposição à luz.
Instruções de uso
Bolsas de perfusão Fresenius Kabi
- Inspeccionar o indicador de integridade (Oxalert TM ) A antes de quitar a sobrebolsa. Se o
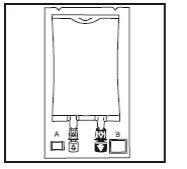 indicador está negro, entrou oxigênio na sobrebolsa e o produto deverá ser rejeitado.
indicador está negro, entrou oxigênio na sobrebolsa e o produto deverá ser rejeitado.
- Eliminar a sobrebolsa rasgando pela muesca e puxando para baixo ao longo do envase. A
bolsa Oxalert A e o absorbente de oxigênio B deverão ser descartados.
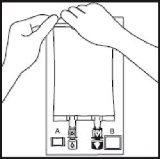
- Se se requer o uso de aditivos, romper o porto de adição branco pela marca em forma de
seta (A). Se não se requer nenhum aditivo, ir ao ponto 5.
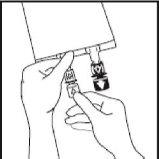
- Inserir a agulha horizontalmente através do centro da membrana do porto de adição e
injetar os aditivos (de compatibilidade conhecida). Utilizar seringas com agulhas de calibre 18-
23 e uma longitude máxima de 40 mm.
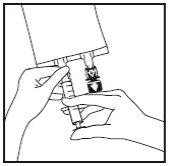
- Usar um equipamento de perfusão sem entrada de ar ou fechar a entrada de ar do equipamento de perfusão. Seguir as instruções de uso do equipamento de perfusão. Utilizar uma ponta com o
diâmetro especificado na norma ISO 8536-4, 5,6 +/- 0,1 mm.
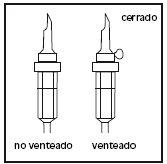
- Romper o porto de perfusão azul pela marca em forma de seta
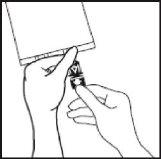
- Segurar a base do porto de perfusão. Inserir a ponta através do porto de perfusão mediante uma ligeira rotação do pulso até que a ponta se insira completamente.
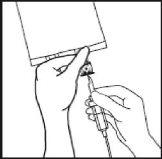
- Pendurar a bolsa no suporte por la muesca perfurada e começar a perfusão.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃOForma farmacêutica: PERFURAÇÃO INJETÁVEL, 200 mg/mlSubstância ativa: fat emulsionsFabricante: Baxter S.L.Requer receita médicaSubstância ativa: fat emulsionsFabricante: B Braun Medical S.A.Requer receita médicaSubstância ativa: fat emulsionsFabricante: B Braun Medical S.A.Requer receita médica
Alternativas a INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO em Польша
Alternativa a INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO em Украина
Médicos online para INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de INTRALIPID 200 mg/ml EMULSÃO PARA PERFUSÃO – sujeita a avaliação médica e regras locais.










