FLUARIX TETRA Suspensão injetável em seringa pré-carregada

Pergunte a um médico sobre a prescrição de FLUARIX TETRA Suspensão injetável em seringa pré-carregada

Como usar FLUARIX TETRA Suspensão injetável em seringa pré-carregada
Introdução
Prospecto: informação para o utilizador
Fluarix Tetra suspensão injetável em seringa pré-carregada
Vacina antigripal (de vírus fracionados e inactivados)
Este prospecto foi escrito assumindo que a pessoa que vai receber a vacina é quem o vai ler. No entanto, a vacina pode ser administrada a adolescentes e crianças, de modo que pode ser que o esteja lendo para o seu filho.
Leia todo o prospecto atentamente antes de si ou seu filho receber esta vacina, porque contém informações importantes para si.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Esta vacina foi-lhe prescrita apenas a si ou ao seu filho, e não deve dá-la a outras pessoas.
- Se si ou seu filho experimentar efeitos adversos, consulte o seu médico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto:
- O que é Fluarix Tetra e para que é utilizado
- O que precisa saber antes de receber Fluarix Tetra
- Como é administrado Fluarix Tetra
- Possíveis efeitos adversos
5Conservação de Fluarix Tetra
- Conteúdo do envase e informação adicional
1. O que é Fluarix Tetra e para que é utilizado
Fluarix Tetra é uma vacina que o ajuda a proteger-se contra a gripe, especialmente em pessoas com alto risco de complicações associadas. O uso de Fluarix Tetra deve basear-se nas recomendações oficiais.
Quando é administrado Fluarix Tetra a uma pessoa, o seu sistema imunitário (o sistema de defesa natural do organismo), produzirá a sua própria proteção (anticorpos) contra a doença. Nenhum dos componentes da vacina pode provocar a gripe.
A gripe é uma doença que se propaga rapidamente e está causada por diferentes tipos de cepas que podem mudar cada ano. Por tanto, é esta a razão pela qual pode precisar ser vacinado anualmente. O período com maior risco de contrair a gripe é durante os meses frios, entre outubro e março. Se não se vacinou no outono, é recomendável que o faça antes da primavera, pois até então corre o risco de se infectar. O seu médico recomendará o melhor momento para ser vacinado.
Fluarix Tetra protegerá contra as quatro cepas do vírus a partir de, aproximadamente, 2 ou 3 semanas após a injeção.
O período de incubação da gripe é de alguns dias, de modo que, se expuser à gripe imediatamente antes ou após a vacinação, ainda pode desenvolver a doença.
A vacina não o protegerá contra o resfriado comum, embora alguns dos sintomas sejam semelhantes aos da gripe.
2. O que precisa saber antes de receber Fluarix Tetra
Para se certificar de que Fluarix Tetra é apropriado para si, é importante que informe o seu médico ou farmacêutico se algum dos pontos que se tratam a seguir o afeta. Se houver algo que não entende, peça ao seu médico ou farmacêutico que o explique.
Não use Fluarix Tetra
- Se é alérgico aos princípios ativos ou a qualquer um dos outros componentes deste medicamento (incluídos na secção 6) ou a qualquer componente que possa estar presente em quantidades muito pequenas, tais como ovos (ovoalbúmina ou proteínas de frango), formaldeído, sulfato de gentamicina ou desoxicolato de sódio.
- Se padece qualquer doença acompanhada de febre elevada ou uma infecção aguda, deve retardar a vacinação até que se tenha recuperado.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de receber Fluarix Tetra:
- se tem uma resposta imunitária débil (devido a uma imunodeficiência ou a medicamentos que afetem o sistema imunitário)
- se, por qualquer razão, se lhe vai realizar um análise de sangue poucos dias após a vacinação antigripal. Isto é devido a que se observaram resultados falsos positivos nos análises de sangue de alguns pacientes que haviam sido recentemente vacinados.
- se tem um problema de coagulação ou lhe aparecem hematomas com facilidade.
O seu médico decidirá se deve receber a vacina.
Antes ou após qualquer injeção, poderá produzir-se um desmaio (especialmente nos adolescentes), por isso deve informar o seu médico ou enfermeiro se se desmaiou em ocasiões anteriores após a administração de uma injeção.
Assim como todas as vacinas, pode ser que Fluarix Tetra não proteja completamente todas as pessoas vacinadas.
Uso de Fluarix Tetra com outros medicamentos
Comunique ao seu médico ou farmacêutico se está a tomar, tomou recentemente ou pode ter que tomar qualquer outro medicamento.
Fluarix Tetra pode ser administrado ao mesmo tempo que outras vacinas se forem injetadas em diferentes extremidades.
Gravidez, lactação e fertilidade
Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de utilizar este medicamento.
O seu médico ou farmacêutico poderá decidir se deve receber Fluarix Tetra. Peça conselho ao seu médico ou farmacêutico antes de tomar qualquer medicamento.
Condução e uso de máquinas
A influência de Fluarix Tetra sobre a capacidade para conduzir e utilizar máquinas é nula ou insignificante.
Fluarix Tetra contém sódio
Este medicamento contém menos de 23 mg de sódio (1 mmol) por dose; isto é, é essencialmente "exento de sódio".
Fluarix Tetra contém potássio
Este medicamento contém menos de 39 mg (1 mmol) de potássio por dose, por isso é considerado essencialmente "exento de potássio".
3. Como é administrado Fluarix Tetra
Dose
Os adultos receberão uma dose de 0,5 ml.
Uso em crianças:
As crianças a partir de 6 meses receberão uma dose de 0,5 ml.
Se o seu filho tem menos de 9 anos e não foi vacinado previamente contra a gripe, deve ser administrada uma segunda dose após um intervalo de pelo menos 4 semanas.
Forma e/ou via de administração
O seu médico administrará a dose recomendada da vacina por meio de uma injeção no músculo.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Assim como todos os medicamentos, esta vacina pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Os seguintes efeitos adversos foram observados durante os ensaios clínicos:
Efeitos adversos ocorridos em crianças entre 6 e 36 meses de idade
Muito frequentes(podem ocorrer com mais de 1 de cada 10 doses da vacina): perda de apetite, irritabilidade, sonolência, dor e/ou vermelhidão no local da injeção.
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): febre, inchaço no local da injeção.
Efeitos adversos ocorridos em crianças entre 3 e 6 anos de idade
Muito frequentes(podem ocorrer com mais de 1 de cada 10 doses da vacina): dor e/ou vermelhidão e/ou inchaço no local da injeção, irritabilidade.
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): perda de apetite, sonolência, febre.
Pouco frequentes(podem ocorrer até com 1 de cada 100 doses da vacina): erupção na pele, picazón no local da injeção.
Efeitos adversos ocorridos em crianças entre 6 e 18 anos de idade
Muito frequentes(podem ocorrer com mais de 1 de cada 10 doses da vacina): dor muscular, dor e/ou vermelhidão e/ou inchaço no local da injeção, cansaço.
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): náuseas, diarreia, vómitos, dor de estômago, dor de cabeça, dor nas articulações, arrepios, febre.
Pouco frequentes(podem ocorrer até com 1 de cada 100 doses da vacina): erupção na pele, picazón no local da injeção.
Efeitos adversos ocorridos em adultos ≥18 anos de idade
Muito frequentes(podem ocorrer com mais de 1 de cada 10 doses da vacina): dor no local da injeção, cansaço, dor muscular (mialgia).
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): dor de cabeça, náuseas, diarreia, vómitos, dor de estômago, dor nas articulações (artralgia), febre, arrepios, vermelhidão e/ou inchaço no local da injeção.
Pouco frequentes(podem ocorrer até com 1 de cada 100 doses da vacina): hematomas, picazón (prurido) ao redor da área onde se injeta a vacina, tontura.
Além disso, os efeitos adversos ocorridos durante os estudos em sujeitos a partir dos 3 anos de idade com Fluarix (vacina antigripal trivalente) foram:
Frequentes(podem ocorrer até com 1 de cada 10 doses da vacina): endurecimento (induração) ao redor da área onde se injeta a vacina, sudorese.
Estas reações desaparecem normalmente em 1-2 dias sem tratamento.
Além dos efeitos adversos mencionados anteriormente, os seguintes efeitos adversos ocorreram durante o uso rotineiro de Fluarix e/ou Fluarix Tetra:
Raros(podem ocorrer até com 1 de cada 1000 doses da vacina):
- Reações alérgicas:
- que conduzem a uma urgência médica por uma falha do sistema circulatório que impede que se forneça um fluxo sanguíneo adequado aos diferentes órgãos do corpo (choque),
- inchaço, mais evidente na cabeça e no pescoço, incluindo a face, lábios, língua, garganta ou qualquer outra parte do corpo (angioedema).
- Reações cutâneas que podem se espalhar pelo corpo, incluindo picazón da pele (prurido, urticária) e vermelhidão (eritema) da pele.
- Distúrbios neurológicos que podem causar rigidez no pescoço, confusão, entorpecimento, dor e fraqueza nos membros, perda do equilíbrio, perda de reflexos, paralisia parcial ou total do corpo (encefalomielite, neurite, síndrome de Guillain-Barré).
- Inchaço temporário dos gânglios do pescoço, axilas ou inguina (linfadenopatia transitória).
- Sintomas semelhantes aos da gripe, mal-estar geral.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano, www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Fluarix Tetra
Mantenha esta vacina fora da vista e do alcance das crianças.
Não utilize esta vacina após a data de validade que aparece no envase após CAD. A data de validade é o último dia do mês que se indica.
Conservar em frigorífico (entre 2 °C e 8 °C).
Não congelar.
Conservar no embalagem exterior para protegê-la da luz.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Fluarix Tetra
Os princípios ativos são: vírus da gripe (fracionados, inativados) das seguintes cepas*:
Cepa semelhante a A/Victoria/4897/2022 (H1N1)pdm09:
(IVR-238) derivada de A/Victoria/4897/202215 microgramas de HA**
Cepa semelhante a A/Croácia/10136RV/2023 (H3N2):
(X-425A) derivada de A/Croácia/10136RV/202315 microgramas de HA**
Cepa semelhante a B/Áustria/1359417/2021:
(BVR-26) derivada de B/Áustria/1359417/202115 microgramas de HA**
Cepa semelhante a B/Phuket/3073/2013:
(salvagem) derivada de B/Phuket/3073/201315 microgramas de HA**
por dose de 0,5 ml
- propagados em ovos embrionados de galinha procedentes de grupos de galinhas saudáveis
**hemaglutinina
Esta vacina cumpre com a recomendação da Organização Mundial da Saúde (OMS) para o hemisfério Norte e com a recomendação da União Europeia para a campanha 2025/2026.
Os demais componentes são: cloreto de sódio, fosfato de sódio dodecahidratado, dihidrogenofosfato de potássio, cloreto de potássio, cloreto de magnésio hexahidratado, succinato de α-tocoferol, polissorbato 80, octoxinol 10 e água para preparações injetáveis.
Aspecto do produto e conteúdo do envase
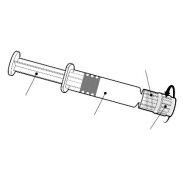
Fluarix Tetra é uma suspensão injetável em seringa pré-carregada.
Fluarix Tetra está disponível em seringa pré-carregada de 1 dose com ou sem agulhas separadas; tamanhos de envase de 1 e 10.
Pode ser que apenas alguns tamanhos de envases estejam comercializados.
Titular da autorização de comercialização e responsável pela fabricação
Titular da autorização de comercialização
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Bélgica
Responsável pela fabricação
GlaxoSmithKline Biologicals NL der SmithKline Beecham Pharma GmbH & Co. KG
Zirkusstrasse 40
D-01069 Dresden
Alemanha
Representante local
GlaxoSmithKline, S.A.
P.T.M. C/ Severo Ochoa, 2
28760 Tres Cantos (Madrid)
Tel.: +34 900 202 700
Este medicamento está autorizado nos Estados-membros do Espaço Económico Europeu com os seguintes nomes:
Estado-membro | Nome |
Áustria, Bulgária, Chipre, Croácia, Dinamarca, Eslováquia, Eslovênia, Espanha, Estônia, Finlândia, Grécia, Hungria, Irlanda, Islândia, Itália, Letônia, Lituânia, Malta, Noruega, Países Baixos, Polônia, Portugal, República Checa, Suécia | Fluarix Tetra |
Bélgica, Luxemburgo | Alpharix-Tetra |
Alemanha | Influsplit Tetra |
França | FluarixTetra |
Data da última revisão deste prospecto:07/2025
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) (http://www.aemps.gob.es/)
--------------------------------------------------------------------------------------------------------------------Esta informação está destinada apenas a profissionais do setor sanitário:
Assim como com todas as vacinas injetáveis, deve dispor-se em todo o momento do tratamento e supervisão médica adequados, para o caso de aparecimento de reações anafiláticas após a administração da vacina.
A imunização deve ser realizada por injeção intramuscular.
Em nenhum caso deve ser administrado Fluarix Tetra por via intravascular.
Fluarix Tetra pode ser administrado ao mesmo tempo que outras vacinas. A imunização deve ser realizada em diferentes extremidades.
Permita que a vacina atinja a temperatura ambiente antes de sua utilização.
Agite antes de usar. Inspeccione visualmente antes da administração.
Instruções para a seringa pré-carregada
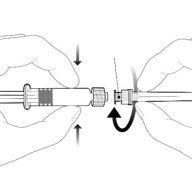
| Sustenha a seringa pelo corpo, não pelo émbolo. Desrosqueie o tampão da seringa girando-a no sentido contrário ao das agulhas do relógio. |
| Para inserir a agulha, conecte a base ao adaptador luer-locke gire-o um quarto de volta no sentido das agulhas do relógio até que sinta que se bloqueia. Não retire o émbolo da seringa do corpo. Se isso ocorrer, não administre a vacina. |
Eliminação de resíduos
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele, será realizada de acordo com a normativa local.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a FLUARIX TETRA Suspensão injetável em seringa pré-carregadaForma farmacêutica: INJETÁVEL, 3,75 microgramasSubstância ativa: influenza, inactivated, split virus or surface antigenFabricante: Glaxosmithkline BiologicalsRequer receita médicaForma farmacêutica: INJETÁVEL, 0,5 mlSubstância ativa: influenza, inactivated, split virus or surface antigenFabricante: Sanofi Winthrop IndustrieRequer receita médicaForma farmacêutica: INJETÁVEL, 60 microgramas de HASubstância ativa: influenza, inactivated, split virus or surface antigenFabricante: Sanofi Winthrop IndustrieRequer receita médica
Alternativas a FLUARIX TETRA Suspensão injetável em seringa pré-carregada noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a FLUARIX TETRA Suspensão injetável em seringa pré-carregada em Polónia
Alternativa a FLUARIX TETRA Suspensão injetável em seringa pré-carregada em Ukraine
Médicos online para FLUARIX TETRA Suspensão injetável em seringa pré-carregada
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de FLUARIX TETRA Suspensão injetável em seringa pré-carregada – sujeita a avaliação médica e regras locais.