
Efluelda
Pergunte a um médico sobre a prescrição de Efluelda

Como usar Efluelda
FOLHETO PARA O DOENTE
Folheto incluído na embalagem: informação para o utilizador
Efluelda, suspensão para injeção em seringa pré-cheia,
Trivalente vacina contra a gripe (vírus dividido), inativada,
60 microgramas HA/dose
Este medicamento estará sujeito a um monitorização adicional. Isto permitirá uma identificação rápida
de novas informações sobre a segurança. O utilizador do medicamento também pode ajudar,
relatando quaisquer efeitos adversos que ocorram após a administração do medicamento. Para saber
como relatar efeitos adversos – ver ponto 4.
Deve ler atentamente o conteúdo do folheto antes de tomar a vacina, pois contém informações importantes para o doente.
- Deve guardar este folheto, para que possa relê-lo se necessário.
- Em caso de alguma dúvida, deve consultar um médico, farmacêutico ou enfermeiro.
- A vacina foi prescrita para uma pessoa específica. Não deve ser transmitida a outros.
- Se o doente apresentar algum sintoma adverso, incluindo qualquer sintoma adverso não listado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é Efluelda e para que é utilizado
- 2. Informações importantes antes de tomar a vacina Efluelda
- 3. Como tomar a vacina Efluelda
- 4. Efeitos adversos possíveis
- 5. Como armazenar a vacina Efluelda
- 6. Conteúdo da embalagem e outras informações
1. O que é Efluelda e para que é utilizado
Efluelda é uma vacina. Esta vacina ajuda a proteger pessoas com 60 anos ou mais contra a gripe.
A administração da vacina Efluelda deve basear-se nas recomendações oficiais sobre vacinação
contra a gripe.
Após a administração da vacina Efluelda, o sistema imunológico (sistema de defesa natural do organismo) produz
sua própria proteção contra a doença (anticorpos). Nenhum dos componentes da vacina pode causar
gripe.
A gripe é uma doença infecciosa do sistema respiratório causada por vírus da gripe, com gravidade desde
leve até grave e pode levar a complicações graves, como pneumonia, que pode resultar em hospitalização,
e até morte. A gripe é uma doença que pode se espalhar rapidamente e é causada por muitos diferentes
tipos de vírus, que podem mudar a cada ano. Devido a essa possível mudança anual dos tipos de vírus circulantes,
além do período de manutenção da proteção fornecida pela vacina, é recomendado realizar a vacinação
todos os anos. O maior risco de contrair gripe ocorre durante os meses frios, entre outubro e março. No caso
de pessoas que não foram vacinadas no outono, ainda é justificável se vacinar durante o período até a primavera,
pois até essa época existe o risco de contrair gripe. O médico poderá recomendar o melhor momento para
se vacinar.
A vacina Efluelda é destinada a proteger contra três tipos de vírus da gripe contidos na vacina, cerca de 2
a 3 semanas após a vacinação. Como o período de incubação da gripe é de alguns dias,

é ainda possível contrair a doença em caso de exposição ao vírus da gripe logo antes ou após a vacinação.
A vacina não protege contra resfriados, embora alguns dos seus sintomas sejam semelhantes aos da gripe.
2. Informações importantes antes de tomar a vacina Efluelda
Deve informar o médico ou farmacêutico se alguma das seguintes afirmações se aplicar à pessoa que vai
tomar a vacina Efluelda. Se algo não for claro, deve pedir ao médico ou farmacêutico para explicar.
Quando não tomar a vacina Efluelda:
- Se a pessoa tiver alergia a:
- substâncias ativas, ou
- qualquer um dos outros componentes da vacina (listados no ponto 6), ou
- qualquer componente que possa estar presente em quantidades muito pequenas, como resíduos de ovo (albumina de ovo de galinha, proteínas de galinha) e formaldeído.
Advertências e precauções
Antes de tomar a vacina Efluelda, deve discutir com o médico, farmacêutico ou enfermeiro.
Antes da vacinação, deve informar o médico se o doente tiver:
- resposta imunológica debilitada (devido a uma deficiência imunológica ou ao uso de medicamentos que afetam o sistema imunológico),
- sangramento ou tendência a hematomas,
- síndrome de Guillain-Barré (GBS) (fraqueza muscular grave) após a administração de uma vacina contra a gripe,
- doença com febre alta ou moderada ou doença aguda. A vacinação deve ser adiada até a recuperação. O médico decidirá se a vacina deve ser administrada.
Desmaio pode ocorrer após, ou mesmo antes de qualquer injeção. Portanto, deve informar o médico ou
enfermeiro se a pessoa tiver tido desmaios em injeções anteriores.
Assim como com qualquer vacina, a vacina Efluelda pode não fornecer proteção total a todas as pessoas
vacinas.
Deve informar o médico se, dentro de alguns dias após a vacinação contra a gripe, estiver planejado um
exame de sangue, devido a resultados falsos positivos de exames de sangue observados em alguns doentes
que receberam a vacina anteriormente.
Uso em crianças
Esta vacina não deve ser usada em crianças. O uso desta vacina é recomendado para pessoas adultas com
60 anos ou mais.
Vacina Efluelda e outros medicamentos
Deve dizer ao médico ou farmacêutico sobre todos os medicamentos ou vacinas que o doente está tomando
atualmente ou recentemente, bem como sobre medicamentos ou vacinas que o doente planeja tomar.
- Se a vacina Efluelda for administrada ao mesmo tempo que outras vacinas, as vacinas devem ser sempre administradas em membros diferentes.
- Deve notar que, com a administração concomitante de vacinas, podem ocorrer efeitos adversos aumentados.
- Se o doente estiver tomando medicamentos ou terapias que reduzem a imunidade, como corticosteroides, medicamentos citotóxicos ou radioterapia, a resposta imunológica à vacinação pode ser reduzida.
Gravidez e amamentação
A vacina Efluelda é indicada para uso exclusivo em pessoas adultas com 60 anos ou mais.
Se a paciente estiver grávida ou amamentando, suspeitar que possa estar grávida ou planejar ter um filho,
deve consultar um médico ou farmacêutico antes de tomar esta vacina. O médico ou farmacêutico ajudará
a decidir se a paciente deve receber a vacina Efluelda.
Condução de veículos e operação de máquinas
A vacina Efluelda não tem efeito ou tem um efeito insignificante na capacidade de conduzir veículos e operar
máquinas. No entanto, não se recomenda conduzir veículos se o doente se sentir mal ou tiver tonturas.
Vacina Efluelda contém sódio
Esta vacina contém menos de 1 mmol de sódio (23 mg) por dose, ou seja, o medicamento é considerado
"livre de sódio".
3. Como tomar a vacina Efluelda
Pessoas adultas com 60 anos ou mais recebem uma dose de 0,5 ml.
Como a vacina Efluelda é administrada
O médico, farmacêutico ou enfermeiro administrará a dose recomendada da vacina como uma injeção no
músculo ou sob a pele.
Em caso de alguma dúvida adicional sobre o uso desta vacina, deve consultar um médico ou farmacêutico.
4. Efeitos adversos possíveis
Como qualquer medicamento, esta vacina pode causar efeitos adversos, embora não todos os doentes os
apresentem.
Reações alérgicas
Deve IMEDIATAMENTEcontatar um médico se o doente apresentar:
- Reações alérgicas graves:
- que possam exigir atendimento médico, com pressão arterial baixa, dificuldade respiratória, sibilação, problema para respirar, pulso rápido e fraco, pele fria e úmida, tonturas que podem levar a desmaio (anafilaxia [incluindo angioedema, ou seja, inchaço mais visível na cabeça e pescoço, incluindo face, lábios, língua, garganta ou outras partes do corpo, que pode causar dificuldade para engolir ou respirar]).
Deve contatar um médico se o doente apresentar:
- Reações alérgicas, como reações cutâneas, que podem afetar todo o corpo, incluindo coceira, urticária, erupção cutânea. Estes efeitos adversos são raros (podem afetar até 1 em 1000 pessoas).
Outros efeitos adversos relatados
Os seguintes efeitos adversos foram relatados em pessoas adultas com 60 anos ou mais.
Muito frequentes (podem afetar mais de 1 em 10 pessoas):
- Reações no local da injeção: dor, vermelhidão (eritema)
- Mal-estar geral (fadiga), dor de cabeça, dor muscular
Frequentes (podem afetar até 1 em 10 pessoas):
- Reações no local da injeção: inchaço, hematoma, endurecimento
- Febre, calafrios
Pouco frequentes (podem afetar até 1 em 100 pessoas):
- Reações no local da injeção: coceira
- Fadiga, sonolência, náuseas, vômitos, diarreia
- Tosse, fraqueza muscular, dispepsia, faringite (dor na boca e garganta)
Raros (podem afetar até 1 em 1000 pessoas):
- Falta de energia (fraqueza), vermelhidão, dor articular, tonturas, suores noturnos, erupção cutânea, formigamento ou sensação de queimadura (parestesia), rinite (rhinite), tonturas (distúrbios do equilíbrio), excesso de sangue na esclera (hiperemia da esclera)
- Dor nas extremidades
Frequência desconhecida: frequência não pode ser estimada com base nos dados disponíveis:
- Redução do número de certos tipos de células no sangue chamadas plaquetas; o nível baixo delas pode causar sangramento excessivo ou hematomas (trombocitopenia)
- Aumento dos gânglios linfáticos na região do pescoço, axila ou virilha (linfadenopatia)
- Distúrbios neurológicos, que podem causar rigidez no pescoço, desorientação, formigamento, dor e fraqueza nas extremidades, perda de equilíbrio, perda de reflexos, paralisia de parte ou de todo o corpo (encefalite e mielite transversa, neurite do braço, síndrome de Guillain-Barré), paralisia facial (paralisia de Bell), distúrbios da visão devido à disfunção dos nervos ópticos (neurite óptica/neuropatia), convulsões (incluindo convulsões febris), desmaios logo após a vacinação
- Viroses, que podem levar a erupções cutâneas e, em casos muito raros, a distúrbios transitórios da função renal, vasodilatação
- Dor no peito
- Sibilação, aperto na garganta, dificuldade para respirar (dispneia)
A maioria dos efeitos adversos ocorreu dentro de 3 dias após a vacinação e desapareceu dentro de 3 dias.
A gravidade desses efeitos adversos foi leve a moderada.
Relato de efeitos adversos
Se ocorrerem algum sintoma adverso, incluindo qualquer sintoma adverso não listado neste folheto, deve
informar o médico, farmacêutico ou enfermeiro. Efeitos adversos podem ser relatados diretamente ao
Departamento de Monitorização de Efeitos Adversos de Medicamentos do Instituto Nacional de Farmacologia,
Medicina e Produtos de Saúde
Rua Alexandre Herculano, 46 – 4º
1250-008 Lisboa
Tel.: +351 21 792 70 00
Fax: +351 21 792 70 99
Site: https://www.infarmed.pt/
Efeitos adversos também podem ser relatados ao titular da autorização de comercialização.
Ao relatar efeitos adversos, pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como armazenar a vacina Efluelda
A vacina deve ser armazenada em local não visível e inacessível a crianças.
Não use esta vacina após o prazo de validade impresso na etiqueta e embalagem após "Validade (EXP)".
O prazo de validade é o último dia do mês indicado.
Armazenar na geladeira (2 ºC – 8 ºC). Não congelar. Armazenar a seringa pré-cheia no embalagem exterior para proteger da luz.
Medicamentos não devem ser jogados no esgoto ou em recipientes de lixo doméstico. Deve perguntar ao
farmacêutico como eliminar os medicamentos que não são mais usados. Este procedimento ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém a vacina Efluelda
- As substâncias ativas são: Vírus da gripe (inativado, dividido) dos seguintes tipos*:
A/Victoria/4897/2022 (H1N1)pdm09-semelhante (A/Victoria/4897/2022, IVR-238)
.....................................................................................................................................60 microgramas HA**
A/Croácia/10136RV/2023 (H3N2)-semelhante (A/Croácia/10136RV/2023, X-425A)
.................................................................................................................................... 60 microgramas HA**
B/Áustria/1359417/2021-semelhante (B/Michigan/01/2021, tipo selvagem)
................................................................................................................................... 60 microgramas HA**
em uma dose de 0,5 ml
*
produzido em ovos de galinha
**
hemaglutinina
A vacina é conforme as recomendações da Organização Mundial da Saúde (OMS) para o hemisfério norte e as recomendações da União Europeia para a temporada 2025/2026.
Os outros componentes são: solução tampão contendo cloreto de sódio, fosfato de sódio monobásico, fosfato de sódio dibásico, água para injeção e octoxinol-9.
Alguns componentes, como resíduos de ovo (albumina de ovo de galinha, proteínas de galinha) ou formaldeído, podem estar presentes em quantidades muito pequenas (ver ponto 2).
Como é a vacina Efluelda e o que o embalagem contém
Após uma agitação suave, a vacina é um líquido incolor e opalescente.
A Efluelda é uma suspensão para injeção em seringa pré-cheia (suspensão para injeção) de 0,5 ml,
com agulha ou sem agulha (em embalagens de 1, 5 ou 10) ou com agulha em capa de proteção (em embalagens de 1 ou 10). Nem todos os tamanhos de embalagem precisam estar disponíveis.
Titular da autorização de comercialização e importador
Titular da autorização de comercialização:
Sanofi Winthrop Industrie
82 avenue Raspail
94250 Gentilly
França
Importador:
Sanofi Winthrop Industrie
Voie de l’Institut - Parc Industriel d'Incarville
B.P 101
27100 Val de Reuil
França
Este medicamento está autorizado para comercialização nos países membros da Área Económica Europeia sob as seguintes denominações:
Data da última revisão do folheto:julho de 2025
As informações atualmente aprovadas sobre este produto estão disponíveis
-----------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico especializado:
Assim como com todas as vacinas administradas por injeção, é necessário garantir o tratamento e supervisão médica adequados no caso de ocorrência de uma reação anafilática após a administração da vacina.
Antes da administração, a vacina deve atingir a temperatura ambiente.
Agite antes de usar. Verifique visualmente antes da administração.
A vacina não deve ser administrada se houver partículas sólidas na suspensão.
A vacina não deve ser misturada com outros medicamentos na mesma seringa.
A vacina não deve ser injetada diretamente nos vasos sanguíneos.
Ver também o ponto 3. Como tomar a vacina Efluelda
˂Preparação para administração
Instruções para o uso da agulha com capa de proteção com a seringa pré-cheia com ponta Luer Lock:
| Austria, Bélgica, Bulgária, Croácia, República Checa, Dinamarca, Estônia, Finlândia, França, Espanha, Holanda, Islândia, Irlanda, Lituânia, Luxemburgo, Letônia, Malta, Alemanha, Noruega, Polônia, Portugal, Romênia, Eslováquia, Eslovênia, Suécia, Hungria, Itália | Efluelda |
| Chipre, Grécia | Efluelda TIV |
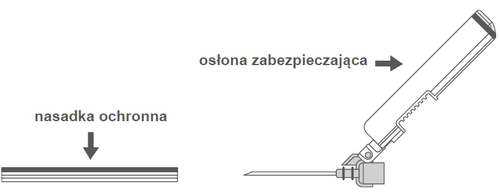
| Figura A: Agulha com capa de proteção (na embalagem) | Figura B: Componentes da capa de proteção da agulha (preparados para uso) |
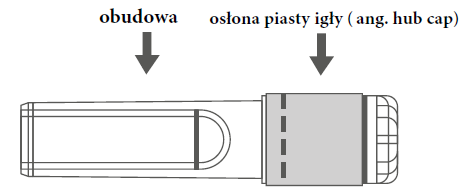 |  |
| Passo 1: Para fixar a agulha à seringa, retire a capa da agulha (tampa do hub), para expor o hub da agulha e, em seguida, rosqueie suavemente a agulha no adaptador Luer Lock da seringa até sentir uma ligeira resistência. | |
Passo 2: Retire a embalagem da agulha. A agulha está protegida por uma capa de proteção e uma capa de proteção da agulha.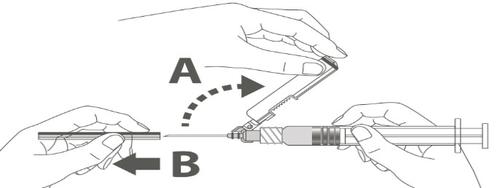 | |
| Krok 3: A: Afaste a capa de proteção da agulha da agulha na direção do corpo da seringa no ângulo mostrado. B: Retire a capa de proteção da agulha. | 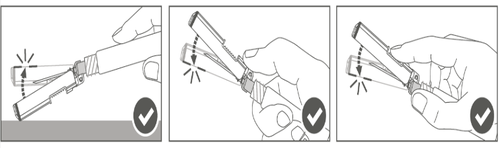 |
| Krok 4: Após a injeção, bloqueie (ative) a capa de proteção da agulha, usando uma das três (3) técnicas de manipulação com uma mão: ativação em uma superfície plana, polegar ou dedo indicador. Observação: A ativação é confirmada por um som audível e/ou um "clic" palpável. | |
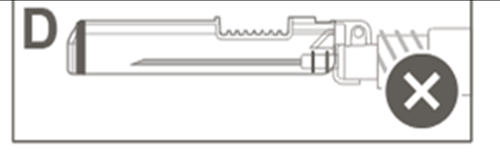
| Krok 5: Verifique visualmente o funcionamento da capa de proteção da agulha. A capa de proteção da agulha deve estar completamente bloqueada (ativada), como mostrado na Figura C. A Figura D mostra que a capa de proteção da agulha NÃO está completamente bloqueada (não está ativada). | 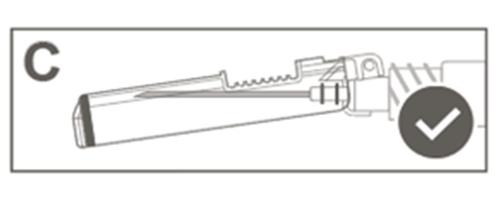 |
 | |
| Advertência: Não tente desbloquear (desativar) o dispositivo de proteção, empurrando a agulha para fora da capa de proteção. | |
Qualquer sobra de medicamento ou resíduos deve ser eliminado de acordo com as regulamentações locais.˃
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorSanofi Winthrop Industrie
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a EflueldaForma farmacêutica: Suspensão, 60 mcg HA/cepa, 1 dose (0.7 ml)Substância ativa: influenza, inactivated, split virus or surface antigenRequer receita médicaForma farmacêutica: Suspensão, 1 dose (0.5 ml)Substância ativa: influenza, inactivated, split virus or surface antigenRequer receita médicaForma farmacêutica: Suspensão, 1 dose (0.5 ml)Substância ativa: influenza, inactivated, split virus or surface antigenRequer receita médica
Alternativas a Efluelda noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Efluelda em Espanha
Alternativa a Efluelda em Ukraine
Médicos online para Efluelda
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Efluelda – sujeita a avaliação médica e regras locais.














