
Fluarix
Pergunte a um médico sobre a prescrição de Fluarix

Como usar Fluarix
Folheto informativo para o utilizador
Fluarix, suspensão para injeção em seringa pré-cheia
Vacina trivalente contra a gripe (vírus dividido, inativado)
O conteúdo deste folheto foi elaborado com a suposição de que será lido pela pessoa que receberá
a vacina. No entanto, como esta vacina pode ser administrada a adultos e crianças, é possível que
o conteúdo do folheto seja lido por um pai ou responsável pela criança.
É importante ler atentamente o conteúdo do folheto antes de administrar a vacina, pois contém informações importantes para o paciente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar um médico, farmacêutico ou enfermeiro.
- Esta vacina foi prescrita para uma pessoa específica. Não deve ser transmitida a outros.
- Se o paciente apresentar algum efeito colateral, incluindo qualquer efeito colateral não mencionado neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto:
- 1. O que é a vacina Fluarix e para que é utilizada
- 2. Informações importantes antes de administrar a vacina Fluarix
- 3. Como administrar a vacina Fluarix
- 4. Efeitos colaterais possíveis
- 5. Como armazenar a vacina Fluarix
- 6. Conteúdo do pacote e outras informações
1. O que é a vacina Fluarix e para que é utilizada
A Fluarix é uma vacina destinada a ser administrada a adultos e crianças a partir de 6 meses de idade
para prevenir a gripe.
A gripe é uma doença das vias respiratórias superiores e dos pulmões causada pelo vírus da gripe. Os sintomas mais comuns da gripe são febre alta, dor de garganta, tosse, dores musculares e articulares, dor de cabeça, fraqueza e fadiga. Complicações pós-gripais podem ocorrer, especialmente em pessoas muito jovens, idosas e com sistema imunológico debilitado.
Como funciona a vacina Fluarix?
- A vacina Fluarix contém vírus inativados que não podem causar gripe.
- A vacina Fluarix estimula o sistema imunológico da pessoa vacinada a produzir anticorpos contra os vírus específicos contra os quais a vacina foi desenvolvida. Isso ajudará a prevenir a doença.
- A vacina foi desenvolvida contra os vírus da gripe com base nas recomendações oficiais.
- Assim como todas as vacinas, a Fluarix pode não proteger completamente todas as pessoas vacinadas.
2. Informações importantes antes de administrar a vacina Fluarix
Quando não administrar a vacina Fluarix:
- Se o paciente tiver alergia aos componentes ativos ou a qualquer um dos outros componentes da vacina (listados no ponto 6) ou a qualquer componente que possa estar presente em quantidades muito pequenas, como albumina de ovo de galinha (ovalbumina, proteína do ovo), hidrocortisona, sulfato de gentamicina, formaldeído e desoxicolato de sódio.
Precauções e advertências:
Antes de administrar a vacina Fluarix, deve discutir com o médico, farmacêutico ou enfermeiro:
- se o paciente tiver uma infecção aguda com febre alta. A vacinação deve ser adiada até que o paciente se sinta melhor. Uma infecção leve, como um resfriado, não é uma contraindicação para a vacinação, mas antes deve ser discutida com o médico, farmacêutico ou enfermeiro.
- se o paciente tiver problemas de coagulação ou tendência a formar hematomas.
Após ou mesmo antes da administração de qualquer vacina por injeção, pode ocorrer síncope (especialmente em adolescentes). Nesse caso, deve informar o médico, farmacêutico ou enfermeiro se o paciente já teve síncope durante a administração de uma injeção.
Se o paciente tiver sistema imunológico debilitado, por exemplo, devido à infecção por HIV ou ao uso de medicamentos que afetam o sistema imunológico, a vacina Fluarix pode não ser completamente eficaz.
Deve informar o médico, farmacêutico ou enfermeiro se qualquer uma das afirmações acima se aplicar à pessoa que receberá a vacina Fluarix ou se o paciente não tiver certeza se alguma delas se aplica.
Vacina Fluarix e outros medicamentos
Deve informar o médico, farmacêutico ou enfermeiro sobre todos os medicamentos que está tomando atualmente ou recentemente, bem como sobre os medicamentos que planeja tomar.
Deve informar sobre todas as vacinas recentemente administradas.
Se a Fluarix for administrada juntamente com outras vacinas, cada vacina deve ser administrada em um local diferente do corpo.
Gravidez, amamentação e fertilidade
Se a paciente estiver grávida ou amamentando, suspeitar que possa estar grávida ou planejar ter um filho, deve consultar o médico ou farmacêutico antes de tomar esta vacina.
Condução de veículos e operação de máquinas
Alguns dos efeitos mencionados abaixo no ponto 4. "Efeitos colaterais possíveis" (por exemplo, fadiga ou tontura) podem ter um efeito temporário na capacidade de conduzir veículos ou operar máquinas.
Não deve conduzir veículos ou operar máquinas ou ferramentas se não se sentir bem.
Fluarix contém sódio
Esta vacina contém menos de 1 mmol de sódio (23 mg) por dose, ou seja, o medicamento é considerado "livre de sódio".
Fluarix contém potássio
Esta vacina contém potássio, menos de 1 mmol (39 mg) por dose, ou seja, o medicamento é considerado "livre de potássio".
Fluarix contém polissorbato 80
Esta vacina contém não mais de 0,415 mg de polissorbato 80 por dose. Os polissorbatos podem causar reações alérgicas. Deve consultar o médico se o paciente tiver alergia a essa substância.
3. Como administrar a vacina Fluarix
A vacina Fluarix é administrada por injeção intramuscular única, em dose de 0,5 ml.
Administração em crianças
Para crianças abaixo de 9 anos que não foram previamente vacinadas contra a gripe, deve ser administrada uma segunda dose após um intervalo de pelo menos 1 mês após a primeira dose.
Deve garantir que a criança receba todas as doses da vacina, o que ajudará a obter uma melhor proteção contra a gripe.
Em caso de dúvidas adicionais sobre a administração desta vacina, deve consultar o médico, farmacêutico ou enfermeiro.
4. Efeitos colaterais possíveis
Como qualquer medicamento, esta vacina pode causar efeitos colaterais, embora não todos os pacientes os experimentem.
Para obter informações adicionais sobre os efeitos colaterais possíveis da vacina Fluarix, deve consultar o médico, farmacêutico ou enfermeiro.
Efeitos colaterais relatados durante o uso geral da vacina Fluarix incluem:
Efeitos colaterais graves
Deve informar imediatamente o médico se o paciente notar algum dos seguintes efeitos colaterais graves; pode ser necessária ajuda médica de emergência.
Raro:pode ocorrer em até 1 em cada 1.000 doses da vacina
- Reações alérgicas graves (reações anafiláticas). Podem ser reconhecidas por:
- erupção cutânea pruriginosa nas mãos e pés
- edema dos olhos e face
- dificuldade para respirar ou engolir
- queda súbita da pressão arterial e perda de consciência. Essas reações geralmente ocorrem dentro de 15 minutos após a vacinação. No entanto, se ocorrer algum desses sintomas, deve procurar ajuda médica imediatamente.
Outros efeitos colaterais
Deve informar o médico, farmacêutico ou enfermeiro se o paciente notar algum dos seguintes efeitos colaterais.
Raro:pode ocorrer em até 1 em cada 1.000 doses da vacina
- Inflamação dos nervos (neurite), inflamação do cérebro e da medula espinhal (encefalomielite), inflamação transitória dos nervos que causa dor, fraqueza e paralisia conhecida como síndrome de Guillain-Barré
- Reações cutâneas que podem se espalhar por todo o corpo, incluindo prurido (coceira, urticária) e eritema (vermelhidão da pele), erupção cutânea
- Inchaço temporário dos gânglios linfáticos no pescoço, axilas ou virilha (linfadenopatia transitória)
- Sintomas semelhantes à gripe, mal-estar geral Deve informar o médico, farmacêutico ou enfermeiro se o paciente notar algum dos efeitos colaterais acima.
Nos estudos clínicos com a vacina Fluarix, foram observados os seguintes efeitos colaterais:
Efeitos colaterais que ocorreram em crianças de 6 meses a menos de 6 anos
Muito comum:pode ocorrer em mais de 1 em cada 10 doses da vacina
- perda de apetite
- irritabilidade
- sonolência
- dor no local da injeção
- vermelhidão no local da injeção
- inchaço no local da injeção
Comum:pode ocorrer em até 1 em cada 10 doses da vacina
- náuseas
- vômitos
- diarreia
- dor abdominal
- febre
Efeitos colaterais que ocorreram em crianças de 6 a menos de 18 anos
Muito comum:pode ocorrer em mais de 1 em cada 10 doses da vacina
- dor de cabeça
- dor muscular
- fadiga
- dor no local da injeção
- vermelhidão no local da injeção
- inchaço no local da injeção
Comum:pode ocorrer em até 1 em cada 10 doses da vacina
- náuseas
- vômitos
- diarreia
- dor abdominal
- dor articular
- calafrios
- febre
Efeitos colaterais que ocorreram em adultos com 18 anos ou mais
Muito comum:pode ocorrer em mais de 1 em cada 10 doses da vacina
- dor no local da injeção
- fadiga
- dor de cabeça
- dor muscular
Comum:pode ocorrer em até 1 em cada 10 doses da vacina
- vermelhidão, inchaço ou nódulo duro no local da injeção
- calafrios
- suor
- dor articular
- náuseas
- vômitos
- diarreia
- dor abdominal
Raro:pode ocorrer em até 1 em cada 100 doses da vacina
- febre
- tontura
Notificação de efeitos colaterais
Se ocorrerem algum efeito colateral, incluindo qualquer efeito colateral não mencionado no folheto, deve informar o médico ou farmacêutico. Os efeitos colaterais podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Colaterais de Medicamentos do Instituto Nacional de Farmacologia, Al. Jerozolimskie 181C, 02-222 Varsóvia, telefone: +48 22 49 21 301, fax: +48 22 49 21 309, site: https://smz.ezdrowie.gov.pl
A notificação de efeitos colaterais ajudará a coletar mais informações sobre a segurança do medicamento.
Os efeitos colaterais também podem ser notificados ao titular da autorização de comercialização.
5. Como armazenar a vacina Fluarix
- A vacina deve ser armazenada em um local seguro e fora do alcance das crianças.
- Não use este medicamento após a data de validade impressa na etiqueta e na caixa de cartão após: EXP. A data de validade indica o último dia do mês indicado.
- O código "Lote" indica o número da série do produto.
- Armazenar na geladeira (2°C - 8°C).
- Não congelar.
- Armazenar no embalagem original para proteger da luz.
- Os medicamentos não devem ser jogados na canalização ou em recipientes de lixo doméstico. Deve perguntar ao farmacêutico como descartar os medicamentos que não são mais utilizados. Isso ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém a Fluarix
O princípio ativo é o vírus da gripe dividido, inativado, derivado das seguintes cepas*:
A/Victoria/4897/2022 (H1N1)pdm09 - cepa semelhante (A/Victoria/4897/2022, IVR-238)
15 microgramas de HA**
A/Croácia/10136RV/2023 (H3N2) - cepa semelhante (A/Croácia/10136RV/2023, X-425A)
15 microgramas de HA**
B/Áustria/1359417/2021 - cepa semelhante (B/Áustria/1359417/2021, BVR-26)
15 microgramas de HA**
em dose de 0,5 ml
* cultivado em ovos de galinha fertilizados provenientes de rebanhos saudáveis
** hemaglutinina
Esta vacina atende às recomendações da Organização Mundial da Saúde (OMS) (para o hemisfério norte) e da União Europeia para a temporada 2025/2026 .
Outros componentes da vacina são: cloreto de sódio, fosfato dissódico dodecahidratado, dihidrogenofosfato de potássio, cloreto de potássio, cloreto de magnésio hexahidratado, α-tocoferol succinato, polissorbato 80, octoxinol 10 e água para injeção.
Como é a vacina Fluarix e o que contém o pacote
- A Fluarix é uma suspensão para injeção em seringa pré-cheia.
- A Fluarix é um líquido incolor e ligeiramente opalescente.
- A Fluarix está disponível em seringas pré-cheias de dose única, com agulhas incluídas no pacote ou sem agulhas, em pacotes de 1 e 10 unidades.
- Nem todos os tamanhos de pacotes precisam estar disponíveis no mercado.
Titular da autorização de comercialização e fabricante
Titular da autorização de comercialização: Fabricante:
GlaxoSmithKline Biologicals S.A.
GlaxoSmithKline Biologicals
Rue de l’Institut 89
Filial SmithKline Beecham Pharma GmbH & Co. KG
1330 Rixensart
Zirkusstrasse 40
Bélgica
01069 Dresden
Alemanha
Este medicamento está autorizado para comercialização nos países membros da Área Econômica Europeia sob os seguintes nomes:
| País membro | Nome |
| Áustria | Fluarix Trivalente |
| Bélgica, Luxemburgo | Alpharix |
| Finlândia, França, Espanha, Holanda, Noruega, Polônia, Portugal, Suécia, Itália | Fluarix |
| Grécia, Alemanha | Influsplit |
Data da última atualização do folheto: julho de 2025
Outras fontes de informação
Informações detalhadas sobre este medicamento estão disponíveis no site do Instituto Nacional de Farmacologia, Medicamentos e Produtos Biocidas.
---------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas ao pessoal médico qualificado:
Antes da administração da vacina, deve-se verificar se há presença de corpos estranhos e/ou alterações físicas.
Deve-se agitar antes de usar para obter um líquido incolor e ligeiramente opalescente. Se ocorrerem alterações, a vacina não deve ser administrada.
Deve-se administrar todo o conteúdo da seringa pré-cheia.
Instruções para a seringa pré-cheia
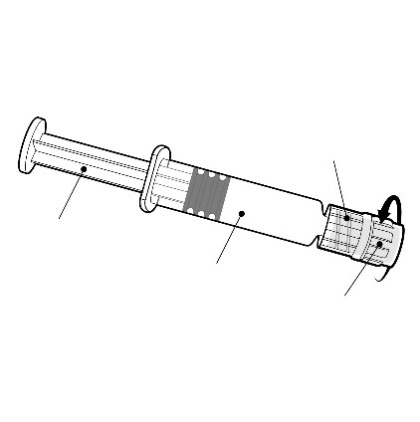
Deve segurar a seringa pré-cheia pelo
corpo, e não pelo êmbolo.
Adaptador do tipo Luer Lock
Deve remover o bico da seringa pré-cheia
girando-o no sentido contrário ao dos ponteiros do relógio.
Êmbolo
Corpo
Bico
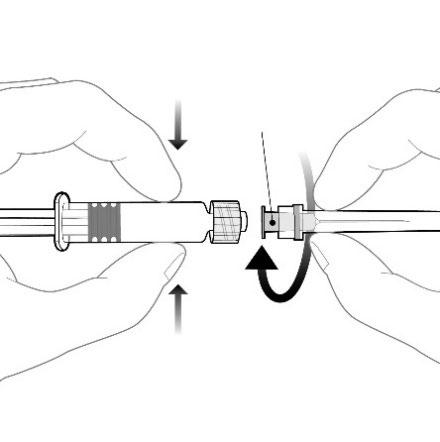
Deve fixar a agulha na seringa pré-cheia
conectando o bico da agulha ao adaptador Luer Lock (ang. Luer
Lock Adaptor , LLA) e girando-o um quarto de volta no sentido horário, até sentir o bloqueio da agulha.
Não se deve retirar o êmbolo do corpo da seringa pré-cheia. Se isso ocorrer, a vacina não deve ser administrada.
Bico da agulha
Remoção
Todos os resíduos do produto medicinal não utilizado ou seus dejetos devem ser eliminados de acordo com as regulamentações locais.
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorGlaxoSmithKline Biologicals Filia SmithKline BeechamPharma GmbH & Co. KG
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a FluarixForma farmacêutica: Suspensão, 60 mcg HA/cepa, 1 dose (0.7 ml)Substância ativa: influenza, inactivated, split virus or surface antigenRequer receita médicaForma farmacêutica: Suspensão, 60 mcg HA/cepa, 1 dose (0.5 ml)Substância ativa: influenza, inactivated, split virus or surface antigenRequer receita médicaForma farmacêutica: Suspensão, 1 dose (0.5 ml)Substância ativa: influenza, inactivated, split virus or surface antigenRequer receita médica
Alternativas a Fluarix noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Fluarix em Hiszpania
Alternativa a Fluarix em Ukraina
Médicos online para Fluarix
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Fluarix – sujeita a avaliação médica e regras locais.














