
FINOMEL EMULSÃO PARA PERFUSÃO
Pergunte a um médico sobre a prescrição de FINOMEL EMULSÃO PARA PERFUSÃO

Como usar FINOMEL EMULSÃO PARA PERFUSÃO
Introdução
Prospecto: informação para o utilizador
Finomel emulsão para perfusão
Leia todo o prospecto detenidamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou enfermeiro.
- Este medicamento foi prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver seção 4.
Conteúdo do prospecto
- O que é Finomel e para que é utilizado
- O que precisa saber antes de começar a usar Finomel
- Como usar Finomel
- Efeitos adversos possíveis
- Conservação de Finomel
- Conteúdo do envase e informações adicionais
1. O que é Finomel e para que é utilizado
Finomel contém aminoácidos (componentes utilizados para construir proteínas), glicose (carboidratos), lípidos (gordura) e sais (electrolitos).
Finomel é utilizado para alimentar adultos quando a alimentação normal por via oral é insuficiente ou não é possível.
2. O que precisa saber antes de começar a usar Finomel
Não use Finomel:
- Se é alérgico às proteínas de peixe, ovo, soja e amendoim, ao milho/produtos de milho (ver também a seção “Advertências e precauções” a seguir) ou a qualquer um dos componentes deste medicamento (ver a lista na seção 6).
- Se tem níveis altos de gorduras no sangue.
- Se tem problemas graves com o fígado.
- Se tem problemas de coagulação sanguínea.
- Se tem um distúrbio que impede o seu corpo de processar os aminoácidos.
- Se tem problemas graves com os rins.
- Se tem demasiado açúcar no sangue.
- Se tem uma quantidade anormalmente elevada de qualquer um dos electrolitos (sódio, potássio, magnésio, cálcio e/ou fósforo) no sangue.
- Se tem problemas para receber grandes volumes de líquidos nas veias, como edema pulmonar agudo, hiperhidratação e problemas cardíacos descompensados.
- Se tem qualquer problema de saúde agudo e grave, como condições pós-traumáticas graves, diabetes mellitus não controlada, infarto agudo do miocárdio, acidente cerebrovascular, embolia, acidose metabólica, sepsis grave (bactérias no sangue), desidratação hipotônica e coma hiperosmolar.
Em todos os casos, o seu médico decidirá se deve administrar este medicamento com base em fatores como a sua idade, peso e estado clínico, juntamente com os resultados de todas as provas realizadas.
Advertências e precauções
Consulte o seu médico ou enfermeiro antes de começar a usar Finomel se tiver:
- algum problema grave de rim. Deve informar também o seu médico se está a receber tratamento de diálise (rim artificial) ou se tem outro tipo de tratamento para limpar o sangue.
- algum problema grave de fígado
- algum problema de coagulação do sangue
- funcionamento anormal das glândulas adrenais (insuficiência adrenal). As glândulas suprarrenais são glândulas em forma de triângulo localizadas na parte superior dos rins.
- insuficiência cardíaca
- doença pulmonar
- acumulação de água no organismo (hiperhidratação)
- quantidade insuficiente de água no organismo (desidratação)
- excesso de açúcar no sangue (diabetes mellitus) sem receber tratamento para isso
- ataque cardíaco ou choque devido a uma falha cardíaca repentina
- acidose metabólica grave (sangue muito ácida)
- infecção generalizada (septicemia)
A perfusão deve ser interrompida imediatamente se se desenvolver qualquer sinal ou sintoma anormal de uma reação alérgica, como febre, calafrios, erupções na pele ou dificuldade para respirar. Este medicamento contém óleo de peixe, óleo de soja, fosfátidos de ovo e glicose derivada do milho que podem causar reações de hipersensibilidade. Foram observadas reações alérgicas cruzadas entre as proteínas da semente de soja e do amendoim.
A dificuldade para respirar também poderia ser um sinal de que nos pulmões se formaram pequenas partículas que bloqueiam os vasos sanguíneos (precipitados vasculares pulmonares). Se experimentar qualquer dificuldade para respirar, informe o seu médico ou enfermeiro. Eles decidirão a ação a tomar.
Durante a perfusão, se observar dor, ardor, rigidez, inchaço ou mudança de cor da pele no local da perfusão, ou alguma fuga durante a perfusão, avise o seu médico ou enfermeiro. A administração será interrompida imediatamente e reiniciada em outra veia.
Existe risco de infecção ou de sepsis (presença de bactérias ou suas toxinas no sangue), especialmente quando se coloca um tubo (catéter intravenoso) na veia. O médico o observará atentamente em busca de sinais de infecção. O uso de "técnicas assépticas" (sem germes) ao colocar e realizar a manutenção do catéter e ao preparar a fórmula nutricional pode reduzir o risco de infecção.
Foram descritos casos de síndrome de sobrecarga de gordura com produtos semelhantes. Uma redução ou limitação da capacidade do corpo para eliminar as gorduras que contém Finomel pode ocasionar um síndrome de sobrecarga de gordura (ver a seção 4: Efeitos adversos possíveis).
Se você está gravemente desnutrido de forma tal que necessite receber alimentação por via intravenosa, recomenda-se iniciar a nutrição parenteral cuidadosamente e com lentidão.
Provas de laboratório adicionais
Antes de começar a perfusão, devem ser corrigidos os distúrbios metabólicos e o equilíbrio de água e electrolitos do seu organismo. Para comprovar a eficácia e a segurança da administração, o seu médico pode realizar provas de laboratório e clínicas enquanto lhe administrar este medicamento. O seu médico supervisionará o seu estado e pode alterar a dose ou adicionar outro medicamento.
Crianças e adolescentes
Não há experiência com o uso de Finomel em crianças e adolescentes.
Outros medicamentos e Finomel
Informa o seu médico ou enfermeira se está a utilizar, utilizou recentemente ou pode ter que utilizar qualquer outro medicamento.
Finomel contém cálcio. Não deve ser administrado junto ou através da mesma via com o antibiótico ceftriaxona porque podem formar-se partículas. Se for utilizado o mesmo dispositivo para administrar estes medicamentos de forma sucessiva, deve ser bem enxaguado.
Os óleos de oliva e de soja presentes em Finomel contêm vitamina K. Isso não costuma afetar os medicamentos para fluidificar o sangue (anticoagulantes), como a cumarina. No entanto, se tomar anticoagulantes, deve dizer ao seu médico.
Os lípidos que contém esta emulsão podem interferir com os resultados de certas provas de laboratório se a amostra de sangue for colhida antes de que sejam eliminados do seu fluxo sanguíneo (são eliminados geralmente após um período de 5 a 6 horas sem receber os lípidos).
Gravidez e amamentação
Se está grávida ou em período de amamentação, acha que pode estar grávida ou tem intenção de engravidar, consulte o seu médico antes de tomar este medicamento. Não há dados sobre o uso de Finomel em mulheres grávidas ou em período de amamentação. Pode ser considerado o uso deste medicamento durante a gravidez e a amamentação se o seu médico determinar que é necessário.
Condução e uso de máquinas
Não se aplica, pois o medicamento é administrado no hospital.
3. Como usar Finomel
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico.
Este medicamento é administrado por perfusão intravenosa (gotejamento) através de um pequeno tubo, diretamente numa veia.
O seu médico decidirá a dose que lhe será administrada de forma individualizada, dependendo do seu peso corporal e do seu estado funcional. Um profissional de saúde lhe administrará Finomel.
Uso em crianças
A segurança e eficácia em crianças e adolescentes com menos de 18 anos de idade não foram estabelecidas.
Se usar mais Finomel do que deve
É pouco provável que receba demasiado medicamento, pois um profissional de saúde lhe administrará Finomel.
4. Efeitos adversos possíveis
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram. Os seguintes efeitos adversos foram comunicados com uma frequência desconhecida:
- reações de hipersensibilidade (que podem dar-lhe sintomas como inchaço, febre, queda da pressão arterial, erupções cutâneas, urticárias (manchas vermelhas elevadas), rubor, cefaleia;
- síndrome de realimentação (uma doença que se desenvolve quando recebe alimentação após longos períodos de jejum);
- concentrações elevadas de açúcar no sangue (hiperglicemia);
- tonturas;
- dor de cabeça;
- inflamação das veias (tromboflebite);
- embolia pulmonar;
- dificuldades para respirar;
- náuseas;
- vómitos;
- leve aumento da temperatura corporal;
- altas concentrações no sangue (plasma) de composto do fígado;
- síndrome de sobrecarga de gordura;
- perda da perfusão no tecido circundante (extravasação).
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Finomel
Mantenha este medicamento fora da vista e do alcance das crianças.
Conservar na sobrebolsa. Não congelar.
Não utilize este medicamento após a data de validade que aparece na etiqueta da bolsa e do embalagem exterior após CAD. A data de validade é o último dia do mês que se indica.
Não utilize este medicamento se observar partículas visíveis na solução ou se a bolsa estiver danificada.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informação adicional
Composição de Finomel Peri
- Os princípios ativos são
g por 1000 ml | |
Alanina | 6,52 |
Arginina | 3,62 |
Glicina | 3,24 |
Histidina | 1,51 |
Isoluecina | 1,89 |
Leucina | 2,30 |
Lisina (equivalente a cloreto) | 2,28 |
Metionina | 1,26 |
Fenilalanina | 1,76 |
Prolina | 2,14 |
Serina | 1,58 |
Treonina | 1,32 |
Triptófano | 0,57 |
Tirosina | 0,13 |
Valina | 1,83 |
Acetato sódio trihidrato | 1,77 |
Cloruro potássico | 1,41 |
Cloruro cálcio dihidrato | 0,23 |
Sulfato magnésio heptahidrato | 0,78 |
Glicerofosfato sódio hidratado | 1,87 |
Sulfato de zinco heptahidrato | 0,007 |
Glucosa (equivalente a monohidrato) | 77,8 |
Azeite de soja refinado | 8,46 |
Azeite de oliva refinado | 7,05 |
Triglicerídeos de cadeia média | 7,05 |
Azeite de peixe rico em ácidos ômega-3 | 5,64 |
- Os demais componentes são: ácido acético glacial, ácido clorídrico, fosfolipídeos de ovo, glicerol, oleato de sódio, todo-rac-α-tocoferol, hidróxido de sódio, água para preparações injetáveis.
Aspecto de Finomel Peri e conteúdo do envase
As soluções de aminoácidos e glicose são transparentes, incolores ou ligeiramente amareladas e livres de partículas. A emulsão de lípidos é homogênea e de cor branca.
Depois de misturar as 3 câmaras, o produto tem o aspecto de uma emulsão branca.
Tamanhos de envases
4 bolsas de 1085 ml
4 bolsas de 1450 ml
4 bolsas de 2020 ml
Título da autorização de comercialização e responsável pela fabricação
Título da autorização de comercialização:
Baxter SL
Pouet de Camilo, 2.
46394 Ribarroja del Turia (Valência)
Espanha
Responsável pela fabricação:
Baxter SA
Boulevard René Branquart 80
7860 Lessines
Bélgica
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu com os seguintes nomes:
Áustria, República Checa, Alemanha, Grécia, Irlanda, Finomel PeriPolônia, Espanha, Reino Unido
Bélgica, Luxemburgo, Holanda Periomegomel
Dinamarca, Finlândia, Islândia, Noruega, Suécia Finomel Perifer
França Fosomelperi
Itália Finomel
Data da última revisão deste prospecto: Dezembro 2023
A informação detalhada e atualizada deste medicamento está disponível no site da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
<------------------------------------------------------------------------------------------------------------------------>
Esta informação está destinada unicamente a profissionais do setor sanitário
- COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Finomel Peri apresenta-se em uma bolsa de plástico com 3 compartimentos. Cada bolsa contém uma combinação estéril e apirógena de solução de glicose a 13 %, uma solução de aminoácidos a 10 % com eletrólitos e uma emulsão de lípidos a 20 %.
Após misturar o conteúdo dos 3 compartimentos, a composição da emulsão reconstituída é indicada na seguinte tabela:
Substância ativa | 1085 ml | 1450 ml | 2020 ml |
Azeite de peixe rico em ácidos ômega-3 | 6,12 g | 8,16 g | 11,40 g |
Azeite de oliva refinado | 7,65 g | 10,20 g | 14,25 g |
Azeite de soja refinado | 9,18 g | 12,24 g | 17,10 g |
Triglicerídeos de cadeia média | 7,65 g | 10,20 g | 14,25 g |
Alanina | 7,08 g | 9,46 g | 13,17 g |
Arginina | 3,93 g | 5,26 g | 7,31 g |
Glicina | 3,52 g | 4,71 g | 6,55 g |
Histidina | 1,64 g | 2,19 g | 3,05 g |
Isoluecina | 2,05 g | 2,74 g | 3,82 g |
Leucina | 2,50 g | 3,34 g | 4,64 g |
Lisina(equivalente a lisina cloreto) | 1,98 g(2,48 g) | 2,65 g(3,31 g) | 3,69 g(4,61 g) |
Metionina | 1,37 g | 1,83 g | 2,54 g |
Fenilalanina | 1,92 g | 2,56 g | 3,56 g |
Prolina | 2,33 g | 3,11 g | 4,32 g |
Serina | 1,71 g | 2,29 g | 3,18 g |
Treonina | 1,44 g | 1,92 g | 2,67 g |
Triptófano | 0,62 g | 0,82 g | 1,14 g |
Tirosina | 0,14 g | 0,18 g | 0,25 g |
Valina | 1,98 g | 2,65 g | 3,69 g |
Acetato sódio trihidrato | 1,92 g | 2,57 g | 3,57 g |
Cloruro potássico | 1,53 g | 2,05 g | 2,85 g |
Cloruro cálcio dihidrato | 0,25 g | 0,34 g | 0,47 g |
Sulfato magnésio heptahidrato | 0,84 g | 1,13 g | 1,57 g |
Glicerofosfato sódio hidratado | 2,03 g | 2,71 g | 3,77 g |
Sulfato de zinco heptahidrato | 0,008 g | 0,011 g | 0,015 g |
Glucosa(equivalente a glicose monohidratada) | 76,7 g(84,4 g) | 102,6 g(112,8 g) | 142,9 g(157,2 g) |
- POSologia E FORMA DE ADMINISTRAÇÃO
Posologia
A dose deve ser individualizada em função do gasto energético do paciente, seu estado clínico, seu peso corporal e sua capacidade para metabolizar os componentes de Finomel Peri, bem como da energia ou das proteínas adicionais administradas por via oral ou enteral. Portanto, deve ser escolhido o tamanho da bolsa apropriado.
As necessidades diárias médias em adultos são:
- Em pacientes com estado de alimentação normal ou em condições de estresse catabólico leve: de 0,6 a 0,9 g de aminoácidos/kg peso corporal/dia (de 0,10 a 0,15 g de nitrogênio/kg peso corporal/dia).
- Em pacientes com estresse metabólico de moderado a alto, com ou sem desnutrição: de 0,9 a 1,6 g de aminoácidos/kg peso corporal/dia (de 0,15 a 0,25 g de nitrogênio/kg peso corporal/dia).
- Em pacientes com condições especiais (p. ex., queimaduras ou anabolismo marcado) as necessidades de nitrogênio podem ser ainda mais altas.
A dose diária máxima varia de acordo com o estado clínico do paciente e pode mudar de um dia para outro.
A velocidade de administração deve aumentar gradualmente durante a primeira hora.
A velocidade de administração deve ser ajustada tendo em conta a dose que é administrada, a ingestão diária de volume e a duração da perfusão.
O tempo de perfusão recomendado é de 14 a 24 horas.
O regime de 20 ml a 40 ml/kg peso corporal/dia corresponde a 0,6-1,3 g de aminoácidos/kg peso corporal/dia (correspondente a 0,10-0,21 g de nitrogênio/kg peso corporal/dia) e a 14-27 kcal/kg peso corporal/dia de energia total (11-22 kcal/kg peso corporal/dia de energia não proteica).
A velocidade de perfusão máxima para a glicose é de 0,25 g/kg peso corporal/h, para aminoácidos 0,1 g/kg peso corporal/h e para lípidos 0,15 g/kg peso corporal/h.
A velocidade de perfusão não deve exceder 3,0 ml/kg peso corporal/h (correspondente a 0,09 g de aminoácidos, 0,21 g de glicose e 0,09 g de lípidos/kg peso corporal/h).
A dose diária máxima recomendada é de 40 ml/kg peso corporal/dia, que fornecerá 1,3 g de aminoácidos/kg peso corporal/dia (correspondente a 0,21 g de nitrogênio/kg peso corporal/dia), 2,8 g de glicose/kg peso corporal/dia, 1,2 g de lípidos/kg peso corporal/dia e uma energia total de 27 kcal/kg peso corporal/dia (correspondentes a 22 kcal/kg peso corporal/dia de energia não proteica).
População pediátrica
Não foram realizados estudos com Finomel Peri na população pediátrica.
Pacientes com insuficiência renal/hepática
Usar com precaução em pacientes com insuficiência hepática, incluindo colestase e/ou enzimas hepáticas elevadas. Os parâmetros da função hepática devem ser controlados cuidadosamente.
Forma de administração
Uso intravenoso, perfusão em uma veia periférica ou central.
Para consultar as instruções de reconstituição do medicamento antes da administração, ver seção E Precauções especiais de eliminação e outras manipulações.
Se forem utilizadas veias periféricas para as perfusões, deve-se ter em conta a osmolaridade das soluções, pois pode produzir-se tromboflebite. Deve ser avaliado diariamente o local de inserção do catéter para detectar sinais localizados de tromboflebite.
Para obter informações sobre a mistura com outras perfusões ou sangue antes ou durante a administração, ver seção C Incompatibilidades.
- INCOMPATIBILIDADES
Este medicamento não deve ser misturado com outros medicamentos para os quais não se tenha documentado a compatibilidade.
Não deve ser misturado nem administrado ceftriaxona junto com soluções intravenosas que contenham cálcio, incluindo Finomel Peri.
Finomel Peri não deve ser administrado junto com sangue através da mesma via de perfusão.
- SOBREDOSIS
Em caso de sobredosagem, podem ocorrer náuseas, vômitos, calafrios, hiperglicemia e alterações dos eletrólitos, bem como sinais de hipervolemia ou acidose. Nesses casos, deve-se interromper a perfusão imediatamente.
Se ocorrer hiperglicemia, deve ser tratada de acordo com a situação clínica, mediante a administração de insulina adequada e/ou o ajuste da velocidade de perfusão. Da mesma forma, uma sobredosagem poderia causar uma sobrecarga de líquidos, desequilíbrios dos eletrólitos e hiperosmolaridade.
Se os sintomas persistirem após interromper a perfusão, pode-se considerar a hemodiálise, hemofiltrção ou hemodiafiltração.
- PRECAUÇÕES ESPECIAIS DE ELIMINAÇÃO E OUTRAS MANIPULAÇÕES
Para abrir:
- Retire a sobrebolsa protetora.
- Descarte o sobrecito com o absorbente de oxigênio.
- Utilize-a apenas se a bolsa não estiver danificada, os selos não permanentes estiverem intactos (ou seja, não se misturaram os conteúdos dos três compartimentos), se a solução de aminoácidos e a solução de glicose em seus respectivos compartimentos estiverem transparentes, incolores ou ligeiramente amareladas e livres de partículas visíveis, e se a emulsão de lípidos for um líquido homogêneo de aspecto leitoso.
Para misturar as câmaras:
- Certifique-se de que o produto está à temperatura ambiente quando se romperem os selos não permanentes.
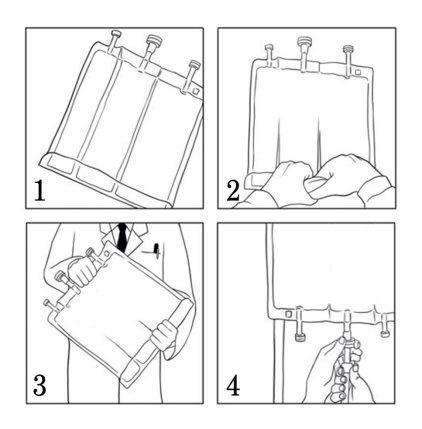
- Enrole manualmente a bolsa sobre si mesma, começando pela parte superior da bolsa (extremo do suporte). (Ilustração 1)Os selos não permanentes desaparecerão do lado próximo às entradas. Continue enrolando até que os selos se abram aproximadamente até a metade de sua longitude. (Ilustração 2)
- Misture a bolsa invertendo-a pelo menos 3 vezes. (Ilustração 3)
- O aspecto após a reconstituição é uma emulsão homogênea de cor leitosa.
Depois de retirar a tampa protetora da via de medicação, podem ser adicionados aditivos compatíveis através da via de medicação (ver a subseção “Adições”).
Retire a tampa protetora da via de perfusão e conecte o equipamento de perfusão. Pendure a bolsa em um suporte de perfusão e realize a perfusão mediante a técnica habitual. (Ilustração 4)
Após abrir a bolsa, deve-se utilizar o conteúdo imediatamente. A bolsa aberta nunca deve ser guardada para perfusão posterior.
Não reconecte uma bolsa a meio utilizar. Não conecte bolsas em série para evitar que se produza uma embolia gasosa.
Adições
Não devem ser realizadas adições à bolsa sem verificar antes a compatibilidade, pois a formação de precipitados ou a desestabilização da emulsão de lípidos poderiam produzir oclusão vascular.
As adições devem ser realizadas em condições assépticas.
Finomel Peri pode ser misturado com os seguintes aditivos:
- preparações multivitamínicas
- preparações de oligoelementos múltiplos
- selênio
- zinc
- sal de sódio
- sal de potássio
- sal de magnésio
- sal de cálcio
- sal de fosfato
A seguinte tabela indicativa de compatibilidades mostra possíveis adições de produtos com oligoelementos múltiplos, como Nutryelt, e produtos multivitamínicos, como Cernevit, bem como genéricos de eletrólitos e oligoelementos em quantidades definidas. A adição de eletrólitos e oligoelementos clinicamente necessários deve levar em conta as quantidades já incluídas na formulação inicial da bolsa.
Aditivo | Conteúdo total após a adiçãopara todos os tamanhos de bolsa de Finomel Peri |
Nutryelt (composição por frasco: zinco 153 µmol; cobre 4,7 µmol; manganês 1,0 µmol; flúor 50 µmol; iodo 1,0 µmol; selênio 0,9 µmol; molibdênio 0,21 µmol; cromo 0,19 µmol; ferro 18 µmol) | 2 frascos/bolsa |
Cernevit (composição por frasco: vit. A (como retinol palmitato) 3500 UI, vit. D3 (colecalciferol) 220 UI, vit. E (alfa-tocoferol) 11,2 UI, vit. C (ácido ascórbico) 125 mg, vit. B1 (tiamina) 3,51 mg, vit. B2 (riboflavina) 4,14 mg, vit. B6 (piridoxina) 4,53 mg, vit. B12 (cianocobalamina) 6 µg, vit. B9 (ácido fólico) 414 µg, vit. B5 (ácido pantotênico) 17,25 mg, vit. B8 (biotina) 69 µg, vit. PP (nicotinamida) 46 mg) | 2 frascos/bolsa |
Sódio | 138 mmol/l |
Potássio | 138 mmol/l |
Magnésio | 5 mmol/l |
Cálcio | 4,6 mmol/l |
Fosfato (orgânico, como glicerofosfato sódio) ou Fosfato (mineral, como fosfato potássico) | 18,5 mmol/l 9,2 mmol/l |
Selênio | 7,6 µmol/l |
Zinco | 0,31 mmol/l |
|
A compatibilidade pode variar entre produtos de diferentes fontes e aconselha-se aos profissionais de saúde a realizar as verificações adequadas ao misturar Finomel Peri com outras soluções parenterais.
Misture bem o conteúdo da bolsa e inspecione visualmente a mistura. Não deve haver sinais de separação de fases da emulsão. A mistura é uma emulsão homogênea de cor branca leitosa.
Ao realizar as adições, deve-se medir a osmolaridade final da mistura antes de administrá-la através de uma veia periférica.
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a FINOMEL EMULSÃO PARA PERFUSÃOForma farmacêutica: PERFURAÇÃO INJETÁVEL, 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 4,76 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 g / 3,5 g / 200 gSubstância ativa: combinationsFabricante: Baxter S.L.Requer receita médicaForma farmacêutica: SOLUÇÃO INJETÁVEL PARA PERFUSÃO, 3,5 g / 200 g / 5,22 g / 1,88 g / 3,92 g / 1,26 g / 7,21 g / 3,36 g / 4,2 g / 5,11 g / 2,94 g / 2,8 g / 662 mg / 1,02 g / 4,76 g / 5,15 g / 5,07 g / 4,06 g / 14,49 g / 0,28 g / 8,05 gSubstância ativa: combinationsFabricante: Baxter S.L.Requer receita médicaForma farmacêutica: PERFURAÇÃO INJETÁVEL, 4,25 g / 300 g / 5,22 g / 1,54 g / 4,76 g / 1,53 g / 8,76 g / 4,08 g / 5,1 g / 6,2 g / 3,57 g / 3,4 g / 662 mg / 1,02 g / 5,78 g / 5,94 g / 6,16 g / 4,93 g / 17,6 g / 0,34 g / 9,78 gSubstância ativa: combinationsFabricante: Baxter S.L.Requer receita médica
Alternativas a FINOMEL EMULSÃO PARA PERFUSÃO noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a FINOMEL EMULSÃO PARA PERFUSÃO em Polónia
Alternativa a FINOMEL EMULSÃO PARA PERFUSÃO em Ukraine
Médicos online para FINOMEL EMULSÃO PARA PERFUSÃO
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de FINOMEL EMULSÃO PARA PERFUSÃO – sujeita a avaliação médica e regras locais.














