DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS

Pergunte a um médico sobre a prescrição de DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS

Como usar DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS
Introdução
Prospecto: informação para o utilizador
Ditralia 25000 UIpelículasbucodispersáveis
colecalciferol (vitamina D3)
Leia todo o prospecto detenidamente antes de começar a tomar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, embora tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Ditralia e para que é utilizado
- O que precisa saber antes de começar a tomar Ditralia
- Como tomar Ditralia
- Possíveis efeitos adversos
- Conservação de Ditralia
- Conteúdo do envase e informações adicionais
1. O que é Ditralia e para que é utilizado
Ditralia contém colecalciferol (vitamina D3). A função principal da vitamina D é garantir uma absorção intestinal correta do cálcio e favorecer a mineralização adequada dos ossos.
Ditralia está indicado para o tratamento inicial da deficiência de vitamina D clinicamente relevante em adultos.
2. O que precisa saber antes de começar a tomar Ditralia
Não tome Ditralia
- se é alérgico ao colecalciferol ou a algum dos outros componentes deste medicamento (incluídos na secção 6)
- se tem uma sensibilidade particular à vitamina D (lesões tissulares em vários órgãos provocadas por sobredosagem de vitamina D) (hipervitaminose D)
- se apresenta níveis altos de cálcio no sangue
- se apresenta níveis altos de cálcio na urina, especialmente se tem cálculos renais
- se tem depósitos de cálcio nos rins (nefrocalcinose)
- se tem uma função renal muito reduzida (insuficiência renal grave)
Se se encontrar em alguma das situações acima, consulte o seu médico ou farmacêutico antes de começar a tomar Ditralia.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a tomar Ditralia.
Informa ao seu médico se está a tomar outros produtos que contenham vitamina D, como alimentos e leite enriquecidos com vitamina D, porque a vitamina D se acumula no organismo e uma sobredosagem pode causar efeitos tóxicos. Ditralia deve ser utilizado com precaução em pacientes imobilizados.
Por isso, é importante não ultrapassar a dose recomendada.
Consulte o seu médico antes de começar a tomar Ditralia:
- se tem tendência elevada à formação de cálculos (pedras) no rim
- se tem um desequilíbrio da hormona paratiroidea (pseudo-hipoparatiroidismo)
Se tiver alguma das seguintes condições, o seu médico controlará os níveis de cálcio ou fosfato no sangue, ou o nível de cálcio na urina:
- se tem problemas de rim,
- se padece «sarcoidose», uma doença do sistema imunológico que pode afetar o fígado, os pulmões, a pele ou os gânglios linfáticos,
- se é uma pessoa de idade avançada em tratamento com glucósidos ou diuréticos.
- se está imobilizado.
Crianças e adolescentes
Este medicamento não é recomendado em crianças e adolescentes menores de 18 anos.
Outros medicamentos e Ditralia
Informa ao seu médico ou farmacêutico se está a tomar, tomou recentemente ou possa ter que tomar qualquer outro medicamento, incluídos os adquiridos sem receita.
Em particular, consulte com o seu médico se está a tomar algum dos seguintes medicamentos:
- diuréticos tiazídicos: os níveis de cálcio no sangue serão controlados regularmente;
- corticosteroides («esteroides», por exemplo, prednisolona ou dexametasona): pode ser necessário aumentar a dose de vitamina D;
- colestiramina (um medicamento para reduzir o colesterol) ou laxantes (por exemplo, óleo de parafina): reduzem a absorção de vitamina D;
- medicamentos para o coração (glucósidos cardíacos): deve estar sob a supervisão de um médico e é possível que supervise o ECG e os níveis de cálcio no sangue;
- anticonvulsivantes (para o tratamento da epilepsia; por exemplo, fenitoína), medicamentos para dormir (por exemplo, hidantoína, barbitúricos) ou primidona: reduzem os efeitos da vitamina D;
- rifampicina, isoniazida (antibióticos): podem reduzir a eficácia da vitamina D;
- actinomicina (um medicamento que se utiliza para tratar alguns tipos de cancro) e antifúngicos derivados do imidazol (por exemplo, clotrimazol e ketoconazol, medicamentos que se utilizam para tratar infecções produzidas por fungos): podem reduzir a eficácia da vitamina D;
- produtos que contenham cálcio em doses elevadas: aumentam o risco de níveis altos de cálcio no sangue;
- produtos que contenham magnésio (por exemplo, antiácidos): não devem ser utilizados durante o tratamento com vitamina D devido ao risco de níveis elevados de magnésio;
- produtos que contenham fósforo em doses elevadas: o seu uso concomitante com vitamina D pode aumentar o risco de níveis elevados de fosfatos no sangue;
- orlistate (um medicamento que se utiliza para tratar a obesidade, incluindo a perda de peso): pode reduzir a absorção de vitamina D. Deve haver um intervalo de 2 horas (antes e depois) entre a administração da vitamina D e a administração de orlistate.
Toma de Ditralia com alimentos e bebidas
Ver secção 3 «Como tomar Ditralia».
Gravidez, lactação e fertilidade
Durante a gravidez e a lactação não devem ser utilizadas doses altas deste produto, mas doses mais baixas. Se está grávida ou em período de lactação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de tomar vitamina D. A vitamina D3 passa para o leite materno. Isto deve ser tido em conta quando se administra ao lactente vitamina D de forma adicional. Não existem dados sobre os efeitos da vitamina D3 na fertilidade. No entanto, não se prevê que níveis normais de vitamina D tenham efeitos negativos na fertilidade.
Condução e uso de máquinas
A influência de Ditralia sobre a capacidade para conduzir e utilizar máquinas é nula ou insignificante.
Ditralia contém amarelo alaranjado:
Amarelo alaranjado (E110), que pode provocar reações de tipo alérgico.
3. Como tomar Ditralia
Siga exatamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, pergunte ao seu médico ou farmacêutico.
Uso em adultos
O seu médico supervisionará o tratamento, porque a dose e a duração da terapia dependem do seu nível de 25-hidroxicolecalciferol (25(OH)D) no sangue, a gravidade da sua doença e a sua resposta ao tratamento.
Dose recomendada: 1 película bucodispersável de 25 000 UI por semana durante o primeiro mês. Depois do primeiro mês de tratamento, o médico pode considerar reduzir a dose
Como alternativa, podem ser seguidas as recomendações nacionais de posologia para o tratamento da deficiência de vitamina D.
Uso em crianças e adolescentes
Não está previsto o uso de Ditralia em crianças e adolescentes menores de 18 anos.
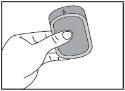
Instruções de uso
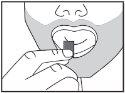
A película bucodispersável deve ser colocada na boca, sobre a língua, e deixar que se dissolva antes de engolir. Deve ser tomada imediatamente após ser retirada do invólucro. Ditralia pode ser tomada com ou sem alimentos.
Importante: Não manipule a película bucodispersável com as mãos húmidas.
|
|
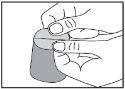
Para isso, segure cada parte com uma mão, com a ajuda dos dedos polegar e indicador. |
|
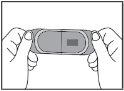
Verá a película bucodispersável colocada em uma das partes separadas do invólucro. |
|
|
|
Se tomar mais Ditralia do que deve
Se tomar uma dose excessiva de Ditralia, consulte imediatamente o seu médico ou farmacêutico. O excesso de vitamina D provoca uma alteração do ciclo do cálcio no organismo. Podem ser experimentados os seguintes sintomas: fraqueza, fadiga, dor de cabeça, náuseas, vómitos, diarreia (e em fases posteriores, constipação), produção excessiva de urina, cálcio urinário, secura bucal, nictúria, sede intensa, perda de apetite, dor muscular e articular, dor abdominal e arritmia.
Em caso de sobredosagem ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone 91 562 04 20, indicando o medicamento e a quantidade ingerida
Tratamento de urgência:
Calcitonina, corticoterapia (que evita a absorção intestinal do cálcio), hidratação abundante, diuréticos para aumentar o conteúdo de cálcio na urina (furosemida), uma dieta baixa em cálcio. Os níveis elevados de cálcio no sangue requerem internamento hospitalar imediato.
Se esquecer de tomar Ditralia
Não tome uma dose dupla para compensar as doses esquecidas.
Se interromper o tratamento com Ditralia
Não deve interromper o tratamento a menos que experimente efeitos adversos. Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico ou farmacêutico.
4. Possíveis efeitos adversos
Como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Interrompa o tratamento com Ditralia e consulte imediatamente o seu médico
- Se experimentar algum dos seguintes sintomas, porque podem ser um sinal de reação alérgica (hipersensibilidade):
- inchaço do rosto, dos lábios, da língua ou da garganta
- dificuldade para engolir
- urticária
- dificuldade para respirar.
Efeitos adversos pouco frequentes (podem afetar até 1 em cada 100 pessoas):
- excesso de cálcio no sangue (hipercalcemia)
- excesso de cálcio na urina (hipercalciúria)
Efeitos adversos raros (podem afetar até 1 em cada 1.000 pessoas):
- prurido, erupção cutânea e urticária
Frequência não conhecida (não pode ser estimada a partir dos dados disponíveis):
- constipação, flatulência, náuseas, dor abdominal, diarreia.
Comunicação de efeitos adversos
Se experimentar algum tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de medicamentos de Uso Humano: https://www.notificaram.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Ditralia
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na caixa após CAD.
Não conserve a uma temperatura superior a 30 °C.
Conservar o produto no embalagem original para protegê-lo da luz.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Deposite os envases e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como se livrar dos envases e dos medicamentos que já não precisa. Desta forma, ajudará a proteger o meio ambiente.
6. Conteúdo do envase e informações adicionais
Composição de Ditralia
O princípio ativo é colecalciferol. Cada película contém 625 microgramas de colecalciferol (vitamina D3), equivalente a 25 000 UI.
Os outros componentes (excipientes) são óleo de oliva refinado, água purificada, maltodextrina, hidroxipropilbetadex, copovidona, manitol (E421), glicerol (E422), polissorbato 80 (E433), monolinoleato de glicerol, dióxido de titânio (E171), sucralosa (E955), aroma de laranja*, ácido ascórbico (E300), todo-rac-alfa-tocoferol (E307), amarelo alaranjado (E110).
*contém:
Aroma: óleo essencial de laranja, óleo de laranja sem terpenos, óleo de limão sem terpenos, óleo de tangerina sem terpenos, hexanoato de etilo, 2-metilbutirato de etilo, butirato de etilo, acetaldeído
Aditivos: butilhidroxianisol (E320), ácido cítrico (E330)
Agentes de carga: maltodextrina, goma arábiga (E414)
Aspecto do produto e conteúdo do envase
Ditralia 25 000 UI é uma película retangular e flexível de cor laranja claro (15 mm x 30 mm).
A película bucodispersável é apresentada em um envase que contém 2 ou 4 películas para cada concentração. Cada invólucro contém uma película bucodispersável.
Titular da Autorização de Comercialização:
IBSA Farmaceutici Italia S.r.l.
Via Martiri di Cefalonia 2
26900 Lodi, Itália
Responsável pela fabricação:
IBSA Farmaceutici Italia S.r.l
S.S. n. 11 Padana Superiore Km 160
20051 Cassina de’ Pecchi (Mi), Itália
ou
Altergon Italia Srl
Zona Industriale
83040 Morra de Sanctis (AV), Itália
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Instituto Bioquímico Ibérico IBSA S.L.
Avenida Diagonal 605,
Planta 8, Local 1,
08028 Barcelona (Espanha)
Data da última revisão deste prospecto:
Agosto 2024
A informação detalhada e atualizada sobre este medicamento está disponível no site da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEISForma farmacêutica: CÁPSULA, 25.000 UISubstância ativa: colecalciferolFabricante: Laboratorios Alter S.A.Requer receita médicaForma farmacêutica: CÁPSULA, 50.000 UISubstância ativa: colecalciferolFabricante: Laboratorios Alter S.A.Requer receita médicaForma farmacêutica: CÁPSULA, 50.000 UISubstância ativa: colecalciferolFabricante: Consilient Health LimitedRequer receita médica
Alternativas a DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS em Polonia
Alternativa a DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS em Ucrania
Médicos online para DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de DITRALIA 25.000 UI COMPRIMIDOS ORODISPERSÍVEIS – sujeita a avaliação médica e regras locais.