
Como usar Sandostatin Lar
Folheto informativo para o doente:
SANDOSTATIN LAR 10 mg pó e solvente para suspensão para injeção
SANDOSTATIN LAR 20 mg pó e solvente para suspensão para injeção
SANDOSTATIN LAR 30 mg pó e solvente para suspensão para injeção
octreotida
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de alguma dúvida, deve consultar o médico, farmacêutico ou enfermeiro.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode ser prejudicial ao outro, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito secundário, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Sandostatin LAR e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Sandostatin LAR
- 3. Como tomar o medicamento Sandostatin LAR
- 4. Efeitos secundários possíveis
- 5. Como conservar o medicamento Sandostatin LAR
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Sandostatin LAR e para que é utilizado
O Sandostatin LAR é um derivado sintético da somatostatina, uma substância que ocorre naturalmente no corpo humano e que inibe a ação de certos hormônios, como o hormônio do crescimento. O medicamento Sandostatin LAR atua mais fortemente do que a somatostatina e o seu efeito dura mais tempo.
O Sandostatin LAR é utilizado
- no tratamento da acromegalia. A acromegalia é uma doença em que o corpo produz demasiada quantidade de hormônio do crescimento. Em pessoas saudáveis, o hormônio do crescimento controla o crescimento dos tecidos, órgãos e ossos. Uma quantidade excessiva de hormônio do crescimento pode causar o aumento do tamanho dos ossos e tecidos, especialmente das mãos e pés. O Sandostatin LAR alivia significativamente os sintomas da acromegalia, que incluem dor de cabeça, suor excessivo, formigamento nas mãos e pés, fadiga e dor nas articulações. Na maioria dos casos, a produção excessiva de hormônio do crescimento é causada pelo aumento da glândula pituitária (adenoma pituitário); o tratamento com o medicamento Sandostatin LAR pode reduzir o tamanho do adenoma.
O Sandostatin LAR é utilizado no tratamento de doentes com acromegalia:
- em quem outros tipos de tratamento da acromegalia (cirurgia ou radioterapia) não são apropriados ou não são eficazes;
- após radioterapia, durante o período de transição, antes de o efeito completo da radioterapia se manifestar.
- para aliviar os sintomas associados à produção excessiva de certos hormônios e outras substâncias pelo estômago, intestinos e pâncreas. A produção excessiva de hormônios e outras substâncias naturais pode ser causada por certas doenças raras do estômago, intestinos ou pâncreas. Isso perturba o equilíbrio hormonal natural do corpo e é a causa de muitos sintomas, como rubor facial, diarreia, baixa pressão arterial, erupções cutâneas e perda de peso. O tratamento com o medicamento Sandostatin LAR ajuda a controlar esses sintomas.
- no tratamento de tumores neuroendócrinos localizados no intestino (por exemplo, no apêndice,
intestino delgado ou cólon)
Os tumores neuroendócrinos são tumores raros localizados em diferentes partes do corpo. O medicamento Sandostatin LAR também é utilizado para inibir o crescimento desses tumores localizados no intestino (por exemplo, no apêndice, intestino delgado ou cólon).
- no tratamento de tumores pituitários que produzem demasiada quantidade de hormônio tireotrópico (TSH) Uma quantidade excessiva de hormônio tireotrópico (TSH) pode causar hipertireoidismo. O medicamento Sandostatin LAR é utilizado em doentes com tumores pituitários que produzem demasiada quantidade de hormônio tireotrópico (TSH):
- quando outros tipos de tratamento (cirurgia ou radioterapia) não são apropriados ou não são eficazes;
- após radioterapia, durante o período de transição, antes de o efeito completo da radioterapia se manifestar.
2. Informações importantes antes de tomar o medicamento Sandostatin LAR
Deve seguir todas as instruções do médico. Elas podem ser diferentes das informações contidas neste folheto.
Deve ler as seguintes informações antes de tomar o medicamento Sandostatin LAR.
Quando não tomar o medicamento Sandostatin LAR:
- se o doente for alérgico à octreotida ou a qualquer outro componente deste medicamento (listados no ponto 6).
Precauções e advertências
Antes de iniciar o tratamento com o medicamento Sandostatin LAR, deve discutir com o médico:
- se o doente souber que tem ou teve pedras na vesícula ou se o doente apresentar algum sintoma como febre, calafrios, dor abdominal ou icterícia; deve informar o médico, pois o tratamento prolongado com o medicamento Sandostatin LAR pode causar a formação de pedras na vesícula. O médico pode solicitar exames regulares da vesícula.
- Se o doente tiver diabetes, pois o medicamento Sandostatin LAR pode afetar os níveis de açúcar no sangue. Se o doente tiver diabetes, os níveis de açúcar no sangue devem ser monitorizados regularmente.
- Se o doente tiver tido níveis baixos de vitamina B no passado, o médico pode solicitar exames regulares dos níveis de vitamina B.
Exames e consultas de acompanhamento
Se o doente estiver a tomar o medicamento Sandostatin LAR por um longo período, o médico pode solicitar exames regulares da função da tireoide.
O médico vai monitorizar a função do fígado do doente.
O médico pode solicitar exames da função dos enzymes pancreáticos.
Crianças
A experiência com o uso do medicamento Sandostatin LAR em crianças é limitada.
Sandostatin LAR e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está a tomar atualmente ou recentemente, bem como sobre os medicamentos que o doente planeia tomar.
Durante o tratamento com o medicamento Sandostatin LAR, é geralmente possível continuar a tomar outros medicamentos.
No entanto, foi relatado que o Sandostatin LAR afeta a ação de certos medicamentos, como a cimetidina, ciclosporina, bromocriptina, quinidina e terfenadina.
Se o doente estiver a tomar um medicamento para controlar a pressão arterial (por exemplo, um antagonista dos receptores beta-adrenérgicos ou um antagonista dos canais de cálcio), o médico pode ajustar a dose.
Em doentes com diabetes, pode ser necessário ajustar a dose de insulina pelo médico.
Se o doente estiver a receber tratamento com oxsodotreotida lutécio (Lu), uma terapia radiofarmacêutica, o médico pode interromper e/ou ajustar o tratamento com o medicamento Sandostatin LAR por um curto período de tempo.
Gravidez e amamentação
Se a doente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planeiar ter um filho, deve consultar o médico antes de tomar este medicamento.
O medicamento Sandostatin LAR só deve ser utilizado durante a gravidez se estritamente necessário.
As mulheres em idade fértil devem utilizar métodos anticoncepcionais eficazes durante o tratamento.
Não se deve amamentar durante o tratamento com o medicamento Sandostatin LAR. Não se sabe se o Sandostatin LAR passa para o leite materno.
Condução de veículos e utilização de máquinas
O Sandostatin LAR não tem ou tem um efeito insignificante na capacidade de conduzir veículos ou utilizar máquinas. No entanto, certos efeitos secundários que podem ocorrer durante o tratamento com o medicamento Sandostatin LAR, como dor de cabeça e fadiga, podem diminuir a capacidade do doente de conduzir veículos ou utilizar máquinas de forma segura.
O medicamento Sandostatin LAR contém sódio
Este medicamento contém menos de 1 mmol (23 mg) de sódio por frasco, ou seja, é considerado "sem sódio".
3. Como tomar o medicamento Sandostatin LAR
O medicamento Sandostatin LAR deve ser administrado exclusivamente por injeção intramuscular na nádega.
Durante o tratamento prolongado, as injeções devem ser administradas alternadamente em cada nádega.
Uso de uma dose maior do que a recomendada do medicamento Sandostatin LAR
Não foram relatados efeitos graves após a sobredosagem do medicamento Sandostatin LAR.
Os sintomas de sobredosagem incluem: ondas de calor, micção frequente, fadiga, depressão, ansiedade e falta de concentração.
Se o doente suspeitar que tomou uma dose maior do que a recomendada e apresentar algum desses sintomas, deve informar imediatamente o médico.
Esquecimento de uma dose do medicamento Sandostatin LAR
Se a injeção não for administrada no prazo estabelecido, deve ser administrada o mais breve possível, e depois continuar o tratamento como antes. A administração de uma dose alguns dias depois não é prejudicial, mas pode causar um retorno temporário dos sintomas da doença até que o esquema de tratamento seja retomado.
Interrupção do tratamento com o medicamento Sandostatin LAR
Após a interrupção do tratamento com o medicamento Sandostatin LAR, os sintomas da doença podem retornar. Por isso, não deve interromper o tratamento com o medicamento Sandostatin LAR sem antes consultar o médico.
Se tiver alguma dúvida adicional sobre o uso deste medicamento, deve consultar o médico, enfermeiro ou farmacêutico.
4. Efeitos secundários possíveis
Como todos os medicamentos, o medicamento Sandostatin LAR pode causar efeitos secundários, embora não todos os doentes os apresentem.
Alguns efeitos secundários podem ser graves. Deve informar imediatamente o médico se o doente apresentar algum dos seguintes sintomas:
Muito frequentes(podem afetar mais de 1 em cada 10 doentes):
- Pedras na vesícula que causam dor nas costas.
- Níveis elevados de açúcar no sangue.
Frequentes(podem afetar até 1 em cada 10 doentes):
- Hipotireoidismo (diminuição da função da tireoide) que afeta o ritmo cardíaco, o apetite ou a perda de peso; fadiga, sensação de frio ou inchaço na parte frontal do pescoço.
- Alterações nos resultados dos exames da função da tireoide.
- Inflamação da vesícula; os sintomas podem incluir dor na parte superior direita do abdômen, febre, náuseas, icterícia.
- Níveis baixos de açúcar no sangue.
- Intolerância à glucose.
- Bradicardia (frequência cardíaca lenta).
Pouco frequentes(podem afetar até 1 em cada 100 doentes):
- Sede, diminuição da quantidade de urina, cor escura da urina, pele seca e vermelha.
- Taquicardia (frequência cardíaca rápida).
Outros efeitos secundários graves
- Reações de hipersensibilidade (alergia), incluindo erupções cutâneas.
- Tipo de reação alérgica (anafilaxia), que pode causar dificuldade em engolir ou respirar, inchaço e formigamento, com possível diminuição da pressão arterial e tontura ou perda de consciência.
- Inflamação do pâncreas; os sintomas podem incluir dor súbita na parte superior do abdômen, náuseas, vómitos, diarreia.
- Inflamação do fígado; os sintomas podem incluir icterícia, náuseas, vómitos, perda de apetite, mal-estar geral, coceira, urina clara.
- Arritmia cardíaca.
- Baixa contagem de plaquetas; pode causar sangramento ou hematoma aumentado.
Se o doente apresentar algum desses sintomas, deve informar imediatamente o médico.
Outros efeitos secundários:
Se o doente apresentar algum dos seguintes efeitos secundários, deve informar o médico, farmacêutico ou enfermeiro. Esses efeitos secundários são geralmente leves e tendem a desaparecer à medida que o tratamento avança.
Muito frequentes(podem afetar mais de 1 em cada 10 doentes):
- Diarreia.
- Dor abdominal.
- Náuseas.
- Constipação.
- Inchaço com flatulência.
- Dor de cabeça.
- Dor no local da injeção.
Frequentes(podem afetar até 1 em cada 10 doentes):
- Desconforto abdominal após as refeições (dispepsia).
- Vómitos.
- Sensação de plenitude no estômago.
- Fezes oleosas.
- Fezes soltas.
- Descoloração das fezes.
- Tontura.
- Perda de apetite.
- Alterações nos resultados dos exames da função do fígado.
- Perda de cabelo.
- Dispneia.
- Fraqueza.
Se ocorrerem algum efeito secundário, deve informar o médico, enfermeiro ou farmacêutico.
Notificação de efeitos secundários
Se ocorrerem algum efeito secundário, incluindo quaisquer efeitos secundários não mencionados neste folheto, deve informar o médico, farmacêutico ou enfermeiro. Os efeitos secundários podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Secundários de Medicamentos da Autoridade de Medicamentos:
Al. Jerozolimskie 181C
02-222 Varsóvia
telefone: 22 49-21-301
fax: 22 49-21-309
Site da Internet: https://smz.ezdrowie.gov.pl
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos secundários permite reunir mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Sandostatin LAR
O medicamento deve ser conservado em um local fora do alcance das crianças.
Conservar no embalagem original para proteger da luz.
Conservar na geladeira (2°C - 8°C). Não congelar.
No dia da administração da injeção, o medicamento Sandostatin LAR pode ser conservado a uma temperatura inferior a 25°C.
Não conservar o medicamento Sandostatin LAR após a reconstituição (a suspensão reconstituída deve ser utilizada imediatamente).
Não utilizar este medicamento após o prazo de validade impresso na etiqueta e embalagem após "EXP" e "Prazo de validade (EXP)". O prazo de validade é o último dia do mês indicado.
Não utilizar este medicamento se verificar a presença de partículas estranhas ou alteração da cor.
Os medicamentos não devem ser eliminados na canalização ou em recipientes de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos que já não são necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Sandostatin LAR
- O princípio ativo do medicamento é a octreotida. Cada frasco contém 10 mg, 20 mg ou 30 mg de octreotida (na forma de octreotida acetato).
- Os outros componentes são: no pó (frasco): poli(DL-lactida-co-glicolida), manitol (E 421). no solvente (ampulheta): carmelose sódica, manitol (E 421), poloxâmero 188,
água para injeção.
Como é o medicamento Sandostatin LAR e que embalagem contém
A embalagem individual contém um frasco de vidro de 6 ml fechado com uma rolha de borracha bromobutilica e uma tampa de alumínio com uma aba de abertura, contendo pó para suspensão para injeção, e uma ampulheta de vidro de 3 ml, protegida por duas rolhas de borracha clorobutilica (na parte da frente e na parte traseira do êmbolo) contendo 2 ml de solvente para suspensão, embalados juntos em um blister selado com um conector de frasco e uma agulha segura para injeção.
Titular da autorização de comercialização
Novartis Portugal - Sociedade Unipessoal, Lda.
Rua da Cêrca, 3470-278 Serpins
Telefone: +351 231 401 400
Fabricante
Novartis Pharma GmbH
Jakov-Lind-Straße 5, Top 3.05
1020 Viena
Áustria
Novartis Pharma NV
Medialaan 40 Bus 1
Vilvoorde, B-1800
Bélgica
Novartis Healthcare A/S
Edvard Thomsens Vej 14
Copenhague S, 2300
Dinamarca
Novartis Finland Oy
Metsäneidonkuja 10
Espoo, FI-02130
Finlândia
Novartis Pharma SAS
8-10 rue Henri Sainte-Claire Deville
92500 Rueil Malmaison
França
Novartis Pharma GmbH
Roonstrasse 25
90429 Nuremberga
Alemanha
Novartis Pharma GmbH
Sophie-Germain-Strasse 10
90443 Nuremberga
Alemanha
Novartis (HELLAS) SA
12º km da estrada nacional Atenas-Lamia
Metamorfosi Attiki, 14451
Grécia
Novartis Hungáry Kft.
Vasút u.13.
Budaörs, 2040
Hungria
Novartis Farma S.p.A.
Via Provinciale Schito 131
80058 Torre Annunziata (NA)
Itália
Novartis Farma S.p.A.
Viale Luigi Sturzo 43
- 20154 – Milão (MI) Itália
Novartis Farma - Produtos Farmacêuticos S.A.
Avenida Professor Doutor Cavaco Silva, n.10E, Taguspark
Porto Salvo, 2740-255
Portugal
Novartis Farmacéutica S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcelona
Espanha
Novartis Sverige AB
Torshamnsgatan 48
164 40 Kista
Suécia
Novartis Pharma B.V.
Haaksbergweg 16
1101 BX Amesterdão
Holanda
Este medicamento está autorizado nos países membros do Espaço Económico Europeu sob as seguintes denominações:
Sandostatin LAR
Áustria, Bulgária, Croácia, Chipre, República Checa, Dinamarca, Estónia,
Finlândia, Alemanha, Grécia, Hungria, Islândia, Irlanda, Letónia,
Lituânia, Malta, Noruega, Polónia, Roménia, Eslováquia, Eslovénia,
Espanha, Suécia
Sandostatine LAR
Bélgica, Luxemburgo, Holanda
Sandostatina LAR
Itália, Portugal
Sandostatine L.P.
França
Data da última revisão do folheto: 10/2024
Informações destinadas apenas a profissionais de saúde:
Qual é a dose de Sandostatin LAR que deve ser utilizada
Acromegalia
Recomenda-se iniciar o tratamento com o medicamento Sandostatin LAR na dose de 20 mg a cada 4 semanas durante 3 meses. Os doentes que estão a tomar o medicamento Sandostatin por via subcutânea devem iniciar o tratamento com o medicamento Sandostatin LAR no dia seguinte à última administração subcutânea do medicamento Sandostatin.
Em seguida, a dose deve ser ajustada com base nos níveis de hormônio do crescimento (GH) e fator de crescimento semelhante à insulina 1/somatomedina C (IGF-1) e nos sintomas clínicos.
Em doentes que, após 3 meses, não apresentam sintomas clínicos e parâmetros bioquímicos (GH; IGF-1) completamente controlados (níveis de GH ainda são maiores que 2,5 microgramas/l), a dose do medicamento pode ser aumentada para 30 mg a cada 4 semanas.
Se, após 3 meses, os parâmetros de GH, IGF-1 e/ou outros sintomas ainda não estiverem suficientemente controlados com a dose de 30 mg, a dose do medicamento pode ser aumentada para 40 mg a cada 4 semanas.
Em doentes que apresentam níveis de GH consistentemente abaixo de 1 micrograma/l, e níveis de IGF-1 normalizados, e que apresentam regressão dos sintomas objetivos e subjetivos da acromegalia após 3 meses de tratamento com a dose de 20 mg, pode ser utilizada a dose de 10 mg a cada 4 semanas. No entanto, especialmente neste grupo de doentes, é recomendável um acompanhamento rigoroso da eficácia do tratamento mediante a determinação dos níveis de GH e IGF-1 e a avaliação dos sintomas clínicos durante o tratamento com esta dose baixa do medicamento Sandostatin LAR.
Em doentes que estão a receber a dose estabelecida do medicamento Sandostatin LAR, deve ser determinado o nível de GH e IGF-1 a cada 6 meses.
Tumores hormonais ativos do estômago, intestinos e pâncreas
- Tratamento de doentes com sintomas associados a tumores neuroendócrinos hormonais ativos do estômago, intestinos e pâncreas Recomenda-se iniciar o tratamento com o medicamento Sandostatin LAR na dose de 20 mg a cada 4 semanas. Os doentes que estão a tomar o medicamento Sandostatin por via subcutânea devem continuar a tomar o medicamento na dose anteriormente eficaz durante 2 semanas após a primeira injeção do medicamento Sandostatin LAR.
Em doentes que, após 3 meses de tratamento, apresentam alívio satisfatório dos sintomas e melhoria dos parâmetros bioquímicos, pode ser reduzida a dose do medicamento Sandostatin LAR para 10 mg a cada 4 semanas.
Em doentes que, após 3 meses de tratamento, apresentam apenas alívio parcial dos sintomas, pode ser aumentada a dose do medicamento Sandostatin LAR para 30 mg a cada 4 semanas.
Nos dias em que, apesar do tratamento com o medicamento Sandostatin LAR, os sintomas associados a tumores do estômago, intestinos e pâncreas são exacerbados, recomenda-se administrar, além disso, o medicamento Sandostatin por via subcutânea na dose anteriormente utilizada antes da introdução do medicamento Sandostatin LAR. Isso pode ocorrer especialmente durante os primeiros 2 meses de tratamento, antes de ser atingido o nível terapêutico do octreotida.
- Tratamento de doentes com tumores neuroendócrinos avançados originados na parte média do prajéjiton ou de localização desconhecida, desde que se tenha excluído a possibilidade de um tumor primário localizado na parte média do prajéjiton A dose recomendada do medicamento Sandostatin LAR é de 30 mg a cada 4 semanas. O tratamento com o medicamento Sandostatin LAR para inibir o crescimento do tumor deve ser continuado na ausência de progressão do tumor.
Tratamento de adenomas que secretam TSH
O tratamento com o medicamento Sandostatin LAR deve ser iniciado com a dose de 20 mg a cada 4 semanas e continuado por 3 meses antes de um possível ajuste da dose.
Em seguida, a dose pode ser ajustada com base na secreção de TSH e hormônio da tireoide.
Instruções para a reconstituição e administração do medicamento Sandostatin LAR
APENAS PARA INJEÇÃO INTRAMUSCULAR PROFUNDA
Conjunto:
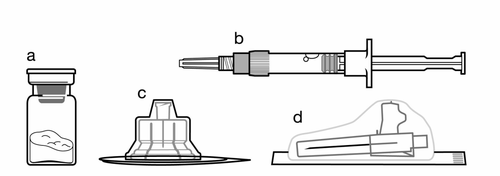
a
Um frasco contendo o medicamento Sandostatin LAR na forma de pó
b
Uma ampulheta contendo o solvente para reconstituir a suspensão
c
Um conector de frasco para reconstituir o medicamento
d
Uma agulha segura para injeção
Deve seguir as instruções abaixo para reconstituir corretamente o medicamento Sandostatin LAR antes de administrar a injeção intramuscular profunda.
Para a reconstituição correta do medicamento Sandostatin LAR, são cruciais 3 pontos.
A não observância destes pontos pode levar a uma administração inadequada do medicamento.
- O conjunto para injeção deve atingir a temperatura ambiente. Deve retirar o conjunto para injeção da geladeira e, antes de reconstituir o medicamento, deixá-lo por pelo menos 30 minutos a uma temperatura ambiente, mas não por mais de 24 horas.
- Após adicionar o solvente, deve deixar o frasco por 5 minutos para garantir a completa dissolução do pó na solução.
- Após a dissolução, deve agitar o frasco com força moderada em movimento horizontal durante pelo menos 30 segundos para formar uma suspensão homogênea. A suspensão do medicamento Sandostatin LAR deve ser preparada imediatamente antes da administração.
O medicamento Sandostatin LAR pode ser administrado apenas por pessoal médico treinado.
Passo 1
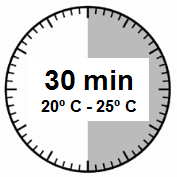
- Retirar o conjunto para injeção do medicamento Sandostatin LAR da geladeira onde foi armazenado.
ATENÇÃO: É muito importante começar o processo de reconstituição apenas quando o conjunto para injeção atingir a temperatura ambiente. Deve deixar o
conjunto em temperatura ambiente por pelo menos
30 minutos antes de reconstituir, mas não por mais de 24 horas.
Observação: O conjunto para injeção pode ser devolvido à geladeira se necessário.
Passo 2
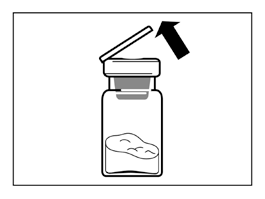
- Remover a tampa plástica do frasco e limpar a rolha de borracha do frasco com um algodão embebido em álcool.
- Remover a cobertura protetora do conector de frasco, mas NÃO remover o conector de frasco da embalagem.
- Segurando o conector de frasco pela embalagem, colocar o conector de frasco no frasco e pressionar até o fim, de modo a que se encaixe com um "clique" audível.
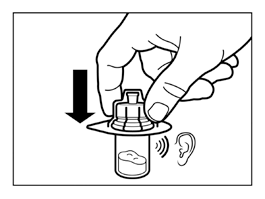
- Remover a embalagem do conector de frasco levantando-a verticalmente para cima.
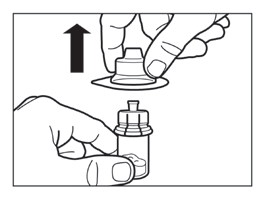
Passo 3
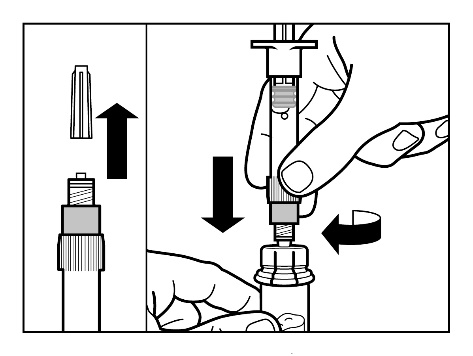
- Remover a tampa da ampulheta com solvente e rosquear a seringa no conector de frasco.
- Pressionar lentamente o êmbolo até o fim para que todo o solvente seja transferido para o frasco.
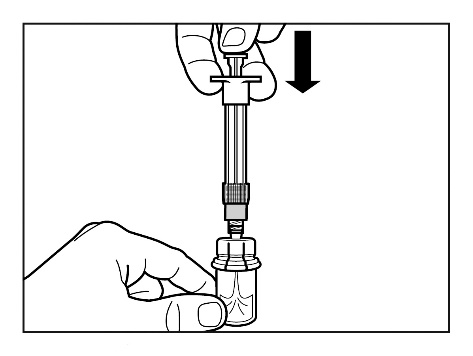
Passo 4
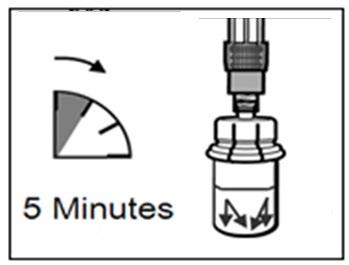
ATENÇÃO: É muito importante deixar o frasco por
5 minutos , para garantir que o pó esteja completamente
dissolvido no solvente.
Observação: Se o êmbolo for empurrado de volta para cima, é uma situação normal,
causada por uma ligeira pressão no frasco.
5 minutos
- Nesta etapa, deve preparar o doente para a administração da injeção.
Passo 5
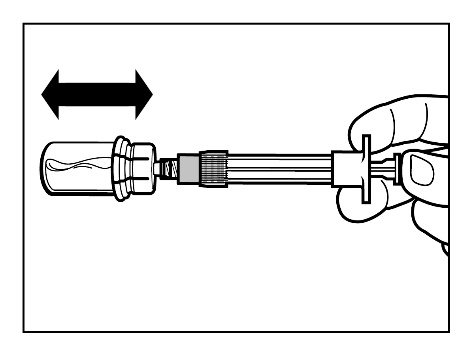
- Após a dissolução completa do pó na solução, deve verificar se o êmbolo está pressionado até o fim da seringa. ATENÇÃO: Segurando o êmbolo pressionado até o fim com força moderada , agite o frasco em movimento horizontal por pelo menos 30 segundos para formar uma suspensão homogênea . Se parte do pó não se dissolver na solução, repita o agitamento moderado por mais 30 segundos.
Passo 6
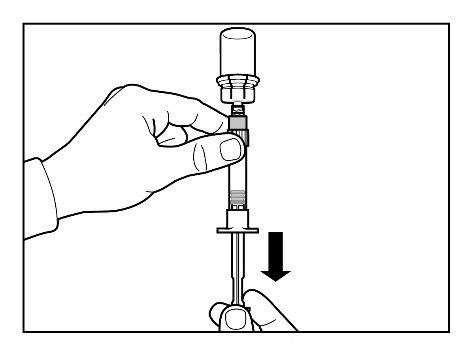
- Preparar o local da injeção limpando com um algodão embebido em álcool.
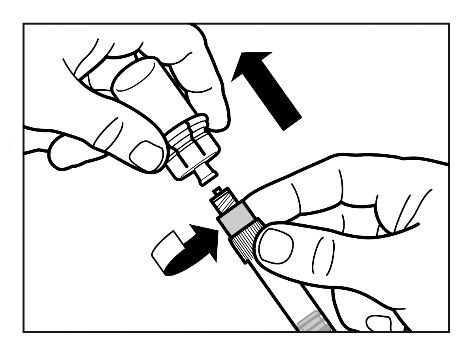
- Inverter a seringa com o frasco para cima e, puxando lentamente o êmbolo, aspirar todo o conteúdo do frasco para a seringa.
- Desrosquear a seringa do conector de frasco.
Passo 7
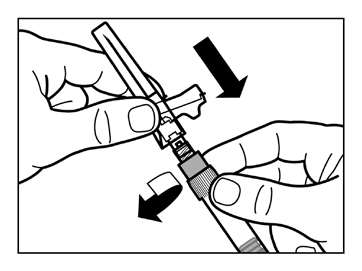
- Aparafusar a agulha segura para injeção na seringa.
- Agitar suavemente a seringa novamente para obter uma suspensão homogênea e leitosa logo antes da administração.
- Remover a cobertura protetora da agulha com um movimento direto para cima.
- Bater levemente com os dedos na seringa para fazer com que as bolhas de ar visíveis sejam deslocadas para cima e, em seguida, removê-las da seringa. Deve verificar se o local da injeção não foi contaminado.
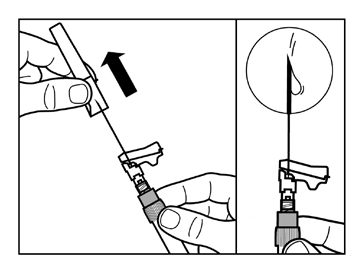
- O medicamento Sandostatin LAR reconstituído agora está pronto para administração imediata - proceder para o Passo 8. Qualquer atraso pode causar a formação de um sedimento.
Passo 8
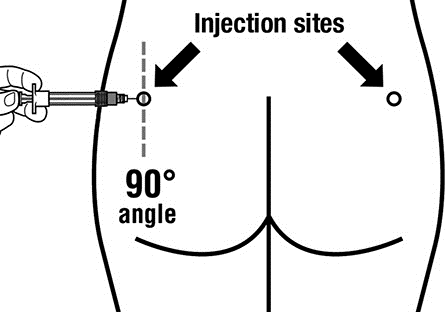
- O medicamento Sandostatin LAR deve ser administrado exclusivamente por injeção intramuscular profunda, NUNCA por via intravenosa.
- Introduzir a agulha completa no músculo da nádega esquerda ou direita a um ângulo de 90 ° com relação à superfície da pele.
- Puxar lentamente o êmbolo da seringa para garantir que a agulha não esteja em um vaso sanguíneo (mudar a posição da agulha se estiver em um vaso sanguíneo).
- Pressionar o êmbolo com força constante até esvaziar a seringa. Retirar a agulha do local da injeção e ativar a cobertura protetora da agulha (conforme as instruções no Passo 9).
Passo 9
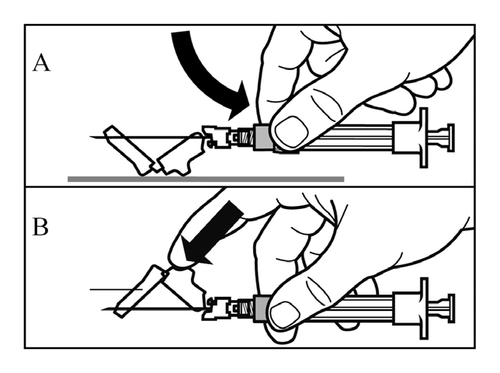
- Ativar a cobertura protetora da agulha utilizando uma das 2 seguintes maneiras:
- pressionar a parte dobrável da cobertura contra uma superfície dura (desenho A)
- ou pressionar a parte dobrável da cobertura com o dedo (desenho B).
- A ativação correta será confirmada por um "clique" audível.
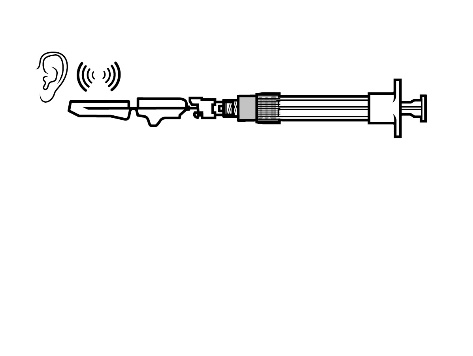
- A seringa deve ser descartada imediatamente (em um recipiente apropriado para objetos cortantes).
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorNovartis Farma - Produtos Farmacêuticos, S.A. Novartis Farma S.p.A. Novartis Farmacéutica, S.A. Novartis Finland Oy Novartis Healthcare A/S Novartis (Hellas) SA Novartis Hungary Kft. Novartis Pharma B.V. Novartis Pharma GmbH Novartis Pharma GmbH Novartis Pharma GmbH Novartis Pharma nv Novartis Pharma SAS Novartis Poland Sp. z o.o. Novartis Sverige AG
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Sandostatin LarForma farmacêutica: Pó, 10 mgSubstância ativa: octreotideRequer receita médicaForma farmacêutica: Pó, 20 mgSubstância ativa: octreotideRequer receita médicaForma farmacêutica: Pó, 30 mgSubstância ativa: octreotideRequer receita médica
Alternativas a Sandostatin Lar noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Sandostatin Lar em Espanha
Alternativa a Sandostatin Lar em Ukraine
Médicos online para Sandostatin Lar
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Sandostatin Lar – sujeita a avaliação médica e regras locais.







