
Oftensin

Pergunte a um médico sobre a prescrição de Oftensin

Como usar Oftensin
Folheto informativo para o doente
Oftensin, 2,5 mg/ml, gotas para os olhos, solução
Oftensin, 5 mg/ml, gotas para os olhos, solução
Timolol
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o doente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Oftensin e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Oftensin
- 3. Como tomar o medicamento Oftensin
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Oftensin
- 6. Conteúdo do pacote e outras informações
1. O que é o medicamento Oftensin e para que é utilizado
A substância ativa do medicamento Oftensin é o timolol. O timolol pertence a um grupo de medicamentos chamados bloqueadores beta-adrenérgicos.
O timolol diminui a pressão intraocular reduzindo a produção de líquido aquoso no olho e aumentando o seu escoamento pela via uveo-escleral. O timolol também tem um efeito mínimo sobre a pressão venosa escleral.
O medicamento não afeta a dilatação da pupila ou a acomodação, pelo que não perturba a visão.
O efeito do medicamento começa cerca de 10-30 minutos após a instilação, e a diminuição máxima da pressão intraocular ocorre 1-2 horas após a administração. O efeito do medicamento dura até 24 horas após a administração única.
As indicações para o uso do medicamento são:
Tratamento da hipertensão ocular em doentes com:
- hipertensão ocular,
- glaucoma crônico de ângulo aberto.
2. Informações importantes antes de tomar o medicamento Oftensin
Quando não tomar o medicamento Oftensin:
- se o doente tiver alergia ao timolol, beta-bloqueadores ou a qualquer outro componente deste medicamento (listados no ponto 6);
- se o doente tiver asma brônquica atual ou prévia;
- se o doente tiver doença pulmonar obstrutiva crônica (DPOC) grave (doença pulmonar grave que pode causar respiração ofegante, dificuldade em respirar e/ou tosse prolongada);
- se o doente tiver bradicardia sinusal;
- se o doente tiver síndrome do nó sinusal;
- se o doente tiver bloqueio auriculoventricular de 2º ou 3º grau;
- se o doente tiver bloqueio sinusal;
- se o doente tiver choque cardiogênico;
- se o doente tiver insuficiência cardíaca descompensada.
Advertências e precauções
Antes de iniciar o tratamento com o medicamento Oftensin, deve discutir com o médico as seguintes situações:
- se o doente apresentar efeitos não desejados semelhantes aos observados com a administração oral de beta-bloqueadores, pois o timolol administrado topicamente no saco conjuntival pode ser absorvido para a corrente sanguínea;
- se o doente estiver a tomar um beta-bloqueador por via oral. Não se recomenda a administração concomitante de dois beta-bloqueadores tópicos;
- se o doente tiver doença cardíaca isquêmica (sintomas podem incluir dor ou pressão no peito, falta de ar ou sufocação), insuficiência cardíaca, pressão arterial baixa;
- se o doente tiver distúrbios do ritmo cardíaco, como bradicardia;
- se o doente tiver distúrbios respiratórios, asma ou DPOC;
- se o doente tiver distúrbios da circulação periférica (por exemplo, doença de Raynaud ou síndrome de Raynaud);
- se o doente tiver diabetes (especialmente instável) tratada com insulina ou medicamentos orais anti-diabéticos, pois o timolol pode mascarar os sintomas de hipoglicemia;
- se o doente tiver glaucoma de ângulo fechado;
- se o doente tiver sido submetido a uma operação de trabeculoplastia;
- se o doente tiver hipertireoidismo, pois o timolol pode mascarar os sintomas objetivos e subjetivos.
Risco de reação anafilática
Os doentes com doença atópica ou reações anafiláticas graves a vários alérgenos no passado podem apresentar uma reação exacerbada ao contacto repetido com esses alérgenos, tanto acidental como durante procedimentos diagnósticos ou terapêuticos. Esses doentes podem não responder às doses de adrenalina normalmente utilizadas no tratamento de reações anafiláticas.
Anestesia durante procedimentos cirúrgicos
Antes da anestesia cirúrgica, deve informar o médico sobre a utilização do medicamento Oftensin, pois o timolol pode alterar a ação de alguns medicamentos utilizados durante a anestesia.
Crianças e jovens
O timolol em forma de gotas para os olhos deve ser utilizado com cautela em crianças e jovens. Em recém-nascidos, lactentes e crianças pequenas, o timolol deve ser utilizado com especial cautela. Se ocorrer tosse, sibilância, respiração anormal ou pausas anormais na respiração (apneia), a administração do medicamento deve ser interrompida imediatamente. Deve contactar o médico o mais rápido possível. Um monitor portátil para detectar apneia pode ser útil.
O timolol foi estudado em lactentes e crianças com idades entre 12 dias e 5 anos que tinham hipertensão ocular aumentada ou glaucoma diagnosticado. Para obter informações mais detalhadas, deve contactar o médico.
Oftensin e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que está a tomar atualmente ou recentemente, bem como sobre os medicamentos que planeia tomar.
O Oftensin pode afetar a ação de outros medicamentos ou a sua ação pode ser alterada por outros medicamentos, incluindo outros colírios para glaucoma. Deve informar o médico se está a tomar ou planeia tomar medicamentos para pressão arterial, medicamentos para doenças cardíacas ou medicamentos para diabetes.
Alguns medicamentos não devem ser tomados em conjunto com o timolol, e em outros casos, o médico pode recomendar uma alteração da dose.
Deve informar o médico sobre a utilização dos seguintes medicamentos:
- outros beta-bloqueadores;
- adrenalina;
- cimetidina, ranitidina, haloperidol e amiodarona, derivados de fenotiazina, reserpina;
- medicamentos antidepressivos, incluindo fluoxetina e paroxetina;
- medicamentos orais que bloqueiam os canais de cálcio (por exemplo, verapamil, diltiazem, nifedipina);
- glicosídeos cardíacos (por exemplo, digoxina);
- quinidina;
- guanetidina;
- parassimpatomiméticos;
- anestésicos inalatórios: enflurano, halotano, isoflurano, metoxiflurano, clorofórmio, ciclopropano, ou tricloroetileno;
- medicamentos anti-diabéticos (insulina ou medicamentos orais anti-diabéticos).
Gravidez e amamentação
Se a paciente estiver grávida ou a amamentar, suspeitar que pode estar grávida ou planeiar ter um filho, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Não deve tomar o medicamento durante a gravidez, a não ser que o médico decida que é necessário.
Não deve tomar o medicamento durante a amamentação, pois o timolol pode passar para o leite materno.
Condução de veículos e utilização de máquinas
Durante o tratamento com o timolol em forma de gotas para os olhos, podem ocorrer distúrbios da visão e tonturas que podem afetar a capacidade de conduzir veículos ou utilizar máquinas. Se ocorrerem esses efeitos não desejados, não deve conduzir veículos ou utilizar máquinas.
Oftensin contém cloreto de benzalcônio, fosfatos
O medicamento contém 0,12 mg de cloreto de benzalcônio em cada ml de solução.
O cloreto de benzalcônio pode ser absorvido por lentes de contato moles e alterar a sua coloração. Deve remover as lentes de contato antes de instilar e esperar pelo menos 15 minutos antes de voltar a colocá-las. Em caso de infecção ocular, não se recomenda o uso de lentes de contato.
O cloreto de benzalcônio também pode causar irritação ocular, especialmente em pessoas com síndrome do olho seco ou distúrbios da córnea (camada transparente da frente do olho). Se ocorrerem sensações anormais no olho, picadas ou dor no olho após a administração do medicamento, deve contactar o médico.
O medicamento Oftensin 2,5 mg/ml contém 12,72 mg de fosfatos em cada ml de solução.
O medicamento Oftensin 5 mg/ml contém 11,78 mg de fosfatos em cada ml de solução.
Em doentes com lesões graves da córnea, os fosfatos podem causar, em casos muito raros, opacidade da córnea devido à acumulação de cálcio durante o tratamento.
O timolol é bem tolerado por doentes que usam lentes de contato rígidas feitas de polimetilmetacrilato (PMMA).
3. Como tomar o medicamento Oftensin
Este medicamento deve ser sempre utilizado de acordo com as recomendações do médico ou farmacêutico. Em caso de dúvidas, deve contactar o médico ou farmacêutico.
Crianças e jovens
Antes de recomendar a utilização do timolol, o médico deve realizar um exame médico detalhado. O médico avaliará cuidadosamente a relação risco-benefício da utilização do timolol.
Se os benefícios superarem os riscos, deve administrar o medicamento na dose mais baixa disponível uma vez por dia.
Em caso de utilização em crianças, a solução 0,1% é geralmente suficiente para diminuir a pressão intraocular. Se a dose não diminuir suficientemente a pressão intraocular, pode ser necessário administrar o medicamento duas vezes por dia, com um intervalo de 12 horas. As crianças, especialmente os recém-nascidos, devem ser observados cuidadosamente durante uma a duas horas após a administração da primeira dose e monitorizados de perto para detectar efeitos não desejados até que sejam submetidos a uma operação cirúrgica.
Período de tratamento
Em crianças e jovens, o medicamento é utilizado para tratamento transitório.
Adultos
Dose recomendada para adultos
Inicialmente, uma gota de solução Oftensin 2,5 mg/ml em cada olho afetado, duas vezes por dia.
Se o resultado do tratamento for insuficiente, o médico pode recomendar a utilização de uma gota de solução Oftensin 5 mg/ml em cada olho afetado, duas vezes por dia.
Deve controlar regularmente a pressão intraocular.
Para diminuir a pressão intraocular, o medicamento Oftensin pode ser utilizado em conjunto com outros medicamentos. No entanto, não se recomenda a administração concomitante de dois beta-bloqueadores tópicos (ver ponto 2. Informações importantes antes de tomar o medicamento Oftensin).
Devido ao facto de que, em alguns doentes, a estabilização da pressão intraocular ocorre apenas após várias semanas de tratamento com timolol, a avaliação da ação do medicamento deve basear-se em medições da pressão intraocular após cerca de 4 semanas de tratamento.
Em muitos casos, se a pressão intraocular estabilizar, o médico pode reduzir a dose do medicamento, recomendando a sua utilização uma vez por dia.
Mudança do tratamento atual
Se o doente tiver tomado previamente outro beta-bloqueador em forma de colírio, deve instilar a dose habitual no último dia de tratamento. No dia seguinte, deve interromper o tratamento com o beta-bloqueador anterior e iniciar o tratamento com Oftensin 2,5 mg/ml - uma gota em cada olho afetado, duas vezes por dia. Se o resultado do tratamento não for satisfatório, o médico pode aumentar a dose para uma gota de solução Oftensin 5 mg/ml em cada olho afetado, duas vezes por dia.
Se o doente tiver tomado previamente um medicamento anti-glaucoma não beta-bloqueador, deve continuar a tomá-lo no dia do tratamento e adicionar uma gota de solução Oftensin 2,5 mg/ml em cada olho afetado, duas vezes por dia. No dia seguinte, deve interromper o tratamento com o medicamento anti-glaucoma anterior e continuar o tratamento com Oftensin.
Se for necessário um aumento da dose do medicamento, o médico pode recomendar a utilização de uma gota de solução Oftensin 5 mg/ml em cada olho afetado, duas vezes por dia.
Modo de administração:
- 1. Deve lavar as mãos e adotar uma posição sentada ou de pé confortável.
- 2. Deve remover a tampa.
- 3. Não deve tocar a ponta do frasco com a ponta do dedo.
- 4. Deve puxar a pálpebra inferior do olho afetado para baixo com a ponta do dedo.
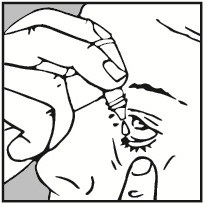
- 5. Deve segurar a parte superior do frasco perto do olho, sem tocar no olho. Deve pressionar suavemente o frasco para que uma gota caia no olho. Deve certificar-se de que não pressiona o frasco com demasiada força, para que não caia mais de uma gota no olho.
- 6. Deve soltar a pálpebra inferior.
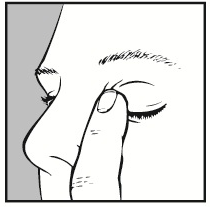
- 7. Após a administração do medicamento, deve fechar os olhos durante o máximo de tempo possível (3-5 minutos) e pressionar a ponta do dedo no canto do olho afetado, perto do nariz. Isso ajudará a evitar que o medicamento entre em outras partes do corpo. Se a gota não cair no olho, deve instilar uma segunda gota.
- 8. Deve fechar o frasco.
Soluções para os olhos podem, em caso de armazenamento e utilização inadequados, estar sujeitas a contaminação bacteriana, o que pode causar infecções oculares graves e perda de visão.
Uso de dose maior do que a recomendada do medicamento Oftensin
Em caso de uso de dose maior do que a recomendada, deve contactar imediatamente o médico, que tomará as medidas adequadas.
Os sintomas de overdose podem incluir: pressão arterial baixa, diminuição da frequência cardíaca, espasmo bronquial e insuficiência cardíaca aguda.
Omissão da administração do medicamento Oftensin
Em caso de omissão de uma dose do medicamento, deve tomá-la assim que possível. No entanto, se estiver perto do horário da próxima dose, não deve tomar a dose omitida. Não deve tomar uma dose dupla para compensar a dose omitida.
Em caso de dúvidas adicionais sobre a utilização deste medicamento, deve contactar o médico ou farmacêutico.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não ocorram em todos. O Oftensin, gotas para os olhos, é geralmente bem tolerado.
Como outros medicamentos tópicos para os olhos, o timolol é absorvido para a corrente sanguínea. Pode causar os mesmos tipos de efeitos não desejados que os beta-bloqueadores administrados por via intravenosa e/ou oral. A frequência de ocorrência de efeitos não desejados gerais após administração tópica para os olhos é menor do que após administração oral ou injeção.
Os efeitos não desejados listados incluem também aqueles observados em toda a classe de beta-bloqueadores para os olhos.
- Reações alérgicas generalizadas, incluindo angioedema, que podem ocorrer em locais como face e extremidades, e podem bloquear as vias aéreas, causando dificuldade em engolir ou respirar. Urticária ou erupção cutânea pruriginosa, erupção cutânea localizada e generalizada, prurido, reação alérgica grave que pode ser fatal.
- Hipoglicemia.
- Dificuldade em dormir (insônia), depressão, pesadelos, perda de memória, alucinações*.
- Desmaio, acidente vascular cerebral, diminuição do fluxo sanguíneo para o cérebro, agravamento dos sintomas objetivos e subjetivos de miastenia (distúrbio muscular), tonturas, sensações anormais, como formigamento e dormência, dores de cabeça.
- Sintomas objetivos e subjetivos de irritação ocular (por exemplo, ardor, picadas, prurido, lacrimejamento, vermelhidão), blefarite, ceratite, visão turva e descolamento da camada sob a retina, que contém vasos sanguíneos, após operações de trabeculoplastia, que podem causar distúrbios da visão, diminuição da sensibilidade da córnea, secura nos olhos, lesões e defeitos da córnea (camada frontal do olho), ptose (olho semi-fechado), visão dupla.
- Diminuição da frequência cardíaca, dor no peito, palpitações, edema (acúmulo de líquido), alterações no ritmo e frequência cardíaca, insuficiência cardíaca congestiva (doença cardíaca com falta de ar e edema nos pés e pernas devido ao acúmulo de líquido), distúrbios do ritmo cardíaco, parada cardíaca, insuficiência cardíaca.
- Pressão arterial baixa, fenômeno de Raynaud, mãos e pés frios.
- Constrição das vias aéreas nos pulmões (principalmente em doentes com doenças pré-existentes), dificuldade em respirar, tosse.
- Distúrbios do paladar, náuseas, dispepsia, diarreia, secura na boca, dores abdominais, vômitos.
- Perda de cabelo, erupção cutânea esbranquiçada (erupção psoríase-like) ou piora da psoríase, erupção cutânea.
- Dores musculares não relacionadas à atividade física.
- Distúrbios sexuais, diminuição da libido.
- Fraqueza e/ou fadiga.
*frequência desconhecida (frequência não pode ser estimada com base nos dados disponíveis)
Outros efeitos não desejados relatados em associação com o uso de gotas para os olhos que contêm fosfatos
Em doentes com lesões graves da córnea, os fosfatos podem causar, em casos muito raros, opacidade da córnea devido à acumulação de cálcio durante o tratamento.
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo quaisquer efeitos não desejados não mencionados neste folheto, deve informar o médico ou farmacêutico, ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitorização de Efeitos Não Desejados de Medicamentos do Instituto Nacional de Farmacologia
Rua Jerozolimskie 181C
02-222 Varsóvia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
Sítio na Internet: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos não desejados pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Oftensin
Deve conservar o medicamento em local não visível e inacessível às crianças.
Deve conservar em temperatura até 25°C, protegido da luz.
Prazo de validade após a primeira abertura do frasco: 28 dias.
Não deve utilizar este medicamento após o prazo de validade impresso nas embalagens após: EXP.
O prazo de validade indica o último dia do mês indicado.
A inscrição na embalagem após o abreviado EXP indica o prazo de validade, e após o abreviado Lot indica o número da série.
Os medicamentos não devem ser eliminados na canalização ou em recipientes de lixo doméstico. Deve perguntar ao farmacêutico como eliminar os medicamentos de que já não precisa. Este procedimento ajudará a proteger o meio ambiente.
6. Conteúdo do pacote e outras informações
O que contém o medicamento Oftensin
- A substância ativa do medicamento é o timolol. Cada ml de solução contém 2,5 mg ou 5 mg de timolol na forma de maleato de timolol.
- Os outros componentes são: di-hidrogenofosfato de sódio di-hidratado, fosfato dissódico dodeca-hidratado, cloreto de benzalcônio, água purificada.
Como é o medicamento Oftensin e que conteúdo tem o pacote
O pacote contém 5 ml de solução.
Titular da autorização de comercialização
Zakłady Farmaceutyczne POLPHARMA S.A.
Rua Pelplińska 19, 83-200 Starogard Gdański
tel. + 48 22 364 61 01
Fabricante
Warszawskie Zakłady Farmaceutyczne Polfa S.A.
Rua Karolkowa 22/24, 01-207 Varsóvia
Data da última atualização do folheto:
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorWarszawskie Zakłady Farmaceutyczne POLFA S.A.
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a OftensinForma farmacêutica: Gotas, 5 mg/mlSubstância ativa: timololFabricante: SIEGFRIED El Masnou, S.A.Requer receita médicaForma farmacêutica: Gotas, 2.5 mg/mlSubstância ativa: timololFabricante: Warszawskie Zakłady Farmaceutyczne POLFA S.A.Requer receita médicaForma farmacêutica: Gotas, 5 mg/mlSubstância ativa: timololFabricante: Ursapharm Arzneimittel GmbHRequer receita médica
Alternativas a Oftensin noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Oftensin em Espanha
Alternativa a Oftensin em Ukraine
Médicos online para Oftensin
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Oftensin – sujeita a avaliação médica e regras locais.














