
Fem 7 Combi

Pergunte a um médico sobre a prescrição de Fem 7 Combi

Como usar Fem 7 Combi
Folheto informativo para o doente:
Fem 7 Combi
Fase I: 50µg/24 h (1,5 mg)
Fase II: 50µg/24 h (1,5 mg) + 10 µg/24 h (1,5 mg)
Sistema transdérmico
(Estradiol + Levonorgestrel)
Deve ler atentamente o conteúdo do folheto antes de usar o medicamento, pois contém informações importantes para o doente.
- Deve conservar este folheto para poder reler se necessário.
- Em caso de dúvidas, deve consultar um médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outras pessoas, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o doente apresentar algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, deve informar o seu médico ou farmacêutico. Ver ponto 4.
Índice do folheto:
- 1. O que é o medicamento Fem 7 Combi e para que é usado
- 2. Informações importantes antes de usar o medicamento Fem 7 Combi
- 3. Como usar o medicamento Fem 7 Combi
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Fem 7 Combi
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Fem 7 Combi e para que é usado
Fem 7 Combi é um sistema transdérmico que contém estradiol e levonorgestrel como substâncias ativas.
O estradiol presente no medicamento Fem 7 Combi é o 17β (beta) estradiol, um hormônio idêntico ao estradiol natural, produzido principalmente pelas células da granulosa do folículo ovariano. Em menor quantidade, os estrogênios são produzidos pelo corpo lúteo, placenta e supra-renais. Após a menopausa (quando as menstruações param completamente), a atividade ovariana diminui, e o organismo produz apenas uma pequena quantidade de estradiol.
A falta de estrogênios é a causa de vários distúrbios em muitas mulheres: ondas de calor, distúrbios do sono, atrofia da mucosa do trato urogenital e outras doenças ósseas, como a osteoporose.
O levonorgestrel pertence a um grupo de hormônios sexuais, os progestágenos, que têm efeito sobre a mucosa do trato urogenital das mulheres com útero conservado. O levonorgestrel diminui o risco de crescimento excessivo da mucosa do útero e de câncer do trato urogenital.
O medicamento Fem 7 Combi está disponível na forma de sistema transdérmico terapêutico. Isso significa que o estrogênio e o levonorgestrel, cuja falta o organismo precisa ser suprida, são liberados lentamente para o organismo através da pele por meio de um adesivo (terapia hormonal substitutiva) para tratar os sintomas desagradáveis da menopausa.
A experiência com o uso em mulheres com mais de 65 anos é limitada.
Fem 7 Combi não é um medicamento anticoncepcional.
2. Informações importantes antes de usar o medicamento Fem 7 Combi
Quando não usar o medicamento Fem 7 Combi
- se o doente tiver alergia às substâncias ativas ou a qualquer um dos outros componentes do medicamento (listados no ponto 6);
- se o doente tiver ou suspeitar de câncer de mama (ver subponto abaixo sobre câncer de mama);
- se o doente tiver ou suspeitar de câncer do endométrio (endométrio - mucosa do útero) ou de qualquer outro tumor maligno dependente de estrogênio (ver subpontos abaixo sobre câncer do endométrio e câncer do ovário);
- se o doente tiver hiperplasia não tratada do endométrio (aumento do número de células da mucosa do útero que reveste a sua cavidade);
- se o doente tiver sangramento genital de causa desconhecida;
- se o doente tiver ou tiver tido trombose venosa profunda ou em outras localizações (trombose venosa profunda) ou embolia pulmonar (ver subponto abaixo sobre trombose);
- se o doente tiver ou tiver tido recentemente um ataque cardíaco, acidente vascular cerebral ou angina de peito (ver ponto abaixo sobre doença cardíaca isquêmica e acidente vascular cerebral);
- se o doente tiver doença hepática ativa ou tiver tido doença hepática no passado, até que os resultados dos testes de função hepática sejam normais;
- se o doente tiver porfiria.
O uso do medicamento em crianças é contraindicado.
Precauções e advertências
Antes de iniciar o uso do Fem 7 Combi, deve discutir com o médico ou farmacêutico.
Antes de iniciar ou reiniciar a terapia hormonal substitutiva, o médico realizará um exame médico detalhado, incluindo um histórico familiar. O exame físico (incluindo o exame dos órgãos pélvicos e das mamas) deve incluir os dados do histórico e as contraindicações e advertências para a terapia hormonal substitutiva. Durante o tratamento, o médico realizará exames de controle periódicos, cuja frequência e tipo devem ser adaptados às necessidades da doente. A terapia hormonal substitutiva deve ser usada por tanto tempo quanto o benefício do tratamento superar o risco.
Se a doente notar mudanças nas mamas que se assemelham a tumores mamários (ver ponto "Câncer de mama" abaixo), deve informar o médico, que pode encaminhá-la para uma mamografia.
Situações que requerem vigilância
Se qualquer uma das seguintes condições ocorrer, ocorreu anteriormente ou piorou durante a gravidez ou terapia hormonal anterior, o estado de saúde da doente deve ser monitorado de perto pelo médico.
Deve ser considerado que as condições listadas podem ocorrer novamente ou piorar durante o tratamento com o produto Fem 7 Combi. Isso se aplica particularmente a condições como:
- tumores benignos do útero (miomas uterinos / leiomiomas uterinos) ou endometriose (presença de fragmentos da mucosa do útero em diferentes locais na pelve);
- distúrbios tromboembólicos prévios ou fatores de risco (ver abaixo);
- fatores de risco para tumores dependentes de estrogênio, como câncer de mama em parentes de primeiro grau;
- hipertensão;
- doenças hepáticas (por exemplo, adenoma hepático);
- diabetes com ou sem lesões vasculares;
- cálculos biliares;
- enxaqueca ou cefaleia intensa;
- lupus eritematoso sistêmico (doença autoimune);
- hiperplasia do endométrio no passado (ver abaixo);
- epilepsia;
- asma;
- otosclerose (doença que afeta a orelha média e pode causar perda auditiva);
- angioedema hereditário ou adquirido.
Interrupção do tratamento. O tratamento deve ser interrompido imediatamente se ocorrer qualquer uma das condições listadas no ponto "Quando não usar o medicamento Fem 7 Combi" ou se ocorrer:
- icterícia ou piora da função hepática;
- aumento significativo da pressão arterial;
- aparecimento de cefaleia de enxaqueca;
- gravidez;
- edema facial, lingual e / ou faríngeo e / ou dificuldade para engolir ou urticária, associados a dificuldade para respirar, que sugerem angioedema.
Segurança do uso da terapia hormonal substitutiva
Além dos benefícios, a terapia hormonal substitutiva está associada a alguns riscos que a doente deve considerar ao decidir sobre este tipo de tratamento ou sua continuação.
Câncer do endométrio (câncer da mucosa do útero)
A administração de estrogênios sozinhos por um período prolongado aumenta o risco de câncer da mucosa do útero (câncer do endométrio). A administração adicional de progestágeno reduz significativamente esse risco.
- As doentes com útero conservado geralmente recebem uma terapia que combina progestágeno e estrogênio. Essas substâncias podem ser prescritas separadamente ou como um medicamento combinado na terapia hormonal substitutiva.
- No caso de doentes com útero removido (após histerectomia), o médico discutirá com a doente a segurança do uso de estrogênio sozinho sem progestágeno.
- No caso de doentes com útero removido devido à endometriose, em que ainda existem focos residuais de endometriose, o risco pode estar relacionado a qualquer fragmento da mucosa do útero que permaneça no organismo. Portanto, o médico pode prescrever uma terapia hormonal substitutiva que combine progestágeno e estrogênio.
Comparação:
Comparando as mulheres com útero conservado que não usam terapia hormonal substitutiva - cerca de 5 em 1.000 delas terão câncer do útero diagnosticado entre 50 e 65 anos de idade.
No caso de mulheres que usam terapia hormonal substitutiva com estrogênios sozinhos, esse número será 2 a 12 vezes maior , dependendo da dose e duração da terapia hormonal substitutiva.
A adição de progestágeno à terapia hormonal substitutiva com estrogênios sozinhos reduz significativamente o risco de câncer do útero.
Se a doente apresentar sangramento intermenstrual ou manchamento, geralmente não deve ser motivo de preocupação, especialmente durante os primeiros meses de tratamento com terapia hormonal substitutiva.
No entanto, se o sangramento ou manchamento
- persistir por mais tempo do que os primeiros meses
- ocorrer pela primeira vez algum tempo após o início da terapia hormonal substitutiva, a doente deve informar o médico. Isso pode indicar que a mucosa do útero engrossou.
Câncer de mama
Mulheres com câncer de mama atual ou prévio não devem usar terapia hormonal substitutiva.
Os dados confirmam que o uso de terapia hormonal substitutiva (com combinação de estrogênio e progestágeno ou estrogênio sozinho) aumenta o risco de câncer de mama. O risco adicional depende de quanto tempo a doente usa a terapia hormonal substitutiva. Esse risco adicional torna-se aparente após 3 anos de uso da terapia hormonal substitutiva.
Após a interrupção da terapia hormonal substitutiva, o risco adicional diminuirá com o tempo, mas o risco pode persistir por 10 anos ou mais se a terapia hormonal substitutiva durar mais de 5 anos.
O risco de câncer de mama também é maior:
- em doentes cuja parente de primeiro grau teve câncer de mama
- em doentes com obesidade significativa
Comparação:
No caso de mulheres entre 50 e 54 anos de idade que não usam terapia hormonal substitutiva , o câncer de mama será diagnosticado em cerca de 13 a 17 em 1.000 mulheres nesse período de 5 anos.
No caso de mulheres de 50 anos de idade que iniciam uma terapia hormonal substitutiva de 5 anos com estrogênio, o número de casos será de 16 a 17 em 1.000 doentes (ou seja, 0 a 3 casos adicionais ).
No caso de mulheres de 50 anos de idade que iniciam uma terapia hormonal substitutiva de 5 anos com estrogênio e progestágeno, o número de casos será de 21 em 1.000 doentes (ou seja, 4 a 8 casos adicionais ).
No caso de mulheres entre 50 e 59 anos de idade que não usam terapia hormonal substitutiva , o câncer de mama será diagnosticado em cerca de 27 em 1.000 mulheres nesse período de 10 anos.
No caso de mulheres de 50 anos de idade que iniciam uma terapia hormonal substitutiva de 10 anos com estrogênio, o número de casos será de 34 em 1.000 doentes (ou seja, 7 casos adicionais ).
No caso de mulheres de 50 anos de idade que iniciam uma terapia hormonal substitutiva de 10 anos com estrogênio e progestágeno, o número de casos será de 48 em 1.000 doentes (ou seja, 21 casos adicionais ).
Se a doente notar mudanças nas mamas, como:
- depressões na pele da mama
- alterações nos mamilos
- quaisquer nódulos visíveis ou palpáveis, deve procurar um médico o mais rápido possível.
Trombose
A terapia hormonal substitutiva está associada a um risco relativo maior de trombose venosa, especialmente no primeiro ano de uso da terapia hormonal substitutiva.
Essas tromboses nem sempre são uma ameaça à saúde e à vida, mas se uma delas se deslocar para os pulmões, pode causar dor no peito, falta de ar, colapso e até morte. Essa condição é chamada de embolia pulmonar.
A trombose venosa profunda e a embolia pulmonar são exemplos de doença tromboembólica venosa (DTMV) .
A ocorrência de tromboses é mais provável:
- em doentes com obesidade significativa
- em doentes com tromboses no passado
- se houver história familiar de tromboses
- se a doente tiver tido um ou mais abortos espontâneos
- se a doente tiver distúrbios de coagulação que requerem tratamento com medicamentos anticoagulantes
- em doentes imobilizadas por um longo período devido a uma grande cirurgia, lesão ou doença
- em doentes com uma doença rara chamada lupus eritematoso sistêmico.
Se qualquer uma dessas condições ocorrer na doente, ela deve consultar um médico para saber se pode iniciar a terapia hormonal substitutiva.
Comparação:
Comparando mulheres de cerca de 50 anos de idade que não usam terapia hormonal substitutiva - cerca de 3 em 1.000 delas terão uma trombose em um período de 5 anos.
No caso de mulheres de cerca de 50 anos de idade que usam terapia hormonal substitutiva, esse número será de 7 em 1.000 .
Comparando mulheres de cerca de 60 anos de idade que não usam terapia hormonal substitutiva - cerca de 8 em 1.000 delas terão uma trombose em um período de 5 anos.
No caso de mulheres de cerca de 60 anos de idade que usam terapia hormonal substitutiva, esse número será de 17 em 1.000 .
Se a doente apresentar:
- inchaço doloroso na perna
- dor no peito súbita
- dificuldade para respirar, deve procurar um médico o mais rápido possível e não usar a terapia hormonal substitutiva até que o médico concorde. Esses podem ser sintomas de trombose.
Se a doente planeja uma cirurgia , deve informar o médico. Pode ser necessário interromper a terapia hormonal substitutiva 4 a 6 semanas antes da cirurgia para reduzir o risco de formação de trombose. O médico informará a doente sobre quando pode reiniciar a terapia hormonal substitutiva.
Doença cardíaca isquêmica
A terapia hormonal substitutiva não é recomendada para mulheres com doença cardíaca atual ou recente. Se a doente já teve doença cardíaca, deve consultar um médico para saber se pode usar a terapia hormonal substitutiva.
A terapia hormonal substitutiva não ajuda a prevenir doenças cardíacas.
Estudos com um tipo de terapia hormonal substitutiva (estrogênios conjugados equinos e medroxiprogesterona) mostraram que o risco de doença cardíaca pode ser ligeiramente maior durante o primeiro ano de uso do medicamento.
No caso de outras terapias hormonais substitutivas, é provável que o risco seja semelhante, mas não há certeza.
Se a doente apresentar:
- dor no peito que irradia para o braço e o pescoço, deve procurar um médico o mais rápido possível e não usar a terapia hormonal substitutiva até que o médico concorde. Esses podem ser sintomas de doença cardíaca.
Acidente vascular cerebral
Estudos recentes sugerem que a terapia hormonal substitutiva aumenta ligeiramente o risco de acidente vascular cerebral. Outros fatores que podem aumentar o risco de acidente vascular cerebral incluem:
- envelhecimento
- hipertensão
- tabagismo
- consumo excessivo de álcool
- arritmia cardíaca
Se a doente tiver algum desses fatores de risco para acidente vascular cerebral ou se já teve um acidente vascular cerebral, deve consultar um médico para saber se pode usar a terapia hormonal substitutiva.
Comparação:
Comparando mulheres de cerca de 50 anos de idade que não usam terapia hormonal substitutiva - cerca de 3 em 1.000 delas terão um acidente vascular cerebral em um período de 5 anos.
No caso de mulheres de cerca de 50 anos de idade que usam terapia hormonal substitutiva, esse número será de 4 em 1.000 .
Comparando mulheres de cerca de 60 anos de idade que não usam terapia hormonal substitutiva - cerca de 11 em 1.000 delas terão um acidente vascular cerebral em um período de 5 anos.
No caso de mulheres de cerca de 60 anos de idade que usam terapia hormonal substitutiva, esse número será de 15 em 1.000 .
Tumor do ovário
O tumor do ovário é raro, ocorrendo muito menos frequentemente do que o câncer de mama.
O uso de terapia hormonal substitutiva que inclui apenas estrogênios ou uma combinação de estrogênios e progestágenos está associado a um risco ligeiramente aumentado de tumor do ovário.
O risco de tumor do ovário depende da idade. Por exemplo, em mulheres entre 50 e 54 anos de idade que não usam terapia hormonal substitutiva, o tumor do ovário será diagnosticado em cerca de 2 em 2.000 mulheres em um período de 5 anos.
Em mulheres que usam terapia hormonal substitutiva por 5 anos, o tumor do ovário ocorrerá em cerca de 3 em 2.000 mulheres que usam o tratamento (ou seja, cerca de 1 caso adicional).
Outras condições
Os estrogênios podem causar retenção de líquidos, portanto, as doentes com distúrbios cardíacos ou renais devem ser monitoradas de perto.
As doentes com insuficiência renal terminal devem ser monitoradas de perto, pois pode ocorrer um aumento na concentração das substâncias ativas do produto Fem 7 Combi no sangue.
As mulheres com endometriose prévia devem ser monitoradas de perto durante a terapia de substituição hormonal com estrogênios ou outras terapias hormonais substitutivas, pois foram relatados casos raros de aumento significativo dos triglicerídeos no sangue, o que pode levar à pancreatite após o uso de estrogênios.
Os estrogênios afetam as concentrações de outros hormônios e proteínas.
Interacções com outros medicamentos
O metabolismo dos estrogênios e progestágenos pode ser aumentado durante o uso concomitante de substâncias que induzem a atividade das enzimas que metabolizam medicamentos (especialmente as enzimas do citocromo P450), como medicamentos anticonvulsivantes (por exemplo, fenobarbital, fenitoína, carbamazepina, primidona) e medicamentos antibacterianos (rifampicina, rifabutina, nevirapina, efavirenz).
O ritonavir e a nelfinavir, embora sejam conhecidos como inibidores potentes das enzimas, têm propriedades indutoras das enzimas quando usados concomitantemente com hormônios esteroides.
Os produtos à base de plantas que contêm a erva de São João (Hypericum perforatum) podem induzir o metabolismo dos estrogênios e progestágenos.
Com a administração transdérmica, não ocorre o "efeito de primeiro passagem" no fígado, portanto, as substâncias indutoras das enzimas têm menos efeito sobre os estrogênios e progestágenos administrados por essa via do que sobre os hormônios administrados por via oral.
Do ponto de vista clínico, o metabolismo aumentado dos estrogênios e progestágenos pode levar a uma redução da eficácia desses hormônios e a distúrbios no perfil de sangramento.
Atenção! Isso também se aplica a medicamentos usados recentemente.
A terapia hormonal substitutiva pode afetar a ação de outros medicamentos:
- medicamento para epilepsia (lamotrigina), pois pode aumentar a frequência de convulsões;
- medicamentos usados no tratamento da hepatite C (como o esquema de tratamento com ombitasvir / paritaprevir / ritonavir com ou sem dasabuvir, e o esquema de tratamento com glecaprevir / pibrentasvir) podem causar um aumento nos parâmetros de função hepática nos testes laboratoriais de sangue (aumento da atividade da enzima hepática ALT) em mulheres que usam medicamentos anticoncepcionais hormonais combinados que contenham etinilestradiol. O medicamento Fem 7 Combi contém estradiol em vez de etinilestradiol. Não se sabe se o aumento da atividade da enzima hepática ALT pode ocorrer durante o uso do medicamento Fem 7 Combi com esse tipo de esquema de tratamento combinado para hepatite C.
A doente deve informar o médico sobre todos os medicamentos que está usando atualmente ou recentemente, e também sobre os medicamentos que planeja usar. O médico dará as instruções apropriadas.
Exames laboratoriais
Se for necessário realizar um exame de sangue, a doente deve informar o médico ou o pessoal do laboratório sobre o uso do medicamento Fem 7 Combi, pois o medicamento pode afetar os resultados de alguns exames.
Gravidez e amamentação
Se a doente estiver grávida ou amamentando, achar que pode estar grávida ou planejar ter um filho, deve consultar um médico ou farmacêutico antes de usar este medicamento.
Gravidez
O medicamento Fem 7 Combi não é indicado para uso durante a gravidez. Se a doente engravidar durante o tratamento com o medicamento Fem 7 Combi, o medicamento deve ser interrompido imediatamente.
Estudos clínicos realizados em um grande número de doentes não mostraram efeitos não desejados do levonorgestrel no feto.
Os resultados dos estudos epidemiológicos até o momento sobre a exposição acidental do feto à ação dos estrogênios e do levonorgestrel não mostraram efeitos prejudiciais ao embrião e ao feto.
Amamentação
O medicamento Fem 7 Combi não é indicado para uso durante a amamentação.
Condução de veículos e uso de máquinas
Não foi detectado efeito do medicamento Fem 7 Combi na capacidade de conduzir veículos ou operar máquinas.
3. Como usar o medicamento Fem 7 Combi
Este medicamento deve ser usado sempre de acordo com as instruções do médico. Em caso de dúvida, a doente deve consultar um médico ou farmacêutico.
Posologia para adultos
- O medicamento Fem 7 Combi deve ser usado 1 vez por semana, ou seja, o adesivo usado deve ser substituído por um novo a cada 7 dias (sempre no mesmo dia da semana). O medicamento Fem 7 Combi é destinado a um tratamento contínuo sequencial.
- Cada ciclo de tratamento consiste em dois tipos de sistemas Fem 7 Combi: dois sistemas que contêm apenas estradiol (fase I) e dois sistemas que contêm estradiol e levonorgestrel (fase II).
Uso em crianças e adolescentes
O uso do medicamento Fem 7 Combi em crianças é contraindicado.
Como iniciar o uso do medicamento Fem 7 Combi.
- O tratamento deve ser iniciado com a aplicação de um adesivo.
- Em mulheres pós-menopáusicas que não estão usando terapia hormonal substitutiva, o tratamento com o medicamento Fem 7 Combi pode ser iniciado a qualquer momento.
- Em mulheres que estão usando outros produtos para terapia hormonal substitutiva contínua combinada, o tratamento com o medicamento Fem 7 Combi pode ser iniciado a qualquer momento.
- Em mulheres que estão usando outros produtos para terapia hormonal substitutiva contínua sequencial, a mudança para o medicamento Fem 7 Combi deve ocorrer após o término do ciclo de tratamento em andamento.
Modo de usar:
As instruções para o uso estão ilustradas nas figuras abaixo.
O sistema transdérmico consiste em uma folha fina, transparente, com forma de octógono, conectada a uma folha protetora retangular, mais resistente, de duas partes.
A parte octogonal do sistema é o adesivo propriamente dito. A face interna adesiva contém os hormônios que são liberados para a pele.
Cada sistema transdérmico Fem 7 Combi é embalado em um sachê individual, fechado hermeticamente.
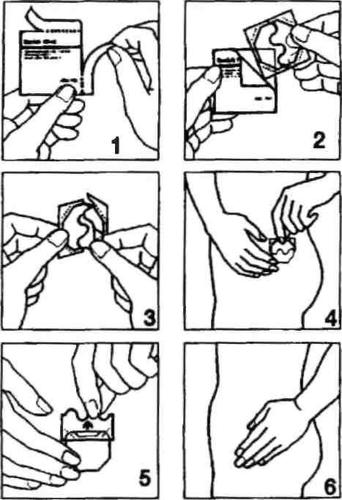
- Abrir um dos sachês ao longo das incisões laterais (não use tesouras), e então remover o adesivo. (Fig. 1 e 2).
- O adesivo deve ser aplicado na pele imediatamente após a remoção da embalagem.
- Remover metade da folha protetora de duas partes. Não tocar a face adesiva do adesivo com os dedos. Aplicar a face adesiva do adesivo na pele. (Fig. 3 e 4).
- Remover a outra metade da folha protetora. Pressionar o adesivo com a mão e segurar por 30 segundos. O adesivo será aquecido à temperatura corporal, o que garantirá uma aderência ótima à pele. (Fig. 5 e 6). Certifique-se de que o adesivo todo está aderido à pele, especialmente nas bordas.
- O local de aplicação do adesivo deve ser alterado a cada vez, ou seja, um novo adesivo pode ser aplicado no mesmo local após 2 semanas.
- A pele no local escolhido deve estar saudável, sem óleo, seca e não danificada.
- Os melhores locais para aplicar o adesivo são os quadris, as partes superiores das nádegas e a parte inferior do abdômen, pois a pele é relativamente lisa nesses locais. Não aplique os adesivos Fem 7 Combi nos seios ou na área ao redor! Não aplique o adesivo na cintura!
- O adesivo adere firmemente à pele. Banhar-se na banheira, tomar chuveiro ou realizar exercícios físicos não deve afetar a ação do adesivo.
- Deve-se evitar esfregar o adesivo com uma esponja ou toalha, pois isso pode fazer com que o adesivo se solte.
- Não use roupas justas que possam fazer com que o adesivo se solte.
- O adesivo deve ser removido lentamente para evitar irritar a pele.
- Se o adesivo se soltar completamente antes de 7 dias, basta aplicar um novo adesivo.
- Cada adesivo deve ser usado por 7 dias. Recomenda-se que, durante o tratamento, os adesivos sejam trocados sempre no mesmo dia da semana.
- O próximo adesivo deve ser aplicado de acordo com o plano de tratamento original.
- Deve-se evitar expor o adesivo à luz solar direta.
- Se, após a aplicação do adesivo na pele, um pouco de cola permanecer, deve-se removê-la suavemente com um creme ou leite cosmético.
Por quanto tempo o medicamento Fem 7 Combi pode ser usado
Cada sistema transdérmico deve ser usado por 7 dias.
A terapia hormonal substitutiva deve ser continuada por tanto tempo quanto o benefício do tratamento superar o risco.
Uso de dose maior do que a recomendada do medicamento Fem 7 Combi
Devido à via de administração, a superdose do medicamento Fem 7 Combi é improvável.
Os sintomas de superdose incluem sensibilidade mamária, inchaço nas áreas do abdômen / pélvis, ansiedade, agitação, náuseas e vômitos. Se ocorrerem sintomas de superdose, o sistema deve ser removido.
Omissão da dose do medicamento Fem 7 Combi
Se a doente esquecer de trocar o adesivo após 7 dias, deve aplicar um novo adesivo o mais rápido possível e, em seguida, trocar o adesivo no dia designado, no horário usual.
Não use uma dose dupla para compensar o adesivo perdido.
Interrupção do uso do medicamento Fem 7 Combi
Podem ocorrer os seguintes sintomas: retorno dos sintomas da menopausa.
Se a doente desejar interromper o tratamento por um período ou permanentemente, deve consultar um médico antes.
4. Efeitos não desejados
Como qualquer medicamento, o medicamento Fem 7 Combi pode causar efeitos não desejados, embora não todos os doentes os apresentem.
Abaixo, estão listados os possíveis efeitos não desejados que podem ocorrer durante o uso da terapia hormonal substitutiva na menopausa.
Os efeitos não desejados ocorrem com mais frequência (> 10%) no local de aplicação do sistema transdérmico.
São eles: vermelhidão da pele (eritema), irritação e inchaço da pele, coceira. Geralmente, esses efeitos desaparecem sem tratamento especial após 2 a 3 dias após a remoção do adesivo.
Efeitos não desejados frequentes (que podem ocorrer com mais frequência do que em 1 em 100 doentes, mas com menos frequência do que em 1 em 10 doentes):
- aumento da libido,
- diminuição da libido,
- cefaleia,
- náuseas,
- vômitos,
- sangramento intermenstrual e manchamento.
Efeitos não desejados não muito frequentes (que podem ocorrer com mais frequência do que em 1 em 1.000 doentes, mas com menos frequência do que em 1 em 100 doentes):
- tontura,
- enxaqueca,
- parestesia,
- inchaço,
- dor abdominal,
- dispepsia,
- hipertensão,
- dor menstrual,
- crescimento da mucosa do útero,
- câncer de mama,
- retenção de líquidos,
- aumento de peso,
- diminuição de peso,
- fadiga
Efeitos não desejados raros (que podem ocorrer com mais frequência do que em 1 em 10.000 doentes, mas com menos frequência do que em 1 em 1.000 doentes):
- depressão,
- cálculos biliares,
- icterícia colestática,
- miomas uterinos.
Outros efeitos
- tumores benignos e malignos dependentes de estrogênio, como câncer da mucosa do útero;
- doença tromboembólica venosa, como trombose venosa profunda ou embolia pulmonar. Esses ocorrem com mais frequência em doentes que usam terapia hormonal substitutiva do que em doentes que não usam terapia hormonal substitutiva (ver ponto "Quando não usar o medicamento Fem 7 Combi" e "Quando ter cuidado com o uso do medicamento Fem 7 Combi");
- infarto do miocárdio e acidente vascular cerebral;
- doenças da vesícula biliar (por exemplo, cálculos biliares);
- distúrbios da pele e tecido subcutâneo: melasma (manchas marrons no rosto), eritema multiforme, eritema nodoso, doença de Schönlein-Henoch (purpura trombocitopênica);
- possível demência (perda de memória).
Notificação de efeitos não desejados
Se ocorrerem algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, a doente deve informar o médico ou farmacêutico. Os efeitos não desejados podem ser notificados diretamente ao
Departamento de Monitoramento de Efeitos Não Desejados de Medicamentos da Agência Nacional de Vigilância Sanitária
Rua São Paulo, 1000
01042-000 São Paulo
Telefone: +55 11 3207 9311
Fax: +55 11 3207 9312
Site: https://www.anvisa.gov.br
Os efeitos não desejados também podem ser notificados ao titular do registro.
A notificação de efeitos não desejados pode ajudar a obter mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Fem 7 Combi
- Conservar em local não visível e inacessível a crianças.
- Conservar em temperatura abaixo de 30°C.
- Não usar o medicamento após o vencimento da data de validade impressa na caixa após "Validade". A data de validade refere-se ao último dia do mês indicado.
- Os sistemas transdérmicos usados devem ser dobrados com a face adesiva para dentro e, em seguida, descartados.
- Os medicamentos não devem ser jogados na canalização ou em lixeiras domésticas. A doente deve perguntar ao farmacêutico como descartar os medicamentos que não são mais necessários. Esse procedimento ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Fem 7 Combi
Substâncias ativas:
Sistema transdérmico da fase I:
estradiol ( Estradiolum ) hemihidratado 1,5 mg
Após a aplicação na pele, o sistema transdérmico libera 50 microgramas de estradiol por dia durante 7 dias. A área ativa do sistema transdérmico é de 15 cm².
Sistema transdérmico da fase II:
estradiol ( Estradiolum ) hemihidratado 1,5 mg
levonorgestrel ( Levonorgestrelum ) 1,5 mg
Após a aplicação na pele, o sistema transdérmico libera 50 microgramas de estradiol e 10 microgramas de levonorgestrel por dia durante 7 dias. A área ativa do sistema transdérmico é de 15 cm².
Outros componentes do medicamento são:
Camada adesiva: copolímero de estireno e isopreno, ésteres de glicerina com ácidos resínicos hidrogenados
Camada protetora externa: polietileno tereftalato (PET)
Camada protetora (para remover): polietileno tereftalato (PET) revestido com silício
Como é o medicamento Fem 7 Combi e o que contém a embalagem
O Fem 7 Combi é um adesivo transparente, elástico, com forma de octógono e bordas arredondadas.
Sua face interna (adesiva) é coberta com uma folha protetora transparente de duas partes.
4 sistemas transdérmicos - 2 sistemas transdérmicos da fase I + 2 sistemas transdérmicos da fase II
12 sistemas transdérmicos - 6 sistemas transdérmicos da fase I + 6 sistemas transdérmicos da fase II
Titular do registro
Theramex Ireland Limited
3º andar, Kilmore House,
Park Lane, Spencer Dock,
Dublin 1
D01 YE64
Irlanda
Fabricante:
LTS Lohmann Therapie-Systeme AG
Lohmannstraße 2
56626 Andernach
Alemanha
Para obter mais informações, a doente pode entrar em contato com o representante local do titular do registro pelo telefone: 22 307 71 66.
Data da última atualização do folheto:
- País de registo
- Substância ativa
- Requer receita médicaSim
- Fabricante
- ImportadorLTS Lohmann Terapie-Systeme AG
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Fem 7 CombiForma farmacêutica: Gel, 0.5 mgSubstância ativa: estradiolFabricante: Orion CorporationRequer receita médicaForma farmacêutica: Gel, 1 mgSubstância ativa: estradiolFabricante: Orion CorporationRequer receita médicaForma farmacêutica: Gel, 1 mg/gSubstância ativa: estradiolRequer receita médica
Alternativas a Fem 7 Combi noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Fem 7 Combi em Espanha
Alternativa a Fem 7 Combi em Ukraine
Médicos online para Fem 7 Combi
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Fem 7 Combi – sujeita a avaliação médica e regras locais.










