
Evertas
Pergunte a um médico sobre a prescrição de Evertas

Como usar Evertas
Folheto informativo para o paciente: informação para o utilizador
Evertas, 4,6 mg/24 h, sistema transdérmico, adesivo
Evertas, 9,5 mg/24 h, sistema transdérmico, adesivo
Evertas, 13,3 mg/24 h, sistema transdérmico, adesivo
Rivastigmina
Deve ler atentamente o conteúdo do folheto antes de tomar o medicamento, pois contém informações importantes para o paciente.
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de dúvidas, deve consultar o médico ou farmacêutico.
- Este medicamento foi prescrito especificamente para si. Não o deve dar a outros. O medicamento pode prejudicar outra pessoa, mesmo que os sintomas da sua doença sejam os mesmos.
- Se o paciente desenvolver algum efeito não desejado, incluindo qualquer possível efeito não desejado não mencionado neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é o medicamento Evertas e para que é utilizado
- 2. Informações importantes antes de tomar o medicamento Evertas
- 3. Como tomar o medicamento Evertas
- 4. Efeitos não desejados
- 5. Como conservar o medicamento Evertas
- 6. Conteúdo da embalagem e outras informações
1. O que é o medicamento Evertas e para que é utilizado
A substância ativa do medicamento Evertas é a rivastigmina.
A rivastigmina pertence a um grupo de substâncias chamadas inibidores da colinesterase. Nos pacientes
com demência do tipo Alzheimer, há uma diminuição do número de células nervosas
no cérebro, o que causa uma diminuição da concentração de acetilcolina, um neurotransmissor (substância que permite a comunicação entre as células nervosas),
produzida por elas. A ação da rivastigmina consiste em bloquear as enzimas que causam a decomposição da acetilcolina:
acetilcolinesterase e butirilcolinesterase. Bloqueando a ação dessas enzimas, a rivastigmina
permite aumentar a concentração de acetilcolina no cérebro, o que ajuda a aliviar os sintomas da doença de Alzheimer.
O medicamento Evertas é utilizado no tratamento de pacientes adultos com demência do tipo Alzheimer leve a moderadamente grave,
uma doença cerebral progressiva que gradualmente perturba a memória, as capacidades intelectuais e o comportamento.
2. Informações importantes antes de tomar o medicamento Evertas
Quando não tomar o medicamento Evertas
- se o paciente tiver alergia à rivastigmina ou a qualquer outro componente deste medicamento (listados no ponto 6);
- se o paciente tiver reação alérgica a medicamentos semelhantes (derivados da carbamamina);
- se o paciente desenvolver reação cutânea que ultrapassa a área da pele ocupada pelo adesivo, se a reação local se agravar (por exemplo, se desenvolverem bolhas, agravamento da inflamação da pele, inchaço) e se essas alterações não desaparecerem dentro de 48 horas após a remoção do adesivo. Se essa situação se aplicar ao paciente, ele deve informar o médico e não deve aplicar o adesivo Evertas.
Precauções e advertências
Antes de iniciar o tratamento com o medicamento Evertas, o paciente deve discutir com o médico ou farmacêutico se:
- o paciente tiver ou já teve doenças cardíacas, como ritmo cardíaco irregular ou lento, prolongamento do intervalo QT, prolongamento do intervalo QT na família, torsades de pointes, ou baixo nível de potássio ou magnésio no sangue;
- o paciente tiver ou já teve úlcera ativa no estômago;
- o paciente tiver ou já teve dificuldades para urinar;
- o paciente tiver ou já teve convulsões;
- o paciente tiver ou já teve asma ou doença respiratória grave;
- o paciente tiver tremores musculares;
- o paciente tiver baixo peso corporal;
- o paciente tiver reações gastrointestinais, como náuseas (enjoo), vômitos e diarreia. O paciente pode desidratar (perder muito líquido) se os vômitos ou diarreia persistirem por um período prolongado;
- o paciente tiver distúrbios da função hepática. Se alguma dessas situações se aplicar ao paciente, pode ser necessária uma observação mais cuidadosa do paciente pelo médico durante o tratamento com este medicamento.
Se o paciente não aplicou o adesivo por mais de três dias, não deve aplicar um novo adesivo antes de falar com o médico.
Crianças e adolescentes
O medicamento Evertas não é adequado para crianças e adolescentes com demência do tipo Alzheimer.
Medicamento Evertas e outros medicamentos
O paciente deve informar o médico ou farmacêutico sobre todos os medicamentos que está tomando atualmente ou recentemente, bem como sobre os medicamentos que planeja tomar.
O medicamento Evertas pode afetar a ação de medicamentos anticolinérgicos, alguns dos quais são utilizados para aliviar espasmos estomacais (por exemplo, dicicloverina), tratar a doença de Parkinson (por exemplo, amantadina)
ou prevenir a doença do movimento (por exemplo, difenidramina, escopolamina ou meclizina).
O medicamento Evertas, sistema transdérmico, adesivo, não deve ser utilizado concomitantemente com metoclopramida (medicamento utilizado para aliviar ou prevenir náuseas e vômitos). A administração concomitante desses dois medicamentos pode causar distúrbios como rigidez dos membros e tremores das mãos.
Se o paciente for submetido a uma operação durante o tratamento com o medicamento Evertas, sistema transdérmico, adesivo, deve informar o médico sobre o uso desses adesivos, pois eles podem aumentar a ação de alguns relaxantes musculares administrados durante a anestesia.
Deve haver cautela quando o medicamento Evertas, sistema transdérmico, adesivo, for utilizado com medicamentos beta-bloqueadores (medicamentos como o atenolol, utilizados para tratar a hipertensão, angina de peito e outras doenças cardíacas). A administração concomitante desses dois medicamentos pode causar distúrbios como bradicardia (frequência cardíaca lenta) que pode levar a desmaio ou perda de consciência.
Deve haver cautela quando o medicamento Evertas for utilizado com outros medicamentos que possam afetar o ritmo cardíaco ou o sistema de condução cardíaca (prolongamento do intervalo QT).
Gravidez, amamentação e fertilidade
Se a paciente estiver grávida ou amamentando, suspeitar que possa estar grávida ou planejar ter um filho, deve consultar o médico ou farmacêutico antes de tomar este medicamento.
Se a paciente estiver grávida, deve ser feita uma avaliação dos benefícios do tratamento com o medicamento Evertas em relação aos possíveis efeitos do medicamento no feto. O medicamento Evertas não deve ser utilizado durante a gravidez, a menos que seja absolutamente necessário.
Durante o tratamento com o medicamento Evertas, sistema transdérmico, adesivo, não se deve amamentar.
Condução de veículos e uso de máquinas
O médico informará o paciente se o seu estado permite a condução de veículos e o uso de máquinas. O medicamento Evertas (adesivo) pode causar desmaio ou confusão intensa. Se o paciente se sentir fraco ou desorientado, não deve conduzir veículos, operar máquinas ou realizar outras tarefas que exijam concentração.
3. Como tomar o medicamento Evertas
Este medicamento deve ser sempre utilizado exatamente como descrito no folheto para o paciente ou de acordo com as instruções do médico. Em caso de dúvidas, deve consultar o médico ou farmacêutico.
ATENÇÃO:
- Antes de aplicar um novo adesivo, o adesivo anterior deve ser removido.
- Apenas UM adesivo do medicamento Evertas deve ser aplicado por dia.
- Não corte o adesivo em pedaços menores.
- Pressione firmemente o adesivo com a parte interna da mão e segure por pelo menos
30 segundos.
Como iniciar o tratamento
O médico informará o paciente sobre quais adesivos do medicamento Evertas são os mais adequados para o seu caso.
- O tratamento geralmente começa com o medicamento Evertas 4,6 mg/24 h.
- A dose diária recomendada do medicamento Evertas é de 9,5 mg/24 h. Se o tratamento for bem tolerado, o médico pode considerar aumentar a dose para 13,3 mg/24 h
- Apenas um adesivo do medicamento Evertas deve ser aplicado de cada vez e deve ser trocado por um novo a cada 24 horas. Durante o tratamento, o médico pode ajustar a dose do medicamento de acordo com as necessidades do paciente.
Se o paciente não aplicou o adesivo por mais de três dias, não deve aplicar um novo adesivo antes de falar com o médico. O tratamento pode ser retomado com a mesma dose, se a interrupção do tratamento não exceder três dias. Caso contrário, o médico recomendará retomar o tratamento com a dose de 4,6 mg/24 h do medicamento Evertas.
O medicamento Evertas pode ser utilizado com alimentos, bebidas e álcool.
Onde o paciente deve aplicar o adesivo do medicamento Evertas
- Antes de aplicar o adesivo, certifique-se de que a pele no local de aplicação planejado está limpa, seca e sem pelos, livre de pó, óleos, cremes hidratantes ou líquidos que possam impedir a aderência adequada do adesivo, livre de cortes, erupções e (ou) irritações.
- Remova cuidadosamente todos os adesivos aplicados antes de aplicar um novo.A aplicação de vários adesivos na pele pode expor o paciente a uma dose excessiva de medicamento, o que pode ser perigoso.
- Deve aplicar APENAS UMadesivo por dia em dos locais possíveis, como mostrado nos desenhos:
- parte superior do braço esquerdo ouparte superior do braço direito
- parte superior do peito, à esquerda ouà direita (evite aplicar adesivos no peito)
- parte superior das costas, à esquerda ouà direita
- parte inferior das costas, à esquerda ouà direita
Ao fim de 24 horas, remova o adesivo antigo antes de aplicar UMnovo adesivo em dos locais mostrados.
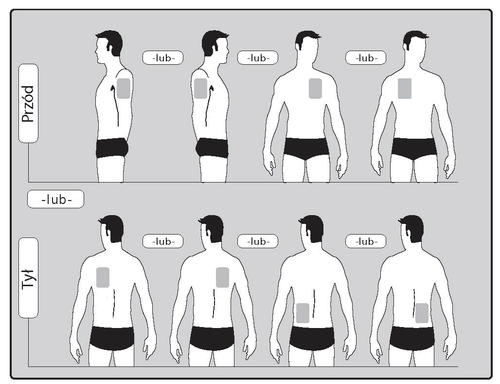
Ao trocar o adesivo, remova o adesivo do dia anterior antes de aplicar um novo adesivo em um local diferente (por exemplo, um dia no lado direito do corpo e no dia seguinte no lado esquerdo, um dia na parte superior do corpo e no dia seguinte na parte inferior). Não aplique o adesivo no mesmo local antes de decorridos 14 dias.
Como o paciente deve aplicar os adesivos do medicamento Evertas
O medicamento Evertas é um adesivo fino, marrom claro, feito de plástico, aplicado na pele. Cada adesivo está em uma sachê fechada. Não abra a sachê ou remova o adesivo até o momento de aplicá-lo na pele.
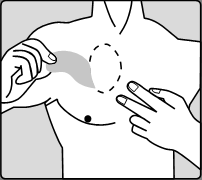
Remova cuidadosamente o adesivo antes de aplicar um novo.
Pacientes que estão iniciando o tratamento pela primeira vez e pacientes que estão retomando o tratamento com a rivastigmina após uma interrupção devem
iniciar com as ações mostradas no segundo desenho.
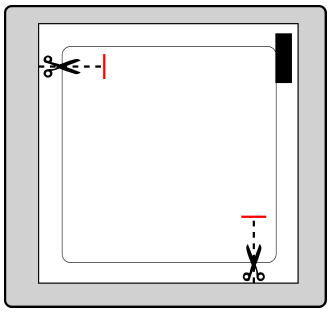
Cada adesivo está em uma sachê fechada. A sachê deve ser aberta logo antes de usar o adesivo.
Corte a sachê nos dois locais indicados pelas tesouras, mas não além da linha indicada. Perfure a sachê para abri-la. Não corte a sachê ao longo de toda a sua extensão para evitar danificar o adesivo.
Remova o adesivo da sachê.
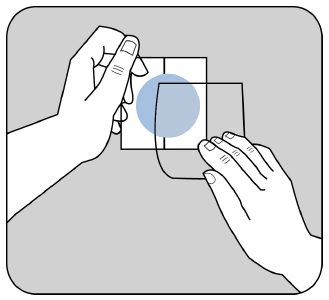
Para os produtos Evertas 4,6 mg/24 h e 9,5 mg/24h
sistema transdérmico, adesivo:
Remova a proteção da parte superior, de cor bege, do adesivo.
A face adesiva do adesivo é protegida por uma camada de proteção.
Remova uma parte da camada de proteção, sem tocar a face adesiva do adesivo.
Para o produto Evertas 13,3 mg/24 h sistema
transdérmico, adesivo:
A face adesiva do adesivo é protegida por uma camada de proteção.
Remova uma parte da camada de proteção, sem tocar a face adesiva do adesivo.
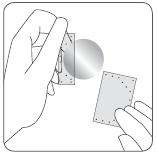
Aplique a face adesiva do adesivo na parte superior ou inferior das costas, parte superior do braço ou no peito,
e, em seguida, remova a segunda parte da camada de proteção.
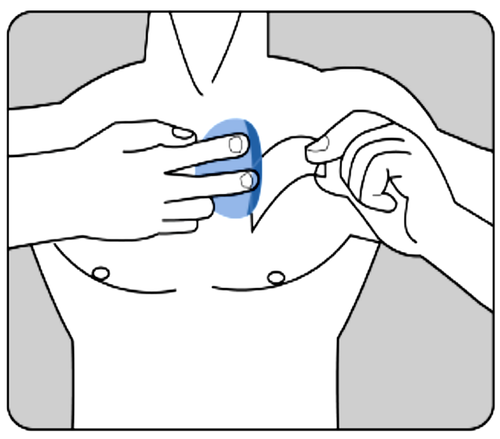
Pressione firmemente o adesivo com a mão por pelo menos 30 segundos,
certificando-se de que as bordas estão bem aderidas à pele.
Agora você pode assinar o adesivo com um marcador, por exemplo, com o nome do dia da semana.
O adesivo deve ser usado constantemente até o momento de trocá-lo por um novo. O paciente pode experimentar diferentes locais de aplicação do novo adesivo para encontrar o mais conveniente e menos propenso a ser arrancado pela roupa.
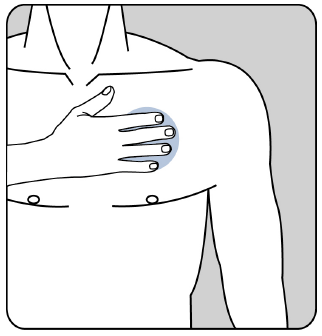
Como o paciente deve remover o adesivo do medicamento Evertas
Deve puxar suavemente uma borda do adesivo e remover-lo lentamente da pele. Se restos de adesivo permanecerem na pele, podem ser removidos lavando a área com água morna e sabonete suave ou óleo infantil. Não use álcool ou outros solventes (removedor de esmalte e outros produtos).
Depois de remover o adesivo, lave as mãos com água e sabonete. Se o medicamento entrar em contato com os olhos ou causar vermelhidão nos olhos após o contato com o adesivo, enxágue os olhos com muita água e, se os sintomas não desaparecerem, consulte um médico.
O paciente pode usar os adesivos do medicamento Evertas durante o banho, natação ou exposição ao sol?
- O banho, natação ou chuveiro não devem afetar a ação do adesivo. Certifique-se de que, durante essas atividades, o adesivo não se solte.
- Não exponha o adesivo a fontes externas de calor por períodos prolongados (por exemplo, exposição excessiva ao sol, sauna, solário).
Como proceder em caso de soltura do adesivo
Se o adesivo se soltar, aplique um novo por o resto do dia e, em seguida, troque-o no horário habitual do dia seguinte.
Quando e por quanto tempo o paciente deve usar os adesivos do medicamento Evertas
- Para que o tratamento seja eficaz, um novo adesivo deve ser aplicado diariamente, preferencialmente no mesmo horário todos os dias.
- Apenas um adesivo do medicamento Evertas deve ser aplicado de cada vez e trocado por um novo a cada 24 horas.
Uso de dose maior do que a recomendada do medicamento Evertas
Se o paciente aplicar acidentalmente mais de um adesivo, remova todos os adesivos e informe o médico sobre a aplicação acidental de mais de um adesivo. O paciente pode precisar de atendimento médico. Em alguns indivíduos que tomaram acidentalmente uma dose excessiva de rivastigmina, ocorreram náuseas, vômitos, diarreia, hipertensão e alucinações. Também pode ocorrer bradicardia e desmaio.
Omissão da dose do medicamento Evertas
Se o paciente esquecer de aplicar um adesivo, deve aplicá-lo assim que lembrar. O próximo adesivo pode ser aplicado no horário habitual do dia seguinte. Não aplique dois adesivos para compensar a dose omitida.
Interrupção do tratamento com o medicamento Evertas
Se o paciente interromper o tratamento, deve informar o médico ou farmacêutico.
Se tiver mais alguma dúvida sobre o uso deste medicamento, consulte o médico ou farmacêutico.
4. Efeitos não desejados
Como qualquer medicamento, este medicamento pode causar efeitos não desejados, embora não todos os pacientes os desenvolvam.
Os efeitos não desejados ocorrem com mais frequência no início do tratamento ou durante o período de aumento da dose. Os efeitos não desejados geralmente desaparecem lentamente à medida que o organismo se adapta ao tratamento.
Se ocorrer algum dos efeitos não desejados listados a seguir, remova o adesivo e informe imediatamente o médico, pois esses efeitos podem ser graves:
Frequentes(ocorrem em menos de 1 paciente em 10):
- perda de apetite;
- tontura;
- agitação ou sonolência;
- incontinência urinária (incapacidade de reter a urina).
Pouco frequentes(ocorrem em menos de 1 paciente em 100):
- distúrbios do ritmo cardíaco, como frequência cardíaca lenta;
- alucinações (ver coisas que não existem);
- úlcera no estômago;
- desidratação (perda excessiva de líquidos);
- agitação excessiva (nível alto de atividade, agitação);
- agressividade.
Raros(ocorrem em menos de 1 paciente em 1000):
- quedas.
Muito raros(ocorrem em menos de 1 paciente em 10.000):
- rigidez dos braços ou pernas;
- tremores das mãos.
Frequência desconhecida(não pode ser estimada a partir dos dados disponíveis):
- reação alérgica no local de aplicação, como bolhas ou inflamação da pele;
- agravamento dos sintomas da doença de Parkinson - como tremores, rigidez ou arrastar os pés;
- pancreatite - com sintomas como dor abdominal superior intensa, frequentemente com náuseas (enjoo) ou vômitos;
- frequência cardíaca rápida ou irregular;
- hipertensão;
- convulsões (ataques epilépticos);
- distúrbios da função hepática (amarelamento da pele, amarelamento da parte branca dos olhos, urina escura ou náuseas, vômitos, fadiga e perda de apetite);
- alterações nos resultados dos exames de função hepática;
- ansiedade,
- pesadelos,
- síndrome de Pisa (condição que inclui contração muscular involuntária com inclinação anormal do corpo e da cabeça para um lado).
Se ocorrer algum dos efeitos não desejados listados a seguir, remova o adesivo e informe imediatamente o médico.
Outros efeitos não desejados relatados após o uso da rivastigmina em cápsulas ou solução oral, que também podem ocorrer com os adesivos:
Frequentes(ocorrem em menos de 1 paciente em 10):
- salivação excessiva;
- perda de apetite;
- ansiedade;
- mal-estar geral;
- tremores ou confusão;
- sudorese excessiva.
Pouco frequentes(ocorrem em menos de 1 paciente em 100):
- distúrbios do ritmo cardíaco (por exemplo, frequência cardíaca rápida);
- dificuldade para dormir;
- quedas acidentais.
Raros(ocorrem em menos de 1 paciente em 1000):
- convulsões (ataques epilépticos);
- doença ulcerosa intestinal;
- dor no peito - pode ser causada por espasmo cardíaco.
Muito raros(ocorrem em menos de 1 paciente em 10.000):
- hipertensão;
- pancreatite - com sintomas como dor abdominal superior intensa, frequentemente com náuseas (enjoo) ou vômitos;
- sangramento gastrointestinal - sangue nas fezes ou vômitos;
- alucinações (ver coisas que não existem);
- vômitos intensos, que podem levar à ruptura da parte do trato gastrointestinal que liga a boca ao estômago (esôfago).
Notificação de efeitos não desejados
Se ocorrer algum efeito não desejado, incluindo qualquer efeito não desejado não mencionado neste folheto, informe o médico, farmacêutico ou enfermeiro. Os efeitos não desejados podem ser notificados diretamente ao Departamento de Monitoramento de Efeitos Não Desejados de Produtos Farmacêuticos da Agência Reguladora de Produtos Farmacêuticos, Dispositivos Médicos e Produtos Biocidas, Al. Jerozolimskie 181 C, 02-222 Varsóvia.
Telefone: +48 22 49 21 301, fax: +48 22 49 21 309, site: https://smz.ezdrowie.gov.pl
Os efeitos não desejados também podem ser notificados ao titular da autorização de comercialização ou ao seu representante na Polônia.
A notificação de efeitos não desejados permitirá reunir mais informações sobre a segurança do medicamento.
5. Como conservar o medicamento Evertas
O medicamento deve ser armazenado em local não visível e inacessível a crianças.
Não use este medicamento após o prazo de validade impresso na embalagem e na sachê após "Prazo de validade (EXP)". O prazo de validade é o último dia do mês indicado.
Não há recomendações especiais para o armazenamento do medicamento.
Antes de usar, o adesivo deve ser armazenado na sachê.
Não use o adesivo se estiver danificado ou mostrar sinais de abertura.
Depois de remover o adesivo, dobre-o ao meio com a face adesiva para dentro e pressione firmemente. Coloque o adesivo usado na sachê e, em seguida, jogue-o fora em local inacessível a crianças. Depois de remover o adesivo, não toque nos olhos com os dedos antes de lavar as mãos com água e sabonete.
Os medicamentos não devem ser jogados na canalização ou em recipientes de lixo doméstico. Pergunte ao farmacêutico como eliminar os medicamentos que não são mais necessários. Essa ação ajudará a proteger o meio ambiente.
6. Conteúdo da embalagem e outras informações
O que contém o medicamento Evertas
- A substância ativa do medicamento é a rivastigmina. Evertas, 4,6 mg/24 h, sistema transdérmico: cada adesivo libera 4,6 mg de rivastigmina em 24 horas. O adesivo tem uma área de 4,6 cm e contém 6,9 mg de rivastigmina. Evertas, 9,5 mg/24 h, sistema transdérmico: cada adesivo libera 9,5 mg de rivastigmina em 24 horas. O adesivo tem uma área de 9,2 cm e contém 13,8 mg de rivastigmina. Evertas, 13,3 mg/24 h, sistema transdérmico: cada adesivo libera 13,3 mg de rivastigmina em 24 horas. O adesivo tem uma área de 12,8 cm e contém 19,2 mg de rivastigmina.
- Os outros componentes são:
Camada ativa:
- Copolímero de acrilato de 2-etilhexilo e acetato de vinila
Camada de matriz adesiva:
- Polímero de poliisobuteno de massa molar média
- Polímero de poliisobuteno de massa molar alta
- Silica coloidal anidra
- Parafina líquida leve
Camada externa:
- Polietileno/liga termoplástica/Alumínio revestido com poliéster
Camada de proteção (removível):
- Poliéster revestido com polímero fluorado
- Tinta laranja
Como é o medicamento Evertas e que conteúdo tem a embalagem
Cada sistema transdérmico é um adesivo fino, de cor marrom clara, feito de plástico. Na camada externa, de cor marrom clara, há uma inscrição laranja:
- “RIV-TDS 4.6 mg/24 h”
- “RIV-TDS 9.5 mg/24 h”
- “RIV-TDS 13.3 mg/24 h”
Cada adesivo está em uma sachê fechada.
Evertas, 4,6 mg/24 h, sistema transdérmico
Evertas, 9,5 mg/24 h, sistema transdérmico
Os adesivos estão disponíveis em embalagens contendo 7 ou 30 sistemas transdérmicos e em embalagens coletivas contendo 60 (2x30) ou 90 (3x30) sistemas transdérmicos.
Evertas, 13,3 mg/24 h, sistema transdérmico
Os adesivos estão disponíveis em embalagens contendo 30 sistemas transdérmicos e em embalagens coletivas contendo 60 (2x30) ou 90 (3x30) sistemas transdérmicos.
Nem todos os tamanhos de embalagem podem estar disponíveis no mercado.
Titular da autorização de comercialização
Zentiva, k.s., U kabelovny 130, Dolní Mĕcholupy, 102 37 Praga 10, República Tcheca
Fabricante
Luye Pharma AG, Am Windfeld 35, 83714 Miesbach, Alemanha
S.C. Zentiva S.A, B-dul Theodor Pallady nr.50, sector 3, 032266 Bucareste, Romênia
Este medicamento está autorizado para comercialização nos estados membros do Espaço Econômico Europeu sob os seguintes nomes:
Polônia
Evertas
Romênia Evertas 4.6 mg/24 h plasture transdermic
Romênia Evertas 9.5 mg/24 h plasture transdermic
Para obter informações mais detalhadas sobre o medicamento, entre em contato com o representante do titular da autorização de comercialização na Polônia:
Zentiva Polska Sp. z o.o.
ul. Bonifraterska 17
00-203 Varsóvia
telefone: +48 22 375 92 00
Data da última atualização do folheto:fevereiro de 2025
- País de registo
- Substância ativa
- Requer receita médicaSim
- ImportadorLuye Pharma AG Zentiva SA
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a EvertasForma farmacêutica: Sistema, 4,6 mg/24 hSubstância ativa: rivastigmineFabricante: Luye Pharma AGRequer receita médicaForma farmacêutica: Sistema, 9,5 mg/24 hSubstância ativa: rivastigmineFabricante: Luye Pharma AGRequer receita médicaForma farmacêutica: Sistema, 4,6 mg/24 hSubstância ativa: rivastigmineRequer receita médica
Alternativas a Evertas noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Evertas em Espanha
Alternativa a Evertas em Ukraine
Médicos online para Evertas
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Evertas – sujeita a avaliação médica e regras locais.











