
Duosol nie zauieraiomci potasu
Pergunte a um médico sobre a prescrição de Duosol nie zauieraiomci potasu

Como usar Duosol nie zauieraiomci potasu
Folheto anexo ao embalagem: informação para o doente
Duosol sem potássio, solução para hemofiltração
Deve ler atentamente o conteúdo do folheto antes de usar o medicamento, pois contém
informações importantes para o doente
- Deve guardar este folheto para poder relê-lo se necessário.
- Em caso de alguma dúvida, deve consultar um médico ou farmacêutico.
- Se o doente apresentar algum efeito secundário, incluindo qualquer efeito secundário não mencionado neste folheto, deve informar o médico ou farmacêutico. Ver ponto 4.
Índice do folheto
- 1. O que é Duosol sem potássio e para que é usado
- 2. Informações importantes antes de usar Duosol sem potássio
- 3. Como usar Duosol sem potássio
- 4. Efeitos secundários possíveis
- 5. Como armazenar Duosol sem potássio
- 6. Conteúdo do embalagem e outras informações
1. O que é Duosol sem potássio e para que é usado
Duosol sem potássio é uma solução para hemofiltração. Este medicamento é destinado a ser usado em doentes com insuficiência renal aguda, nos quais os rins não conseguem remover os produtos do metabolismo do sangue. O processo de hemofiltração contínua consiste na remoção do organismo dos produtos do metabolismo que, em condições normais, são excretados pelos rins. A solução equilibra o balanço de líquidos e fornece suplementos de sais (eletrólitos) perdidos.
2. Informações importantes antes de usar Duosol sem potássio
Duosol sem potássio não deve ser usado se:
- o doente tiver níveis baixos de potássio no sangue (hipocalemia);
- o doente tiver níveis baixos de ácidos no sangue (alcalose metabólica).
A hemofiltração não deve ser usada nos seguintes casos:
- insuficiência renal combinada com processos metabólicos intensos (hipercatabolismo); nesse caso, os produtos do metabolismo acumulados não podem ser removidos por hemofiltração por um período prolongado;
- fluxo sanguíneo insuficiente do acesso venoso;
- qualquer condição que aumente o risco de sangramento, pois o doente está a receber medicamentos que impedem a formação de coágulos (anticoagulação sistémica).
Advertências e precauções
Antes de iniciar o uso de Duosol sem potássio, deve discutir com o médico ou farmacêutico.
Antes e durante a hemofiltração, deve monitorizar a pressão arterial, o balanço de líquidos, o balanço de sais (eletrólitos), o balanço ácido-base e a função renal. Deve verificar regularmente a concentração de açúcar e fosfatos no sangue.
Antes e durante a hemofiltração, deve também monitorizar a concentração de potássio no sangue.
Duosol sem potássio e outros medicamentos
Deve informar o médico ou farmacêutico sobre todos os medicamentos que o doente está a tomar atualmente ou recentemente, bem como sobre os medicamentos que o doente planeia tomar.
A concentração de outros medicamentos no sangue pode diminuir durante a hemofiltração e o médico terá isso em conta.
Ao usar doses apropriadas da solução para hemofiltração e monitorizar cuidadosamente, pode evitar a ocorrência de interações com outros medicamentos.
Serão consideradas as seguintes interações:
- Infusões administradas no âmbito dos cuidados intensivos podem alterar a composição do sangue e o estado de líquidos do doente.
- Os efeitos tóxicos de alguns medicamentos usados no tratamento da fraqueza cardíaca (medicamentos que contêm digital) podem não ser aparentes quando a concentração de potássio ou magnésio for demasiado alta ou a concentração de cálcio for demasiado baixa. Se essas concentrações forem corrigidas pela hemofiltração, podem ocorrer efeitos tóxicos e causar, por exemplo, distúrbios do ritmo cardíaco. Se o doente tiver níveis baixos de potássio ou níveis altos de cálcio no sangue, a digital pode ter efeitos tóxicos em doses mais baixas do que as usualmente usadas no tratamento.
- A administração de vitamina D e medicamentos que contêm cálcio pode aumentar o risco de níveis altos de cálcio no sangue (hipercalcemia).
- A administração adicional de bicarbonato de sódio pode aumentar o risco de níveis baixos de ácidos no sangue (alcalose metabólica).
Gravidez, amamentação e fertilidade
Se a doente estiver grávida ou a amamentar, suspeitar que possa estar grávida ou planeiar ter um filho, deve consultar um médico ou farmacêutico antes de receber este medicamento.
Não há dados sobre o uso de soluções para hemofiltração em mulheres grávidas. No entanto, como todos os componentes deste medicamento são substâncias que ocorrem naturalmente e apenas substituem as mesmas substâncias perdidas do organismo durante a hemofiltração, não se espera que haja riscos para o feto durante a gravidez e amamentação e não se espera que haja impacto na fertilidade.
Condução de veículos e utilização de máquinas
Este medicamento é geralmente administrado a doentes imobilizados no hospital ou na unidade de diálise. Isso exclui a condução de veículos e a operação de máquinas.
3. Como usar Duosol sem potássio
Este medicamento será administrado ao doente apenas sob supervisão de um médico com experiência em técnicas de hemofiltração.
O médico decidirá a dose apropriada para o doente, considerando o estado clínico, o peso corporal e as condições metabólicas. A menos que seja recomendado de outra forma, em doentes de todas as idades, recomenda-se uma velocidade de filtração de 20-25 ml/kg de peso corporal por hora, para garantir a eliminação das substâncias que normalmente são excretadas na urina.
O doente receberá a solução para hemofiltração pronta para usar através de tubos do aparelho de hemofiltração (chamado de circuito extracorpóreo) com uma bomba de infusão.
O tratamento da insuficiência renal aguda é conduzido por um período limitado de tempo e termina quando a função renal é restaurada.
Uso de uma dose maior do que a recomendada de Duosol sem potássio
Após a administração de doses recomendadas deste medicamento, não foram relatados casos que ameacem a vida. Se necessário, a administração pode ser interrompida a qualquer momento.
Um equilíbrio inadequado de líquidos pode levar à presença de demasiado ou demasiado pouco líquido no organismo (sobrecarga de líquidos ou desidratação). Essas condições são caracterizadas por alterações na pressão arterial ou frequência cardíaca.
Pode ocorrer uma sobredose de bicarbonato de sódio se for administrada uma quantidade excessiva da solução para hemofiltração. Isso pode levar a níveis baixos de ácidos no sangue (alcalose metabólica), menor quantidade de cálcio dissolvido no sangue (diminuição da concentração de cálcio ionizado) ou espasmos musculares (tetania).
A sobredose pode causar insuficiência cardíaca congestiva e (ou) congestão pulmonar e pode causar alterações no equilíbrio de sais (eletrólitos) e no equilíbrio ácido-base.
O médico decidirá o tratamento apropriado.
Em caso de dúvidas adicionais sobre o uso deste medicamento, deve consultar um médico ou farmacêutico.
4. Efeitos secundários possíveis
Como qualquer medicamento, este medicamento pode causar efeitos secundários, embora não todos os doentes os experimentem .
Não foram relatados efeitos secundários associados ao uso deste medicamento, mas são possíveis os seguintes efeitos secundários. A frequência desses efeitos secundários é desconhecida (não pode ser estimada com base nos dados disponíveis):
Sobrecarga de líquidos ou desidratação, níveis anormais de sais (eletrólitos), níveis baixos de fosfato no sangue (hipofosfatemia), níveis altos de açúcar no sangue (hiperglicemia), níveis baixos de ácidos no sangue (alcalose metabólica), pressão arterial alta ou baixa (hipertensão, hipotensão), náuseas, vômitos e espasmos musculares.
Notificação de efeitos secundários
Após a autorização do medicamento, é importante notificar suspeitas de efeitos secundários. Isso permite o monitoramento contínuo da relação benefício-risco do medicamento.
Os profissionais de saúde devem notificar qualquer suspeita de efeito secundário por meio do Departamento de Monitoramento de Efeitos Secundários de Medicamentos da Agência Reguladora de Medicamentos, Produtos Médicos e Produtos Biocidas, Al. Jerozolimskie 181C, 02-222 Varsóvia
Tel.: + 48 22 49 21 301
Fax: + 48 22 49 21 309
site da internet: https://smz.ezdrowie.gov.pl
Os efeitos secundários também podem ser notificados ao titular da autorização de comercialização.
A notificação de efeitos secundários permite reunir mais informações sobre a segurança do uso deste medicamento.
5. Como armazenar Duosol sem potássio
O medicamento deve ser armazenado em um local inacessível e invisível para crianças.
Não use este medicamento após a data de validade impressa no saco e na caixa após:
“Data de validade”. A data de validade é o último dia do mês indicado.
Condições de armazenamento
Não armazene a uma temperatura superior a 25°C. Não armazene na geladeira ou congele.
Condições de armazenamento após a preparação da solução pronta para uso
O produto misturado deve ser usado imediatamente. O produto misturado mantém a estabilidade física e química por 24 horas a 25°C.
6. Conteúdo do embalagem e outras informações
O que contém Duosol sem potássio
| Substâncias ativas: | Câmara menor Solução de eletrólitos | Câmara maior Solução de bicarbonato | ||
| 555 ml contém | por 1000 ml | 4445 ml contém | por 1000 ml | |
| cloreto de sódio | 2,34 g | 4,21 g | 27,47 g | 6,18 g |
| cloreto de cálcio di-hidratado | 1,10 g | 1,98 g | ||
| cloreto de magnésio hexa-hidratado | 0,51 g | 0,91 g | ||
| glicose mono-hidratada que corresponde a glicose anidra | 5,49 g 5,0 g | 9,90 g 9,0 g | ||
| bicarbonato de sódio | 15,96 g | 3,59 g | ||
| Eletrólitos: | [mmol/ câmara] | [mmol/l] | [mmol/ câmara] | [mmol/l] |
| Na+ | 40,0 | 72 | 660 | 149 |
| Ca2+ | 7,5 | 13,5 | ||
| Mg2+ | 2,5 | 4,5 | ||
| Cl | 75,0 | 135 | 470 | 106 |
| HCO 3 | 190 |
| ||
| osmolalidade teórica [mOsm/l] | 275 | 297 | ||
Composição da solução pronta para uso após a mistura:
1000 ml da solução pronta para uso contém [mmol/l]:
Na
140
Ca
1,5
Mg
0,5
Cl
109
HCO
35,0
glicose anidra
5,6 (que corresponde a 1,0 g)
osmolalidade teórica [mOsm/l]
292
pH
7,0–8,0
Outros componentes são:
Solução de eletrólitos (câmara menor)
ácido clorídrico 25% (para ajustar o pH), água para injeção
Solução de bicarbonato (câmara maior)
dióxido de carbono (para ajustar o pH), água para injeção
Como é Duosol sem potássio e o que o embalagem contém
Solução para hemofiltração
Líquido transparente e incolor, sem partículas visíveis
Este medicamento é fornecido em um saco de duas câmaras. Ao misturar as duas soluções após a abertura da divisória entre as câmaras, obtém-se a solução pronta para uso.
2 sacos de 5000 ml (sacos de duas câmaras, 4445 ml e 555 ml) em uma caixa de papelão
Titular da autorização de comercialização e fabricante
- B. Braun Avitum AG Schwarzenberger Weg 73-79 34212 Melsungen Alemanha
Este medicamento é autorizado para comercialização nos países membros da Área Económica Europeia sob os seguintes nomes:
República Checa:
Duosol sem potássio
Estónia:
Duosol ilma kaaliumita, hemofiltratsioonilahus
Finlândia:
Duosol sine Kalium hemofiltraationeste
Itália:
Duosol senza potassio soluzione per emofiltrazione
Letónia:
Duosol bez kālija šķīdums hemofiltrācijai
Lituânia:
Duosol K 0 hemofiltracijos tirpalas
Alemanha, Luxemburgo:
Duosol ohne Kalium Hämofiltrationslösung
Polónia:
Duosol nie zawierający potasu
Eslovénia:
Duosol brez kalija raztopina za hemofiltracijo
Espanha:
Priosol sin Potasio solución para hemofiltración
Países Baixos:
Duosol zonder Kalium, oplossing voor hemofiltratie
Reino Unido:
Duosol without Potassium solution for haemofiltration
Data da última atualização do folheto: 05.05.2023
---------------------------------------------------------------------------------------------------------------------------------
Informações destinadas apenas a profissionais de saúde:
Instruções para a preparação da solução pronta para uso
Antes de usar, deve submeter o recipiente e a solução a um controle visual. A solução para hemofiltração só pode ser usada se o recipiente (embalagem de proteção externa e saco de duas câmaras), a divisória entre as câmaras e as conexões estiverem intactos e não danificados, e a solução for transparente, incolor e livre de partículas visíveis.
A embalagem de proteção externa deve ser removida imediatamente antes do uso.
1
Remova a embalagem de proteção externa.
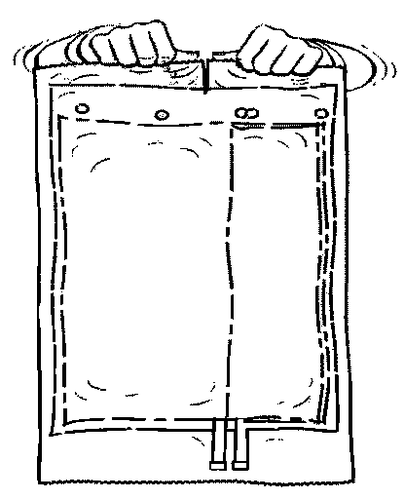
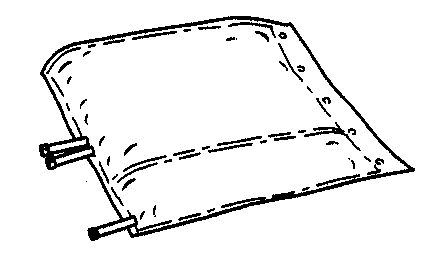
- 2. Estique o saco e coloque-o em uma superfície plana e limpa.
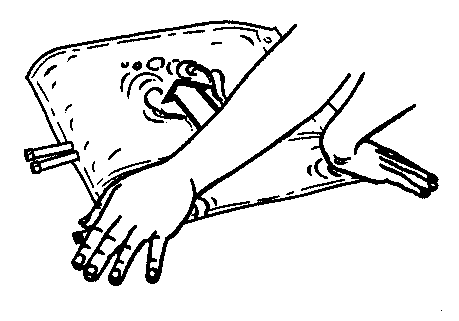
- 3. Pressione a câmara menor do saco com as duas mãos, de modo a abrir completamente a divisória entre as câmaras ao longo de toda a sua extensão.
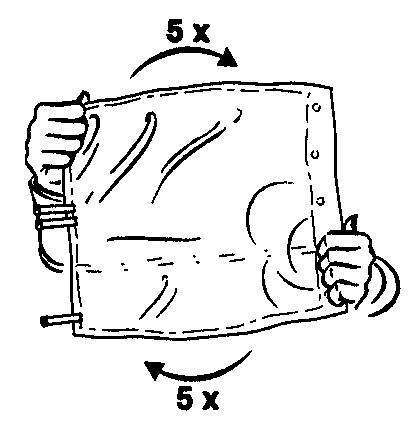
- 4. Certifique-se de que a mistura seja completa, girando o saco cinco vezes em ambos os sentidos.
Administração da solução pronta para uso
A solução para hemofiltração deve ser aquecida aproximadamente à temperatura corporal usando um aquecedor integrado ou externo. Em nenhum caso deve ser administrada a solução se estiver abaixo da temperatura ambiente.
Durante o uso deste medicamento, foram observados casos raros de formação de um sedimento branco de carbonato de cálcio nos tubos, especialmente perto da bomba e do dispositivo de aquecimento. Portanto, durante a hemofiltração, deve-se controlar visualmente a solução nos tubos de infusão a cada 30 minutos para garantir que a solução nos tubos seja transparente e livre de sedimentos.
Os sedimentos também podem ocorrer com um atraso significativo após o início do tratamento. Se sedimentos forem detectados, deve-se substituir imediatamente a solução e os tubos de infusão e monitorizar cuidadosamente o doente.
Para uso único. O conteúdo não utilizado da solução e quaisquer recipientes danificados devem ser descartados.
- País de registo
- Requer receita médicaNão
- Fabricante
- ImportadorB. Braun Avitum AG
- Esta informação é apenas para referência e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
- Alternativas a Duosol nie zauieraiomci potasuForma farmacêutica: Solução, 9 mg/mlSubstância ativa: sodium chlorideRequer receita médicaForma farmacêutica: Solução, 100 mg/mlSubstância ativa: dextranFabricante: Fresenius Kabi Italia S.r.L.Não requer receita médicaForma farmacêutica: Concentrado, -Substância ativa: electrolytes in combination with other drugsFabricante: Fresenius Kabi Norge ASNão requer receita médica
Alternativas a Duosol nie zauieraiomci potasu noutros países
As melhores alternativas com o mesmo princípio ativo e efeito terapêutico.
Alternativa a Duosol nie zauieraiomci potasu em Ukraine
Alternativa a Duosol nie zauieraiomci potasu em Espanha
Médicos online para Duosol nie zauieraiomci potasu
Avaliação de posologia, efeitos secundários, interações, contraindicações e renovação da receita de Duosol nie zauieraiomci potasu – sujeita a avaliação médica e regras locais.














