
Jak stosować Treosulfan Zentiva
Ulotka dołączona do opakowania: informacja dla użytkownika
Treosulfan Zentiva, 5 g, proszek do sporządzania roztworu do infuzji
Treosulfan
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub pielęgniarki.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe objawy niepożądane niewymienione w ulotce,należy powiedzieć o tym lekarzowi lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1.Co to jest lek Treosulfan Zentiva i w jakim celu się go stosuje
- 2.Informacje ważne przed zastosowaniem leku Treosulfan Zentiva
- 3.Jak stosować lek Treosulfan Zentiva
- 4.Możliwe działania niepożądane
- 5.Jak przechowywać lek Treosulfan Zentiva
- 6.Zawartość opakowania i inne informacje
1. Co to jest lek Treosulfan Zentiva i w jakim celu się go stosuje
Lek Treosulfan Zentiva zawiera substancję czynną treosulfan. Treosulfan należy do grupy
leków przeciwnowotworowych nazywanych lekami alkilującymi. Leki te hamują wzrost
guza.
Lek Treosulfan Zentiva został przepisany pacjentowi przez lekarza do stosowania w
leczeniu zaawansowanego raka jajnika po co najmniej jednej wcześniejszej terapii
standardowej.
2. Informacje ważne przed zastosowaniem leku Treosulfan Zentiva
Kiedy nie stosować leku Treosulfan Zentiva
- jeśli pacjent ma uczulenie na treosulfan
- jeśli pacjent ma zbyt małą liczbę krwinek (ciężka depresja szpiku kostnego). Przed każdym podaniem pacjent będzie miał badanie krwi w celu sprawdzenia, czy liczba krwinek umożliwia podanie leku Treosulfan Zentiva.
- w okresie karmienia piersią.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania Treosulfan Zentiva należy omówić to z lekarzem lub
pielęgniarką, jeśli:
- u pacjenta wystąpi zapalanie płuc, który powoduje duszność (alergiczne zapalenie pęcherzyków płucnych lub włóknienie płuc). W takim przypadku leczenie Treosulfan Zentiva należy przerwać. Stosując lek Treosulfan Zentiva pacjent powinien wiedzieć o:
- podwyższonym ryzyku rozwoju niektórych rodzajów zakażeń;
- możliwości wystąpienia różnych nowotworów krwi po długotrwałym leczeniu;
- ponieważ treosulfan jest wydalany przez nerki, należy ściśle monitorować morfologię krwi i odpowiednio zmodyfikować dawkę, jeśli u pacjenta wystąpią zaburzenia czynności nerek;
- leczenie lekami przeciwnowotworowymi może zwiększyć ryzyko uogólnionego zakażenia po niektórych szczepieniach. Dlatego nie należy stosować tego leku razem ze szczepionkami żywymi;
- w związku z możliwością wystąpienia stanu zapalnego pęcherza moczowego lub częstszego oddawania moczu lub uczucia parcia na mocz z obecnością lub bez obecności krwi w moczu (krwotoczne zapalenie pęcherza moczowego), zaleca się picie większej niż zwykle ilości płynów do 24 godzin po leczeniu treosulfanem; W przypadku kobiet w wieku rozrodczym w trakcie leczenia i przez sześć miesięcy po jego zakończeniu konieczne jest także stosowanie skutecznej antykoncepcji (np. pigułek antykoncepcyjnych) (patrz punkt „Ciąża i karmienie piersią”).
Lek Treosulfan Zentiva a inne leki
Należy powiedzieć lekarzowi lub pielęgniarce o wszystkich lekach przyjmowanych przez
pacjenta obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować.
Działanie ibuprofenu lub /chlorochiny może być zmniejszone w przypadku podawania w
skojarzeniu z lekiem Treosulfan Zentiva.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy
planuje mieć dziecko, powinna poradzić się lekarza przed zastosowaniem tego leku. Brak
danych lub istnieją tylko ograniczone dane dotyczące stosowania leku Treosulfan Zentiva,
5-gramowego proszku do sporządzania roztworu do infuzji u kobiet w okresie ciąży lub
karmiących piersią.
Ciąża
W związku z tym, że nie można wykluczyć uszkodzenia płodu, nie należy stosować leku
Treosulfan Zentiva, 5-gramowego proszku do sporządzania roztworu do infuzji w okresie
ciąży, o ile lekarz nie uzna tego za absolutnie niezbędne. Nie należy zachodzić w ciążę w
trakcie leczenia lekiem Treosulfan Zentiva, 5-gramowym proszkiem do sporządzania
roztworu do infuzji.
W przypadku zajścia w ciążę w trakcie leczenia lekiem Treosulfan Zentiva, 5-gramowym
proszkiem do sporządzania roztworu do infuzji należy niezwłocznie poinformować
lekarza.
Antykoncepcja u kobiet
W przypadku kobiet w wieku rozrodczym w trakcie leczenia lekiem Treosulfan Zentiva,
5-gramowym proszkiem do sporządzania roztworu do infuzji i przez sześć miesięcy po
jego zakończeniu konieczne jest stosowanie odpowiedniej antykoncepcji.
Karmienie piersią
W związku z tym, że nie można wykluczyć możliwości przeniknięcia substancji do mleka
matki, nie należy karmić piersią w trakcie leczenia lekiem Treosulfan Zentiva, 5-
gramowym proszkiem do sporządzania roztworu do infuzji.
Prowadzenie pojazdów i obsługiwanie maszyn
W przypadku wystąpienia nudności lub wymiotów może dojść do pogorszenia zdolności
do prowadzenia pojazdów i obsługiwania maszyn. Jeśli u pacjenta wystąpią takie objawy,
nie należy prowadzić pojazdów ani obsługiwać maszyn.
3. Jak stosować lek Treosulfan Zentiva
Lek Treosulfan Zentiva będzie podawany przez lekarza lub pielęgniarkę w postaci
kroplówki do żyły. Będzie to trwało od 15 do 30 minut (wlew dożylny), a lek zostanie
podany w dawce obliczonej specjalnie dla pacjenta przez lekarza.
Lekarz obliczy potrzebną dawkę leku Treosulfan Zentiva na podstawie morfologii krwi.
Lekarz zmniejszy dawkę, jeśli pacjent otrzymał inny lek przeciwnowotworowy lub
radioterapię. Dawka, którą otrzymuje pacjent zależy także od rozmiarów ciała pacjenta i
różni się w zależności od powierzchni ciała (BSA).
W trakcie leczenia lekiem Treosulfan Zentiva wlewy podawane są zwykle co 3 do
4 tygodni. Zasadniczo podaje się 6 cykli leczenia.
Lekarz może zmienić dawkę i częstość podawania w zależności od wyników badań krwi,
ogólnego stanu zdrowia, innych terapii stosowanych przez pacjenta oraz jego odpowiedzi
na leczenie lekiem Treosulfan Zentiva. W razie jakichkolwiek wątpliwości dotyczących
leczenia należy zwrócić się do lekarza lub pielęgniarki.
Jeśli u pacjenta wystąpi ból w miejscu iniekcji, należy natychmiast powiadomić o tym
lekarza lub pielęgniarkę.
Stosowanie u dzieci
Nie zaleca się stosowania tego leku u dzieci.
Zastosowanie większej niż zalecana dawki leku Treosulfan Zentiva
Jeśli pacjent otrzyma zbyt dużą dawkę tego leku, może zachorować lub może dojść u
niego do zmniejszenia liczby krwinek. Lekarz może zastosować przetoczenie krwi lub w
razie konieczności podejmie inne działania.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego, leku
należy zwrócić się do lekarza lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one
wystąpią. Lekarz omówi je z pacjentem oraz wyjaśni zagrożenia i korzyści wynikające z
leczenia.
O wystąpieniu któregokolwiek z wymienionych poniżej objawów należy niezwłocznie poinformować lekarza lub pielęgniarkę:
- Reakcje alergiczne [rzadko (mogą wystąpić nie częściej niż u 1 na 1000 pacjentów)]: jeśli u pacjenta wystąpi świąd, wysypka, obrzęk twarzy, ust, języka i/lub gardła, który może spowodować trudności w przełykaniu lub oddychaniu bądź spadek ciśnienia krwi.
- Gorączka lub zakażenie [bardzo często (mogą wystąpić częściej niż u 1 na10 pacjentów)]: jeśli u pacjenta występuje gorączka 38°C lub wyższa, pocenie się lub objawy zakażenia (ponieważ u pacjenta może występować niższa niż zazwyczaj liczba krwinek białych).
- Osłabienie [bardzo często (może wystąpić częściej niż u 1 na 10 osób)]duszność lub bladość skóry (ponieważ u pacjenta może występować niższa niż zazwyczaj liczba krwinek czerwonych).
- Krwawienie [bardzo często (może wystąpić częściej niż u 1 na 10 osób)]z dziąseł, jamy ustnej lub nosa bądź nieoczekiwane podbiegnięcia krwawe lub bladość skóry (ponieważ u pacjenta może występować niższa niż zazwyczaj liczba płytek krwi).
- Trudności w oddychaniu [ bardzo rzadko (mogą wystąpić nie częściej niż u 1 na10 000 pacjentów)](ponieważ u pacjenta może wystąpić reakcja alergiczna, zapalenie lub zakażenie płuc).
Bardzo często (mogą wystąpić częściej niż u 1 na 10 osób):
- Niestrawność, w tym nudności (mdłości) z wymiotami lub bez wymiotów.
- Łagodne wypadanie włosów. Po zabiegu wzrost włosów powinien wrócić do normy.
- Brązowe przebarwienie skóry.
Często (mogą wystąpić nie częściej niż u 1 na 10 osób):
- Zakażenia wywołane przez bakterie, wirusy lub grzyby.
Niezbyt często (mogą wystąpić nie częściej niż u 1 na 100 osób):
- Różne nowotwory krwi (po długotrwałym leczeniu).
Bardzo rzadko (mogą wystąpić nie częściej niż u 1 na 10 000 osób):
- Ciężkie zakażenie ogólne (sepsa)
- Choroba Addisona, stan zaburzenia pracy nadnerczy, który prowadzi do wystąpienia brązowego zabarwienia skóry, niestrawności, niskiego ciśnienia krwi (uczucie omdlenia) oraz ogólnego osłabienia.
- Pocenie się, drżenie i głód w wyniku spadku stężenia glukozy we krwi (hipoglikemia).
- Uczucie mrowienia i drętwienia (parestezje).
- Osłabienie mięśnia sercowego wywołane przez zmianę strukturalną (kardiomiopatia).
- Pokrzywka lub swędząca wysypka; zapalenie skóry z łuszczeniem się lub bez (twardzina i łuszczyca), zaczerwienienie skóry (rumień).
- Zapalenie pęcherza moczowego, powodujące ból oraz częstsze oddawanie moczu i uczucie parcia na mocz z obecnością lub bez obecności krwi w moczu (krwotoczne zapalenie pęcherza moczowego).
- Złe samopoczucie (objawy grypopodobne).
- Bolesne zaczerwienienie lub obrzęk w miejscu zakażenia (w przypadku wycieku roztworu treosulfanu do sąsiedniej tkanki). Należy natychmiast poinformować lekarza lub pielęgniarkę, jeśli wystąpi którykolwiek z powyższych objawów.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane nie
wymienione w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce.
Działania niepożądane można zgłaszać bezpośrednio do Departament Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów
Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
PL-02 222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu. Dzięki
zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Treosulfan Zentiva
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie fiolki i
pudełku tekturowym po: Termin ważności (EXP). Termin ważności oznacza ostatni dzień
podanego miesiąca.
Produktu po rekonstytucji nie przechowywać w lodówce (2–8°C), ponieważ może to
spowodować wytrącenie osadu. Roztworów, z których wytrącił się osad nie należy
używać.
Nie umieszczać w lodówce.
Wykazano stabilność chemiczną i fizyczną produktu podczas stosowania w ciągu
12 godzin w temperaturze 30°C. Z mikrobiologicznego punktu widzenia, o ile metoda
rekonstytucji nie wyklucza ryzyka skażenia mikrobiologicznego, produkt należy zużyć
natychmiast. Jeśli produkt nie zostanie zużyty natychmiast, za ustalenie okresu i
warunków przechowywania produktu podczas stosowania odpowiada użytkownik.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki.
Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa. Takie
postępowanie pomoże chronić środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Treosulfan Zentiva
- Substancją czynną leku jest treosulfan. Każda fiolka zawiera 5 g treosulfanu.
- Po rekonstytucji, 1 ml roztworu zawiera 50 mg treosulfanu.
Jak wygląda lek Treosulfan Zentiva i co zawiera opakowanie
Lek Treosulfan Zentiva to biały, krystaliczny zbrylony proszek lub proszek, który jest
dostarczany w fiolkach z przezroczystego szkła typu I; każda fiolka zawiera 5 g
treosulfanu.
Przed podaniem suchy proszek jest mieszany z wodą do wstrzykiwań w fiolce, tworząc
roztwór.
Lek Treosulfan Zentiva jest dostępny w pudełku tekturowym zawierającym 1 fiolkę lub
5 fiolek.
Fiolki mogą, ale nie muszą, być umieszczone w kurczliwym rękawie z tworzywa
sztucznego/mieć dno wykonane z tego materiału (podstawkę). Rękaw z tworzywa
sztucznego nie styka się z produktem leczniczym i stanowi dodatkowe zabezpieczenie
podczas transportu. Ułatwia to bezpieczną pracę z produktem leczniczym zarówno dla
członków fachowego personelu medycznego, jak i dla personelu farmaceutycznego.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Zentiva, k.s.
U kabelovny 130
Dolní Měcholupy
102 37, Praga 10
Republika Czeska
Importer
MIAS Pharma Limited
Suite 2, Stafford House, Strand Road
Portmarnock, Co. Dublin
Irlandia
Tillomed Malta Limited,
Malta Life Sciences Park,
LS2.01.06 Industrial Estate,
San Gwann, SGN 3000, Malta
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich
Europejskiego Obszaru Gospodarczego pod następującymi nazwami:
Wielka Brytania:
Treosulfan 5g powder for solution for infusion
Niemcy:
Treosulfan Tillomed 5g Pulver zur Herstellung einer
Infusionslösung
Francja:
Treosulfan Tillomed 5g poudre pour solution pour perfusion
Włochy:
Treosulfan Tillomed
Hiszpania:
Treosulfano Tillomed 5g polvo para solución para perfusión
EFG
Austria:
Treosulfan Tillomed 5g Pulver zur Herstellung einer
Infusionslösung
Czechy:
Treosulfan Tillomed
Grecja:
Treosulfan Tillomed 5g κόνις για διάλυμα προς έγχυση
Polska:
Treosulfan Zentiva
Rumunia:
Treosulfan Tillomed 5g Pulbere pentru soluţie perfuzabilă
Dania:
Treosulfan Tillomed
Finlandia:
Treosulfan Tillomed infuusiokuiva-aine liuosta varten 5g
Norwegia:
Treosulfan Tillomed 5g Pulver til infusjonsvæske, oppløsning
Szwecja:
Treosulfan Tillomed 5g Pulver till infusionsvätska, lösning
Belgia:
Treosulfan Tillomed 5g Poeder voor oplossing voor infusie
Treosulfan Tillomed 5g poudre pour solution pour perfusion
Treosulfan Tillomed 5g Pulver zur Herstellung einer
Infusionslösung
Irlandia:
Treosulfan Tillomed 5g powder for solution for infusion
Holandia:
Treosulfan Tillomed 5g Poeder voor oplossing voor infusie
Portugalia:
Treossulfano Tillomed 5g pó para solução para perfusão
Data ostatniej aktualizacji ulotki:marzec 2024
------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Wyłącznie do jednorazowego użycia.
Wytyczne dotyczące bezpiecznego postępowania z lekami przeciwnowotworowymi:
- 1. Rekonstytucję produktu leczniczego powinien przeprowadzać przeszkolony fachowy personel medyczny.
- 2. Należy to wykonywać w wyznaczonym obszarze.
- 3. Należy nosić rękawiczki ochronne, maski i odzież.
- 4. Należy zachować środki ostrożności, aby uniknąć przypadkowego kontaktu produktu leczniczego z oczami. W razie przypadkowego kontaktu roztworu ze skórą lub oczami zanieczyszczony obszar należy spłukać dużą ilością wody lub normalnego roztworu soli fizjologicznej. W celu usunięcia przemijającego pieczenia skóry można zastosować łagodny krem. W przypadku kontaktu z oczami należy zasięgnąć porady lekarskiej.
- 5. Z preparatami cytotoksycznymi nie mogą pracować osoby, które mogą być w ciąży.
- 6. Podczas usuwania materiałów (strzykawek, igieł itd.) wykorzystywanych do rekonstytucji leków cytotoksycznych należy zastosować odpowiednią ostrożność i środki ostrożności.
- 7. Powierzchnię roboczą należy osłonić jednorazowym arkuszem z tworzywa sztucznego z chłonnym papierem na odwrocie.
- 8. Na wszystkich strzykawkach i zestawach należy stosować złącza Luer-Lock. Zaleca się użycie igieł z dużymi otworami, aby zminimalizować ciśnienie i możliwość utworzenia aerozolu. Możliwość tą można także zmniejszyć, używając igły odpowietrzającej.
Instrukcje dotyczące rekonstytucji produktu leczniczego Treosulfan Zentiva
Aby uniknąć problemów z rozpuszczalnością w trakcie rekonstytucji, należy uwzględnić
następujące aspekty:
- 1. Rozpuszczalnik, woda do wstrzykiwań, musi zostać ogrzana do 25–30ºC (nie wyższej) w łaźni wodnej.
- 2. Treosulfan należy ostrożnie usunąć z wewnętrznej powierzchni fiolki infuzyjnej poprzez potrząsanie. Procedura ta jest bardzo ważna, ponieważ zwilżenie proszku spowoduje jego przywarcie do powierzchni, co doprowadzi do zbrylenia. W razie wystąpienia zbrylenia należy mocno potrząsać fiolką przez dłuższy czas.
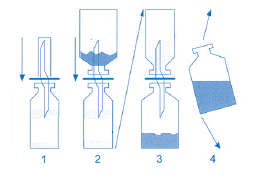
- 3. Jedną stronę dwustronnej kaniuli należy umieścić w gumowym korku fiolki z wodą. Fiolkę z treosulfanem należy następnie umieścić na drugim końcu kaniuli, ustawiając dno na górze. Całą konstrukcję należy odwrócić. Podczas delikatnego potrząsania fiolką woda spływa do fiolki znajdującej się na dole. W przypadku postępowania zgodnie z tymi instrukcjami cała procedura rekonstytucji nie powinna potrwać dłużej niż 2 minuty. Poniższy schemat ułatwia przeprowadzenie procesu rekonstytucji.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- ImporterMIAS Pharma Limited Tillomed Malta Limited
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Treosulfan Zentiva
Odpowiedniki Treosulfan Zentiva w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Treosulfan Zentiva – Hiszpania
Lekarze online w sprawie Treosulfan Zentiva
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Treosulfan Zentiva – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.






