
TREOSULFANO ZENTIVA 5 G POLVO PARA SOLUCION PARA PERFUSION EFG

Cómo usar TREOSULFANO ZENTIVA 5 G POLVO PARA SOLUCION PARA PERFUSION EFG
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Treosulfano Zentiva 5 g polvo para solución para perfusión EFG
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o enfermero.
- Si experimenta efectos adversos, consulte a su médico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Treosulfano Zentiva y para qué se utiliza
- Qué necesita saber antes de empezar a usar Treosulfano Zentiva
- Cómo usar Treosulfano Zentiva
- Posibles efectos adversos
- Conservación de Treosulfano Zentiva
- Contenido del envase e información adicional
1. Qué es Treosulfano Zentiva y para qué se utiliza
Treosulfano Zentiva contiene el principio activo treosulfano. Treosulfano pertenece al grupo de los agentes alquilantes. Estos agentes actúan deteniendo el crecimiento de células cancerosas.
Treosulfano Zentiva le ha sido recetado por su médico para el tratamiento del cáncer de ovario avanzado después de, al menos, un tratamiento estándar previo.
2. Qué necesita saber antes de empezar a usar Treosulfano Zentiva
No use Treosulfano Zentiva:
- si es alérgico al treosulfano;
- si no tiene suficientes células sanguíneas (supresión severa de la médula ósea);
- si se encuentra en periodo de lactancia.
Antes de cada administración, se deberá realizar un análisis de sangre para verficar que tiene suficientes células sanguineas para recibir Treosulfano Zentiva.
Advertencias y precauciones
Consulte a su médico o enfermero antes de empezar a usar Treosulfano Zentiva:
Daño en la médula ósea y controles del recuento sanguíneo
La reacción adversa que limita la dosis de treosulfano es la restricción de la función de la médula ósea, que generalmente desaparece tras la interrupción del tratamiento. Se manifiesta en una reducción de los glóbulos blancos (leucocitos) y las plaquetas (trombocitos) y en una disminución de los glóbulos rojos (hemoglobina).
Dado que los trastornos de la función de la médula ósea se acumulan, su médico le controlará el recuento sanguíneo a intervalos más cortos a partir del tercer ciclo. Esto es especialmente importante cuando se combina con otras formas de terapia que atacan la médula ósea, como la radioterapia. Si la función de la médula ósea se ve afectada, existe un mayor riesgo de infección.
En general, los glóbulos blancos (leucocitos) y las plaquetas (trombocitos) vuelven a sus niveles basales después de 28 días.
Toxicidad pulmonar
La dificultad para respirar, la tos o la fiebre alta pueden indicar una enfermedad pulmonar. Si existen limitaciones graves de la función pulmonar, como inflamación, cicatrices o infecciones, se debe interrumpir el tratamiento con treosulfán.
Ha de tener en cuenta los siguientes aspectos mientras está en tratamiento con Treosulfano Zentiva:
- aumenta su riesgo de desarrollar ciertos tipos de infección;
- pueden ocurrir diferentes tipos de cáncer de sangre después de un tratamiento prolongado;
- si tiene problemas renales, el treosulfano se excreta a través de los riñones, por esta razón, se deberá realizar un control estricto de sus recuentos sanguíneos y si es necesario ajustar su dosis;
- el tratamiento con medicamentos contra el cáncer puede aumentar el riesgo de infección generalizada después de algunas vacunaciones. Por lo tanto, debe evitar ser vacunado con vacunas vivas;
- debido al posible desarrollo de inflamación en la vejiga que causa dolor u orinar con mayor frecuencia o urgencia, con o sin presencia de sangre en orina (cistitis hemorrágica), se le recomienda beber más líquidos de lo normal hasta 24 horas después de su tratamiento con treosulfano.
- si es mujer en edad fértil, debe utilizar también métodos anticonceptivos eficaces (es decir, de prevención del embarazo) durante y hasta seis meses después del tratamiento (ver sección Embarazo y lactancia).
Extravasación
La perfusión de treosulfano se debe realizar utilizando una técnica segura, dado que la extravasación de la solución de treosulfano en el tejido circundante puede producir reacciones inflamatorias y dolorosas en el lugar de la inyección. Si se produce extravasación, se debe interrumpir la perfusión inmediatamente y administrar la dosis restante en otra vena.
Otros medicamentos y Treosulfano Zentiva
Informe a su médico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento, incluso los medicamentos adquiridos sin receta. Esto incluye medicamentos a base de plantas.
El efecto del tratamiento con ibuprofeno/cloroquina puede verse reducido cuando se administra junto con Treosulfano Zentiva.
Embarazo ylactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes de utilizar este medicamento. No existen datos, o estos son escasos, en relación con el uso de Treosulfano Zentiva 5 g polvo para solución para perfusión en mujeres embarazadas o en periodo de lactancia.
Embarazo
Debido a que no se pueden descartar lesiones en el feto, Treosulfano Zentiva 5 g polvo para solución para perfusión no debe usarse durante el embarazo, a menos que su médico lo considere absolutamente necesario. No debe quedarse embarazada durante el tratamiento con Treosulfano Zentiva 5 g polvo para solución para perfusión.
Si se queda embarazada durante el tratamiento con Treosulfano Zentiva 5 g polvo para solución para perfusión, debe informar de inmediato a su médico.
Anticoncepción en mujeres
Durante y hasta seis meses después del tratamiento con Treosulfano Zentiva 5 g polvo para solución para perfusión, debe utilizar métodos anticonceptivos adecuados si se encuentra en edad fértil.
Lactancia
Puesto que no se puede descartar una posible transferencia de la sustancia a la leche materna, no debe dar el pecho durante el tratamiento con Treosulfano Zentiva 5 g polvo para solución para perfusión.
Conducción y uso de máquinas
No se han realizado estudios sobre el efecto en la capacidad para conducir y utilizar máquinas. No conduzca y no utilice máquinas si tiene nausea y vómitos, ya que estos efectos puede disminiur su capacidad de conducir o manejar maquinaria.
3. Cómo usar Treosulfano Zentiva
Treosulfano Zentiva se administra normalmente por un médico o enfermero directamente en el torrente circulatorio. Su médico calculará la dosis correcta para usted y le será administrado (perfusión intravenosa) durante 15 a 30 minutos.
Su médico calculará la dosis correcta de Treosulfano Zentiva, según los valores de sus recuentos sanguíneos. Su médico le reducirá la dosis si le han administrado otro medicamento anticanceroso o un tratamiento de radioterapia. La dosis también dependerá del tamaño de su cuerpo y variará de acuerdo con su área de superficie corporal.
Durante el tratamiento con Treosulfano Zentiva, las perfusiones normalmente se administrarán cada 3 a 4 semanas. En general, se dan 6 ciclos de tratamiento.
Su médico podrá cambiar la dosis y la frecuencia de su tratamiento según los resultados de su análisis de sangre, su estado general, cualquier tratamiento adicional que esté recibiendo y su respuesta al tratamiento con Treosulfano Zentiva. En caso de duda, pregunte a su médico o enfermero.
Si siente dolor en el lugar de la inyección, informe a su médico o enfermero inmediatamente.
Uso en niños
No se recomienda su uso en niños
Si recibe más Treosulfano Zentiva del que debe
Si le han administrado demasiada dosis de este medicamento, puede sentirse enfermo o sus células sanguíneas pueden verse reducidas. Su médico puede administrarle una transfusión de sangre y tomará otras medidas si es necesario
Si usted tiene cualquier duda sobre el uso de este medicamento, pregunte a su médico, farmacéutico o enfermero.
En caso de sobredosis o ingestión accidental consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono: 91 562 04 20, indicando el medicamento y la cantidad ingerida.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Si sufre algún efecto adverso, es importante que informe a su médico antes del siguiente tratamiento.
Informe a su médico inmediatamente si nota alguno de los siguientes síntomas:
- Reacciones alérgicas [raros (pueden afectar hasta a 1 de cada 1000 personas)]: si desarrolla picazón, erupción cutánea, hinchazón de la cara, labios, lengua y / o garganta, que puede causar dificultad para tragar o respirar o una disminución de la presión arterial.
- Fiebre o infección [muy frecuentes (pueden afectar a más de 1 de cada 10 personas)]: si tiene una temperatura corporal de 38°C o más, experimente sudoración u observa cualquier otro signo de infección (puede tener menos glóbulos blancos de lo normal).
- Debilidad [muy frecuentes (pueden afectar a más de 1 de cada 10 personas)], dificultad para respirar o si su piel se pone pálida (puede tener menos glóbulos rojos de lo normal).
- Sangrado [muy frecuentes (pueden afectar a más de 1 de cada 10 personas)]de las encías, la boca o la nariz o aparición anómala de hematomas (puede tener menos plaquetas de lo normal).
- Dificultad para respirar [muy raros (pueden afectar hasta 1 de cada 10000 personas)](puede tener una reacción alérgica, inflamación o infección del pulmón)
Efectos adversos muy frecuentes (pueden afectar a más de 1 de cada 10 personas):
- Reducción de los glóbulos blancos (aumenta el riesgo de infección), plaquetas (puede causar hematomas y sangrado de las encías y sangrado de la boca y la nariz) y glóbulos rojos (puede causar palidez, debilidad y dificultad para respirar) - por lo tanto, se debe controlar regularmente el recuento sanguíneo.
- Problemas estomacales, incluyendo náuseas (sentirse enfermo) con o sin vómitos (estar enfermo).
- Pérdida de cabello leve. Después de su tratamiento, regresa el crecimiento normal del cabello.
- Decoloración bronceada de la piel.
Efectos adversos frecuentes (pueden afectar hasta a 1 de cada 10 personas):
- Infecciones causadas por hongos, virus o bacterias (pueden dar lugar a fiebre, sudor y sensación general de malestar).
- Molestias gastrointestinales.
Efectos adversos poco frecuentes (pueden afectar hasta a 1 de cada 100 personas):
- Diferentes tipos de cáncer de sangre (después de tratamientos de larga duración).
- Inflamación de la membrana mucosa oral (estomatitis).
Efectos adversos muy raros (pueden afectar hasta 1 de cada 10.000 personas):
- Reducción grave y simultánea de todas las células sanguíneas (pancitopenia); puede causar debilidad y hematomas y aumentar el riesgo de infección.
- Enfermedad de Addison, una enfermedad en la que las glándulas suprarrenales no funcionan correctamente, lo que produce piel bronceada, malestar estomacal, presión arterial baja (sensación de mareo) y una sensación general de debilidad.
- Sudor, temblores y hambre como resultado de un descenso en los niveles de glucosa dentro de su sangre (hipoglucemia).
- Hormigueo y sensación de entumecimiento (parestesia).
- Debilidad del músculo cardíaco causado por un cambio estructural (cardiomiopatía).
- Dificultad para respirar (inflamación y cicatrización de los pulmones e infecciones pulmonares).
- Aumento de los valores de la función hepática (puede provocar cansancio, sensación de presión en la parte superior derecha del abdomen y coloración amarillenta de la esclerótica y la piel).
- Urticaria o sarpullido con picazón; inflamación de la piel con o sin formación de escamas (esclerodermia y psoriasis), enrojecimiento de la piel (eritema).
- Inflamación de la vejiga, que causa dolor o una micción más frecuente y urgente, con o sin sangre en la orina (cistitis hemorrágica).
- Sensación de malestar (síntomas parecidos a los de la gripe).
- Enrojecimiento o hinchazón dolorosos en el sitio de inyección (en caso de que la solución de treosulfano salga y entre en contacto con la piel).
Frecuencia no conocida: no puede estimarse a partir de los datos disponibles
- Septicemia (sepsis).
Informe a su médico o personal de enfermería inmediatamente si nota cualquiera de los síntomas anteriores.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Treosulfano Zentiva
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el envase después de CAD. La fecha de caducidad es el último día del mes que se indica.
Una vez reconstituido no conserve el medicamento en nevera (2 - 8°C) porque podría precipitar. No usar si la solución contiene precipitados.
No refrigerar.
La estabilidad fisicoquímica en uso se ha demostrado durante 12 horas a 30°C. Desde el punto de vista microbiológico, a menos que la dilución se haya efectuado en condiciones asépticas controladas y validadas, se debe utilizar de forma inmediata. De no ser así, los tiempos de conservación durante el uso y las condiciones previas al mismo son responsabilidad del usuario.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Treosufano Zentiva
- El principio activo es treosulfano. Cada vial contiene 5 g de treosulfano.
- Tras su reconstitución, cada mililitro de solución contiene 50 mg de treosulfano
Aspecto del producto y contenido del envase
Polvo o agregado compacto cristalino de color blanco que se suministra en viales de vidrio transparentes, cada vial contiene 5 g de treosulfano.
El polvo se reconstituye con agua para preparaciones inyectables en el vial formando una solución antes de su administración.
Treosulfano Zentiva está disponible en envases con 1 vial o 5 viales.
Viales con o sin envoltura de plástico retráctil con base protectora (disco). La envoltura retractil no está en contacto con el producto y proporciona una protección adicional durante el transporte. Además mejora la manipulación segura del producto por los profesionales sanitarios.
Titular de la autorización de comercialización
Zentiva k.s.,
U kabelovny 130,
Praga 10 – Dolní Mecholupy,
102 37 República Checa
Responsable de la fabricación
MIAS Pharma Limited
Suite 2, Stafford House, Strand Road
Portmarnock, Co. Dublin
Irlanda
Tillomed Malta Limited,
Malta Life Sciences Park,
LS2.01.06 Industrial Estate,
San Gwann, SGN 3000, Malta
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Zentiva Spain S.L.U.
Avenida de Europa, 19, Edificio 3, Planta 1.
28224 Pozuelo de Alarcón, Madrid
España
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo con los siguientes nombres:
Alemania | Treosulfan Tillomed 5g Pulver zur Herstellung einer Infusionslösung |
Francia | Treosulfan Tillomed 5g poudre pour solution pour perfusion |
España | Treosulfano Zentiva 5 g polvo para solución para perfusión EFG |
Austria: | Treosulfan Tillomed 5g Pulver zur Herstellung einer Infusionslösung |
República Checa: | Treosulfan Tillomed |
Grecia: | Treosulfan Tillomed 5g κ?νις για δι?λυμα προς ?γχυση |
Polonia: | Treosulfan Tillomed |
Rumanía: | Treosulfan Tillomed 5g Pulbere pentru solutie perfuzabila |
Dinamarca: | Treosulfan Tillomed |
Finlandia: | Treosulfan Tillomed infuusiokuiva-aine liuosta varten 5g |
Noruega: | Treosulfan Tillomed 5g Pulver til infusjonsvæske, oppløsning |
Suecia: | Treosulfan Tillomed 5g Pulver till infusionsvätska, lösning |
Bélgica: | Treosulfan Tillomed 5g Poeder voor oplossing voor infusie Treosulfan Tillomed 5g poudre pour solution pour perfusion Treosulfan Tillomed 5g Pulver zur Herstellung einer Infusionslösung |
Irlanda: | Treosulfan Tillomed 5g powder for solution for infusion |
Países Bajos: | Treosulfan Tillomed 5g Poeder voor oplossing voor infusie |
Portugal: | Treossulfano Tillomed 5g pó para solução para perfusão |
Fecha de la última revisión de esteprospecto:Mayo 2025
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/)
--------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario:
Para un solo uso.
Procedimientos para manipulación y eliminación de medicamentos citotóxicos:
- Sólo personal instruido debe reconstituir la solución.
- Se requiere un área de preparación reservada para ello.
- El personal deberá llevar ropa, mascarilla y guantes de protección adecuados.
- Se deben tomar precauciones para evitar que el medicamento entre accidentalmente en contacto con los ojos. Si la solución entra en contacto con la piel u ojos enjuague inmediatamente la zona con agua abundante o solución salina. Se puede usar una crema para tratar el escozor transitorio de la piel. En caso de irritación ocular, contactar con un oftalmólogo.
- Las personas embarazadas no deben manipular este medicamento.
- Se deben tomar precauciones adecuadas para la eliminación de los artículos utilizados para reconstituir los medicamentos citotóxicos (jeringas, agujas, etc.).
- La superficie de trabajo debe cubrirse con plástico desechable y papel absorbente.
- Utilizar accesorios Luer-lock para todos los equipos y jeringas. Se recomienda agujas de gran calibre para minimizar la presión y la posible formación de aerosoles. Esto último también puede reducirse mediante el uso de una aguja de venteo.
Instrucciones para la reconstitución de Treosulfano Zentiva
Para evitar problemas de solubilidad durante la reconstitución, se deben considerar los siguientes aspectos:
- El solvente, agua para preparaciones inyectables, se debe calentar a 25 - 30° C usando un baño de agua.
- El treosulfano debe ser retirado cuidadosamente de la superficie interna del vial de perfusión agitando.
Este procedimiento es muy importante, porque la humectación del polvo que se adhiere a la superficie da como resultado el apelmazamiento. En caso de que se produzca apelmazamiento, se debe sacudir el vial vigorosamente.
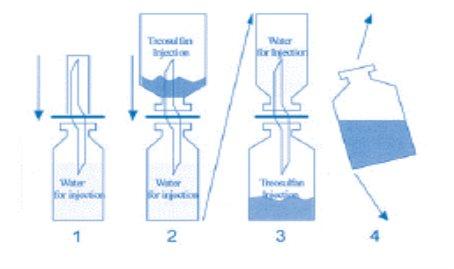
- Un lado de la cánula se coloca en el tapón de goma del vial agua y en el otro extremo de la cánula se coloca el vial de treosulfano boca abajo.
Girar todo el sistema para permitir que el agua entre en el vial inferior mientras se agita suavemente.
Siguiendo estas instrucciones, el procedimiento de reconstitución no debería tardar más de 2 minutos. Vea el diagrama de abajo para ayudar en el proceso de reconstitución:
- País de registro
- Disponibilidad en farmacias
Problema de suministro reportado
Los datos de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) indican un problema de suministro que afecta a este medicamento.<br><br>La disponibilidad puede ser limitada en algunas farmacias.<br><br>Para actualizaciones o alternativas, consulte a su farmacéutico. - Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a TREOSULFANO ZENTIVA 5 G POLVO PARA SOLUCION PARA PERFUSION EFGForma farmacéutica: INYECTABLE PERFUSION, 5 gPrincipio activo: TreosulfanoRequiere recetaForma farmacéutica: INYECTABLE PERFUSION, 6 mg/mlPrincipio activo: BusulfanoFabricante: Accord Healthcare S.L.U.Requiere recetaForma farmacéutica: COMPRIMIDO, 2 mg busulfanoPrincipio activo: BusulfanoFabricante: Aspen Pharma Trading LimitedRequiere receta
Médicos online para TREOSULFANO ZENTIVA 5 G POLVO PARA SOLUCION PARA PERFUSION EFG
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de TREOSULFANO ZENTIVA 5 G POLVO PARA SOLUCION PARA PERFUSION EFG, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes






