
Jak stosować Okteva
Ulotka dołączona do opakowania: informacja dla pacjenta
Okteva, 10 mg, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań o
przedłużonym uwalnianiu
Okteva, 20 mg, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań o przedłużonym uwalnianiu
Okteva, 30 mg, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań o przedłużonym uwalnianiu
oktreotyd
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Okteva i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Okteva
- 3. Jak stosować lek Okteva
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Okteva
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Okteva i w jakim celu się go stosuje
Lek Okteva jest syntetyczną pochodną somatostatyny, substancji występującej w
organizmie ludzkim, która hamuje działanie niektórych hormonów, np. hormonu wzrostu. Lek Okteva
działa silniej niż somatostatyna i jego działanie utrzymuje się dłużej.
Lek Okteva jest stosowany
- w leczeniu akromegalii, Akromegalia jest chorobą, w której organizm wytwarza zbyt wiele hormonu wzrostu. U osób zdrowych hormon wzrostu wpływa na wzrost tkanek, narządów i kości. Zbyt duża ilość hormonu wzrostu powoduje zwiększenie wymiarów kości i tkanek, zwłaszcza dłoni i stóp. Okteva znacząco łagodzi objawy akromegalii, do których należy ból głowy, nadmierne pocenie się, drętwienie dłoni i stóp, zmęczenie i ból stawów. W większości przypadków nadmierne wytwarzanie hormonu wzrostu jest wynikiem powiększenia przysadki (gruczolak przysadki); leczenie lekiem Okteva może zmniejszyć rozmiary gruczolaka.
Lek Okteva jest stosowany w leczeniu osób z akromegalią:
- u których inne rodzaje leczenia akromegalii (leczenie chirurgiczne lub radioterapia) są niewskazane lub nieskuteczne;
- po radioterapii, będących w okresie przejściowym, przed wystąpieniem całkowitego efektu działania radioterapii;
- w celu złagodzenia objawów związanych z nadmiernym wytwarzaniem pewnych specyficznych hormonów i innych zbliżonych substancji przez żołądek, jelita i trzustkę; Nadmierne wytwarzanie hormonów i innych zbliżonych substancji naturalnych może być spowodowane pewnymi rzadkimi chorobami żołądka, jelit lub trzustki. Zaburza to naturalną równowagę hormonalną organizmu i jest przyczyną wielu objawów, takich jak zaczerwienienie twarzy, biegunka, niskie ciśnienie krwi, wysypka i utrata masy ciała. Stosowanie leku Okteva pomaga łagodzić te objawy:
- w leczeniu guzów neuroendokrynnych zlokalizowanych w jelicie (np. w wyrostku robaczkowym, jelicie cienkim lub okrężnicy); Guzy neuroendokrynne są rzadko występującymi guzami, umiejscowionymi w różnych częściach organizmu. Lek Okteva stosuje się również do hamowania wzrostu tego typu guzów, jeśli są one zlokalizowane w jelicie (np. w wyrostku robaczkowym, jelicie cienkim lub okrężnicy);
- w leczeniu guzów przysadki wydzielających zbyt dużą ilość hormonu tyreotropowego (TSH); Zbyt duża ilość hormonu tyreotropowego (TSH) prowadzi do nadczynności tarczycy. Lek Okteva jest stosowany u osób z guzami przysadki wydzielającymi zbyt dużą ilość hormonu tyreotropowego (TSH):
- gdy inne rodzaje leczenia (leczenie chirurgiczne lub radioterapia) są nieodpowiednie lub nieskuteczne;
- po radioterapii w okresie przejściowym, zanim radioterapia osiągnie pełną skuteczność.
2. Informacje ważne przed zastosowaniem leku Okteva
Należy postępować zgodnie ze wszystkimi zaleceniami lekarza. Mogą one różnić się od informacji
zawartych w tej ulotce.
Należy zapoznać się z poniższymi informacjami przed zastosowaniem leku Okteva.
Kiedy nie stosować leku Okteva:
- jeśli pacjent ma uczulenie na oktreotyd lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Okteva, należy omówić to z lekarzem:
- jeżeli pacjent wie, że ma lub miał w przeszłości kamienie żółciowe; lub wystąpią jakiekolwiek komplikacje, takie jak gorączka, dreszcze, ból brzucha lub zażółcenie skóry lub oczu; należy powiedzieć o tym lekarzowi, ponieważ długotrwałe stosowanie leku Okteva może powodować powstawanie kamieni żółciowych. Lekarz może zlecić okresową kontrolę pęcherzyka żółciowego;
- jeśli pacjent choruje na cukrzycę, ponieważ lek Okteva może wpływać na stężenie cukru we krwi. Jeśli pacjent choruje na cukrzycę, stężenie cukru we krwi powinno być u niego regularnie kontrolowane;
- jeśli pacjent miał w przeszłości zmniejszone stężenie witaminy B , lekarz może zlecić okresową kontrolę stężenia witaminy B .
Badania i wizyty kontrolne
Jeśli pacjent jest długotrwale leczony lekiem Okteva, lekarz może zlecić okresową kontrolę
czynności tarczycy.
Lekarz będzie kontrolował czynność wątroby pacjenta.
Lekarz może zlecić sprawdzenie działania enzymów trzustki.
Dzieci
Doświadczenie dotyczące stosowania leku Okteva u dzieci jest niewielkie.
Okteva a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio, a także o lekach, które pacjent planuje przyjmować.
Podczas leczenia lekiem Okteva można na ogół kontynuować przyjmowanie innych leków.
Zgłaszano jednak, że Okteva wpływa na działanie pewnych leków, takich jak cymetydyna,
cyklosporyna, bromokryptyna, chinidyna i terfenadyna.
Jeśli pacjent przyjmuje lek zmniejszający ciśnienie krwi (np. lek adrenolityczny - tzw. beta-bloker,
lub antagonistę wapnia) bądź lek utrzymujący równowagę wodno-elektrolitową, lekarz może
dostosować dawkowanie.
U pacjentów z cukrzycą może zajść konieczność dostosowania dawki insuliny przez lekarza.
Jeśli pacjent ma otrzymywać leczenie oksodotreotydem lutetu ( Lu), terapię radiofarmaceutyczną,
lekarz może przerwać i (lub) dostosować leczenie lekiem Okteva na krótki okres czasu.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza, że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed zastosowaniem tego leku.
Lek Okteva może być stosowany podczas ciąży tylko w razie wyraźnej konieczności.
Pacjentki w wieku rozrodczym powinny podczas leczenia stosować skuteczne metody zapobiegania
ciąży.
Nie należy karmić piersią podczas stosowania leku Okteva. Nie wiadomo, czy lek Okteva przenika do
mleka kobiecego.
Prowadzenie pojazdów i obsługiwanie maszyn
Lek Okteva nie ma wpływu lub wywiera znikomy wpływ na zdolność prowadzenia pojazdów i
obsługiwania maszyn. Jednak pewne działania niepożądane mogące wystąpić podczas stosowania leku
Okteva, takie jak ból głowy i zmęczenie mogą zmniejszać zdolność pacjenta do bezpiecznego
prowadzenia pojazdów i obsługiwania maszyn.
Lek Okteva zawiera sód
Lek Okteva zawiera mniej niż 1 mmol (23 mg) sodu na dawkę, tzn. zasadniczo jest „wolny od sodu”.
3. Jak stosować lek Okteva
Lek Okteva należy podawać wyłącznie w postaci wstrzyknięcia domięśniowego w pośladek.
Podczas długotrwałego podawania należy wykonywać wstrzyknięcia na przemian raz w lewy, raz w
prawy pośladek.
Zastosowanie większej niż zalecana dawki leku Okteva
Po przedawkowaniu leku Okteva nie zgłaszano występowania reakcji zagrażających życiu.
Objawy przedawkowania to: uderzenia gorąca, częste oddawanie moczu, zmęczenie, depresja,
niepokój i brak koncentracji.
W przypadku odczucia, że doszło do przedawkowania i u pacjenta występują powyższe objawy,
należy natychmiast powiedzieć o tym lekarzowi.
Pominięcie zastosowania leku Okteva
W przypadku, gdy wstrzyknięcie nie zostało wykonane w odpowiednim terminie, należy je wykonać
jak najszybciej, a następnie kontynuować leczenie jak poprzednio. Podanie dawki kilka dni później nie
jest szkodliwe, ale może spowodować czasowy nawrót objawów choroby do momentu powrotu do
zaplanowanego schematu leczenia.
Przerwanie stosowania leku Okteva
Po przerwaniu leczenia lekiem Okteva objawy choroby mogą nawrócić. Dlatego nie należy
przerywać stosowania leku Okteva bez porozumienia z lekarzem.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się
do lekarza, pielęgniarki lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Niektóre działania niepożądane mogą być ciężkie. Należy natychmiast poinformować lekarza, jeśli u pacjenta wystąpi którykolwiek z tych objawów:
Bardzo często(mogą dotyczyć więcej niż 1 na 10 osób):
- Kamica żółciowa powodująca nagły ból pleców
- Zbyt duże stężenie cukru we krwi
Często(mogą dotyczyć maksymalnie 1 na 10 osób):
- Niedoczynność tarczycy (hipotyroidyzm) wpływająca na zmiany rytmu serca, łaknienie lub zmiany masy ciała; zmęczenie, uczucie zimna lub obrzęk przedniej części szyi
- Zmiany w wynikach testów czynności tarczycy
- Zapalenie pęcherzyka żółciowego; objawy mogą obejmować ból w prawej górnej części brzucha, gorączkę, nudności, zażółcenie skóry i oczu (żółtaczka)
- Zbyt małe stężenie cukru we krwi
- Zaburzona tolerancja glukozy
- Wolna akcja serca
Niezbyt często(mogą dotyczyć maksymalnie 1 na 100 osób):
- Pragnienie, mała ilość wydalanego moczu, ciemne zabarwienie moczu, sucha, zaczerwieniona skóra
- Szybka akcja serca
Inne ciężkie działania niepożądane
- Reakcje nadwrażliwości (uczulenie), w tym wysypka skórna
- Rodzaj reakcji alergicznej (anafilaksja), która może powodować trudności w przełykaniu lub oddychaniu, obrzęk i mrowienie, z możliwym obniżeniem ciśnienia krwi z zawrotami głowy lub utratą przytomności.
- Zapalenie trzustki; objawy mogą obejmować nagły ból w górnej części brzucha, nudności, wymioty, biegunkę
- Zapalenie wątroby; objawami może być zażółcenie skóry i oczu (żółtaczka), nudności, wymioty, brak apetytu, złe samopoczucie ogólne, świąd, jasne zabarwienie moczu
- Nieregularna akcja serca
- Mała liczba płytek krwi; może to spowodować nasilone krwawienie lub powstawanie sińców.
Jeśli pacjent zauważy u siebie którykolwiek z wymienionych wyżej objawów, należy natychmiast
powiedzieć o tym lekarzowi.
Inne działania niepożądane:
Jeśli pacjent zauważy u siebie którekolwiek z podanych niżej działań niepożądanych, należy
powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania te są zazwyczaj łagodne i mają
tendencję do ustępowania w miarę postępu leczenia.
Bardzo często(mogą dotyczyć ponad 1 na 10 osób):
- Biegunka
- Bóle brzucha
- Nudności
- Zaparcia
- Wzdęcia z oddawaniem gazów
- Bóle głowy
- Ból w miejscu wstrzyknięcia.
Często(mogą dotyczyć maksymalnie 1 na 10 osób):
- Dyskomfort w żołądku po posiłku (niestrawność)
- Wymioty
- Uczucie pełności w żołądku
- Stolce tłuszczowe
- Luźne stolce
- Odbarwienie kału
- Zawroty głowy
- Utrata apetytu
- Zmiany w wynikach testów czynnościowych wątroby
- Łysienie
- Duszność
- Osłabienie
Jeśli wystąpią jakiekolwiek objawy niepożądane, należy powiedzieć o tym lekarzowi, pielęgniarce lub
farmaceucie.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane
można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów
Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
Biobójczych:
Al. Jerozolimskie 181C
02-222 Warszawa
tel.: 22 49-21-301
fax: 22 49-21-309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Okteva
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
Przechowywać w lodówce (2°C – 8°C). Nie zamrażać.
W dniu wykonania wstrzyknięcia lek Okteva można przechowywać w temperaturze poniżej 25°C.
Nie przechowywać leku Okteva po odtworzeniu. Przygotowaną zawiesinę trzeba zużyć natychmiast.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie i opakowaniu po
„EXP” i „Termin ważności (EXP)”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie stosować tego leku, jeśli zauważy się obce cząstki lub zmianę barwy.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Okteva
- Substancją czynną leku jest oktreotyd. Jedna fiolka zawiera 10 mg, 20 mg lub 30 mg oktreotydu (w postaci oktreotydu octanu).
- Pozostałe składniki to: w proszku (fiolka): kopolimer D,L-laktydu i glikolidu (55:45) i mannitol (E 421). w rozpuszczalniku (ampułko-strzykawka): karmeloza sodowa, mannitol (E 421), poloksamer 188 i woda do wstrzykiwań.
Jak wygląda lek Okteva i co zawiera opakowanie
Okteva 10 mg
Każde opakowanie jednostkowe zawiera: 1 szklaną fiolkę zawierającą 10 mg oktreotydu zamkniętą
korkiem z gumy i aluminiowym uszczelnieniem z ciemnoniebieskim wieczkiem typu flip-off, 1
szklaną ampułko-strzykawkę zawierającą 2 ml rozpuszczalnika, 1 bezpieczną igłę do wstrzykiwań i 1
łącznik fiolki lub,
3 szklane fiolki zawierające po 10 mg oktreotydu, 3 ampułko-strzykawki zawierające po 2 ml
rozpuszczalnika, 3 bezpieczne igły do wstrzykiwań i 3 łączniki do fiolek.
Okteva 20 mg
Każde opakowanie jednostkowe zawiera: 1 szklaną fiolkę zawierającą 20 mg oktreotydu zamkniętą
korkiem z gumy i aluminiowym kapslem z pomarańczowym wieczkiem typu flip-off, 1 szklaną
ampułko-strzykawkę zawierającą 2 ml rozpuszczalnika, 1 bezpieczną igłę do wstrzykiwań i 1 łącznik
fiolki lub,
3 szklane fiolki zawierające po 20 mg oktreotydu, 3 ampułko-strzykawki zawierające po 2 ml
rozpuszczalnika, 3 bezpieczne igły do wstrzykiwań i 3 łączniki do fiolek.
Okteva 30 mg
Każde opakowanie jednostkowe zawiera: 1 szklaną fiolkę zawierającą 30 mg oktreotydu zamkniętą
korkiem z gumy i aluminiowym kapslem z ciemnoczerwonym wieczkiem typu flip-off, 1 szklaną
ampułko-strzykawkę zawierającą 2 ml rozpuszczalnika, 1 bezpieczną igłę do wstrzykiwań i jeden
łącznik fiolki lub,
3 szklane fiolki zawierające po 30 mg oktreotydu, 3 ampułko-strzykawki zawierające po 2 ml
rozpuszczalnika, 3 bezpieczne igły do wstrzykiwań i 3 łączniki do fiolek.
Nie wszystkie wielkości opakowania muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Teva B.V.
Swensweg 5
2031 GA Haarlem
Holandia
Wytwórca
PLIVA HRVATSKA d.o.o. (PLIVA CROATIA Ltd.)
Prilaz baruna Filipovića 25
Zagreb 10000
Chorwacja
Merckle GmbH,
Ludwig-Merckle-Str. 3
Blaubeuren
89143
Niemcy
Pharmathen International S.A
Industrial Park Sapes
Rodopi Prefecture, Block No 5
Rodopi 69300
Grecja
W celu uzyskania bardziej szczegółowych informacji o leku oraz jego nazwach w innych państwach członkowskich Europejskiego Obszaru Gospodarczego należy zwrócić się do przedstawiciela podmiotu odpowiedzialnego:
Teva Pharmaceuticals Polska Sp. z o.o., ul. Emilii Plater 53, 00-113 Warszawa, tel. (22) 345 93 00.
Data ostatniej aktualizacji ulotki:luty 2024 r.
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Jaką ilość leku Okteva należy zastosować
Akromegalia
Zaleca się rozpoczęcie leczenia od podawania produktu Okteva w dawce 20 mg co 4 tygodnie
przez 3 miesiące. Pacjenci przyjmujący podskórnie (sc.)oktreotyd mogą rozpocząć leczenie
produktem Okteva następnego dnia po ostatnim podaniu podskórnym oktreotydu. Następnie należy
dostosować dawkę leku na podstawie stężenia w surowicy hormonu wzrostu (ang. GH - growth
hormone) i insulinopodobnego czynnika wzrostu 1/somatomedyny C (ang. IGF-1- insulin-like growth
factor) oraz objawów klinicznych.
U pacjentów, u których po 3 miesiącach objawy kliniczne i parametry biochemiczne (GH; IGF-1) nie
są całkowicie kontrolowane (stężenia GH nadal są większe niż 2,5 mikrograma/l), dawkę leku można
zwiększyć do 30 mg co 4 tygodnie. Jeśli po kolejnych 3 miesiącach parametry GH, IGF-1 i (lub) inne
objawy nadal są niewłaściwie kontrolowane podczas podawania dawki 30 mg, dawkę można
zwiększyć do 40 mg co 4 tygodnie.
U pacjentów, u których stężenie GH utrzymuje się stale poniżej 1 mikrograma/l, a stężenie IGF-1 w
surowicy uległo normalizacji oraz u których najszybciej ustępujące objawy przedmiotowe i
podmiotowe akromegalii cofnęły się po 3 miesiącach leczenia dawką 20 mg, można zastosować
produkt Okteva w dawce 10 mg co 4 tygodnie. Jednakże, szczególnie w tej grupie pacjentów,
wskazane jest ścisłe monitorowanie skuteczności leczenia przez oznaczanie stężeń GH i IGF-1 w
surowicy oraz ocenę klinicznych objawów przedmiotowych i podmiotowych podczas leczenia tą małą
dawką produktu Okteva.
U pacjentów otrzymujących ustaloną dawkę produktu leczniczego Okteva należy określać stężenie
GH i IGF-1 co 6 miesięcy.
Hormonalnie czynne guzy żołądka, jelit i trzustki
- Leczenie pacjentów z objawami związanymi z hormonalnie czynnymi guzamineuroendokrynnymi żołądka, jelit i trzustki
Zaleca się rozpoczęcie leczenia od podawania produktu Okteva w dawce 20 mg co 4 tygodnie.
Pacjenci przyjmujący podskórnie oktreotyd powinni kontynuować to leczenie w dawce uprzednio
skutecznej przez 2 tygodnie po pierwszym wstrzyknięciu produktu Okteva.
U pacjentów, u których po 3 miesiącach leczenia wystąpiło zadowalające złagodzenie objawów i
poprawa wskaźników biologicznych, można zmniejszyć dawkę produktu leczniczego Okteva do 10
mg co 4 tygodnie.
U pacjentów, u których po 3 miesiącach leczenia wystąpiło tylko częściowe złagodzenie objawów
można zwiększyć dawkę produktu Okteva do 30 mg co 4 tygodnie.
W dniach, gdy mimo leczenia produktem Okteva, objawy związane z guzami żołądka, jelit i
trzustki są nasilone, zaleca się podać dodatkowo, podskórnie oktreotyd w dawce stosowanej przed
wprowadzeniem produktu leczniczego Okteva. Może się to zdarzyć szczególnie podczas pierwszych 2
miesięcy leczenia, zanim zostanie osiągnięte terapeutyczne stężenie oktreotydu.
- Leczenie pacjentów z zaawansowanymi guzami neuroendokrynnymi wywodzącymi się ześrodkowej części prajelita lub o nieznanym ognisku pierwotnym, w przypadku którychwykluczono ognisko pierwotne nieznajdujące się w środkowej części prajelita
Zalecana dawka produktu leczniczego Okteva wynosi 30 mg, podawane co 4 tygodnie. Leczenie
produktem Okteva w celu zahamowania rozwoju guza należy kontynuować w sytuacji braku
progresji guza.
- Leczenie gruczolaków wydzielających TSH
Leczenie produktem Okteva należy rozpoczynać od dawki 20 mg podawanej co 4 tygodnie
kontynuować przez 3 miesiące przed ewentualnym dostosowaniem dawki. Następnie dawkę można
dostosować w zależności od wydzielania TSH i hormonu tarczycy.
Instrukcja przygotowania i podawania domięśniowego (iniekcja) produktu leczniczego Okteva
WYŁĄCZNIE DO GŁĘBOKIEGO WSTRZYKNIĘCIA W MIĘŚNIE POŚLADKA
Zestaw:
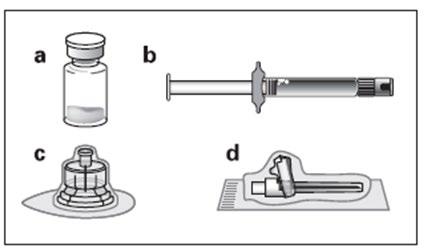
aJedna fiolka zawierająca produkt Okteva w postaci proszku
bJedna ampułko-strzykawka zawierająca rozpuszczalnik do sporządzenia zawiesiny
cJeden łącznik fiolki do odtworzenia produktu leczniczego
dJedna bezpieczna igła do wstrzyknięć
Należy postępować zgodnie z podaną poniżej instrukcją, aby właściwie odtworzyć produkt leczniczy
Okteva przed wykonaniem głębokiego wstrzyknięcia do mięśnia pośladka.
Dla prawidłowego odtworzenia produktu leczniczego Okteva krytyczne znaczenie mają 3 wymagania.
Niespełnienie tych wymagań może być przyczyną niewłaściwego podania leku.
- Zestaw do wstrzyknięć musi osiągnąć temperaturę pokojową.Należy wyjąć zestaw do wstrzyknięć z lodówki i przed odtworzeniem leku pozostawić go na minimum 30 minut w temperaturze pokojowej, jednak nie dłużej niż na 24 godziny.
- Po dodaniu rozpuszczalnika należy odstawić fiolkę na 5 minut, aby zapewnić pełnenasycenie proszku roztworem.
- Po nasyceniu należy wstrząsać fiolką z umiarkowaną siłąw płaszczyźnie poziomej przez minimum 30 sekund do utworzenia jednolitej zawiesiny.Zawiesina produktu leczniczego Okteva musi zostać przygotowana bezpośrednioprzed podaniem.
Produkt leczniczy Okteva może być podawany wyłącznie przez wyszkolony personel
medyczny.
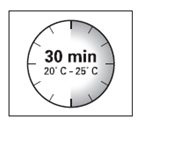
Krok 1
- Wyjąć zestaw do wstrzyknięć z produktem Okteva z lodówki, w której był przechowywany.
UWAGA: Bardzo istotne jest, by rozpocząć proces odtwarzania dopiero, gdy zestaw do wstrzyknięć osiągnie temperaturę pokojową.
Należy pozostawić zestaw w temperaturze pokojowej przez minimum 30 minut przed odtworzeniem, jednak nie na dłużej niż przez 24
godziny.
Uwaga: Zestaw do wstrzyknięć można w razie
potrzeby ponownie włożyć do lodówki.
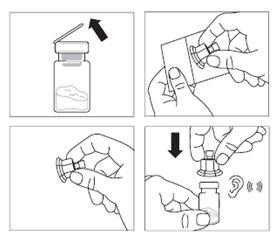
Krok 2
- Zdjąć z fiolki plastikowe wieczko i przetrzeć gumowy korek fiolki wacikiem nasączonym alkoholem.
- Oderwać folię pokrywającą opakowanie łącznika fiolki, wyjąć łącznik fiolki z opakowania, trzymając pomiędzy białym łącznikiem Luera a kołnierzem. NIE DOTYKAĆ końcówki łącznika w żadnym punkcie.
- Postawić fiolkę na płaskiej powierzchni. Umieścić łącznik fiolki na fiolce i docisnąć do końca tak, by wsunął się na miejsce z głośnym „kliknięciem”.
- Przetrzeć końcówkę łącznika fiolki wacikiem nasączonym alkoholem.
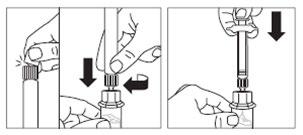
Krok 3
- Zdjąć osłonę końcówki z ampułko-strzykawki wypełnionej rozpuszczalnikiem i przykręcić strzykawkę do łącznika fiolki.
- Powoli wcisnąć tłok do samego końca, aby cały roztwór rozpuszczalnika znalazł się w fiolce.
Krok 4
UWAGA: Bardzo istotne jest, by odstawić fiolkę
na 5 minut,aby zapewnić całkowite nasycenie
proszku rozpuszczalnikiem.
Uwaga: Tłok może zostać odepchnięty z powrotem
do góry, co jest normalne, z powodu niewielkiego
nadciśnienia w fiolce. Na tym etapie należy
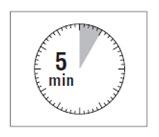
przygotować pacjenta do wykonania
wstrzyknięcia.
Krok 5
- Po czasie wystarczającym do nasycenia proszku, należy sprawdzić, czy tłok jest dociśnięty w dół do samego końca strzykawki.
UWAGA:Trzymając tłok dociśnięty do samego
końca umiarkowaniewstrząsać fiolką w
płaszczyźnie poziomej przezminimum30 sekund,
tak aby cały proszek utworzył zawiesinę
(jednorodna mleczna zawiesina). Jeśli część
proszku nie połączyła się z roztworem,
powtórzyć umiarkowane wstrząsanie przez
kolejne 30 sekund.
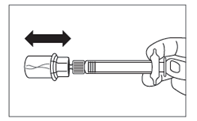
Krok 6
- Odwrócić strzykawkę z fiolką dnem do góry i powoli odciągając tłok pobrać całą zawartość fiolki do strzykawki.
- Odkręcić strzykawkę od łącznika fiolki.
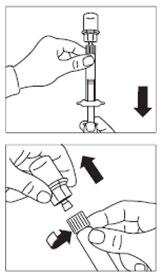
Krok 7
- Przygotować miejsce wstrzyknięcia przecierając je wacikiem nasączonym alkoholem.
- Przykręcić bezpieczną igłę do wstrzyknięć do strzykawki.
- Jeżeli natychmiastowe podanie nie jest możliwe, ponownie delikatnie wstrząsać strzykawką, aby uzyskać mleczną jednorodną zawiesinę tuż przed podaniem.
- Zdjąć nakładkę ochronną z igły prostym ruchem do góry.
- Delikatnie opukać palcami strzykawkę powodując przesunięcie widocznych pęcherzyków powietrza ku górze, a następnie usunąć je ze strzykawki. Przejść natychmiastdo punktu Krok 8. Każde opóźnienie może spowodować powstanie osadu.
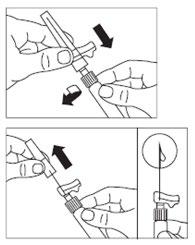
Krok 8
- Produkt leczniczy Okteva musi być podawany
wyłącznie w głębokim wstrzyknięciu do
mięśnia pośladka, NIGDY dożylnie.
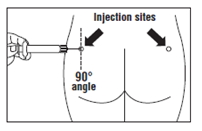
- Wprowadzić całą igłę w lewy lub prawy pośladek pod kątem 90 ° do powierzchni skóry.
- Powoli odciągnąć tłok ampułko-strzykawki, aby upewnić się, że igła nie znajduje się w naczyniu krwionośnym (zmienić położenie igły, jeśli znajduje się ona w naczyniu krwionośnym).
- Powoli, ze stałym naciskiem przesuwać tłok, aż do opróżnienia strzykawki. Wyjąć igłę z miejsca wkłucia i uruchomić nakładkę ochronną igły (zgodnie ze wskazówkami podanymi w punkcie Krok 9).
Krok 9
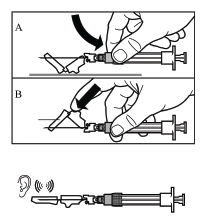
- Uruchomić nakładkę ochronną igły, stosując jedną z 2 następujących metod:
- docisnąć składaną część osłonki do twardej powierzchni (rysunek A)
- lub przycisnąć składaną część osłonki palcem (rysunek B).
- Prawidłowe uruchomienie zostanie potwierdzone głośnym kliknięciem.
- Uwaga: należy zapisać miejsce wstrzyknięcia na karcie pacjenta, zmieniając je co miesiąc.
- Strzykawkę natychmiast wyrzucić (do odpowiedniego pojemnika na ostre odpady).
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterMerckle GmbH Pharmathen International S.A. PLIVA Hrvatska d.o.o. (PLIVA Croatia Ltd.)
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki OktevaPostać farmaceutyczna: Proszek, 20 mgSubstancja czynna: octreotidePostać farmaceutyczna: Proszek, 30 mgSubstancja czynna: octreotidePostać farmaceutyczna: Proszek, 30 mgSubstancja czynna: octreotideWymaga recepty
Odpowiedniki Okteva w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Okteva – Hiszpania
Odpowiednik Okteva – Ukraina
Lekarze online w sprawie Okteva
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Okteva – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.






