
Jak stosować Lanreotide Zentiva
Ulotka dołączona do opakowania: informacja dla użytkownika
Lanreotide Zentiva, 60 mg, roztwór do wstrzykiwań w ampułko-strzykawce
Lanreotide Zentiva, 90 mg, roztwór do wstrzykiwań w ampułko-strzykawce
Lanreotide Zentiva, 120 mg, roztwór do wstrzykiwań w ampułko-strzykawce
Lanreotidum
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Lanreotide Zentiva i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Lanreotide Zentiva
- 3. Jak stosować lek Lanreotide Zentiva
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Lanreotide Zentiva
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Lanreotide Zentiva i w jakim celu się go stosuje
Co to jest lek Lanreotide Zentiva i jak działa
Ten lek nosi nazwę Lanreotide Zentiva.
Substancja czynna tego leku zapewnia długotrwałe działanie.
Lanreotyd - substancja czynna - należy do grupy leków zwanych hormonami hamującymi wzrost. Jest
on podobny do innej substancji (hormonu) o nazwie somatostatyna.
Lanreotyd powoduje w organizmie zmniejszenie aktywności hormonów takich jak hormon wzrostu
(GH) oraz insulinopodobnego czynnika wzrostu 1 (IGF-1), a także hamuje uwalnianie niektórych
hormonów przewodu pokarmowego oraz wydzielanie jelitowe. Ponadto, wywiera również wpływ na
niektóre zaawansowane rodzaje guzów (zwanych guzami neuroendokrynnymi) występujące w
obrębie jelit i trzustki, poprzez zahamowanie lub opóźnienie ich wzrostu
W jakim celu stosuje się lek Lanreotide Zentiva:
- w długotrwałym leczeniu chorych na akromegalię (stan, w którym organizm wytwarza zbyt wiele hormonu wzrostu)
- w łagodzeniu objawów związanych z akromegalią - takich jak zmęczenie, bóle głowy, pocenie się, ból stawów, uczucie drętwienia stóp i dłoni
- w łagodzeniu objawów takich jak uderzenia gorąca i biegunka, które czasami występują u pacjentów z guzami neuroendokrynnymi (guzy NET)
- w leczeniu i hamowaniu wzrostu niektórych zaawansowanych guzów występujących w obrębie jelit i trzustki, zwanych guzami neuroendokrynnymi żołądkowo-jelitowo-trzustkowymi (GEP- NET). Jest stosowany, gdy tych guzów nie można usunąć operacyjnie.
2. Informacje ważne przed zastosowaniem leku Lanreotide Zentiva
Kiedy nie stosować leku Lanreotide Zentiva
- jeśli pacjent ma uczulenie (nadwrażliwość) na lanreotyd, somatostatynę lub leki należące do tej samej grupy (analogi somatostatyny) lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Lanreotide Zentiva należy omówić to z lekarzem lub farmaceutą:
- jeśli pacjent choruje na cukrzycę, ponieważ lanreotyd powoduje wahania stężenia cukru we krwi. Podczas stosowania lanreotydu lekarz może zalecić sprawdzanie stężenia cukru we krwi oraz prawdopodobnie zmienić schemat leczenia cukrzycy.
- jeśli u pacjenta zdiagnozowano kamicę pęcherzyka żółciowego, ponieważ lanreotyd sprzyja tworzeniu kamieni w pęcherzyku żółciowym. W tym przypadku wskazane będzie okresowe badanie. Lekarz może zdecydować o przerwaniu leczenia lanreotydem, jeśli wystąpią powikłania wynikające z tworzenia się kamieni żółciowych.
- jeśli u pacjenta występują jakiekolwiek zaburzenia czynności tarczycy, ponieważ lanreotyd może nieznacznie zaburzać czynność tego narządu.
- jeśli u pacjenta występują zaburzenia czynności serca, ponieważ podczas stosowania lanreotydu może wystąpić bradykardia zatokowa (wolne bicie serca). W przypadku pacjentów z bradykardią, lanreotyd należy stosować szczególnie ostrożnie.
Jeśli którykolwiek z powyższych punktów dotyczy pacjenta, przed przyjęciem leku Lanreotide
Zentiva należy omówić to z lekarzem lub farmaceutą.
Należy skonsultować się z lekarzem lub farmaceutą jeśli podczas leczenia:
- U pacjenta występują stolce tłuszczowe, luźne stolce, wzdęcia brzucha lub utrata masyciała, ponieważ lanreotyd może wpływać na wydzielanie enzymów trzustkowych biorących udział w trawieniu pokarmu.
Dzieci i młodzież
Lek Lanreotide Zentiva nie jest zalecany dla dzieci i młodzieży.
Lek Lanreotide Zentiva a inne leki
Niektóre leki mają wpływ na działanie innych leków. Należy powiedzieć lekarzowi lub farmaceucie o
wszystkich lekach przyjmowanych przez pacjenta obecnie lub ostatnio, a także o lekach, które pacjent
planuje przyjmować.
Należy zachować szczególne środki ostrożności w przypadku równoczesnego stosowania z:
- cyklosporyną(lekiem obniżającym odpowiedź układu odpornościowego, stosowanym po transplantacji lub w przypadku choroby autoimmunologicznej),
- bromokryptyną(agonistą receptorów dopaminowych, stosowaną w leczeniu niektórych rodzajów guzów mózgu oraz choroby Parkinsona lub w celu zahamowania laktacji występującej po porodzie),
- lekami przeciwcukrzycowymi(lekami obniżającymi duże stężenie glukozy we krwi),
- lekami wywołującymi bradykardię(leki zwalniające akcję serca, np. beta-blokery).
Lekarz może rozważyć modyfikację dawkowania powyższych leków stosowanych jednocześnie.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku. Lek Lanreotide
Zentiva powinien być podawany tylko w przypadku wyraźnej konieczności.
Prowadzenie pojazdów i obsługiwanie maszyn
Jest mało prawdopodobne, aby lek Lanreotide Zentiva wpływał na zdolność prowadzenia pojazdów
lub obsługiwanie maszyn, jednak podczas stosowania leku Lanreotide Zentiva mogą wystąpić
działania niepożądane, takie jak zawroty głowy. Jeżeli takie działanie niepożądane wystąpi u pacjenta,
nie powinien on prowadzić pojazdów ani obsługiwać maszyn.
3. Jak stosować lek Lanreotide Zentiva
Lek Lanreotide Zentiva należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości
należy zwrócić się do lekarza lub farmaceuty.
Zalecana dawka
Leczenie akromegalii
Zalecana dawka to jedno wstrzyknięcie co 28 dni. Dawka leku użyta do wstrzyknięcia zostanie
dobrana przez lekarza spośród trzech dostępnych mocy leku Lanreotide Zentiva (60 mg, 90 mg lub
120 mg).
W przypadku uzyskania pożądanej odpowiedzi, lekarz może zalecić zmianę częstości podawania
wstrzyknięć leku Lanreotide Zentiva 120 mg na jedno wstrzyknięcie co 42 lub 56 dni.
Lekarz zadecyduje również o czasie trwania leczenia.
Łagodzenie objawów (takich jak uderzenia gorąca i biegunka) związanych z guzami
neuroendokrynnymi
Zalecana dawka to jedno wstrzyknięcie leku co 28 dni. Dawka leku użyta do wstrzyknięcia zostanie
dobrana przez lekarza spośród trzech dostępnych mocy leku Lanreotide Zentiva (60 mg, 90 mg lub
120 mg).
W przypadku uzyskania pożądanej odpowiedzi na leczenie analogiem somatostatyny lub lekiem
Lanreotide Zentiva 60 mg lub 90 mg, lekarz może zalecić zmianę częstości podawania wstrzyknięć
leku Lanreotide Zentiva 120 mg na jedno wstrzyknięcie co 42 lub 56 dni.
Lekarz zadecyduje również o czasie trwania leczenia.
Leczenie zaawansowanych guzów występujących w obrębie jelit i trzustki zwanych guzami
neuroendokrynnymi żołądkowo-jelitowo-trzustkowymi (GEP-NET). Lek stosuje się wówczas, gdy
guzów tych nie można usunąć operacyjnie.
Zalecana dawka to 120 mg co 28 dni. Lekarz zadecyduje o czasie trwania leczenia lekiem Lanreotide
Zentiva w celu hamowania wzrostu guza.
Sposób podawania
Lek Lanreotide Zentiva należy podawać w postaci głębokiego wstrzyknięcia podskórnego.
Wstrzyknięcie powinno być wykonane przez pracownika służby zdrowia lub osobę przeszkoloną
(członek rodziny lub przyjaciel) albo samodzielnie przez pacjenta po odpowiednim przeszkoleniu
przez pracownika służby zdrowia.
Decyzję dotyczącą samodzielnego podawania lub podawania przez inną przeszkoloną osobę
powinien podjąć lekarz. Jeśli pacjent ma jakiekolwiek wątpliwości co do sposobu wstrzyknięcia leku,
powinien poradzić się lekarza lub pracownika służby zdrowia w celu uzyskania porady lub dalszego
szkolenia.
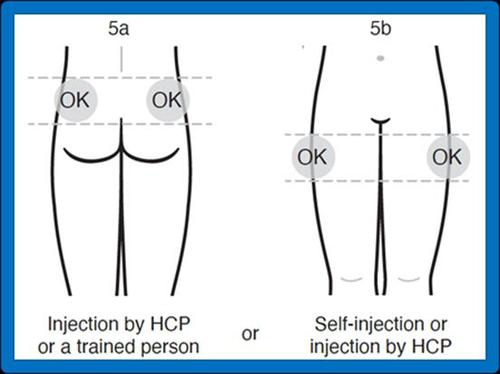
W przypadku wykonywania wstrzyknięcia przez pracownika służby zdrowia lub osobę przeszkoloną
(członek rodziny lub przyjaciel), zastrzyk powinien być podawany w górny, zewnętrzny kwadrant
pośladka lub w górną, zewnętrzną część uda (patrz rys. 5a i 5b poniżej).
W przypadku samodzielnego wykonywania zastrzyku po odpowiednim przeszkoleniu, zastrzyk
należy podawać w górną, zewnętrzną część uda (patrz rys. 5b poniżej).
Instrukcja stosowania
Uwaga: Należy dokładnie zapoznać się z całą treścią instrukcji przed wykonaniem wstrzyknięcia. Głęboko podskórne wstrzyknięcie wymaga specjalnej techniki, różniącej się od tej stosowanej w przypadku standardowego wstrzyknięcia podskórnego.
Poniższa instrukcja wyjaśnia jak wykonać wstrzyknięcie leku Lanreotide Zentiva.
Lek Lanreotide Zentiva jest dostarczany w postaci gotowej do użycia ampułko-strzykawki,
wyposażonej w automatyczny system zabezpieczający. Igła wycofa się automatycznie
po dokonaniu pełnego wstrzyknięcia zawartości, aby zapobiec skaleczeniu pacjenta.
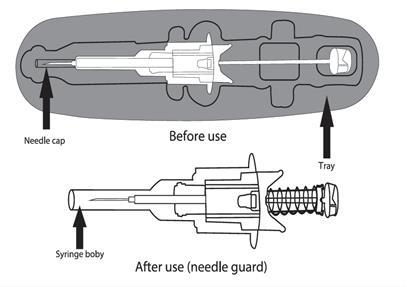
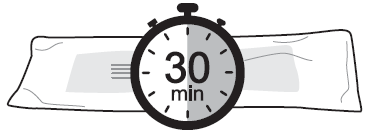
- 1. Wyjąć lek Lanreotide
Zentiva z lodówki na 30 minut przed podaniem.
Wstrzyknięcie zimnej
zawartości może być
bolesne. Przechowywać
laminowaną torebkę
szczelnie zamkniętą aż do
momentu tuż przed
wstrzyknięciem.
- 2. Uwaga: Przed otwarciem torebkinależy sprawdzić czy jest ona nienaruszona oraz czy nieminęła data ważności leku.
Nie należy używać ampułko-strzykawki:
- Jeśli uległa uszkodzeniu lub jeśli ampułko-strzykawka albo jej opakowanie wydają się w jakikolwiek sposób uszkodzone.
- Jeśli upłynęła data ważności leku; data ważności jest wydrukowana na torebce oraz pudełku.
Jeśli występuje którakolwiek z powyższych sytuacji, należy skontaktować się z lekarzem lub
farmaceutą.
- 3. Umyj ręce mydłem.
- 4. Otworzyć torebkę wzdłuż przerywanej linii i wyjąć ampułko- strzykawkę. Zawartość ampułko-strzykawki to półstała substancja przypominająca wyglądem lepki żel o barwie białej do jasnożółtej. Przesycony roztwór może również zawierać mikropęcherzyki, które mogą zniknąć podczas wstrzyknięcia. Różnice te są normalne i nie wpływają na jakość produktu.
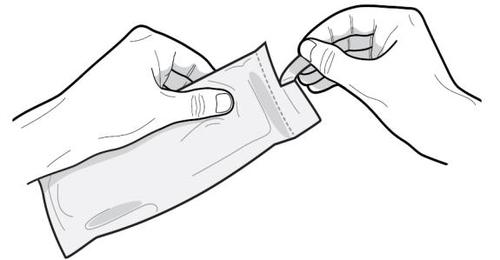
Po otwarciu laminowanej torebki ochronnej lek należy natychmiast
podać.
- 5. Wybrać miejsce wstrzyknięcia:
Jeśli wstrzyknięcie
wykonuje pracownik
służby zdrowia lub inny
przeszkolony członek
rodziny lub przyjaciel:
górny zewnętrzny
kwadrant pośladka (5a) lub
górna zewnętrzna część
uda (5b).
Jeśli pacjent dokonuje
samodzielnego
wstrzyknięcia: górna
zewnętrzna część uda (5b).
- Miejsce wstrzyknięcialeku Lanreotide Zentiva należy zmieniaćprzy każdym podaniu, wstrzykując raz z jednej, raz z drugiej strony. Unikać miejsc, gdzie znajdują się pieprzyki, blizny, zaczerwienienia lub nierówności skóry.
- 6. Oczyścić miejsce wstrzyknięcia.
- 7. Przed wstrzyknięciem należy zdjąć ampułko- strzykawkę z tacki. Wyrzucić tackę.
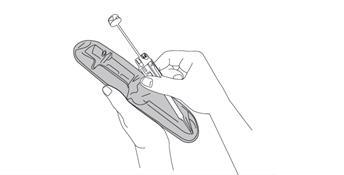
- 8. Pociągając, zdjąć ochraniacz igły i wyrzucić go.
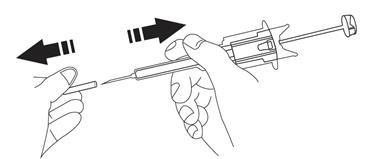
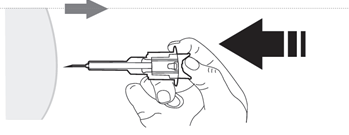
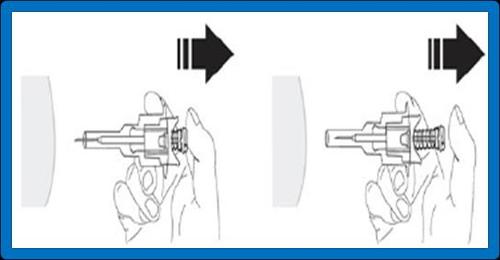
- 9. Spłaszczyćskórę w miejscu wstrzyknięcia przy użyciu kciuka i palca wskazującego dłoni, w której nie jest trzymana ampułko-strzykawka, aby ją naciągnąć. Nie należytworzyć fałduskóry. Zdecydowanym, płynnym ruchem należy szybkowbićcałą igłę prostopadledo powierzchni skóry (kąt 90º). Ważne jest, aby igła wcałościznalazła się w ciele. Po wbiciu igły nie powinien być widoczny żaden jej fragment.
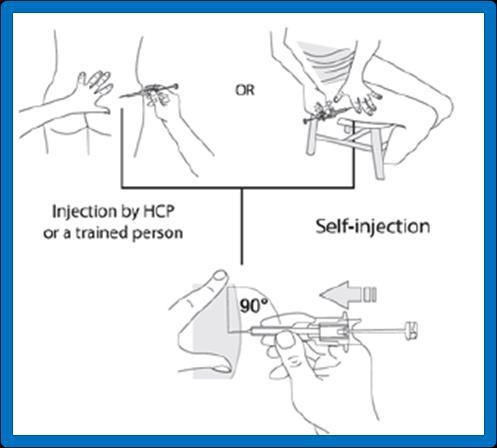
Nienależy wyciągaćigły.
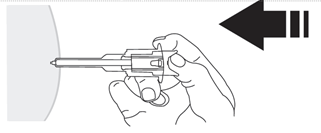
- 10. Puścić miejsce wstrzyknięcia, które zostało spłaszczone przez twoją dłoń. Nacisnąć tłok jednostajnym, zdecydowanym ruchem. Lek jest gęstszy i trudniejszy do podania niż można by się spodziewać. Zazwyczaj wstrzyknięcie zawartości trwa 20 sekund. Należywstrzyknąć pełną dawkę i dopchnąć tłok tak,aby upewnić się, że w opakowaniu nie pozostała żadna ilość leku.

UWAGA: Nie zwalniać nacisku na tłok, aby zapobiec aktywacji automatycznego systemu zabezpieczającego.
|  |
| |
 | |
| |
Zastosowanie większej niż zalecana dawki leku Lanreotide Zentiva
Jeżeli doszło do wstrzyknięcia większej dawki leku Lanreotide Zentiva niż jest to zalecane, należy
powiadomić lekarza.
Jeżeli doszło do wstrzyknięcia większej dawki leku Lanreotide Zentiva niż zalecana, istnieje ryzyko
wystąpienia dodatkowych lub bardziej nasilonych działań niepożądanych (patrz punkt 4. Możliwe
działania niepożądane).
Pominięcie zastosowania leku Lanreotide Zentiva
Gdy tylko pacjent uświadomi sobie, że pominął wstrzyknięcie, należy skontaktować się ze swoim
lekarzem, który udzieli informacji na temat terminu kolejnego podania leku.
Nie należy samodzielnie wykonywać dodatkowych wstrzyknięć w celu uzupełnienia pominiętej
dawki bez omówienia tego z lekarzem.
Przerwanie stosowania leku Lanreotide Zentiva
Pominięcie więcej niż jednej dawki lub wcześniejsze zakończenie stosowania leku Lanreotide Zentiva
może wpłynąć na skuteczność terapii. Należy porozumieć się z lekarzem przed zaprzestaniem
przyjmowania leku.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić
się do lekarza lub farmaceuty.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Jeśli u pacjenta wystąpi którekolwiek z poniższych działań niepożądanych, należy natychmiast skontaktować się z lekarzem:
- uczucie większego niż zazwyczaj pragnienia lub zmęczenie oraz suchość w ustach - może to oznaczać, że u pacjenta występuje duże stężenie cukru we krwi lub rozwija się cukrzyca.
- uczucie głodu, drżenie, nasilone pocenie się lub splątanie - mogą to być objawy małego stężenia cukru we krwi.
Powyższe działania niepożądane obserwuje się często, mogą one wystąpić u 1 na 10 osób.
Należy natychmiast skontaktować się z lekarzem, jeśli pacjent zauważy:
- zaczerwienienie lub obrzęk twarzy, wypryski lub wysypkę
- ucisk w klatce piersiowej, duszność lub świszczący oddech
- zasłabnięcie, które może wynikać ze spadku ciśnienia krwi.
Mogą to być objawy reakcji alergicznej.
Częstość występowania tego działania niepożądanego nie jest znana; nie można jej oszacować na
podstawie dostępnych danych.
Inne działania niepożądane
Jeśli u pacjenta wystąpi którekolwiek z poniższych działań niepożądanych, należy natychmiast
skontaktować się z lekarzem lub farmaceutą.
Do najczęściej spodziewanych działań niepożądanych występujących podczas stosowania leku
Lanreotide Zentiva należą zaburzenia przewodu pokarmowego, zaburzenia czynności pęcherzyka
żółciowego oraz reakcje w miejscu podania. Poniżej przedstawiono działania niepożądane związane
ze stosowaniem leku Lanreotide Zentiva z uwzględnieniem częstości ich występowania.
Bardzo często (mogą wystąpić u więcej niż 1 na 10 osób):
- biegunka, luźne stolce, ból brzucha
- kamica żółciowa oraz inne dolegliwości związane z pęcherzykiem żółciowym. Może wystąpić silny i nagły ból brzucha, wysoka gorączka, żółtaczka (zażółcenie skóry i białek oczu), dreszcze, utrata apetytu, swędzenie skóry.
Często (mogą wystąpić nie więcej niż u 1 na 10 osób):
- spadek masy ciała
- brak energii
- wolne bicie serca
- uczucie silnego zmęczenia
- zmniejszenie apetytu
- ogólne osłabienie
- nadmiar tłuszczu w stolcu
- zawroty głowy, ból głowy
- wypadanie włosów lub słabsze owłosienie ciała
- ból mięśni, więzadeł, ścięgien i kości
- reakcje w miejscu podania zastrzyku takie jak ból, stwardnienie skóry lub świąd
- nieprawidłowe wyniki badań czynności wątroby i trzustki oraz zmiany stężenia cukru we krwi
- nudności, wymioty, zaparcia, gazy, wzdęcia lub dyskomfort w jamie brzusznej, niestrawność
- poszerzenie przewodów żółciowych (powiększenie przewodów żółciowych między wątrobą a pęcherzykiem żółciowym i jelitem). Może wystąpić ból brzucha, nudności, żółtaczka i gorączka.
Niezbyt często (mogą wystąpić nie więcej niż u 1 na 100 osób):
- uderzenia gorąca
- trudności w zasypianiu
- zmiana zabarwienia stolca
- zmiany zawartości sodu i fosfatazy alkalicznej wykazane w badaniach krwi.
Częstość nieznana: częstość nie może zostać oszacowana na podstawie dostępnych danych
- nagły, silny ból w podbrzuszu - może to być objaw zapalenia trzustki
- występujące w miejscu wstrzyknięcia zaczerwienienie, ból, ciepło, obrzęk, który po naciśnięciu może sprawiać wrażenie wypełnionego płynem, gorączka - mogą to być objawy ropnia
- nagły, silny ból w prawej górnej lub środkowej części brzucha, promieniujący do ramienia lub pleców, nadwrażliwość brzucha, nudności, wymioty i wysoka gorączka - mogą to być objawy zapalenia pęcherzyka żółciowego
- ból w prawej górnej części brzucha, gorączka, dreszcze, zażółcenie skóry i oczu (żółtaczka), nudności, wymioty, stolce w kolorze gliny, ciemny mocz, zmęczenie - mogą to być objawy zapalenia dróg żółciowych
- zmniejszenie aktywności enzymów trzustkowych. Ponieważ lanreotyd może wpływać na uwalnianie enzymów trzustkowych biorących udział w trawieniu pokarmu, u pacjenta mogą wystąpić objawy takie jak stolce tłuszczowe, luźne stolce, wzdęcia brzucha lub utrata masy ciała.
Ponieważ lek Lanreotide Zentiva może powodować wahania stężenia cukru we krwi, lekarz może
zalecić systematyczne badanie stężenia cukru, szczególnie na początku leczenia.
Podobnie, z uwagi na możliwość występowania zaburzeń pęcherzyka żółciowego podczas stosowania
tego typu leków, lekarz może zalecić systematyczne badanie pęcherzyka żółciowego na początku
leczenia Lanreotide Zentiva, a następnie w określonych odstępach czasu.
Jeśli wystąpi którekolwiek z powyższych działań niepożądanych, należy powiedzieć o tym lekarzowi
lub farmaceucie.
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane
niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Działania
niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań
Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i
Produktów Biobójczych,
Al. Jerozolimskie 181C,
02-222 Warszawa,
tel.: + 48 22 49 21 301,
faks: + 48 22 49 21 309,
strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można również zgłaszać podmiotowi odpowiedzialnemu lub
przedstawicielowi podmiotu odpowiedzialnego w Polsce.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać Lanreotide Zentiva
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku i etykiecie po
„EXP”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Lek Lanreotide Zentiva należy przechowywać w lodówce w temperaturze 2˚C - 8˚C w oryginalnym
opakowaniu w celu ochrony przed światłem.
Po wyjęciu z lodówki produkt pozostawiony w szczelnie zamkniętej torebce może być ponownie
umieszczony w lodówce (liczba zmian temperatury nie może przekroczyć trzech razy) w celu
dalszego przechowywania i późniejszego użycia, pod warunkiem, że był przechowywany nie dłużej
niż łącznie 72 godziny w temperaturze poniżej 30°C.
Każda strzykawka jest pakowana osobno.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Lanreotide Zentiva
Substancją czynną jest:
lanreotyd 60 mg, 90 mg lub 120 mg
Pozostałe składniki to:
woda do wstrzykiwań
kwas octowy lodowaty (do ustalenia pH)
Jak wygląda lek Lanreotide Zentiva i co zawiera opakowanie
Lek Lanreotide Zentiva to lepki roztwór do wstrzykiwań w ampułko-strzykawce gotowej do użycia,
zaopatrzonej w automatyczny system zabezpieczający. Lek ma postać półstałą o barwie białej do
jasnożółtej.
Każda ampułko-strzykawka jest zapakowana w laminowaną torebkę i tekturowe pudełko.
Wielkości opakowań:
Pudełko z 0,5 mL ampułko-strzykawką z automatycznym systemem zabezpieczającym i jedną igłą
(1,2 mm x 20 mm).
Pudełko z trzema torebkami, każda zawierająca jedną 0,5 mL ampułko-strzykawkę oraz jedną igłę
(1,2 mm x 20 mm).
1 ampułko-strzykawka po 0,5 mL (60 mg), 3 ampułko-strzykawki po 0,5 mL (60 mg)
1 ampułko-strzykawka po 0,5 mL (90 mg), 3 ampułko-strzykawki po 0,5 mL (90 mg)
1 ampułko-strzykawka po 0,5 mL (120 mg), 3 ampułko-strzykawki po 0,5 mL (120 mg)
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny:
Zentiva, k.s.
U kabelovny 130
Dolní Měcholupy
102 37 Praga 10
Republika Czeska
Importer:
Terapia S.A.
124 Fabricii Street
400632 Cluj-Napoca
Rumunia
Sun Pharmaceutical Industries Europe B.V.
Polarisavenue 87
2132 JH Hoofddorp
Holandia
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego pod następującymi nazwami:
Republika Czeska, Dania, Finlandia, Norwegia, Szwecja: Lanreotid Zentiva
Polska, Włochy: Lanreotide Zentiva
Niemcy: Lanreotid Zentiva 60 mg, 90 mg, 120 mg Injektionslösung in einer Fertigspritze
Estonia: Lanreotida Zentiva 60 mg, 90 mg, 120 mg solución inyectable en jeringa precargada EFG
Francja: LANREOTIDE ZENTIVA LP 60 mg, 90 mg, 120 mg solution injectable à libération
prolongée en seringue préremplie
Rumunia: Lanreotidă Zentiva 120 mg soluţie injectabilă în seringă preumplută
Słowacja: Lanreotid Zentiva 60 mg, 120 mg injekčný roztok v naplnenej injekčnej striekačke
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do miejscowego przedstawiciela podmiotu odpowiedzialnego:
Zentiva Polska Sp. z.o.o.
ul. Bonifraterska 17
00-203 Warszawa, Polska
tel.: +48 22 375 92 00
Data ostatniej aktualizacji ulotki:
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- ImporterSun Pharmaceutical Industries Europe B.V. Terapia S.A.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Lanreotide ZentivaPostać farmaceutyczna: Roztwór, 90 mgSubstancja czynna: lanreotideWymaga receptyPostać farmaceutyczna: Roztwór, 120 mgSubstancja czynna: lanreotideWymaga receptyPostać farmaceutyczna: Roztwór, 60 mgSubstancja czynna: lanreotideWymaga recepty
Odpowiedniki Lanreotide Zentiva w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Lanreotide Zentiva – Hiszpania
Lekarze online w sprawie Lanreotide Zentiva
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Lanreotide Zentiva – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.






