
Furosemid Laboratórios Basi
Zapytaj lekarza o receptę na Furosemid Laboratórios Basi

Jak stosować Furosemid Laboratórios Basi
Ulotka dołączona do opakowania: Informacja dla użytkownika
Furosemid Laboratórios Basi, 10 mg/mL, roztwór do wstrzykiwań/do infuzji
Furosemidum
Należy uważnie zapoznać się z treścią ulotki przed podaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest Furosemid Laboratórios Basi i w jakim celu się go stosuje
- 2. Informacje ważne przed otrzymaniem leku Furosemid Laboratórios Basi
- 3. Jak podaje Furosemid Laboratórios Basi
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Furosemid Laboratórios Basi
- 6. Zawartość opakowania i inne informacje
1. Co to jest Furosemid Laboratórios Basi i w jakim celu się go stosuje
Furosemid Laboratórios Basi 10 mg//mL roztwór do wstrzykiwań/do infuzji zawiera substancję
czynną furosemid. Furosemid należy do grupy leków zwanych lekami moczopędnymi.
Furosemid Laboratórios Basi jest stosowany w:
- 1. Leczeniu obrzęków (obrzęk spowodowany nadmiarem płynów w organizmie), występujących u pacjentów z:
- chorobą wątroby
- chorobą serca (np. obrzęk płuc)
- chorobą nerek
- 2. Leczeniu skrajnie wysokiego ciśnienia krwi (przełom nadciśnieniowy).
Furosemid Laboratórios Basi jest wskazany do stosowania u dorosłych i młodzieży w wieku 15 lat i
starszych. Lek można stosować u niemowląt i dzieci w wieku poniżej 15 lat tylko wyjątkowo.
Jak działa Furosemid Laboratórios Basi roztwór do wstrzykiwań/do infuzji
- Roztwór Furosemid Laboratórios Basi do wstrzykiwań/do infuzji pomaga usunąć więcej wody (moczu) niż zwykle. Jeśli nadmiar wody w organizmie nie zostanie usunięty, może to spowodować nadmierne obciążenie serca, naczyń krwionośnych, płuc, nerek lub wątroby.
2. Informacje ważne przed otrzymaniem leku Furosemid Laboratórios Basi
Nie należy podawać leku Furosemid Laboratórios Basi
- jeśli pacjent ma uczulenie na furosemid lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
- jeśli pacjent ma uczulenie na antybiotyki z grupy sulfonamidów, takie jak sulfadiazyna i kotrimoksazol;
- jeśli pacjent ma problemy z nerkami. W niektórych rodzajach niewydolności nerek nadal można otrzymać ten lek. Lekarz będzie w stanie określić, czy pacjent może otrzymać ten lek;
- jeśli pacjent nie produkuje moczu;
- jeśli u pacjenta występuje ciężka choroba wątroby;
- jeśli u pacjenta występuje bardzo małe stężenie potasu lub sodu we krwi (potwierdzone badaniami krwi);
- jeśli u pacjenta występuje zmniejszenie objętości krwi (hipowolemia) lub odwodnienie;
- jeśli pacjentka karmi piersią (patrz punkt „Ciąża i karmienie piersią”).
Ostrzeżenia i środki ostrożności
Przed otrzymaniem leku Furosemid Laboratórios Basi należy omówić to z lekarzem lub pielęgniarką
w przypadku:
- niskiego ciśnienia krwi;
- cukrzycy;
- dny moczanowej (ból związany ze stanem zapalnym stawów) spowodowanej wysokim stężeniem kwasu moczowego we krwi;
- niedrożności dróg moczowych (np. powiększony gruczoł krokowy, obrzęk nerki spowodowany nagromadzeniem moczu, zwężenie moczowodu);
- bardzo małego stężenia białka we krwi, np. w zespole nerczycowym;
- choroby wątroby;
- szybko postępującego zaburzenia czynności nerek związanego z ciężką chorobą wątroby (np. marskością wątroby);
- ryzyka niepożądanego ciężkiego nadciśnienia tętniczego (np. jeśli u pacjenta występują zaburzenia krążenia w naczyniach mózgowych lub tętnicach wieńcowych);
- choroby zapalnej zwanej „toczniem rumieniowatym układowym (SLE)”;
- pacjentów w podeszłym wieku, którzy jednocześnie przyjmują inne leki, które mogą powodować niskie ciśnienie krwi, lub jeśli występują inne schorzenia związane z ryzykiem niskiego ciśnienia krwi.
Szczególnie podczas długotrwałego leczenia lekarz może regularnie kontrolować stężenie potasu,
sodu, wapnia, wodorowęglanów, kreatyniny, mocznika, kwasu moczowego i glukozy we krwi.
Utrata masy ciała spowodowana utratą płynów ustrojowych nie powinna być większa niż 1 kg masy
ciała na dobę.
Dzieci
W przypadku podania wcześniakom furosemid może powodować kamienie moczowe lub zwapnienia.
U wcześniaków kanał między tętnicą płucną a aortą, który jest otwarty u nienarodzonego dziecka,
może pozostać otwarty.
Lek Furosemid Laboratórios Basi a inne leki
Należy powiedzieć lekarzowi o wszystkich lekach obecnie przez pacjenta obecnie lub ostatnio, a także
o lekach, które pacjent planuje przyjmować.
Jest to ważne, ponieważ niektórych leków nie należy przyjmować razem z furosemidem lub może być
konieczne dostosowanie dawki furosemidu lub innego jednocześnie przyjmowanego leku.
W szczególności należy powiedzieć lekarzowi lub pielęgniarce o stosowaniu:
- litu (stosowany w leczeniu zaburzeń nastroju);
- leków nasercowych (np. digoksyny);
- terfenadyny (stosowana w leczeniu alergii);
- lewotyroksyny (stosowana w leczeniu niedoczynności tarczycy);
- leków stosowanych w nadciśnieniu tętniczym, w tym tiazydowe leki moczopędne (np. bendroflumetiazyd lub hydrochlorotiazyd), inhibitory konwertazy angiotensyny (np. lizynopryl), antagoniści angiotensyny II (np. losartan);
- leków stosowanych w cukrzycy (np. metformina i insulina);
- leków przeciwzapalnych, w tym NLPZ (stosowane w leczeniu bólu i stanów zapalnych, takie jak diklofenak, ibuprofen, indometacyna, celekoksyb) oraz kwas acetylosalicylowy w dużych dawkach (aspiryna);
- kortykosteroidów (leki stosowane w leczeniu stanów zapalnych lub alergii, np. prednizolon, deksametazon);
- karbenoksolonu (stosowany w leczeniu wrzodów żołądka);
- środków przeczyszczających;
- chloralu wodzianu (stosowany w leczeniu problemów ze snem);
- fenytoiny (stosowana w leczeniu padaczki);
- teofiliny (stosowana w leczeniu astmy);
- probenecydu (stosowany w leczeniu dny moczanowej);
- metotreksatu (stosowany w leczeniu niektórych nowotworów lub ciężkiego zapalenia stawów);
- cyklosporyny (zapobiegająca odrzucaniu przeszczepów);
- leków podwyższających ciśnienie krwi (aminy presyjne, takie jak adrenalina, noradrenalina), ponieważ mogą one nie działać właściwie, gdy są przyjmowane z furosemidem;
- antybiotyków (takich jak cefalosporyny, aminoglikozydy, polimyksyny, chinolony). Wpływ antybiotyków aminoglikozydowych (np. kanamycyny, gentamycyny i tobramycyny) na słuch może być nasilony przez furosemid, zwłaszcza u pacjentów z problemami dotyczącymi nerek;
- foskarnetu (stosowany w leczeniu chorób wywołanych przez organizmy jednokomórkowe znane jako pierwotniaki);
- jodowanych środków kontrastowych;
- cisplatyny (stosowana w chemioterapii przeciwnowotworowej);
- rysperydonu (stosowany w leczeniu zaburzeń psychicznych).
Furosemid Laboratórios Basi z jedzeniem
Duże ilości lukrecji w skojarzeniu z furosemidem mogą prowadzić do zwiększonej utraty potasu.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed podaniem tego leku.
Furosemidu nie należy stosować w czasie ciąży, chyba że istnieją ku temu wyraźne medyczne
przesłanki, ponieważ furosemid przenika przez barierę łożyskową. Podawanie furosemidu w czasie
ciąży może prowadzić do zwiększenia stężenia bilirubiny u płodu, a w konsekwencji żółtaczki i
uszkodzenia mózgu u dziecka. Ten lek może również prowadzić do zwiększenia produkcji moczu u
płodu.
Furosemid przenika do mleka kobiecego. Nie należy karmić piersią podczas leczenia furosemidem.
Prowadzenie pojazdów i obsługiwanie maszyn
Ten lek może zmieniać zdolność reagowania w takim stopniu, że zdolność prowadzenia pojazdów,
obsługiwania maszyn lub wykonywania niebezpiecznych zadań może być zaburzona. Dotyczy to
zwłaszcza początku leczenia, zwiększania dawki lub zmiany leków oraz w przypadku spożywania
alkoholu.
Furosemid Laboratórios Basi zawiera sód
Lek zawiera mniej niż 1 mmol (23 mg) sodu na ampułkę, to znaczy lek uznaje się za „wolny od sodu”.
3. Jak podaje się Furosemid Laboratórios Basi
Lekarz zdecyduje, ile leku pacjent potrzebuje, kiedy ma być podany i jak długo trwa leczenie. Będzie
to zależeć od wieku, masy ciała, historii choroby, innych stosowanych leków oraz charakteru i
nasilenia choroby. Zawsze stosowana będzie najniższa dawka, przy której uzyskane zostanie pożądane
działanie.
Wstrzyknięcie furosemidu jest zwykle podawane przez lekarza lub pielęgniarkę:
- jako powolne wstrzyknięcie do żyły lub
- wyjątkowo w mięsień.
W niektórych przypadkach zamiast wstrzyknięć lekarz może zalecić podawanie tego leku w ciągłym
wlewie dożylnym (kroplówce).
Gdy tylko pozwoli na to stan pacjenta, włączone zostanie podawanie doustne.
Dorośli
W leczeniu zatrzymania płynów w tkankach (obrzęk) i (lub) gromadzenia się płynu w jamie
brzusznej (wodobrzusze) z powodu choroby serca lub wątroby, obrzęku spowodowanego
chorobą nerek obrzękiem płuc, dawka początkowa wynosi od 20 mg do 40 mg furosemidu.
Następnie dawka ta będzie stopniowo zwiększana do maksymalnej dawki 1500 mg na dobę.
W leczeniu skrajnie wysokiego ciśnienia krwipojedyncza dawka wynosi od 20 mg do 40 mg
furosemidu.
U osób dorosłych maksymalna dawka dobowa furosemidu nie powinna być większa niż 1 500 mg.
Osoby w podeszłym wieku
Zazwyczaj stosowana dawka początkowa u osób w podeszłym wieku wynosi 20 mg na dobę.
Dorośli z zaburzeniami czynności nerek
U pacjentów z ciężkimi zaburzeniami czynności nerek (stężenie kreatyniny w surowicy >5 mg/dl)
zaleca się nie przekraczać szybkości infuzji 2,5 mg furosemidu na minutę.
Stosowanie u dzieci
Średnia dawka zwykle stosowana u dzieci wynosi 0,5 mg furosemidu/kg masy ciała na dobę.
Wyjątkowo można podać do 1 mg furosemidu/kg masy ciała na dobę.
Otrzymanie większej niż zalecana dawki Furosemidu
Jeśli pacjent uważa, że otrzymał zbyt dużą dawkę tego leku, powinien natychmiast powiedzieć o tym
lekarzowi. Objawy ostrego lub przewlekłego przedawkowania zależą od stopnia utraty soli i płynów.
Objawy przedawkowania to suchość w jamie ustnej, zwiększone pragnienie, nieregularne bicie serca,
zmiany nastroju, kurcze lub ból mięśni, nudności lub wymioty, niezwykłe zmęczenie lub osłabienie,
słaby puls lub utrata apetytu.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się
do lekarza lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
U pacjentów leczonych furosemidem może wystąpić niskie ciśnienie krwi z zawrotami głowy,
omdleniami lub utratą przytomności.
W przypadku zauważenia następujących działań niepożądanych należy natychmiastskontaktować się
z lekarzem lub pielęgniarką:
- Ciężka reakcja alergiczna, która może powodować wysypkę skórną, obrzęk twarzy, warg, języka lub gardła, trudności w oddychaniu i utratę przytomności (reakcja anafilaktyczna lub anafilaktoidalna) (może wystąpić u mniej niż 1 na 1 000 osób);
- Zespół Stevensa-Johnsona, martwica toksyczna rozpływna naskórka; ich objawy to początkowo czerwonawe, przypominające tarcze plamy lub okrągłe plamy, często z centralnymi pęcherzami na tułowiu. Mogą również wystąpić owrzodzenia jamy ustnej, gardła, nosa, narządów płciowych i oczu (czerwone i opuchnięte oczy). Te ciężkie wykwity skórne mogą być poprzedzone gorączką i objawami grypopodobnymi. Wysypki mogą prowadzić do rozległego złuszczania się skóry i zagrażających życiu powikłań lub prowadzić do zgonu (nieznana).
- Rabdomioliza: rzadka choroba charakteryzująca się bólem, tkliwością i osłabieniem mięśni; takiemu uszkodzeniu mięśni często towarzyszy ciężki niedobór potasu (nieznana).
Inne działania niepożądane
Bardzo często(mogą wystąpić u więcej niż 1 na 10 osób)
- Zaburzenia elektrolitowe (w tym objawowe), odwodnienie i zmniejszona objętość krwi krążącej, zwłaszcza u osób w podeszłym wieku (objawy, takie jak zwiększone pragnienie, ból głowy, zawroty głowy, omdlenia, dezorientacja, ból lub osłabienie stawów lub mięśni, kurcze lub skurcze, niestrwaność, przyspieszony lub nieregularny rytm serca); podwyższone stężenie niektórych tłuszczów we krwi (triglicerydy)
- Niskie ciśnienie krwi, w tym zaburzenia krążenia podczas zmiany pozycji z leżącej na pionową (przy podaniu dożylnym)
- Podwyższone stężenie kreatyniny we krwi
Często(mogą wystąpić u mniej niż 1 na 10 osób)
- Zagęszczenie krwi (w przypadku nadmiernego wydalania moczu)
- Zmniejszone stężenie sodu i chlorków we krwi, małe stężenie potasu we krwi, podwyższone stężenia cholesterolu we krwi, podwyższone stężenie kwasu moczowego we krwi i zaostrzenie dny moczanowej
- Zaburzenia czynności mózgu u pacjentów z ciężkimi zaburzeniami czynności wątroby (encefalopatia wątrobowa)
- Zwiększona objętość moczu
Niezbyt często(mogą wystąpić u mniej niż 1 na 100 osób)
- Mała liczba płytek krwi (małopłytkowość)
- Zmieniona tolerancja glukozy Może to prowadzić do pogorszenia stanu metabolicznego u pacjentów z istniejącą cukrzycą (cukrzyca jawna). Może ujawnić się nierozpoznana cukrzyca (cukrzyca utajona).
- Zaburzenia słuchu, chociaż zwykle są to stany przejściowe, zwłaszcza u pacjentów z zaburzeniami czynności nerek lub zmniejszonym stężeniem białka we krwi (np. w przypadku zespołu nerczycowego) i (lub) jeśli lek dożylny jest wstrzykiwany zbyt szybko do żyły
- Głuchota (czasami nieodwracalna)
- Złe samopoczucie
- Świąd, pokrzywka, wysypka, skóra
- Reakcje błony śluzowej z zaczerwienieniem, powstawaniem pęcherzy lub łuszczeniem się (np. pęcherzowe zapalenie skóry, rumień wielopostaciowy, pemfigoid, złuszczające zapalenie skóry, plamica)
- Zwiększona wrażliwość skóry na światło słoneczne
Rzadko(mogą wystąpić u mniej niż 1 na 1 000 osób)
- Zwiększona liczba pewnego rodzaju białych krwinek (eozynofilia)
- Zmniejszona liczba białych krwinek (leukopenia)
- Mrowienie, drętwienie lub bolesne pieczenie kończyn
- Dzwonienie w uszach (szum w uszach)
- Zapalenie naczyń krwionośnych
- Wymioty, biegunka
- Uszkodzenie nerek (śródmiąższowe zapalenie nerek)
- Gorączka
Bardzo rzadko(mogą wystąpić u mniej niż 1 na 10 000 osób)
- Niedokrwistość spowodowana nieprawidłowym rozpadem krwinek czerwonych (niedokrwistość hemolityczna)
- Stan, w którym szpik kostny przestaje wytwarzać wystarczającą ilość nowych krwinek (niedokrwistość aplastyczna)
- Duże zmniejszenie liczby niektórych rodzajów białych krwinek (agranulocytoza) Objawami mogą być: gorączka z dreszczami, zmiany błony śluzowej i ból gardła
- Ostre zapalenie trzustki
- Zaburzenie wątroby zwane „cholestazą wewnątrzwątrobową”
- Zwiększona aktywność enzymów wątrobowych we krwi, co może powodować żółtaczkę (zażółcenie skóry, ciemne zabarwienie moczu, zmęczenie)
Nieznana(częstość nie może być określona na podstawie dostępnych danych)
- Toczeń rumieniowaty układowy (SLE) może się nasilić lub zostać aktywowany.
- Małe stężenie wapnia we krwi, małe stężenie magnezu we krwi, zmniejszenie pH krwi (kwasica metaboliczna), zespół pseudo-Barttera (niewydolność nerek związana z niewłaściwym i (lub) długotrwałym stosowaniem furosemidu).
Często obserwowanymi objawami małego stężenia sodu we krwi są apatia, kurcze łydek, utrata
apetytu, osłabienie, senność, wymioty i dezorientacja.
Małe stężenie potasu we krwi może objawiać się osłabieniem mięśni, zaburzeniami czucia w
kończynach (mrowienie, drętwienie lub bolesne pieczenie), niezdolnością do poruszania częścią ciała
(niedowład), objawami żołądkowo-jelitowymi (wymioty, zaparcia, nadmierne gromadzenie się gazów
w przewodzie pokarmowym), objawy ze strony nerek (nadmierne wydalanie moczu, nienaturalnie
zwiększone pragnienie) i objawy ze strony serca (lub wolne lub nieregularne bicie serca). Duża utrata
potasu może prowadzić do paraliżu jelit (porażennej niedrożności jelit) lub zaburzeń świadomości, a
nawet śpiączki.
Małe stężenie wapnia we krwi może w rzadkich przypadkach prowadzić do tężyczki. W wyniku
małego steżenia magnezu we krwi w rzadkich przypadkach obserwowano tężyczkę lub występowanie
zaburzeń rytmu serca.
- Zawroty głowy, omdlenia i utrata przytomności, ból głowy
- Zakrzepica, zwłaszcza u pacjentów w podeszłym wieku
- Nadmierne wydalanie moczu, zwłaszcza u pacjentów w podeszłym wieku i u dzieci
- Mogą wystąpić problemy z krążeniem (do zapaści krążeniowej), objawiające się głównie bólem głowy, zawrotami głowy, niewyraźnym widzeniem, suchością w jamie ustnej i pragnieniem, niskim ciśnieniem krwi i zaburzeniami krążenia przy zmianie pozycji z leżącej na stojącą.
- Ciężkie reakcje skórne (mogą dotyczyć również błony śluzowej), takie jak ostra uogólniona osutka krostkowa (AGEP), polekowe wysypki z eozynofilią i objawami ogólnoustrojowymi oraz reakcje liszajowate, które objawiają się małymi, swędzącymi, czerwonawo-purpurowymi zmianami na skórze, narządach płciowych lub w ustach.
- Podwyższone stężenie sodu w moczu, podwyższone stężenie chlorków w moczu, podwyższone stężenie mocznika we krwi, objawy niedrożności dróg moczowych, a nawet zatrzymanie moczu;
- Odkładanie się wapnia w nerkach i (lub) kamieni moczowych u wcześniaków, niewydolność nerek
- Zwiększone ryzyko przetrwałego przewodu tętniczego u wcześniaków leczonych furosemidem w pierwszych tygodniach życia
- Ból po wstrzyknięciu do mięśnia
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania niepożądane
można zgłaszać bezpośrednio do Departament Monitorowania Niepożądanych Działań Produktów
Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
Biobójczych
Al. Jerozolimskie 181C
PL-02-222 Warszawa
tel.: + 48 22 49 21 301
faks: + 48 22 49 21 309
strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać Furosemid Laboratórios Basi
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie przechowywać w temperaturze powyżej 25°C.
Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku: „Termin ważności
EXP”. Termin ważności oznacza ostatni dzień podanego miesiąca.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera Furosemid Laboratórios Basi
- Substancją czynną leku jest furosemid. Każdy 1 mL roztworu zawiera 10 mg furosemidu. Każda ampułka z 2 mL roztworu zawiera 20 mg furosemidu.
- Pozostałe składniki to sodu chlorek, sodu wodorotlenek (do ustalenia pH) i woda do wstrzykiwań.
Jak wygląda Furosemid Laboratórios Basi i co zawiera opakowanie
Klarowny i bezbarwny roztwór, wolny od cząstek stałych.
Ampułka z oranżowego szkła typu I, z punktem OPC, zawierająca 2 mL roztworu do wstrzykiwań /
do infuzji, w tekturowym pudełku.
Wielkość opakowań: 50 ampułek
Podmiot odpowiedzialny
Laboratórios Basi – Indústria Farmacêutica, S.A.
Parque Industrial Manuel Lourenço Ferreira, Lote 15
3450-232 Mortágua, Portugalia
Tel.: +351 231 920 250
Faks: +351 231 921 055
e-mail: [email protected]
Wytwórca
Laboratórios Basi – Indústria Farmacêutica SA
Parque Industrial Manuel Lourenço Ferreira Lotes 8, 15 e 16
3450-232 Mortágua
Portugalia
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego pod następującymi nazwami:
Portugalia
Furosemida Basi
Republika Czeska
Furosemid Basi
Polska
Furosemid Laboratórios Basi
Bułgaria
Фуроземид Basi 10 mg//mL Инжекционен/инфузионен разтвор
Litwa
Furosemide Basi 10 mg//mL Injekcinis ar infuzinis tirpalas
Rumunia
Furosemid Basi 10 mg//mL soluţie injectabilă/perfuzabilă
Szwecja
Furosemide Basi 10 mg//mL Injektions-/infusionsvätska, lösning
Finlandia
Furosemide Basi 10 mg//mL Injektio-/infuusioneste, liuos
Dania
Furosemid Basi
Norwegia
Furosemide Basi 10 mg//mL Injeksjons-/infusjonsvæske, oppløsning
Niemcy
Furosemid Basi 10 mg//mL Injektions-/Infusionslösung
Estonia
Furosemide Basi
Łotwa
Furosemide Basi 10 mg//mL šķīdums injekcijām/infūzijām
Data ostatniej aktualizacji ulotki:
------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Niezgodności farmaceutyczne
Roztworów do wstrzykiwań/do infuzji, wykazujących odczyn kwaśny lub lekko kwaśny i znaczną
pojemność buforową w zakresie kwasowości, nie należy mieszać z roztworem do wstrzykiwań/infuzji
Furosemid Laboratórios Basi 10 mg/mL. W przypadku tych mieszanin wartość pH zostaje przesunięta
do zakresu kwasowego, a słabo rozpuszczalny furosemid wytrąca się w postaci krystalicznego osadu.
Furosemid Laboratórios Basi 10 mg//mL roztwór do wstrzykiwań/do infuzji nie może być podawany z
innymi produktami leczniczymi w jednej strzykawce.
Instrukcje dotyczące rozcieńczania produktu leczniczego przed podaniem, patrz punkt „Instrukcje
dotyczące usuwania i przygotowania produktu leczniczego do stosowania”.
W zespole nerczycowym dawkę należy ustalać ostrożnie ze względu na ryzyko nasilenia działań
niepożądanych.
Okres ważności
Po pierwszym otwarciu:
Podczas stosowania produkt leczniczy wykazał stabilność fizyczną i chemiczną przez 24 godziny w
temperaturze pokojowej.
Z mikrobiologicznego punktu widzenia produkt leczniczy należy zużyć natychmiast. W przeciwnym
razie użytkownik ponosi odpowiedzialność za okres przydatności do podania i warunki przed
użyciem.
Okres ważności po rozcieńczeniu:
Wykazano stabilność chemiczną i fizyczną przez 24 godziny w temperaturze 25 °C.
Z mikrobiologicznego punktu widzenia produkt należy zużyć natychmiast. Jeśli nie zostanie
natychmiast zużyty, za czas i warunki przechowywania w trakcie użytkowania odpowiada
użytkownik.
Instrukcje dotyczące usuwania i przygotowania produktu leczniczego do stosowania
Tylko do jednorazowego użytku.
Produkt leczniczy należy zużyć natychmiast po otwarciu ampułki. Pozostałą zawartość po użyciu
należy wyrzucić.
Produkt leczniczy należy obejrzeć przed użyciem. Produktu leczniczego nie należy stosować, jeśli
widoczne są oznaki zepsucia (np. cząstki lub przebarwienia).
Można rozcieńczać z:
- chlorkiem sodu 9 mg//mL (0,9%) roztworu do wstrzykiwań,
- roztworem Ringera,
- płynem Ringera z mleczanami.
Należy zwrócić uwagę, aby pH używanego roztworu mieściło się w zakresie od słabo zasadowego do
obojętnego (pH nie niższe niż 7). Nie wolno stosować roztworów kwasu, ponieważ może dojść do
wytrącenia substancji czynnej (patrz punkt „Niezgodności farmaceutyczne”).
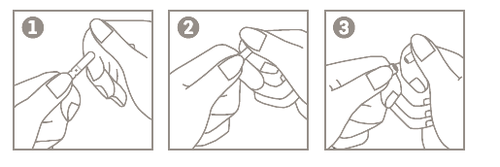
Instrukcja otwierania ampułek (z nacięciem w jednym punkcie)
- 1. Przytrzymać korpus ampułki między kciukiem a palcem wskazującym, czubkiem skierowanym do góry;
- 2. Przyłożyć palec wskazujący drugiej ręki, podtrzymując górną część ampułki. Umieścić kciuk nad punktem;
- 3. Zbliżając palce wskazujące do siebie, nacisnąć obszar oznaczony punktem, aby otworzyć ampułkę.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z
lokalnymi przepisami.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- Producent
- ImporterLaboratórios Basi – Indústria Farmaceutica, S.A.
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Furosemid Laboratórios BasiPostać farmaceutyczna: Roztwór, 10 mg/mlSubstancja czynna: furosemideBez receptyPostać farmaceutyczna: Roztwór, 10 mg/mlSubstancja czynna: furosemideWymaga receptyPostać farmaceutyczna: Tabletki, 40 mgSubstancja czynna: furosemideWymaga recepty
Odpowiedniki Furosemid Laboratórios Basi w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Furosemid Laboratórios Basi – Hiszpania
Odpowiednik Furosemid Laboratórios Basi – Ukraina
Lekarze online w sprawie Furosemid Laboratórios Basi
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Furosemid Laboratórios Basi – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.










