
Fluarix
Zapytaj lekarza o receptę na Fluarix

Jak stosować Fluarix
Ulotka dołączona do opakowania: informacja dla użytkownika
Fluarix, zawiesina do wstrzykiwań w ampułko-strzykawce
Trzywalentna szczepionka przeciw grypie (rozszczepiony wirion, inaktywowana)
Treść tej ulotki została sformułowana zgodnie z założeniem, że będzie ona czytana przez osobę otrzymującą
szczepionkę. Ponieważ jednak szczepionka ta może być podawana dorosłym i dzieciom, jest możliwe, że
z treścią ulotki zapoznawać się będzie rodzic lub opiekun dziecka.
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem szczepionki, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Szczepionka ta została przepisana ściśle określonej osobie. Nie należy jej przekazywać innym.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki:
- 1. Co to jest szczepionka Fluarix i w jakim celu się ją stosuje
- 2. Informacje ważne przed zastosowaniem szczepionki Fluarix
- 3. Jak stosować szczepionkę Fluarix
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać szczepionkę Fluarix
- 6. Zawartość opakowania i inne informacje
1. Co to jest szczepionka Fluarix i w jakim celu się ją stosuje
Fluarix jest szczepionką przeznaczoną do stosowania u osób dorosłych i dzieci od ukończenia 6. miesiąca życia
w celu zapobiegania zachorowaniu na grypę.
Grypa to choroba górnych dróg oddechowych i płuc wywołana zakażeniem wirusem grypy. Najczęstsze
objawy grypy to wysoka temperatura, ból gardła, kaszel, ogólne bóle i dolegliwości, ból głowy, osłabienie i
zmęczenie. Powikłania pogrypowe mogą wystąpić zwłaszcza u osób bardzo młodych, starszych i tych z
obniżoną odpornością na infekcje.
Jak działa szczepionka Fluarix?
- Szczepionka Fluarix zawiera zabite wirusy, które nie mogą wywołać grypy.
- Szczepionka Fluarix pobudza układ odpornościowy osoby zaszczepionej do wytwarzania przeciwciał przeciwko konkretnym wirusom, przeciwko którym została opracowana szczepionka. Pomoże to zapobiec chorobie.
- Szczepionka została opracowana przeciwko wirusom grypy, na podstawie oficjalnych zaleceń.
- Podobnie jak w przypadku wszystkich szczepionek, Fluarix może nie w pełni chronić wszystkie zaszczepione osoby.
2. Informacje ważne przed zastosowaniem szczepionki Fluarix
Kiedy nie stosować szczepionki Fluarix:
- Jeśli pacjent ma uczulenie na substancje czynne lub którykolwiek z pozostałych składników tej szczepionki (wymienionych w punkcie 6) lub na którykolwiek składnik, który może być obecny w bardzo małych ilościach, taki jak albumina jaja kurzego (ovalbumina, białko kurze), hydrokortyzon, siarczan gentamycyny, formaldehyd i dezoksycholan sodu.
Ostrzeżenia i środki ostrożności:
Przed podaniem szczepionki Fluarix należy omówić to z lekarzem, farmaceutą lub pielęgniarką:
- jeśli u pacjenta występuje ostra infekcja przebiegająca z wysoką gorączką. Szczepienie należy odłożyć do chwili, kiedy pacjent poczuje się lepiej. Łagodna infekcja, taka jak przeziębienie, nie jest przeciwwskazaniem do szczepienia, ale przedtem należy porozmawiać o tym z lekarzem, farmaceutą lub pielęgniarką.
- jeśli pacjent ma problemy z krwawieniem lub tendencję do tworzenia się siniaków.
Po lub nawet przed podaniem każdej szczepionki w postaci wstrzyknięcia może dojść do omdlenia
(szczególnie u nastolatków). W związku z tym należy poinformować lekarza, farmaceutę lub pielęgniarkę,
jeżeli u pacjenta kiedyś wystąpiło omdlenie podczas podawania zastrzyku.
Jeśli u pacjenta występuje osłabienie układu odpornościowego, np. z powodu zakażenia HIV lub
przyjmowania leków wpływających na układ immunologiczny, szczepionka Fluarix może nie być w pełni
skuteczna.
Należy poinformować lekarza, farmaceutę lub pielęgniarkę, jeżeli którekolwiek z powyższych stwierdzeń
dotyczy osoby, której ma zostać podana szczepionka Fluarix lub gdy pacjent nie ma pewności czy
którekolwiek z powyższych stwierdzeń go dotyczy.
Szczepionka Fluarix a inne leki
Należy powiedzieć lekarzowi, farmaceucie lub pielęgniarce o wszystkich lekach przyjmowanych obecnie lub
ostatnio, a także o lekach, które pacjent planuje stosować. Należy poinformować o wszystkich niedawno
przyjętych szczepionkach.
Jeśli Fluarix jest podawany jednocześnie z innymi szczepionkami, każda szczepionka powinna być podana w
inne miejsce ciała.
Ciąża, karmienie piersią i wpływ na płodność
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć dziecko,
powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tej szczepionki.
Prowadzenie pojazdów i obsługiwanie maszyn
Niektóre z efektów wymienionych niżej w punkcie 4. „Możliwe działania niepożądane” (np. zmęczenie lub
zawroty głowy) mogą mieć tymczasowy wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Nie należy prowadzić pojazdów lub obsługiwać maszyn ani narzędzi, jeśli pacjent nie czuje się dobrze.
Fluarix zawiera sód
Ta szczepionka zawiera mniej niż 1 mmol sodu (23 mg) na dawkę, to znaczy lek uznaje się za „wolny od
sodu”.
Fluarix zawiera potas
Ta szczepionka zawiera potas, mniej niż 1 mmol (39 mg) na dawkę, to znaczy lek uznaje się za „wolny od
potasu”.
Fluarix zawiera polisorbat 80
Ta szczepionka zawiera nie więcej niż 0,415 mg polisorbatu 80 na dawkę. Polisorbaty mogą powodować
reakcje alergiczne. Należy skonsultować się z lekarzem, jeśli pacjent ma alergię na tę substancję.
3. Jak stosować szczepionkę Fluarix
Szczepionkę Fluarix podaje się w postaci pojedynczego wstrzyknięcia domięśniowego, w dawce 0,5 ml.
Stosowanie u dzieci
Dzieciom poniżej 9 lat, które nie były uprzednio szczepione na grypę, należy podać drugą dawkę po upływie
co najmniej 1 miesiąca od otrzymania pierwszej dawki. Należy upewnić się, że dziecko otrzymało wszystkie
dawki szczepionki, pomoże to uzyskać lepszą ochronę przed zachorowaniem.
W przypadku dodatkowych pytań dotyczących stosowania tej szczepionki, należy zwrócić się do lekarza,
farmaceuty lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, ta szczepionka może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
W celu uzyskania dodatkowych informacji o możliwych działaniach niepożądanych szczepionki Fluarix,
należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
Działania niepożądane zgłaszane podczas ogólnego stosowania szczepionki Fluarix obejmują:
Ciężkie działania niepożądane
Należy natychmiast powiadomić lekarza, jeśli pacjent zauważy u siebie którekolwiek z następujących
ciężkich działań niepożądanych; może być potrzebna pilna pomoc lekarska.
Rzadko:mogą wystąpić nie częściej niż 1 na 1 000 dawek szczepionki
- Ciężkie reakcje alergiczne (reakcje anafilaktyczne). Można je rozpoznać po:
- swędzącej wysypce dłoni i stóp
- obrzęku oczu i twarzy
- trudnościach w oddychaniu lub połykaniu
- nagłym spadku ciśnienia krwi i utracie przytomności. Te reakcje zwykle występują w ciągu 15 minut po szczepieniu. Jednak jeśli wystąpi którykolwiek z tych objawów, należy pilnie skontaktować się z lekarzem.
Inne działania niepożądane
Należy powiadomić lekarza, farmaceutę lub pielęgniarkę, jeśli pacjent zauważy u siebie którekolwiek z
następujących działań niepożądanych.
Rzadko:mogą wystąpić nie częściej niż 1 na 1 000 dawek szczepionki
- Zapalenie nerwów (neuritis), zapalenie mózgu i rdzenia kręgowego (encefalomyelitis), przejściowe zapalenie nerwów powodujące ból, osłabienie i paraliż znane jako zespół Guillain-Barré
- Reakcje skórne, które mogą rozprzestrzeniać się na całe ciało, w tym świąd (swędzenie, pokrzywka) i zaczerwienienie skóry (rumień), wysypka
- Tymczasowy obrzęk węzłów chłonnych na szyi, pod pachami lub w pachwinie (przejściowa limfadenopatia)
- Objawy grypopodobne, ogólne złe samopoczucie Należy poinformować lekarza, farmaceutę lub pielęgniarkę, jeśli pacjent zauważy u siebie którekolwiek z powyższych działań niepożądanych.
W badaniach klinicznych z zastosowaniem szczepionki Fluarix obserwowano następujące działania niepożądane:
Działania niepożądane, które wystąpiły u dzieci w wieku od 6 miesięcy do mniej niż 6 lat
Bardzo często:mogą występować częściej niż 1 na 10 dawek szczepionki
- utrata apetytu
- drażliwość
- senność
- ból w miejscu podania
- zaczerwienienie w miejscu podania
- obrzęk w miejscu podania
Często:mogą występować nie częściej niż 1 na 10 dawek szczepionki
- nudności
- wymioty
- biegunka
- ból brzucha
- gorączka
Działania niepożądane, które wystąpiły u dzieci w wieku od 6 do mniej niż 18 lat
Bardzo często:mogą występować częściej niż 1 na 10 dawek szczepionki
- ból głowy
- ból mięśni
- zmęczenie
- ból w miejscu podania
- zaczerwienienie w miejscu podania
- obrzęk w miejscu podania
Często:mogą występować nie częściej niż 1 na 10 dawek szczepionki
- nudności
- wymioty
- biegunka
- ból brzucha
- ból stawów
- dreszcze
- gorączka
Działania niepożądane, które wystąpiły u dorosłych w wieku 18 lat i starszych
Bardzo często:mogą występować częściej niż 1 na 10 dawek szczepionki
- ból w miejscu podania
- zmęczenie
- ból głowy
- bóle mięśni
Często:mogą występować nie częściej niż 1 na 10 dawek szczepionki
- zaczerwienienie, obrzęk lub twardy guzek w miejscu podania
- dreszcze
- potliwość
- ból stawów
- nudności
- wymioty
- biegunka
- ból brzucha
Rzadko:mogą występować nie częściej niż 1 na 100 dawek szczepionki
- gorączka
- zawroty głowy
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w
ulotce, należy powiedzieć o tym lekarzowi lub farmaceucie. Działania niepożądane można zgłaszać
bezpośrednio do Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu
Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, Al. Jerozolimskie
181C, 02-222 Warszawa, tel.: + 48 22 49 21 301, faks: + 48 22 49 21 309, Strona
internetowa: https://smz.ezdrowie.gov.pl
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
5. Jak przechowywać szczepionkę Fluarix
- Szczepionkę należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
- Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie i pudełku tekturowym po: EXP. Termin ważności oznacza ostatni dzień podanego miesiąca.
- Skrót „Lot” oznacza numer serii produktu.
- Przechowywać w lodówce (2˚C - 8˚C).
- Nie zamrażać.
- Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
- Leków nie należy wyrzucać do kanalizacji lub domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera Fluarix
Substancją czynną jest rozszczepiony, inaktywowany wirus grypy pochodzący z następujących
szczepów*:
A/Victoria/4897/2022 (H1N1)pdm09- podobny szczep (A/Victoria/4897/2022, IVR-238)
15 mikrogramów HA**
A/Croatia/10136RV/2023 (H3N2)- podobny szczep (A/Croatia/10136RV/2023, X-425A)
15 mikrogramów HA**
B/Austria/1359417/2021- podobny szczep (B/Austria/1359417/2021, BVR-26)
15 mikrogramów HA**
w dawce 0,5 ml
* namnażane w zapłodnionych jajach kurzych pochodzących ze zdrowych stad
** hemaglutynina
Ta szczepionka odpowiada zaleceniom Światowej Organizacji Zdrowia (WHO) (dla półkuli północnej) i Unii
Europejskiej na sezon 2025/2026.
Inne składniki szczepionki to: sodu chlorek, disodu fosforan dwunastowodny, potasu
diwodorofosforan, potasu chlorek, magnezu chlorek sześciowodny, α -tokoferylu wodorobursztynian,
polisorbat 80, oktoksynol 10 i woda do wstrzykiwań.
Jak wygląda szczepionka Fluarix i co zawiera opakowanie
- Fluarix jest zawiesiną do wstrzykiwań w ampułko-strzykawce.
- Fluarix jest bezbarwną i lekko opalizującą cieczą.
- Fluarix jest dostępny w postaci 1-dawkowej ampułko-strzykawki, z igłami dołączonymi do opakowania lub bez igieł, w opakowaniach po 1 i 10 sztuk.
- Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny: Wytwórca:
GlaxoSmithKline Biologicals S.A.
GlaxoSmithKline Biologicals
Rue de l’Institut 89
Filia SmithKline Beecham Pharma GmbH&Co. KG
1330 Rixensart
Zirkusstrasse 40
Belgia
01069 Drezno
Niemcy
Ten produkt leczniczy jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego pod następującymi nazwami:
| Państwo członkowskie | Nazwa |
| Austria | Fluarix Trivalent |
| Belgia, Luksemburg | Alpharix |
| Finlandia, Francja, Hiszpania, Holandia, Norwegia, Polska, Portugalia, Szwecja, Włochy | Fluarix |
| Grecja, Niemcy | Influsplit |
Data ostatniej aktualizacji ulotki: lipiec 2025
Inne źródła informacji
Szczegółowa informacja o tym leku jest dostępna na stronie internetowej Urzędu Rejestracji Produktów
Leczniczych, Wyrobów Medycznych i Produktów Biobójczych.
---------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla wykwalifikowanego personelu medycznego:
Przed podaniem szczepionki należy obejrzeć pod kątem ewentualnej obecności ciał obcych i/lub zmian
fizycznych.
Należy wstrząsnąć przed użyciem, aby uzyskać bezbarwną i lekko opalizującą ciecz. W przypadku
zaobserwowania jakichkolwiek zmian, szczepionki nie należy podawać.
Należy podać całą zawartość ampułko-strzykawki.
Instrukcje dotyczące ampułko-strzykawki
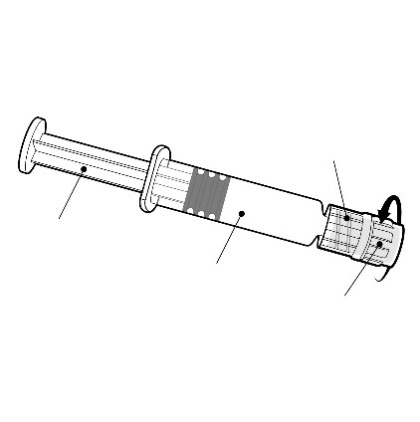
Należy trzymać ampułko-strzykawkę za
korpus, a nie za tłok.
Adapter typu Luer Lock
Należy odkręcić nasadkę ampułko-strzykawki
poprzez przekręcenie jej w kierunku
przeciwnym do ruchu wskazówek zegara.
Tłok
Korpus
Nasadka
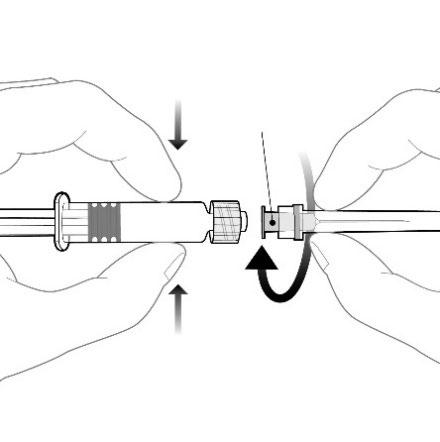
Należy przymocować igłę do
ampułko-strzykawki poprzez przyłączenie
nasadki igły do adaptera Luer Lock (ang. Luer
Lock Adaptor, LLA) i obrócenie jej ćwierć
obrotu w kierunku zgodnym z ruchem
wskazówek zegara, do chwili aż poczuje się
zablokowanie igły.
Nie wolno wyciągać tłoka z korpusu
ampułko-strzykawki. Jeśli tak się stanie,
nie należy podawać szczepionki.
Nasadka igły
Usuwanie
Wszelkie resztki niewykorzystanego produktu leczniczego lub jego odpady należy usunąć zgodnie
z lokalnymi przepisami.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- ImporterGlaxoSmithKline Biologicals Filia SmithKline BeechamPharma GmbH & Co. KG
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki FluarixPostać farmaceutyczna: Zawiesina, 60 mcg HA/szczep, 1 dawka (0,7 ml)Substancja czynna: influenza, inactivated, split virus or surface antigenWymaga receptyPostać farmaceutyczna: Zawiesina, 60 mcg HA/szczep, 1 dawka (0,5 ml)Substancja czynna: influenza, inactivated, split virus or surface antigenWymaga receptyPostać farmaceutyczna: Zawiesina, 1 dawka (0,5 ml)Substancja czynna: influenza, inactivated, split virus or surface antigenWymaga recepty
Odpowiedniki Fluarix w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Fluarix – Hiszpania
Odpowiednik Fluarix – Ukraina
Lekarze online w sprawie Fluarix
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Fluarix – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.














