
Eligard 7,5 mg

Zapytaj lekarza o receptę na Eligard 7,5 mg

Jak stosować Eligard 7,5 mg
Ulotka dołączona do opakowania: informacja dla użytkownika
Eligard 7,5 mg,
proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
Octan leuproreliny
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Lek ten przepisano ściśle określonej osobie. Nie należy go przekazywać innym. Lek może zaszkodzić innej osobie, nawet jeśli objawy jej choroby są takie same.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest lek Eligard i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Eligard
- 3. Jak stosować lek Eligard
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać lek Eligard
- 6. Zawartość opakowania i inne informacje
1. Co to jest lek Eligard i w jakim celu się go stosuje
Substancja czynna leku Eligard należy do grupy leków zwanych gonadoliberynami. Leki te są
stosowane w celu zahamowania wytwarzania określonych hormonów płciowych (testosteronu).
Eligard jest stosowany u dorosłych mężczyzn w leczeniu raka gruczołu krokowegoz
przerzutami, wrażliwego na terapię hormonalną oraz w połączeniu z radioterapią - w leczeniu
raka gruczołu krokowego dużego ryzyka bez przerzutów, wrażliwego na terapię hormonalną.
2. Informacje ważne przed zastosowaniem leku Eligard
Kiedy nie stosować leku Eligard
- U kobiet i dzieci.
- Jeśli pacjent ma uczuleniena substancję czynną - octan leuproreliny, na jakikolwiek związek działający podobnie do naturalnie występującego hormonu - gonadotropiny lub na którykolwiek z pozostałych składników leku Eligard (wymienionych w punkcie 6).
- Po operacyjnym usunięciu jąder, ponieważ Eligard nie powoduje dalszego zmniejszenia stężenia testosteronu w surowicy.
- Jako jedynego leczenia, jeśli u pacjenta występują dolegliwości związane z uciskiem na rdzeń kręgowy lub przerzutami do kręgosłupa. W takim przypadku Eligard można stosować jedynie w połączeniu z innymi lekami stosowanymi w leczeniu raka gruczołu krokowego.
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania leku Eligard należy omówić to z lekarzem, farmaceutą lub pielęgniarką:
- Jeżeli występuje którykolwiek z następujących przypadków: jakiekolwiek choroby serca
lub naczyń krwionośnych, w tym zaburzenia rytmu serca (arytmia) lub pacjent stosuje
leki na te choroby. Ryzyko zaburzeń rytmu serca może się zwiększyć podczas stosowania
leku Eligard.
- Jeżeli występują trudności w oddawaniu moczu. W takim przypadku należy kontrolować stan pacjenta przez pierwsze tygodnie leczenia.
- Jeżeli ucisk na rdzeń kręgowy lub trudności w oddawaniu moczu nasilą się. Podczas jednoczesnego stosowania leków o podobnym działaniu jak Eligard, obserwowano ciężkie przypadki ucisku na rdzeń kręgowy oraz zwężenia moczowodów, w wyniku czego mogą wystąpić objawy takie, jak w przypadku porażenia. W takim przypadku konieczne jest zastosowanie standardowego leczenia.
- Jeżeli u pacjenta wystąpi nagły ból głowy, wymioty, zmiana stanu psychicznego lub zapaść krążeniowa w ciągu dwóch tygodni od podania leku Eligard. W takim przypadku należy natychmiast zawiadomić lekarza lub personel medyczny. Są to objawy rzadko występującego stanu nazywanego zawałem przysadki, który stwierdzano w związku z przyjmowaniem INNYCH LEKÓW o podobnym działaniu jak Eligard.
- Jeżeli u pacjenta występuje cukrzyca(zwiększone stężenie cukru we krwi). W takim przypadku należy kontrolować stan pacjenta podczas leczenia.
- Leczenie produktem Eligard może zwiększyć ryzyko złamań spowodowanych osteoporozą (zmniejszenie gęstości kości).
- Istnieją doniesienia o występowaniu depresji u pacjentów przyjmujących Eligard. Jeśli w trakcie przyjmowania leku Eligard wystąpią nastroje depresyjne, należy poinformować o tym lekarza.
- Istnieją doniesienia o występowaniu chorób układu sercowo-naczyniowego u pacjentów przyjmujących leki podobne do leku Eligard - nie wiadomo, czy ich występowanie jest związane ze stosowaniem tych leków. Jeżeli podczas stosowania leku Eligard pojawią się objawy chorób sercowo-naczyniowych, należy poinformować o tym lekarza.
- Istnieją doniesienia o występowaniu drgawek u pacjentów, którym podawano lek Eligard. Jeśli w trakcie przyjmowania leku Eligard wystąpią drgawki, należy poinformować o tym lekarza.
- Jeśli u pacjenta występują silne lub nawracające bóle głowy, trudności z związane widzeniem i dzwonienie lub brzęczenie w uszach, należy niezwłocznie zwrócić się do lekarza.
- Jeśli pacjent ma stłuszczoną wątrobę
W związku ze stosowaniem leuproreliny zgłaszano ciężkie wysypki skórne, w tym zespół Stevensa-
Johnsona i toksyczną martwicę rozpływną naskórka (SJS/TEN). W przypadku zauważenia
któregokolwiek z objawów związanych z ciężkimi reakcjami skórnymi opisanymi w punkcie 4,
stosowanie leuproreliny należy przerwać i natychmiast skontaktować się z lekarzem.
Powikłania występujące w pierwszym okresie stosowania leku Eligard
Podczas pierwszego tygodnia stosowania obserwuje się krótkotrwałe zwiększenie stężenia
testosteronu we krwi, co może prowadzić do przemijającego nasileniaobjawów choroby lub
pojawienia się nowych, niewystępujących dotychczas. Objawy te obejmują w szczególności: ból
kości, zaburzenia w oddawaniu moczu, ucisk na rdzeń kręgowy, pojawienie się krwi w moczu.
Objawy te zwykle ustępują podczas dalszego leczenia. Jeżeli objawy nie ustąpią, należy
skontaktować się z lekarzem prowadzącym.
Brak działania leku Eligard
U niektórych pacjentów stwierdza się guzy, które nie są wrażliwe na zmniejszenie stężenia
testosteronu w surowicy. W przypadku poczucia, że lek Eligard nie wywiera dostatecznego
działania, należy powiedzieć o tym lekarzowi prowadzącemu.
Lek Eligard a inne leki
Lek Eligard może wpływać na działanie niektórych leków stosowanych w leczeniu zaburzeń rytmu
serca (np. chinidyna, prokainamid, amiodaron i sotalol) lub zwiększać ryzyko wystąpienia zaburzeń
rytmu serca, gdy stosuje się go z niektórymi, innymi lekami (np. metadon (stosowany w łagodzeniu
bólu i detoksykacji u narkomanów), moksyfloksacyna (antybiotyk), leki przeciwpsychotyczne
stosowane w leczeniu ciężkich chorób psychicznych).
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez
pacjenta obecnie lub ostatnio, również tych, które wydawane są bez recepty.
Ciąża i karmienie piersią
Eligard jest przeciwwskazany do stosowania u kobiet.
Prowadzenie pojazdów i obsługiwanie maszyn
Zmęczenie, zawroty głowy i zaburzenia widzenia mogą być działaniami niepożądanymi leku
Eligard lub wynikać z choroby podstawowej. Jeżeli występują działania niepożądane wymienione
powyżej, należy zachować ostrożność podczas prowadzenia pojazdów i obsługiwania maszyn.
3. Jak stosować lek Eligard
Dawkowanie
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie
wątpliwości należy zwrócić się do lekarza lub farmaceuty.
Jeżeli lekarz nie zaleci inaczej, Eligard 7,5 mg podaje się raz na miesiąc.
Wstrzyknięty roztwór tworzy rezerwuar substancji czynnej, z którego następuje ciągłe uwalnianie
substancji czynnej - octanu leuproreliny, przez jeden miesiąc.
Dodatkowe badania
Odpowiedź na leczenie lekiem Eligard powinna być kontrolowana przez lekarza prowadzącego na
podstawie objawów klinicznych oraz stężenia specyficznego antygenu gruczołu krokowego
(ang. Prostate Specific Antigen,PSA) we krwi.
Sposób podawania
Eligard powinien być podawany wyłącznie przez lekarzalub pielęgniarkę,którzy również zajmą
się przygotowaniem produktu.
Po przygotowaniu, Eligard podaje się w postaci podskórnego wstrzyknięcia (wstrzyknięcie w
tkankę pod skórą). Należy bezwzględnie unikać wstrzyknięcia dotętniczego (do tętnicy) lub
dożylnego (do żyły). Podobnie jak w przypadku innych substancji czynnych stosowanych we
wstrzyknięciach podskórnych, należy okresowo zmieniać miejsca wstrzyknięć.
Zastosowanie większej niż zalecana dawki leku Eligard
Lek jest podawany zwykle przez lekarza lub odpowiednio przeszkolony personel medyczny, nie
wydaje się zatem prawdopodobne podanie większej dawki leku.
Jeżeli jednak zostanie podana większa niż zalecana dawka leku, lekarz prowadzący zaleci
obserwację pacjenta i odpowiednie leczenie, jeżeli będzie to konieczne.
Pominięcie zastosowania leku Eligard
Jeżeli zaistnieje podejrzenie, że pominięto miesięczną dawkę leku, należy poinformować o tym
lekarza prowadzącego.
Przerwanie stosowania leku Eligard
Leczenie zaawansowanej postaci raka gruczołu krokowego wymaga długotrwałego podawania
leku Eligard.
Dlatego też nie należy przerywać stosowania leku nawet wtedy, gdy stan pacjenta poprawi się lub
gdy objawy choroby ustąpią.
W przypadku przedwczesnego przerwania leczenia objawy choroby mogą się zaostrzyć.
Nie należy przedwcześnie przerywać leczenia, bez uprzedniej konsultacji z lekarzem.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, Eligard może powodować działania niepożądane, chociaż nie u każdego one
wystąpią.
Działania niepożądane obserwowane podczas stosowania Eligard wynikają przede wszystkim ze
specyficznego działania octanu leuproreliny, który zwiększa lub zmniejsza stężenia
poszczególnych hormonów. Najczęściej obserwowane działania niepożądane to uderzenia gorąca
(u około 58% pacjentów), nudności, złe samopoczucie i zmęczenie oraz przemijające
podrażnienia w miejscu wstrzyknięcia.
Działania niepożądane w pierwszym okresie leczenia
Podczas pierwszych tygodni leczenia lekiem Eligard może dojść do zaostrzenia objawów choroby,
w związku z początkowym, krótkotrwałym zwiększeniem stężenia męskiego hormonu płciowego –
testosteronu we krwi. Dlatego też lekarz może zalecić przyjmowanie odpowiedniego
przeciwandrogenu (substancja, która zmniejsza działanie testosteronu) w początkowej fazie
leczenia, w celu zmniejszenia powyższego działania leku (patrz również punkt 2. Informacje ważne
przed zastosowaniem leku Eligard; Powikłania występujące w pierwszym okresie stosowania leku
Eligard).
Miejscowe działania niepożądane
Miejscowe działania niepożądane opisane po wstrzyknięciu leku Eligard są takie, jak działania
często występujące po wstrzyknięciu podskórnym (wstrzyknięcie w tkankę pod skórą)
podobnych leków. Łagodne uczucie pieczenia tuż po wstrzyknięciu występuje bardzo często.
Uczucie kłucia i
bólu po wstrzyknięciu, jak również zasinienie w miejscu podania występują często. Zaczerwienienie
w miejscu podania zgłaszano często. Stwardnienie tkanek i owrzodzenia w miejscu podania
występują niezbyt często.
Wyżej wymienione miejscowe działania niepożądane występujące po podaniu podskórnym są
łagodne i opisywane jako krótkotrwałe. Nie pojawiają się ponownie pomiędzy kolejnymi
wstrzyknięciami.
Działania niepożądane występujące bardzo często (mogą wystąpić u więcej niż u 1 na 10 osób)
- Uderzenia gorąca
- Samoistne krwawienia ze skóry i błon śluzowych, zaczerwienienie skóry
- Zmęczenie, działania niepożądane w miejscu wstrzyknięcia (patrz powyżej:Miejscowe działania niepożądane)
Działania niepożądane występujące często (mogą wystąpić rzadziej niż u 1 na 10 osób)
- Zapalenie jamy nosowo-gardłowej (objawy przeziębienia)
- Nudności, złe samopoczucie, biegunka, zapalenie żołądka i jelit (żołądka i jelit/okrężnicy)
- Swędzenie, nocne poty
- Ból stawów
- Nieregularne wizyty w toalecie w celu oddania moczu (również w nocy), trudności w oddawaniu moczu, bolesne oddawanie moczu, zmniejszenie ilości oddawanego moczu
- Nadwrażliwość piersi, obrzęk piersi, zanik jąder, ból jąder, bezpłodność, zaburzenia wzwodu, zmniejszenie wielkości prącia
- Dreszcze (epizody wzmożonego drżenia z wysoką gorączką), osłabienie
- Wydłużenie czasu krwawienia, zmiany w wartościach parametrów krwi, zmniejszenie liczby krwinek czerwonych/mała liczba krwinek czerwonych
Działania niepożądane występujące niezbyt często (mogą wystąpić rzadziej niż u 1 na 100 osób)
- Zakażenia dróg moczowych, miejscowe zakażenia skóry
- Nasilenie objawów cukrzycy
- Niezwykłe sny, depresja, zmniejszenie popędu płciowego
- Zawroty głowy, ból głowy, zaburzenia czucia skórnego, bezsenność, zaburzenia smaku, zaburzenia czucia zapachu
- Nadciśnienie (podwyższone ciśnienie krwi), niedociśnienie (obniżone ciśnienie krwi)
- Skrócenie oddechu
- Zaparcia, suchość w ustach, niestrawność (zaburzone trawienie z uczuciem pełności żołądka, ból żołądka, odbijanie się, nudności, wymioty, uczucie pieczenia w żołądku), wymioty
- Zwiększenie wilgotności skóry, nadmierne pocenie się
- Ból pleców, skurcz mięśni
- Hematuria (obecność krwi w moczu)
- Skurcz pęcherza, częstsze niż zwykle wizyty w toalecie w celu oddania moczu, niemożność oddawania moczu
- Powiększenie piersi u mężczyzn, impotencja
- Letarg (senność), ból, gorączka
- Zwiększenie masy ciała
- Utrata równowagi, uczucie pustki w głowie
- Zanik mięśni/utrata tkanki mięśniowej po długotrwałym stosowaniu
Działania niepożądane występujące rzadko (mogą wystąpić rzadziej niż u 1 na 1000 osób)
- Ruchy mimowolne
- Nagła utrata świadomości, omdlenie
- Wzdęcie z oddawaniem wiatrów, odbijanie się
- Wypadanie włosów, wykwity skórne (krosty na skórze)
- Ból piersi
- Owrzodzenie w miejscu wstrzyknięcia
Działania niepożądane występujące bardzo rzadko (mogą wystąpić rzadziej niż u 1 na 10 000 osób)
- Martwica w miejscu podania
Częstość nieznana (nie może być określona na podstawie dostępnych danych)
- Zmiany w elektrokardiogramie (wydłużenie odstępu QT)
- Zapalenie płuc, choroba płuc
- Idiopatyczne nadciśnienie wewnątrzczaszkowe (zwiększone ciśnienie wewnątrzczaszkowe wokół mózgu, charakteryzujące się bólem głowy, podwójnym widzeniem i innymi objawami dotyczącymi widzenia oraz dzwonieniem lub brzęczeniem w jednym uchu lub obu uszach)
- Czerwonawe, niewyniesione, tarczowate lub okrągłe plamy na tułowiu, często z pęcherzami pośrodku, łuszczenie się skóry, owrzodzenia jamy ustnej, gardła, nosa, narządów płciowych i oczu. Te ciężkie wysypki skórne mogą być poprzedzone gorączką i objawami grypopodobnymi (zespół Stevensa-Johnsona, toksyczna martwica rozpływna naskórka)
- Zaczerwienienie skóry i swędząca wysypka (toksyczne wykwity skórne)
- Reakcja skórna powodująca wystąpienie czerwonych punktów lub plam na skórze, które mogą wyglądać jak tarcza strzelnicza z ciemnoczerwonym środkiem otoczonym jaśniejszymi czerwonymi pierścieniami (rumień wielopostaciowy)
Pozostałe działania niepożądane
Inne działania niepożądane opisane w literaturze jako związane z leczeniem leuproreliną - substancją
czynną zawartą w leku Eligard to: obrzęk obwodowy (gromadzenie się płynu w tkankach,
objawiające się jako opuchnięcie dłoni i stóp), zatorowość płucna (objawiająca się brakiem tchu,
trudnością w oddychaniu i bólem w klatce piersiowej), kołatanie serca (odczuwalne bicie serca),
zmniejszenie siły mięśni, dreszcze, wysypka, zaburzenia pamięci i zaburzenia widzenia. W
przypadku długotrwałego leczenia lekiem Eligard można oczekiwać zwiększonej częstości
występowania objawów zmniejszenia gęstości kości (osteoporozy). W związku z osteoporozą
zwiększa się ryzyko złamań.
Po stosowaniu produktów należących do tej samej grupy co Eligard rzadko zgłaszano ciężkie reakcje
alergiczne, powodujące trudności w oddychaniu lub zawroty głowy.
Po stosowaniu produktów należących do tej samej grupy co Eligard zgłaszano wystąpienie drgawek.
Zgłaszanie działań niepożądanych
Jeżeli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane
niewymienione w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce.
Działania niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C, 02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać lek Eligard
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku po: EXP.
Termin ważności oznacza ostatni dzień podanego miesiąca.
Instrukcje dotyczące przechowywania
Przechowywać w lodówce (2°C do 8°C).
Przechowywać w oryginalnym opakowaniu w celu ochrony przed wilgocią.
Przed wstrzyknięciem produkt leczniczy musi mieć temperaturę pokojową. Należy go wyjąć z
lodówki około 30 minut przed przygotowaniem. Po wyjęciu produktu leczniczego z lodówki, można
go przechowywać w oryginalnym opakowaniu w temperaturze pokojowej (poniżej 25°C) do 4
tygodni.
Po pierwszym otwarciu plastikowej tacki zamkniętej folią, należy natychmiast sporządzić roztwór i
jak najszybciej podać go pacjentowi. Produkt jest przeznaczony do jednorazowego użycia.
Instrukcje dotyczące postępowania z nieużytym lub przeterminowanym lekiem Eligard
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera lek Eligard
Substancją czynną leku Eligard jest octan leuproreliny.
Jedna z ampułko -strzykawek (Strzykawka B) zawiera 7,5 mg octanu leuproreliny.
Pozostałe składniki leku to kwas poli (DL-mleczano-ko-glikolowy) (50:50) oraz N-metylopirolidon
zawarte w ampułko -strzykawce z rozpuszczalnikiem do sporządzania roztworu do wstrzykiwań
(Strzykawka A).
Jak wygląda lek Eligard i co zawiera opakowanie
Eligard to proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań.
Eligard 7,5 mg jest dostępny w następujących opakowaniach:
- Zestaw składający się z formowanej termicznie tacki zamkniętej folią oraz jałowej igły o średnicy 20G, w tekturowym pudełku. Tacka zawiera torebkę ze środkiem pochłaniającym wilgoć oraz system połączonych strzykawek składający się z: ampułko-strzykawki A zawierającej rozpuszczalnik ampułko-strzykawki B zawierającej proszek łącznika z przyciskiem zatrzaskowym do strzykawek A i B.
- Opakowanie zbiorcze zawierające 3 zestawy, z których każdy zawiera jeden system połączonych strzykawek.
Nie wszystkie wielkości opakowań muszą znajdować się w obrocie.
Podmiot odpowiedzialny i wytwórca
Recordati Industria Chimica e Farmaceutica S.p.A.
Via Matteo Civitali 1
20148 Mediolan
Włochy
W celu uzyskania bardziej szczegółowych informacji należy zwrócić się do miejscowego
przedstawiciela podmiotu odpowiedzialnego:
Recordati Polska sp. z o.o.
Al. Armii Ludowej 26
00-609 Warszawa
tel: + 48 22 206 84 50
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego pod następującymi nazwami:
Austria:
Eligard Depot 7,5 mg
Belgia:
Depo-Eligard 7,5 mg
Cypr:
Eligard
Czechy:
Eligard
Dania:
Eligard
Estonia:
Eligard
Finlandia:
Eligard
Francja:
Eligard 7,5 mg
Niemcy:
Eligard 7,5 mg
Węgry:
Eligard 7,5 mg
Islandia:
Eligard
Irlandia:
Eligard 7,5 mg
Włochy:
Eligard
Łotwa:
Eligard 7,5 mg
Litwa:
Eligard 7,5 mg
Luxemburg:
Depo-Eligard 7,5 mg
Holandia:
Eligard 7,5 mg
Norwegia:
Eligard
Polska:
Eligard 7,5 mg
Portugalia:
Eligard 7,5 mg
Słowacja:
Eligard 7,5 mg
Słowenia:
Eligard 7,5 mg
Szwecja:
Eligard
Data ostatniej aktualizacji ulotki: 10/2024
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Przed otwarciem należy doprowadzić produkt leczniczy do temperatury pokojowej wyjmując go z lodówki około 30 minut przed użyciem.
W pierwszej kolejności należy przygotować pacjenta do podania produktu, a następnie przygotować roztwór według poniższej instrukcji. Jeżeli roztworu nie przygotuje się z zastosowaniem odpowiedniej techniki, nie należy go podawać pacjentowi, gdyż w wyniku
nieprawidłowej rekonstytucji produktu leczniczego może wystąpić brak skuteczności
klinicznej.
Krok 1
Na czystym podłożu, otworzyć tackę poprzez zdarcie folii zaczynając od rogów w celu wyjęcia
zawartości. Usunąć torebkę ze środkiem pochłaniającym wilgoć. Wyjąć system połączonych
strzykawek (Ryc. 1.1) z tacki. Otworzyć opakowanie zawierające igłę z osłoną zabezpieczającą
(Ryc. 1.2), odrywając papierową część opakowania.
Uwaga: Strzykawka A i Strzykawka B nie powinny być jeszcze ustawione w jednej linii.
Ryc. 1.1
Zawartość tacki: system połączonych strzykawek
Ryc. 1.2
Pod tacką: Igła z osłoną zabezpieczającą
i nasadka
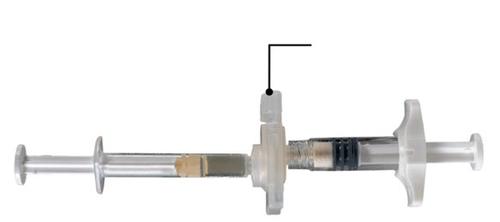
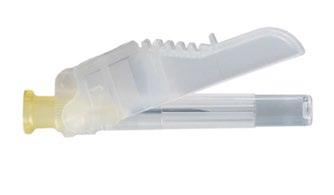
Krok 2
Palcem i kciukiem chwycić przycisk zatrzaskowy na łączniku i naciskać (Ryc. 2), do momentu
usłyszenia zatrzaśnięcia .Dwie strzykawki zostaną ustawione w jednej linii. Uruchomienie łącznika
nie wymaga żadnego specjalnego położenia systemu połączonych strzykawek. Nie należy wyginać
systemu połączonych strzykawek (należy zwrócić uwagę, że może to spowodować wyciek,
ponieważ strzykawki mogą zostać częściowo odkręcone).
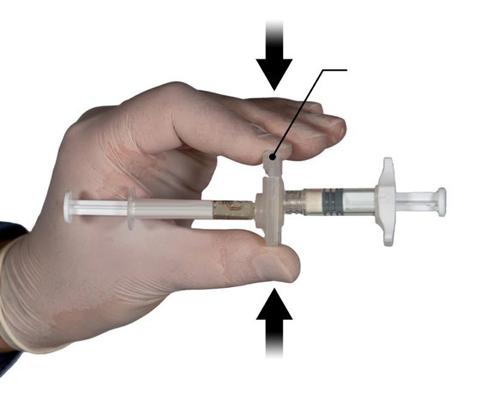
Krok 3
Trzymając strzykawki w pozycji poziomej, przemieścić płynną zawartość Strzykawki A do
octanu leuproreliny w postaci proszku znajdującego się w Strzykawce B. Dokładnie wymieszać
produkt przez 60 cykli, delikatnie przemieszczając zawartość obu strzykawek pomiędzy obiema
strzykawkami (jeden cykl oznacza jedno naciśnięcie tłoka Strzykawki A i jedno naciśnięcie tłoka
Strzykawki B) ustawionymi w pozycji poziomej, do uzyskania jednorodnego, lepkiego roztworu
(Ryc. 3). Nie należy wyginać systemu połączonych strzykawek (należy zwrócić uwagę, że może
to spowodować wyciek, ponieważ strzykawki mogą zostać częściowo odkręcone).
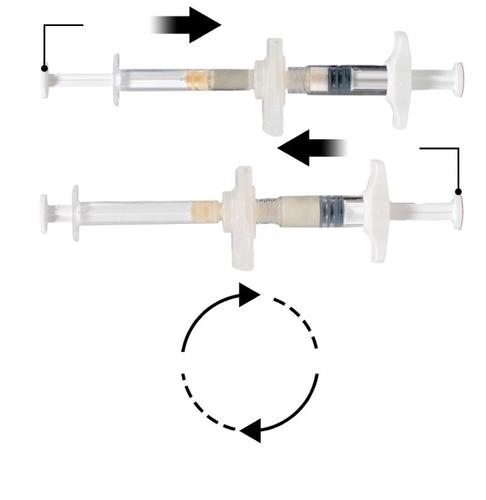
Powtórzyć 60x
Po dokładnym wymieszaniu lepki roztwór ma kolor bezbarwny do białego lub do jasnobrązowego (odcienie białego do jasnożółtego).
Ważne: Po wymieszaniu należy natychmiast przejść do następnego kroku ponieważ w miarę upływu czasu zwiększa się lepkość produktu. Nie należy zamrażać wymieszanego produktu.
Uwaga: Produkt należy mieszać zgodnie z instrukcją; wstrząsanie NIE zapewni właściwego
wymieszania produktu.
Krok 4
Po wymieszaniu, trzymać strzykawki w pozycji pionowej tak, aby Strzykawka B była na dole.
Strzykawki powinny pozostać prawidłowo połączone. Przemieścić cały wymieszany produkt do
Strzykawki B (krótka, szeroka strzykawka) naciskając tłok Strzykawki A i nieznacznie pociągając
tłok strzykawki (Ryc. 4)
Ryc. 4
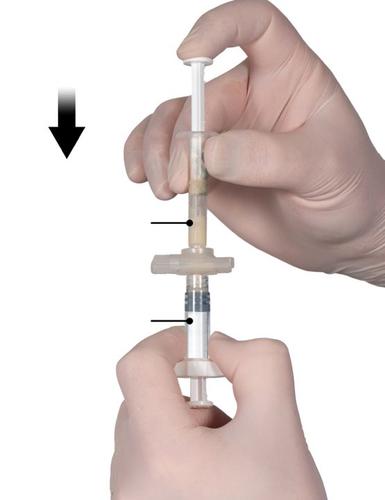
Krok 5
Upewniając się, że tłok Strzykawki A jest całkowicie wciśnięty, trzymając za łącznik należy
wykręcić go ze Strzykawki B. Strzykawka A pozostanie połączona z łącznikiem (Ryc. 5). Upewnić
się, że produkt nie wycieka, gdyż w przeciwnym razie igła, po nałożeniu, nie zabezpieczy
prawidłowo strzykawki.
Uwaga: W mieszaninie mogą pozostać jeden duży lub kilka małych pęcherzyków powietrza – jest
to zjawisko normalne.
Nie należy usuwać pęcherzyków powietrza ze Strzykawki B na tym etapie, ponieważ może to spowodować stratę produktu!
Ryc. 5
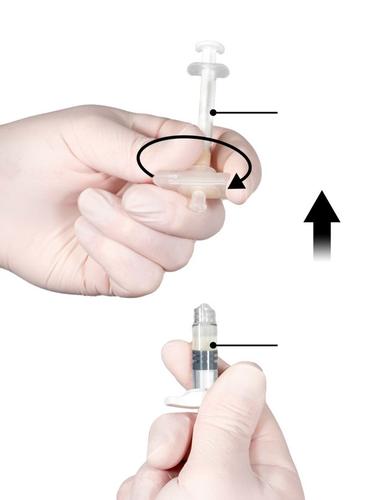
Krok 6
- Trzymać Strzykawkę B pionowo i przytrzymać biały tłok, aby zapobiec stracie produktu.
- Nałożyć igłę z osłoną zabezpieczającą na Strzykawkę B, trzymając strzykawkę, i delikatnie przekręcić igłę o około trzy czwarte obrotu w kierunku zgodnym z ruchem wskazówek zegara, aż do umocowania igły (Ryc. 6). Nie należy dokręcać zbyt mocno,gdyż może to spowodować pęknięcie nasadki igły i w konsekwencji wyciek produktu podczas wstrzykiwania .W przypadku dokręcania igły ze zbyt dużą siłą, uszkodzeniu może ulec również osłona zabezpieczająca.
Jeśli nasadka igły będzie pękniętą lub będzie wyglądała na uszkodzoną, bądź zaobserwuje się
wyciek, nie należy podawać produktu leczniczego. Uszkodzonej igły nie należy zastępować
inną/wymieniać na inną a produktu nie należy wstrzykiwać. Wszystkie elementy niezużytego
produktu należy usunąć w bezpieczny sposób.
W przypadku uszkodzenia nasadki igły należy podać nowy produkt leczniczy.
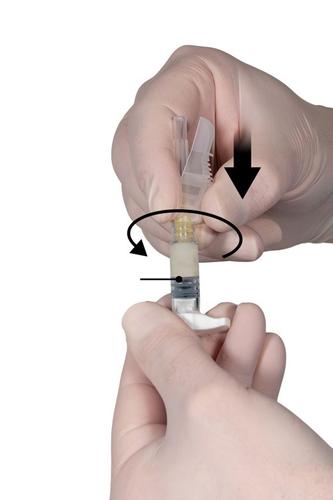
Krok 7
Odgiąć osłonę zabezpieczającą od igły i zdjąć osłonkę zakrywającą końcówkę igły bezpośrednio
przed podaniem produktu leczniczego (Ryc. 7).
Ważne: Przed podaniem produktu nie należy manipulować przy mechanizmie osłony zabezpieczającej igłę. Jeśli nasadka igły będzie wyglądała na uszkodzoną lub zaobserwowany zostanie wyciek, NIE należy używać produktu. Uszkodzonej igły NIE należy wymieniać na
inną, a produktu NIE należy wstrzykiwać. W przypadku uszkodzenia nasadki igły należy użyć
nowego zestawu produktu leczniczego Eligard.
Ryc. 7
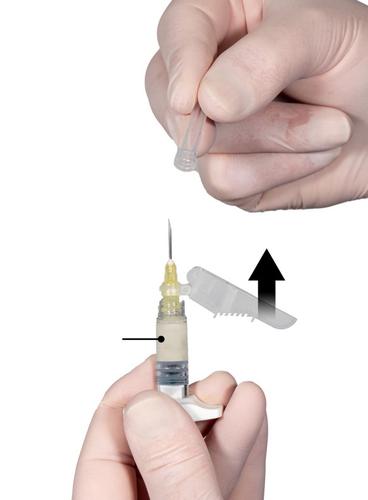
Krok 8
Przed podaniem produktu leczniczego należy usunąć wszystkie dużepęcherzyki powietrza ze
Strzykawki B. Podać ten produkt podskórnie tak, aby osłona zabezpieczająca pozostała odgięta od
igły.
Procedura podania:
Ryc. 8
- Wybrać miejsce wstrzyknięcia, które nie było ostatnio używane, na brzuchu, w górnym obszarze pośladków lub innej lokalizacji z dostateczną ilością tkanki podskórnej i bez przebarwień, guzków, zmian lub włosów.
- Oczyścić obszar w miejscu wstrzyknięcia przy użyciu gazika nasączonego alkoholem (nie dołączony).
- Kciukiem i palcem wskazującym chwycić i ścisnąć obszar skóry wokół miejsca wstrzyknięcia.
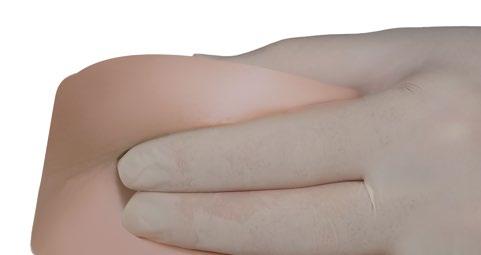
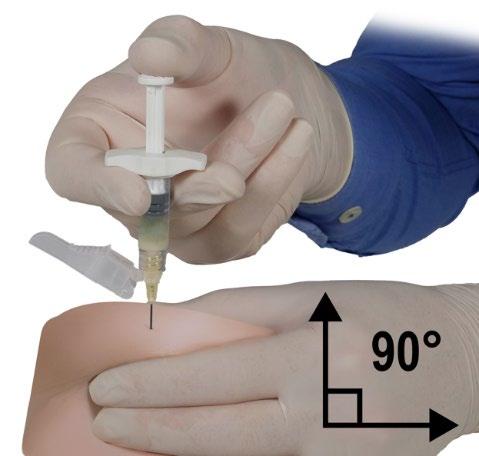
- Ręką dominującą szybko wkłuć igłę pod kątem 90° w stosunku do powierzchni skóry. Głębokość penetracji będzie zależeć od ilości i zagęszczenia tkanki podskórnej oraz długości igły. Po wkłuciu igły puścić skórę.
- Wstrzyknąć produkt powoli i równomiernie naciskając tłok do momentu opróżnienia strzykawki. Przed usunięciem igły należy upewnić się, że wstrzyknięto całą ilość produktu ze Strzykawki B.
- Utrzymując nacisk na tłok, szybko wycofać igłę pod takim samym kątem 90°, jakiego użyto do wkłucia.
Krok 9
Po wstrzyknięciu produktu leczniczego należy zamknąć osłonę zabezpieczającą igłę, stosując jedną
z metod wymienionych poniżej.
1. Zamykanie na płaskiej powierzchni
Przycisnąć osłonę zabezpieczającą, skierowaną dźwignią w dół, do płaskiej powierzchni (Ryc. 9a)
w celu zakrycia igły i zamknięcia osłony zabezpieczającej.
Osłona jest zamknięta jeżeli usłyszy się i wyczuje kliknięcie. W pozycji zamkniętej końcówka igły
będzie całkowicie zakryta.
2. Zamykanie kciukiem
Umieścić kciuk na osłonie zabezpieczającej (Ryc. 9b), zakryć końcówkę igły i zamknąć osłonę
zabezpieczającą.
Osłona jest zamknięta jeżeli usłyszy się i wyczuje kliknięcie. W pozycji zamkniętej końcówka
igły będzie całkowicie zakryta.
Ryc. 9a
Zamykanie na płaskiej powierzchni
Ryc. 9b
Zamykanie kciukiem
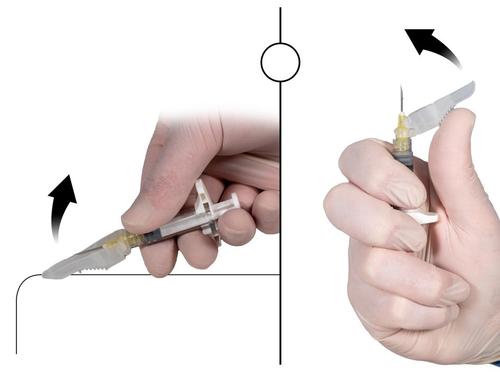
Po zamknięciu osłony zabezpieczającej natychmiast wyrzucić igłę i strzykawkę do pojemnika
przeznaczonego na ostre przedmioty.
- Kraj rejestracji
- Substancja czynna
- Wymaga receptyTak
- ImporterRecordati Industria Chimica e Farmaceutica S.p.A
- Te informacje mają charakter wyłącznie poglądowy i nie stanowią porady medycznej. Przed zastosowaniem jakiegokolwiek leku zawsze skonsultuj się z lekarzem. Oladoctor nie ponosi odpowiedzialności za decyzje medyczne podjęte na podstawie tych treści.
- Zamienniki Eligard 7,5 mgPostać farmaceutyczna: Proszek, 22,5 mgSubstancja czynna: leuprorelinWymaga receptyPostać farmaceutyczna: Proszek, 45 mgSubstancja czynna: leuprorelinWymaga receptyPostać farmaceutyczna: Implant, 3,6 mgSubstancja czynna: leuprorelinWymaga recepty
Odpowiedniki Eligard 7,5 mg w innych krajach
Najlepsze odpowiedniki z tą samą substancją czynną i działaniem terapeutycznym.
Odpowiednik Eligard 7,5 mg – Іспанія
Odpowiednik Eligard 7,5 mg – Україна
Lekarze online w sprawie Eligard 7,5 mg
Konsultacja w sprawie dawkowania, działań niepożądanych, interakcji, przeciwwskazań i odnowienia recepty na Eligard 7,5 mg – decyzja należy do lekarza, zgodnie z lokalnymi przepisami.











