
BRIMONIDINA VIR 2 mg/ml COLIRIO EN SOLUCION

Cómo usar BRIMONIDINA VIR 2 mg/ml COLIRIO EN SOLUCION
Traducción generada por IA
Este contenido ha sido traducido automáticamente y se ofrece solo con fines informativos. No sustituye la consulta con un profesional sanitario.
Ver originalContenido del prospecto
Introducción
Prospecto: información para el usuario
Brimonidina Vir 2 mg/ml, colirio en solución
Tartrato de brimonidina
Lea todo el prospecto detenidamente antes de empezar a usar el medicamento, ya que contiene información importante para usted.
- Conserve este prospecto ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted y no debe dárselo a otras personas, aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver la sección 4.
Contenido del prospecto:
- Qué es Brimonidina Vir y para qué se utiliza
- Qué necesita saber antes de usar Brimonidina Vir
- Cómo usar Brimonidina Vir
- Posibles efectos adversos
- Conservación de Brimonidina Vir
- Contenido del envase e información adicional
1. Qué es Brimonidina Vir y para qué se utiliza
El ingrediente activo de Brimonidina Vir es tartrato de brimonidina que reduce la presión intraocular.
Brimonidina Vir es un medicamento que se utiliza para reducir la presión intraocular. Puede usarse solo en pacientes en los que la terapia con betabloqueantes tópicos esté contraindicada o con otro colirio, cuando no se consigue disminuir la presión intraocular (PIO) en pacientes con glaucoma de ángulo abierto o hipertensión ocular
2. Qué necesita saber antes de usar Brimonidina Vir
No use Brimonidina Vir si:
- Es alérgico (hipersensible) a la brimonidina o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
- En recién nacidos/niños (menores de 2 años).
- Está tomando inhibidores de la monoamino oxidasa o ciertos antidepresivos. Informe a su médico si está tomando algún medicamento para tratar la depresión.
- Está en periodo de lactancia.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Brimonidina Vir si:
- se administra a niños de 2 a 12 años. No se recomienda el uso de Brimonidina Vir en niños de esta edad.
- sufre o ha sufrido depresión, reducción de la capacidad mental, reducción del aporte de sangre al cerebro, problemas de corazón, trastornos del aporte de sangre a las extremidades o alteración de la presión sanguínea.
- tiene o ha tenido problema de hígado o riñón.
Si cree que cualquiera de estos puntos son aplicables para usted, no use Brimonidina Vir hasta que haya consultado de nuevo con el médico.
Niños y adolescentes
No se recomienda el uso de brimonidina en niños menores de 12 años. No existen estudios que demuestran su seguridad y eficacia en niños. Esto es particularmente importante en los niños menores de 2 años.
Uso de otros medicamentos con Brimonidina Vir
Informe a su médico o farmacéutico si está tomando, o ha tomado recientemente o podría tener que tomar algún otro medicamento, incluso los adquiridos sin receta médica.
Informe a su médico si está tomando los siguientes medicamentos:
- analgésicos, sedantes, opiáceos, barbitúricos o consume alcohol de forma regular.
- anestésicos.
- medicamentos para el tratamiento de su presión sanguínea elevada o para el corazón.
- medicamentos que pueden afectar a su metabolismo como la clorpromazina, metilfedinato y reserpina.
- que funcionan en el mismo receptor que Brimonidina Vir, por ejemplo isoprenalina y and prazosina.
- inhibidores de la MAO y otros antidepresivos.
- medicamentos para cualquier otra enfermedad, aunque no estén relacionados con su enfermedad ocular.
- o si se cambia la dosis de cualquiera de sus medicamentos.
Esto podría afectar su tratamiento con Brimonidina Vir.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
No utilice Brimonidina Vir si está en periodo de lactancia.
Conducción y uso de máquinas
Brimonidina Vir puede causar visión borrosa o alterada, especialmente por la noche o cuando exista poca luz.
Brimonidina Vir también puede causar somnolencia y/o cansancio en algunos pacientes.
No conduzca o maneje máquinas hasta que los síntomas hayan desaparecido.
Brimonidina Vir contiene cloruro de benzalconio.
Este conservante puede causar irritación ocular y también se sabe que altera el color de las lentes de contacto blandas. Por lo tanto, evite el contacto con las lentes blandas. Si usa lentes de contacto blandas retírelas antes de utilizar este colirio y luego espere 15 minutos tras la aplicación de colirio para volver a ponérselas.
3. Cómo usar Brimonidina Vir
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
Adultos (incluyendo mayores de 65 años)
La dosis habitual recomendada es una gota en el ojo o los ojos afectados dos veces al día, con un intervalo de dosis de aproximadamente 12 horas.
Niños menores de 12 añosBrimonidina Vir no debe utilizarse en niños menores de 2 años.
No se recomienda el uso de Brimonidina Vir en niños entre 2 y 12 años.
Instrucciones de uso
Brimonidina Vir se presenta en forma de gotas oftálmicas. Siempre se deben labar las manos antes de la aplicación del colirio. El prospecto indica cuántas gotas debe utilizar en cada dosis. Si está utilizando más de un medicamento por vía oftálmica, los medicamentos se deben aplicar con un intervalo de entre 15 minutos de diferencia entre ellos.
Aplíquese su colirio de la siguiente forma:
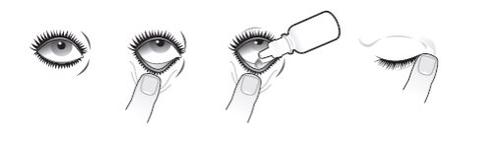
- Incline la cabeza hacia atrás y mire al techo
- Tire del párpado inferior suavemente hacia abajo hasta que haya un pequeño hueco
- Ponga el frasco boca abajo y apriete hasta que entre una gota en cada ojo que necesite tratamiento
- Mantenga el ojo cerrado y presione con el dedo la esquina del ojo (esquina interna del ojo) durante un minuto
Evite que la punta del envase toque el ojo u otra superficie.
Cierre el envase inmediatamente después de usarlo.
Si usa más Brimonidina Vir del que debiera
Adultos
Las reacciones adversas son las mismas que se conocen con Brimonidina Vir y han sido notificadas para adultos que han usado más colirio en solución de la recomendada.
En casos de adultos que habían tragado accidentalmente Brimonidina Vir, se informó de presión arterial baja, seguida de un fuerte aumento de la presión arterial. En caso de que esto ocurriera, consulte inmediatamente con su médico.
Niños
Se han notificado casos de sobredosis de niños que habían ingerido accidentalmente Brimonidina Vir. Los síntomas incluyen somnolencia, decaimiento, baja temperatura corporal, palidez y dificultad para respirar. Si sufre cualquiera de estos síntomas, consulte inmediatamente a su médico.
Adultos y niños
En caso de sobredosis o ingestión accidental de Brimonidina Vir consulte inmediatamente a su médico o farmacéutico o llame al Servicio de Información Toxicológica, teléfono: 91 562 04 20, indicando el medicamento y la cantidad ingerida.
Si olvidó usar Brimonidina Vir
Si olvidó tomar Brimonidina Vir, aplíquese la dosis olvidada tan pronto como se acuerde. Si no se ha acordado de la dosis olvidada hasta poco antes de la siguiente dosis, no se aplique la dosis olvidada y aplíquese la siguiente dosis cuando corresponda.
No tome una dosis doble para compensar las dosis olvidadas.
Si interrumpe el tratamiento con Brimonidina Vir
Para resultar efectivo, Brimonidina Vir debe utilizarse cada día. No interrumpa el tratamiento con Brimonidina Vir sin haberlo consultado previamente con su médico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede causar efectos adversos, aunque no todas las personas los sufran.
Se han notificado los siguientes efectos adversos:
Efectos adversos en el ojo
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- irritación de los ojos (rubor, dolor y quemazón, picor, sensación de tener un cuerpo extraño, conjuntivitis folicular), conjuntivitis folicular
- Visión borrosa
- Reacción alérgica en el ojo.
Frecuentes(pueden afectar a entre 1 y 10 de cada 100 personas):
- Irritación local del ojo (rubor y edema de párpado, edema conjuntival y descarga, dolor ocular y lagrimeo)
- Hipersensibilidad a la luz
- Daño superficial y coloración de la córnea
- Sequedad ocular
- Palidez conjuntival
- Visión anormal
- Conjuntivitis.
Muy raras(afectan a 1-10 usuarios de cada 1.000):
- Iritis (inflamación del iris)
- Contracción de las pupilas.
Frecuencia no conocida(la frecuencia no puede estimarse a partir de los datos disponibles):
- Prurito de los párpados
Efectos adversos en el cuerpo
Muy frecuentes(pueden afectar a más de 1 de cada 10 personas):
- Dolor de cabeza
- Sequedad de la boca
- Cansancio/somnolencia
Frecuentes(pueden afectar a entre 1 y 10 de cada 100 personas):
- Vértigo
- Síntomas de resfriado
- Síntomas que afectan al estómago y la digestión
- Alteración del sabor
- Debilidad sistémica.
Poco frecuentes(pueden afectar a entre 1 y 10 de cada 1.000 personas):
- Depresión
- Palpitaciones o arritmias,
- Sequedad nasal
- Reacciones alérgicas sistémicas.
Raras(pueden afectar a entre 1 y 10 de cada 10.000 personas):
- Disnea (dificultad respiratoria)
Muy raras(pueden afectar a menos de 1 de cada 10.000 personas):
- Insomnio
- Pérdida de conocimiento
- Hipertensión (Alta presión sanguínea)
- Hipotensión (Baja presión sanguínea)
Frecuencia no conocida(la frecuencia no puede estimarse a partir de los datos disponibles):
- Reacciones cutáneas que incluyen: hinchazón de la cara, enrojecimiento de la piel, picor de la piel, erupción, baja presión arterial.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaRAM.es. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Brimonidina Vir
Mantener este medicamento fuera del alcance y de la vista de los niños.
No utilice Tarobrim después de la fecha de caducidad que aparece en el envase y el frasco después de CAD. La fecha de caducidad es el último día del mes que se indica.
Una vez abierto el frasco, puede conservarse hasta un máximo de 28 días.
Este medicamento no requiere condiciones especiales de conservación.
Los medicamentos no se deben tirar por los desagües ni a la basura. Deposite los envases y los medicamentos que no necesita en el Punto SIGRE de la farmacia. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma, ayudará a proteger el medio ambiente
6. Información adicional
Composición de Brimonidina Vir
La sustancia active es tartrato de brimonidina.
1 ml de solución contiene 2 mg de tartrato de brimonidina, equivalente a 1,3 mg de brimonidina.
1 gota de solución contiene 65,2 microgramos de tartrato de brimonidina que equivale a 43 microgramos de brimonidina.
Los demás componentes son: cloruro de benzalconio, alcohol polivinílico, citrato de sodio, ácido cítrico monohidratado, cloruro sódico, agua purificada, acido clorhídrico (para el ajuste del pH), hidróxido sódico (para el ajuste del pH).
Aspecto de Brimonidina Vir y contenido del envase
Colirio en solución transparente de color amarillo verdoso pálido en frasco de plástico.
Cada frasco contiene de 5 ml de colirio en solución.
Tamaño del envase: 1 frasco de 5 ml
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización
INDUSTRIA QUIMICA Y FARMACEUTICA VIR, S.A.
Laguna, 66-68-70. Poligono Industrial Urtinsa II
28923 Alcorcón (Madrid)
España
Responsable de la fabricación
JADRAN-GALENSKI LABORATORIJ d.d.
Svilno 20
51000 Rijeka,
Croacia
Este medicamento está autorizado en los Estados Miembros de la EEA bajo las siguientes denominaciones:
Dinamarca Tarobrim, øjendråber, opløsning
España Brimonidina Vir 2 mg/ml, colirio en solución
Portugal Tarobrim 2 mg/ml colírio, soluçao
Fecha de la última revisión de este prospecto: septiembre 2016
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) (http://www.aemps.gob.es/).
- País de registro
- Precio medio en farmacia7.31 EUR
- Principio activo
- Requiere recetaSí
- Fabricante
- Esta información es de carácter general y no sustituye la consulta con un profesional sanitario.
- Alternativas a BRIMONIDINA VIR 2 mg/ml COLIRIO EN SOLUCIONForma farmacéutica: COLIRIO, 2 mg/mlPrincipio activo: BrimonidinaFabricante: Tiedra Farmaceutica S.L.Requiere recetaForma farmacéutica: COLIRIO, 2 mg/ml de tartrato de brimonidinaPrincipio activo: BrimonidinaFabricante: Abbvie Spain, S.L.U.Requiere recetaForma farmacéutica: COLIRIO, 2 MG/MLPrincipio activo: BrimonidinaFabricante: Viatris LimitedRequiere receta
Médicos online para BRIMONIDINA VIR 2 mg/ml COLIRIO EN SOLUCION
Comenta la dosis, los posibles efectos secundarios, interacciones, contraindicaciones o la revisión de receta de BRIMONIDINA VIR 2 mg/ml COLIRIO EN SOLUCION, sujeto a valoración médica y a la normativa local.
Preguntas frecuentes















